Zusammenfassung
- Definition:Unerwünschte Arzneimittelwirkung in Form einer Hautreaktion.
- Häufigkeit:Ca. 1–10 % der behandelten Patient*innen. Gehäuft bei Frauen und älteren Menschen.
- Symptome und Befunde:Bei Sofortreaktionen Urtikaria, Angioödem bis hin zur Anaphylaxie. Bei Spätreaktionen Exantheme bis hin zu schweren Hautreaktionen (toxische epidermale Nekrolyse).
- Diagnostik:Evtl. Eosinophilie im Blut. Im Rahmen einer allergologischen Abklärung Hauttest (Pricktest, Intradermaltest, Epikutantest), Provokationstest, Test auf spezifische IgE-Antikörper.
- Therapie:Absetzen des auslösenden Medikaments als wichtigste Maßnahme. Supportive Medikation durch Glukokortikoide, Antihistaminika. Bei schweren Hautreaktionen intensivmedizinische Behandlung.
Allgemeine Informationen
Definition
- Unerwünschte Hautreaktion auf ein Arzneimittel, die die Struktur oder Funktion von Haut, Hautanhangsgebilden oder Schleimhäuten betrifft.1
Allgemeine Einteilung unerwünschter Arzneimittelreaktionen
- Unerwünschte Arzneimittelwirkungen (UAW) werden gegliedert in Typ A (pharmakologisch-toxisch) und Typ B (Überempfindlichkeit).
- Typ A („augmented“)
- dosisabhängig voraussehbare pharmakologisch-toxische Wirkung eines Arzneimittels
- Typ B („bizarre“)
- individuell nicht vorhersehbare Reaktion, Auftreten nur bei Prädisponierten
- Zwei Formen können unterschieden werden:
- Arzneimittel-Allergie
- immunologische Reaktion (Typen I–IV nach Coombs u. Gell)
- nichtimmunologische Arzneimittelüberempfindlichkeit (Hypersensitivität)
- kein immunologischer Mechanismus nachweisbar
- Arzneimittel-Allergie
Problemstellung
- Beinahe jedes Arzneimittel kann Hautreaktionen auslösen, bei einigen Substanzklassen wie Antibiotika und Antikonvulsiva beträgt die Häufigkeit bis 1–5 %.2
- Typ-B-Reaktionen sind aufgrund ihrer Abhängigkeit von individuellen Faktoren der Patient*innen im Allgemeinen nicht vorhersehbar.
- Meist lässt die Art des Exanthems keine eindeutigen Rückschlüsse auf das verantwortliche Medikament zu.
- Auch wenn die meisten Hautreaktionen leichteren Grades sind, gibt es auch schwere und potenziell lebensbedrohliche Verläufe.2
- Wichtig ist daher:
- die Einteilung in milde und schwere Formen, um eine adäquate Therapie einzuleiten.
- die Unterscheidung in allergische/nichtallergische Genese, da bei allergischen Reaktionen eine erneute Exposition fatal verlaufen kann.
Häufigkeit
- Hautreaktionen sind die häufigste Form von UAW.3
- Prävalenz
- Unterschiedliche epidemiologische Daten, betroffen sind ca. 1–10 % der ambulanten Patient*innen.4-5
- Geschlecht
- Frauen zu Männern ca. 2:1
- Alter
- häufiger bei Älteren4
- bei geriatrischen Patient*innen 2–3 x häufiger auf als bei Patient*innen < 30 Jahre
Ätiologie
- Grundsätzlich kann jedes Medikament jede unerwünschte Arzneimittelreaktion verursachen.
Häufige Auslöser verschiedener Hautreaktionen
- Makulöse/makulopapulöse Exantheme
- Penizilline, Sulfonamide, Allopurinol, Antiepileptika
- Fixe Arzneimittelexantheme
- Tetrazykline, Sulfonamide, NSAR
- Urtikarielle Exantheme
- Penizilline, NSAR
- Dermatosen-imitierende Exantheme
- lichenoide Exantheme: Thiazide, Captopril, Gold, Betablocker
- psoriasiforme Exantheme: Gold, Lithium, Betablocker, Kalziumantagonisten
- Akneiforme Exantheme: Steroidhormone, Lithium
- Phototoxische/photoallergische Reaktion
- Tetrazykline, Gyrasehemmer, Diuretika
- Schwere Hautreaktionen
- DRESS (Drug Reaction with Eosinophilia and Systemic Symptoms): Carbamazepin, Phenytoin, Allopurinol, Sulfonamide
- SJS (Stevens-Johnson-Syndrom), TEN (toxische epidermale Nekrolyse: Allopurinol, Sulfonamide, Antiepileptika
Pathogenese
- Spezifisches Merkmal immunologischer Reaktionen ist eine pathologische Aktivierung des erworbenen Immunsystems, hingegen können Teile des angeborenen Immunsystems bei allen Typ-B-Reaktionen beteiligt sein.
Immunologische Reaktionen
- Eine Sensibilisierungsphase ist Voraussetzung für die Aktivierung des adaptiven Immunsystems und Auslösung einer Immunreaktion bei erneutem Kontakt.
- Nach Coombs und Gell können vier immunologisch vermittelte Reaktionen unterschieden werden:4
- Typ I (IgE-vermittelt): Urtikaria, Angioödem, Anaphylaxie
- Reaktionszeit: 0–6 Stunden (selten bis 12 Stunden)
- Typ II (zytotoxisch): Purpura, hämolytische Anämie
- Typ III (immunkomplex-vermittelt): Vaskulitis
- Typ IV (T-Zell-vermittelt): verschieden Formen von Exanthemem, Kontaktdermatitis, photoallergische Reaktion.
- Typ I (IgE-vermittelt): Urtikaria, Angioödem, Anaphylaxie
- Typ 1- und Typ 4- Reaktionen treten am häufigsten auf.6
- Siehe auch Artikel Arzneimittelinduzierte allergische Reaktionen.
Nichtimmunologische Reaktionen
- Nichtimmunologische Reaktionen beruhen auf direkter Komplement- oder Zellaktivierung, entzündlichen Signalkaskaden oder Enzymhemmung.
- Da gleiche Effektormechanismen und klinische Symptome wie bei immunologischen Typ-B-Reaktionen auftreten können, wird manchmal auch von Pseudoallergie gesprochen.
- Nichtimmunologischen Pathomechanismen sind:
- Histaminfreisetzung
- Komplementaktivierung
- Enzyminhibition.
- Reaktionszeit: 0–6 Stunden (selten bis 12 Stunden)
Wichtige Auslöser von immunologischen und nichtimmunologischen Reaktionen
- Auslöser immunologischer Reaktionen (Beispiele)
- Penizilline
- Cephalosporine
- Insuline
- Heparine
- Pyrazolone
- Muskelrelaxanzien
- Biologika7
- Auslöser nichtimmunologischer Reaktionen (Beispiele)
- Sulfonamide und andere Nicht-Beta-Laktam-Antibiotika
- Lokalanästhetika
- NSAR
- ACE-Hemmer
- Antiepileptika
- Opiate
Allgemeines zur klinischen Manifestation
Zeitabhängigkeit
Zeitintervall bis zur Hautreaktion
- Bei bereits überempfindlichen Patient*innen
- Sofortreaktion („immediate“): sofort bis 60 min
- verzögerte Reaktion („non-immediate“) > 1 Stunde bis mehrere Wochen
- ca. 80 % der kutanen Hautreaktionen
- Bei Neusensibilisierung unter Therapie: typische Sensibilisierungslatenz 5–10 Tage
Manifestation abhängig vom zeitlichen Auftreten
- Abhängig vom zeitlichen Aufreten können unterschieden werden:
- soforttypähnliche Symptome, z. B.:
- Flush, Urtikaria, Angioödem, Bronchospasmus, Anaphylaxie
- spättypähnliche Symptome, z. B.:
- makulopapulöse Arzneimittelexantheme
- schwere Hautreaktionen (u. a. Stevens-Johnson-Syndrom, toxische epidermale Nekrolyse)
- soforttypähnliche Symptome, z. B.:
Häufigkeit verschiedener Hautreaktionen
- Die häufigsten benignen Hautreaktionen sind:5,8
- Seltenere arzneimittelinduzierte Hautreaktionen
- Dermatosen-imitierende Reaktionen
- Vaskulitis
- photochemische Reaktionen
- schwere arzneimittelinduzierte Hautreaktionen
Spezielle klinische Manifestationen
Makulopapulöses Exanthem
- Häufigste Form der kutanen Arzneimittelreaktion
- Folge einer Spättyp-Reaktion (Typ-IV-Allergie)
- Häufige Auslöser: Antibiotika (insbesondere Beta-Laktam-Antibiotika und Sulfonamide), Antikonvulsiva, Allopurinol und NSAR
- Auftreten meist 8–10 Tage nach Einnahme (Beginn auch nach Absetzen noch möglich)
- Üblicherweise Beginn an Stamm und Nacken, zentrifugale Ausbreitung über die Extremitäten
- Ausgespart sind im Allgemeinen Kopf, Handflächen/Fußsohlen und Schleimhäute.
Urtikaria
- Urtikaria kann sowohl immunologisch als auch nichtimmunologisch ausgelöst werden.
- Häufige Auslöser sind Beta-Laktam-Antibiotika und NSAR
- Auftreten meist innerhalb von Minuten bis zu 1 h nach Arzneimittelaufnahme
- Juckende Quaddeln unterschiedlicher Größe, die einzelne Quaddel besteht nicht länger als 24 h.
- Evtl. gleichzeitiges Auftreten von Angioödemen
- Auftreten im Rahmen einer Anaphylaxie bis hin zum anaphylaktischen Schock möglich (siehe auch Anaphylaxie, Erste Hilfe)
Fixes Arzneimittelexanthem
- Verzögerte immunologische Reaktion vom Typ IV, typische Auslöser sind Antibiotika (insbesondere Cotrimoxazol) und Analgetika (NSAR, Paracetamol).
- Beginn meist innerhalb von 2 Wochen nach Exposition
- Auftreten gewöhnlich als einzelne oder mehrere, gut abgrenzbare Makulä oder Plaques; Größe der Läsionen ca. 1–10 cm
- Häufig akrale Lokalisation (Hände, Füße, Lippen, Genitale), aber auch an Extremitäten, Rumpf, Kopf und Schleimhäuten,
- Bei erneuter Exposition Auftreten an derselben Stelle, schnelle Reaktivierung innerhalb 12 Stunden möglich,
Dermatosen-imitierende Reaktionen
- Arzneimittelreaktionen können Dermatosen imitieren, die Abgrenzung ist häufig schwierig und die Nomenklatur uneinheitlich.
- Manche Arzneimittel können sowohl eine bestehende Dermatose verschlechtern als auch eine Arzneimittelreaktion auslösen (z. B. TNF-Alpha-Blocker: Psoriasis bzw. psoriasiformes Exanthem).
- Auslöser sind zahlreiche klassische aber auch neue (Biologika) Substanzen.7
- Ausgelöst werden u. a.:
- pityriasiformes Exanthem
- psoriasiformes Exanthem
- lichenoides Exanthem
- Arzneimittelinduzierte Varianten, die formal zu den Dermatosen gezählt werden:
- medikamentös induzierter Lupus erythematodes
- Pemphigus vulgaris
- bullöses Pemphigoid.
Vaskulitis
- Typ-III-Reaktion mit Ablagerung von Immunkomplexen2
- Auslöser sind u. a. Penicilline, Sulfonamide, NSAR und Thiazide.
- Präsentation häufig als Purpura im Bereich der Beine, weitere Manifestationsformen sind erythematöse Makulä, hämarrhagische Blasen oder Ulzerationen.2
Photosensitivität
- Phototoxizität9
- Symptome sind sonnenbrandähnlich und auf die sonnenexponierten Bereiche beschränkt.
- Auftreten in Minuten bis Stunden
- Zahlreiche auslösende Medikamente, z. B. Diuretika, ACE-Hemmer, Ca-Antagonisten, u. v. a.
- Photoallergie9
- Symptome ähnlich einem Kontaktekzem
- Auftreten 24–72 h nach Exposition
- Überwiegend sind sonnenexponierte Areale betroffen, Ausdehnung auf den nicht exponierten Bereich ist möglich.
- Siehe auch Artikel Lichtdermatosen.
Schwere Hautreaktionen
- Schwere Hautreaktionen sind T-Zell-vermittelt (Typ-IV-Reaktion).
- Seltene, aber potenziell lebensbedrohliche Reaktionen (vor allem SJS/TEN, jährliche Inzidenz 1–2/1.000.000), im Einzelnen können unterschieden werden:
- AGEP (akute, generalistierte exanthematische Pustulose)
- rasches Auftreten von Dutzenden bis Hunderten stecknadelkopfgroßen Pusteln (betont in den Beugen) auf diffusem Erythem, akut häufig Fieber über 38 °C, gelegentlich Schleimhaut- und Organbeteiligung
- DRESS (Drug Reaction with Eosinophilia and Systemic Symptoms)
- variierendes Bild, häufig makulo-papulöses Exanthem bis hin zur Erythrodermie
- begleitend Fieber, Gesichtsödem, Lymphadenopathie, Bluteosinophilie, Organbeteiligungen (v. a. Leber, Niere, Lunge)
- SJS (Stevens-Johnson-Syndrom), TEN (toxische epidermale Nekrolyse)
- Erytheme mit Übergang in z. T. ausgedehnte Blasenbildung, ähnlich einer großflächigen zweitgradigen Verbrennung oder Verbrühung, erosive Schleimhautveränderungen, Fieber
- definitionsgemäß Hautablösung bei SJS < 10 %, bei TEN > 30 %, Übergangsform 10–30 %
- Medikamente mit hohem Risiko sind u. a. Allopurinol, Antiepileptika (Carbamazepin, Phenytoin, Lamotrigin), Sulfonamide (Cotrimoxazol).
Prädisponierende Faktoren
Patient*innen
- Alter
- häufiger bei Älteren
- Geschlecht
- Frauen sind häufiger betroffen.
- Allergische Disposition
- Chronische Erkrankungen
- Alkoholismus
- Infektionen (z. B. HIV)
Medikation
- Substanz
- Polypharmazie
- Applikationsform
- Das Risiko einer Arzneimittelreaktion nimmt in folgender Reihenfolge zu:
- peroral
- intravenös
- intramuskulär
- subkutan
- topisch
- Das Risiko einer Arzneimittelreaktion nimmt in folgender Reihenfolge zu:
ICPC-2
- A85 Unerwünschte Wirkung eines Medikaments
- S99 Hautkrankheit, andere
ICD-10
- L27.- Dermatitis durch oral, enteral oder parenteral aufgenommene Substanzen
- L27.0 Generalisierte Hauteruption durch Drogen oder Arzneimittel
- L27.1 Lokalisierte Hauteruption durch Drogen oder Arzneimittel
- L27.2 Dermatitis durch aufgenommene Nahrungsmittel
- L27.8 Dermatitis durch sonstige oral, enteral oder parenteral aufgenommene Substanzen
- L27.9 Dermatitis durch nicht näher bezeichnete oral, enteral oder parenteral aufgenommene Substanz
Sonstige
- L10.5 Arzneimittelinduzierter Pemphigus
- L23.3 Allergische Kontaktdermatitis durch Drogen oder Arzneimittel bei Hautkontakt
- L24.4 Toxische Kontaktdermatitis durch Drogen oder Arzneimittel bei Hautkontakt
- L25.1 Nicht näher bezeichnete Kontaktdermatitis durch Drogen oder Arzneimittel bei Hautkontakt
- L50.- Urtikaria
- L56.0 Phototoxische Reaktion auf Arzneimittel
- L56.1 Photoallergische Reaktion auf Arzneimittel
- L51.2 Toxische epidermale Nekrolyse
- T78.4 Allergie, nicht näher bezeichnet
- T88.7 Nicht näher bezeichnete unerwünschte Nebenwirkung eines Arzneimittels oder einer Droge
Diagnostik
- Eine allergologische Diagnostik ist nur bei allergischen oder nicht allergischen Überempfindlichkeitsreaktionen (Typ-B-Reaktionen) sinnvoll.
- nicht sinnvoll bei pharmakologisch-toxischen Arzneimittelnebenwirkungen (Typ-A-Reaktionen)
Diagnostische Kriterien
- Die Zuordnung zu einem Medikament als Auslöser kann als ausreichend gesichert angesehen werden bei:
- typischer Anamnese und Symptomatik einer Hautreaktion und
- eindeutigen Befunden validierter Haut- und/oder Labortests (bei nicht sicher aussagekräftigen Tests evtl. kontrollierte Provokationstestung).
- Ein sicherer Ausschluss einer Arzneimittelüberempfindlichkeit ist auch bei Anwendung aller verfügbaren Testverfahren nicht immer möglich, jedoch bessere Risikoeinschätzung.
Differenzialdiagnosen
- Differenzialdiagnosen sind u. a.:1
- virale Infektionen
- andere Infektionen
- Psoriasis
- Pityriasis
- Lichen ruber planus
- kutaner Lupus erythematodes
- bullöse Autoimmundermatosen (Pemphigus vulgaris, bullöses Pemphigoid)
- disseminierte Kontaktdermatitiden
- Vaskulitiden.
Anamnese und Untersuchungsbefunde
Anamnese
- Medikation
- Substanz(en), Dosierung
- Dauermedikation, kurzzeitig eingenommene Medikation
- Art der Anwendung (oral, s. c., topisch)
- Verträglichkeit bei früherer Anwendung
- Hautreaktion
- zeitlicher Abstand zwischen Medikation und Hautreaktion (Sofortreaktion, Spätreaktion)
- Art des Ausschlags
- Lokalisation
- Dauer
- Änderungen im Verlauf
- Juckreiz
- Weitere Symptome
- Atemnot
- gastrointestinale Beschwerden
- Kreislaufreaktion: Schwindel, Palpitationen
- Vorerkrankungen
- Allergien (Allergiepass)
- Asthma bronchiale
- Urtikaria
- Mastozytose
- Intoleranzen
- Kofaktoren für allergische Reaktion
- Infektion
- Stress
- Nahrungsaufnahme
- Alkohol
- körperliche Anstrengung
- Sonnenexposition
Klinische Untersuchung
- Klinisch-morphologischer Befund (evtl. Fotodokumentation)
- Haut
- Schleimhäute
- Kreislauf (bei V. a. Anaphylaxie)
- RR/Puls
- Atemwege (bei V. a. Anaphylaxie)
- auskultatorisch Obstruktion
- Körpertemperatur
Ergänzende Untersuchungen in der Hausarztpraxis
Labor
- Differenzialblutbild: evtl. Eosinophilie
Karenzversuch
- Kann bei Besserung der Symptomatik einen Hinweis (jedoch keinen Beweis) auf möglichen Auslöser geben.
- Zuvor sollte geklärt werden, ob das Präparat verzichtbar ist, bzw. ob auf ein nicht strukturverwandtes Medikament ausgewichen werden kann.
Red Flags
- Warnzeichen für einen schweren Reaktionsverlauf:5-6
- bullöse Hautreaktion
- schmerzhafte Hautveränderungen
- Beteiligung von Gesicht und Schleimhäuten
- Allgemeinsymptome wie Fieber > 38,5 °C
- Lymphadenopathie
- Dyspnoe
Diagnostik bei Spezialist*innen
- Eine allergologische Klärung möglichst innerhalb von 4 Wochen bis 6 Monaten nach Abheilung der Symptome ist anzustreben.
- Der Verzicht auf eine Diagnostik kann einerseits schwere Reaktionen bei erneuter Exposition zur Folge haben, andererseits zu ungerechtfertigter Einschränkung der Therapiemöglichkeiten führen.
- Eine allergologische Diagnostik bei Patient*innen ohne Vorgeschichte einer Arzneimittelüberempfindlichkeit („prophetische Testung“) ist nicht sinnvoll.
Hauttests
- Geeignet zur Diagnostik immunologischer Arzneimittelreaktionen
- Sofortreaktionen: vorwiegend Pricktest, Intrakutantest (Ablesung nach 20 min)
- Bei Exanthemen sollte bei Prick- und Intrakutantests auch eine Spätablesung nach 48 und 72 Stunden erfolgen (z. B. Abklärung eines Amoxicillin-Exanthems).
- Spätreaktionen: vorwiegend Epikutantest (Ablesung nach 48–72 h)
- Sofortreaktionen: vorwiegend Pricktest, Intrakutantest (Ablesung nach 20 min)
- Pricktest
- Methode der 1. Wahl zur Abklärung von Sofortreaktionen
- Durchführung an der Volarseite der Unterarme (alternativ am oberen Rücken)
- Jeweils ein Tropfen der Testlösung wird mit einer Pipette aufgebracht, durch den Tropfen wird die Haut oberflächlich angestochen.
- Intrakutantest
- sensitiver als der Pricktest, Durchführung vor allem bei unauffälligem Pricktest
- Die Testlösung wird streng intrakutan injiziert, Ziel ist eine ca. 3mm große Quaddel.
- Nachteile sind Schmerzhaftigkeit, höherer Aufwand und höheres Risiko systemischer Reaktionen.
- Epikutantest („Pflastertest“)
- Wird eingesetzt zur Diagnostik T-Zell-mediierter Arzneimittelreaktionen (Typ IV), z. B. makulopapulöses Exanthem.
- Durchführung frühestens nach einem Monat nach Abheilung einer nicht IgE-vermittelten unerwünschten Reaktion
- Aufbringen der Testallergene auf dem Rücken, Expositionsdauer von zwei Tagen (Erhöhung der Sensitivität), Ablesen nach 48 h und 7 2h (oder 96 h)
Spezielle Laboruntersuchungen
- Können hilfreich sein bei negativen Hauttests sowie lebensbedrohlichen Reaktionen mit Gefährdung durch Hauttest (z. B. anaphylaktische Reaktionen auf Beta-Laktam-Antibiotika)
- Tests zur Messung spezifischer IgE-Antikörper auf verschiedene Arzneimittel werden angeboten, allerdings stehen nur für wenige Substanzen validierte Tests zur Verfügung (z. B. Beta-Laktam-Antibiotika).
- Interpretation immer im Zusammenhang, sicherer Nachweis oder Ausschluss einer Arzneimittelüberempfindlichkeit allein durch In-vitro-Tests ist nicht möglich.
Provokationstest
- Test mit der größten diagnostischen Aussagekraft
- Durchführung nach kritischer Nutzen-Risiko-Analyse, Bedeutung z. B. bei dringender Notwendigkeit des verdächtigen Medikaments oder zur Überprüfung einer Verträglichkeit möglicher Ausweichmedikamente
- Testsubstanzen sollten in der Form verabreicht werden, die zur Überempfindlichkeitsreaktion geführt hat.
- Durchführung stationär mit Möglichkeit zur Notfallversorgung durch erfahrenes Personal
Biopsie/Histologie
- Im Rahmen einer erweiterten Abklärung, z. B. zur Abgrenzung von Arzneimittelreaktionen gegen Dermatosen
Indikationen zur Überweisung/Klinikeinweisung
- Patient*innen mit SJS/TEN müssen intensivmedizinisch behandelt werden (evtl. auf einer Verbrennungseinheit).
Therapie
Therapieziele
- Unerwünschte Arzneimittelreaktionen vermeiden
- Symptome lindern
- Komplikationen behandeln
Allgemeines zur Therapie
Absetzen des Medikaments
- Wichtigste Maßnahme ist – wenn möglich – das Absetzen des auslösenden Medikaments.10
- Verabreichung alternativer Präparate mit andersartiger chemischer Struktur
Sofortreaktionen
- Medikamente mit Sofortreaktionen dürfen im Allgemeinen nicht mehr verabreicht werden.
- Bei unverzichtbaren Präparaten kann evtl. eine Toleranzinduktion durchgeführt werden (z. B. ASS).
- rasche Dosissteigerung (innerhalb weniger Stunden bis Tage) von initial sehr geringer bis zur therapeutischen Dosis
- Toleranz besteht nur für die Dauer der Applikation, bei zwischenzeitlicher Pausierung muss erneute Toleranzinduktion erfolgen!
- Zu Details der Notfalltherapie siehe Anaphylaxie, Erste Hilfe
Spätreaktionen
- Die Reaktion kann nur supportiv und nicht kausal behandelt werden.6
- Therapeutische Optionen sind:5
- topische Glukokortikoide
- systemische Glukokortikoide
- z. B. 0,5–0,75 mg/kg Prednisolonäquivalent
- Antihistaminika
- Sehr leichte Verläufe
- Bei mangelnder Alternativmedikation kann auch ein Durchbehandeln erwogen werden unter engmaschiger Kontrolle.
- begleitende Therapie mit Glukokortikoiden und/oder Antihistaminika zur Symptomlinderung
- Leichte bis mittelgradige Verläufe
- Absetzen des Arzneimittels
- je nach Symptomatik Therapie mit topischen/systemischen Glukokortikoiden sowie Antihistaminika
Schwere arzneimittelinduzierte Hautreaktionen
- Bei Stevens-Johnson-Syndrom (SJS) und toxischer epidermaler Nekrolyse (TEN) ist eine intensivmedizinische Therapie erforderlich (evtl. Spezialeinheit für Verbrennungen).
- Medikamentöse Behandlung
Verlauf, Komplikationen und Prognose
Komplikationen
- Sofortreaktionen: Anaphylaxie
- Spätreaktionen: Entwicklung einer schweren Hautreaktion bis hin zur toxischen epidermalen Nekrolyse (TEN)
Verlauf und Prognose
- Die meisten Hautreaktionen nehmen einen benignen Verlauf.5
- In der Mehrzahl der Fälle klingen die Symptome nach Absetzen eines Medikaments innerhalb von 1–2 Wochen ab.10
- Ca. 2 % der Reaktionen nehmen einen schweren oder sogar lebensbedrohlichen Verlauf.3
- Mortalität des SJS bei 1–5 %, TEN bei 25–35 %
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen
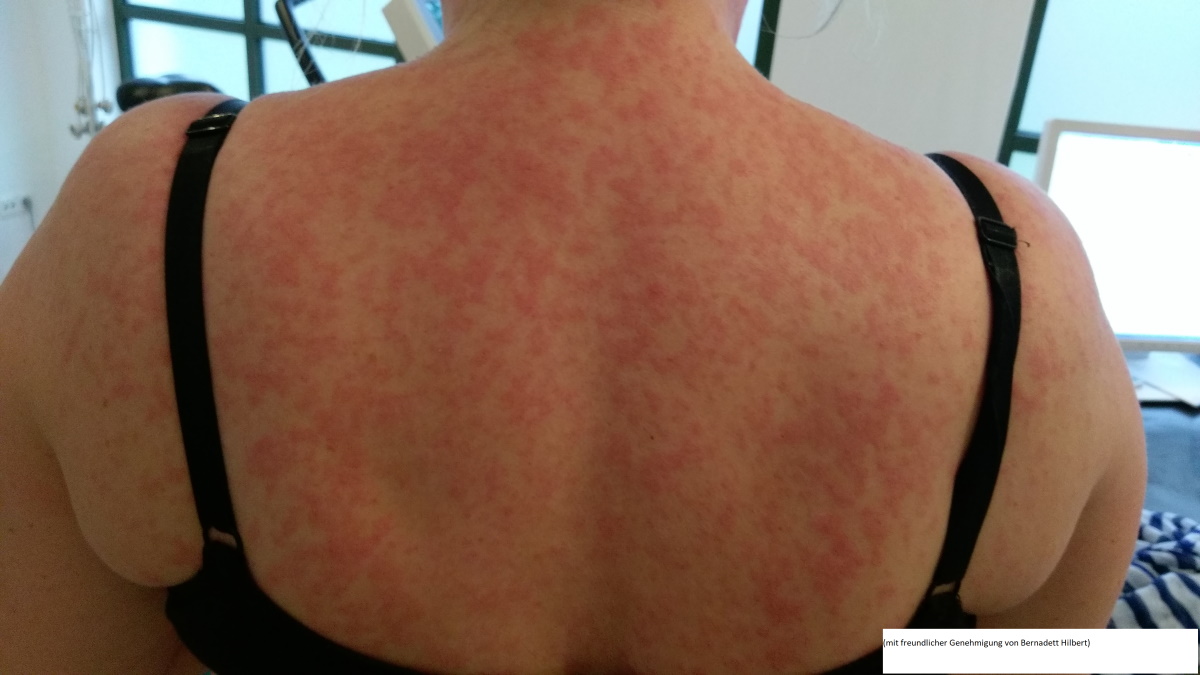
Arzneimittelexanthem (mit freundlicher Genehmigung von Bernadett Hilbert)
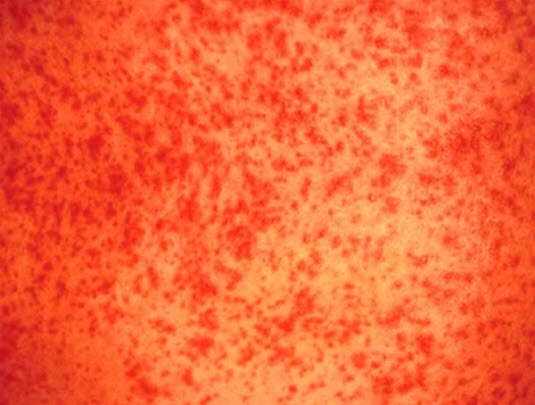
Arzneimittelinduzierte Hautreaktion mit generalisiertem makulopapulösem Exanthem
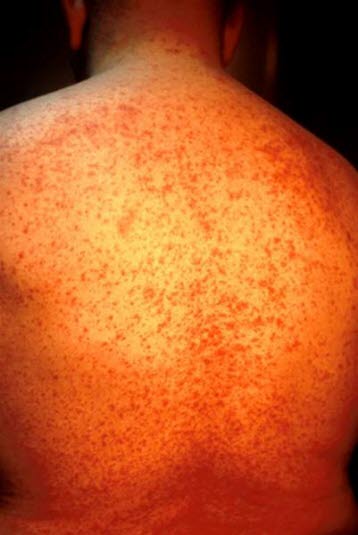
Makulopapulöses Arzneimittelexanthem
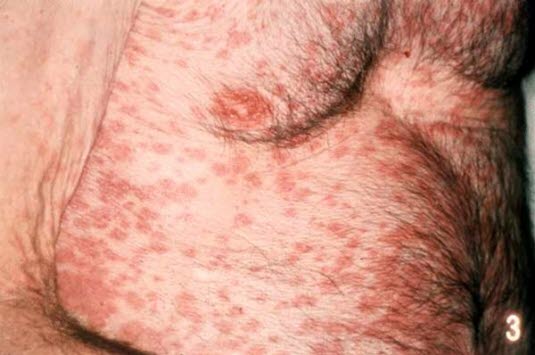
Arzneimittelexanthem
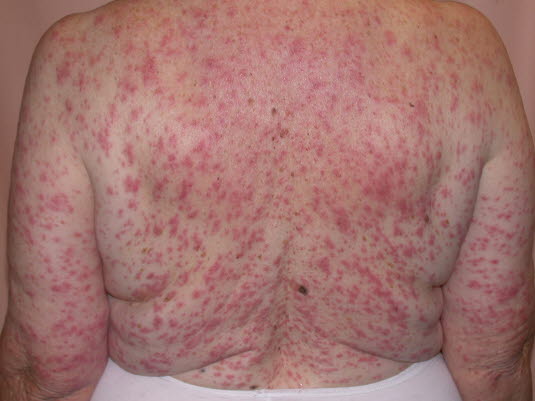
Arzneimittelexanthem
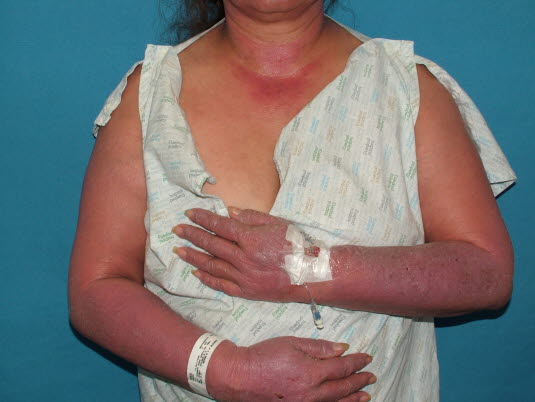
Photochemische Reaktion
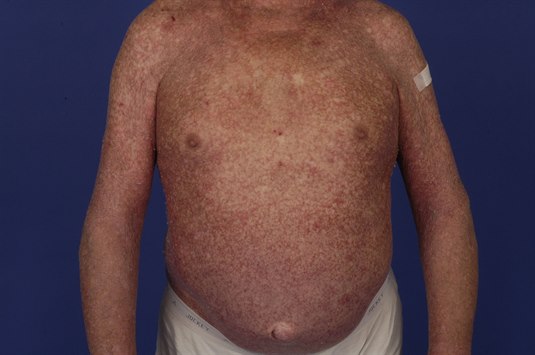
Arzneimittelinduzierte Hautreaktion
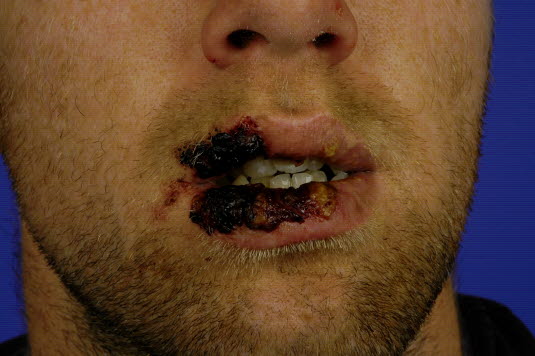
Stevens-Johnson-Syndrom
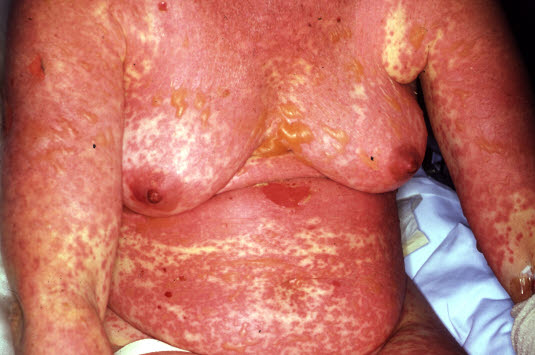
Toxische epidermale Nekrolyse
Quellen
Literatur
- Common cutaneous drug reactions. BMJ Best Practice. Last updated 20 May 2020. Zugriff 15.12.22. bestpractice.bmj.com
- Lee A. Adverse drug reactions - Chapter 5: Drug-induced skin reactions. London - Chicago: Pharmaceutical Press, 2005.
- Farshchian M, Ansar M, Zamanian M, et al. Drug-induced skin reactions: a 2-year study. Clinical, Cosmetic and Investigational Dermatology 2015; 8: 53-56. doi:10.2147/CCID.S75849 DOI
- Blume J. Drug eruptions. Medscape, updated July 07, 2022. Zugriff 15.12.22. emedicine.medscape.com
- Hoetzenecker W, Nägeli M, Nehra W, et al. Adverse cutaneous drug eruptions: current understanding. Semin Immunopathol 2016; 38: 75-86. doi:10.1007/s00281-015-0540-2 DOI
- Böhm R, Proksch E, Schwarz T, et al. Drug hypersensitivity—diagnosis, genetics, and prevention. Dtsch Arztebl Int 2018; 115: 501–12. DOI: 10.3238/arztebl.2018.0501 www.aerzteblatt.de
- Pasadyn S, Knabel D, Fernandez A, et al. Cutaneous adverse effects of biologic medications. Clevel Clin J Med 2020; 87: 288-289. doi:10.3949/ccjm.87a.19119 DOI
- Goutham S, Rajendran N. Patterns of Cutaneous Drug Reactions: A Review. Journal of Basic, Clinical and Applied Health Science 2019. doi:10.5005/jp-journals-10082-02223 DOI
- Zuba E, Koronowska S, Osmola-Mankowska A, et al. Drug-induced Photosensitivity. Acta Dermatovenerol Croat 2016; 24: 55-64. pmid:27149132 PubMed
- Riedl M, Casillas A. Adverse Drug Reactions: Types and Treatment Options. Am Fam Physician 2003; 68: 1781-1790. www.aafp.org
- Zhang J, Zixian L, Xu C, et al. Current Perspectives on Severe Drug Eruption. Clinical Reviews in Allergy & Immunology 2021; 61: 282-298. doi:10.1007/s12016-021-08859-0 DOI
Autor*innen
- Michael Handke, Prof. Dr. med., Facharzt für Innere Medizin, Kardiologie und Intensivmedizin, Freiburg i. Br.