Allgemeine Informationen
- Zahlreiche Schilddrüsenerkrankungen führen zu einer Veränderung des Parenchyms und/oder der Größe und Form der Schilddrüse.
- Die Sonografie ist ein kostengünstiges, nichtinvasives und risikoarmes Untersuchungsverfahren zur Darstellung der Schilddrüse.
- Bei der Schilddrüsensonografie sind detaillierte Kenntnisse der betreffenden Untersuchungsregion essenziell.
Technische Grundlagen
- Eingesetzt wird ein Schallkopf, der Ultraschallwellen aussendet. Diese werden an Grenzflächen von Geweben reflektiert, und der Schallkopf registriert Amplitude und Verzögerung der reflektierten Wellen.
- Verschiedene Schallköpfe mit unterschiedlicher Eindringtiefe und Auflösung stehen zur Verfügung.
- Aus der Intensität der reflektierten Schallwellen wird eine Darstellung in Graustufen errechnet, die dem Bild der Sonografie im B-Mode entspricht.
- Die Reflektions- und Streuungseigenschaften eines Gewebes werden als Echogenität bezeichnet.
- Die Darstellung von Strukturen niedriger Echogenität (z. B. Flüssigkeit, Hämatome) ist dunkel.
- Die Darstellung von Strukturen hoher Echogenität (z. B. Luft) ist hell.
- Weitere ultraschallbasierte Anwendungen
- Doppler-Verfahren: Erfassung und Darstellung von Strömungen durch Doppler-Effekt
- Basiert auf unterschiedlicher Reflektion von Grenzflächen in Bewegung.
- Continuous Wave Doppler (CW-Doppler)
- Pulsed Wave Doppler (PW-Doppler)
- Duplexsonografie: Kombination aus B-Mode und PW-Doppler
- Farbkodierte Duplexsonografie: Farbige Darstellung der Strömungsrichtungen im Bild. Rot entspricht üblicherweise einer Strömung auf den Schallkopf zu, blau von dem Schallkopf weg.
- Doppler-Verfahren: Erfassung und Darstellung von Strömungen durch Doppler-Effekt
Apparative Voraussetzungen
- Für die Schilddrüsen-Sonografie wird ein B-Mode-Ultraschallgerät benötigt.
- Ein 6 cm breiter Linearschallkopf ist für die Untersuchung ideal, aber auch ein 5 cm breiter Schallkopf ist akzeptabel.
- Ein sektorialer Schallkopf mit kürzerer Auflagefläche ist nicht optimal.
- Schallfrequenz 7,5–12 MHz
- Ein niederfrequenter Sektorschallkopf ist nur in Einzelfällen (sehr große und tiefliegende Strumen) erforderlich.
Indikationen
- Bestimmung der Schilddrüsen-Größe, z. B. bei V. a. Struma
- Darstellung und Verlaufskontrolle von Herdbefunden, wie Knoten und Zysten
- Beurteilung der Echostruktur, z. B. bei Autoimmunerkrankungen
- Einschätzung der Durchblutung (z. B. bei V. a. M. Basedow)
- Beurteilung der regionalen Lymphknoten und der Nebenschilddrüsen
- Beurteilung bei V. a. Schilddrüsenkarzinom
- Kontrolle nach Schilddrüsenoperation (totale Thyreoidektomie, subtotale Thyreoidektomie, Lobektomie)
- Kontrolle nach Radiojodtherapie
Untersuchung
Vorbereitung
- Der Raum sollte abgedunkelt werden.
- Das Gerät sollte für die Dokumentation auf Papier, Film oder elektronisch eingerichtet sein.
- Erläutern Sie der Patientin/dem Patienten den Zweck und den Ablauf der Untersuchung.
- Die Patientin/der Patient wird in Rückenlage mit überstrecktem Hals untersucht.
- Wenn der Hals nicht überstreckt ist, ist keine optimale Darstellung der Schilddrüse möglich.
- Um den Kontakt zwischen Schallkopf und Haut zu verbessern, wird Ultraschallgel verwendet.
Durchführung
- Für die Untersuchung ist ein standardisierter Ablauf wichtig, um nichts zu übersehen.
- immer systematisch: zuerst rechter, dann linker Lappen
Querschnitt
- Aufsetzen des Schallkopfes in der mittleren Halsregion zur ersten Orientierung
- ggf. Optimierung der Geräteeinstellungen
- Untersuchung der beiden Schilddrüsenlappen von kranial nach kaudal
- Beurteilung des Isthmus
Längsschnitt
- Leicht schräg platzierter Schallkopf: von kraniolateral nach kaudomedial
- Untersuchung des gesamten Lappens durch langsames Kippen des Schallkopfes
Volumenberechnung
- Berechnung des Lappenvolumens: Länge x Breite x Tiefe x 0,5
- Moderne Ultraschallgeräte berechnen das Volumen nach Speicherung der Messwerte.
- Normwerte
- Gesamtvolumen beider Lappen, der rechte Lappen ist meist um 20 % größer.
- bei Frauen 4–18 ml
- bei Männern 5–25 ml
- bei Kindern (basierend auf österreichischen Daten von 539 Kindern)
- 6 Jahre: Mittelwert 2,0 ml, SD 0,7 ml
- 7 Jahre: Mittelwert 2,4 ml, SD 1,1 ml
- 8 Jahre: Mittelwert 3,0 ml, SD 1,3 ml
- 9 Jahre: Mittelwert 3,1 ml, SD 1,1 ml
- 10 Jahre: Mittelwert 3,8 ml, SD 1,9 ml
- 11 Jahre: Mittelwert 4,3 ml, SD 1,6 ml
- 12 Jahre: Mittelwert 5,0 ml, SD 1,9 ml
- 13 Jahre: Mittelwert 6,9 ml, SD 2,9 ml
- 14 Jahre: Mittelwert 7,5 ml, SD 2,5 ml
Beurteilung der Echogenität
- Referenzregion: M. sternocleidomastoideus
- Normales Schilddrüsengewebe ist im Vergleich dazu echoreicher (heller) und hat ein homogenes Echomuster.
- Echoarmes Echomuster z. B. bei lymphozytärer Infiltration, kleinerer Follikelstruktur
- Gefäße können durch Zuschaltung des Farbduplex abgegrenzt werden.
Beurteilung von Herdbefunden
- Solid vs. zystisch (echofrei, also schwarz)
- Größe, gemessen in 3 Ebenen
- Lage
- Echogenität
- Randbegrenzung
- Halo
- Kalk (echodicht, weiß)
- Durchblutung
Erstellung eines Befundes
- Diese Punkte sollen in einen Befund einfließen.
- Schilddrüsengröße
- Volumen rechts, Volumen links
- Lage- und Formbesonderheiten
- Echostruktur
- Beschreibung von Lokalisation, Größe, Echogenität, Begrenzung und Durchblutung von Herdbefunden
- Beurteilung benachbarter Strukturen (Lymphknoten, Nebenschilddrüsen, Trachea, Ösphagus, Gefäße)
- Schilddrüsengröße
Interpretation
Differenzialdiagnosen pathologischer Befunde
Die gesamte Schilddrüse betreffende Veränderungen
- Euthyreote Struma diffusa
- vergrößertes Organ, echonormales, bis echoreiches Grundmuster
- TSH normal
- Aplasie eines Schilddrüsenlappens (Hemiagenesie)
- Fehlende Anlage eines Schilddrüsenlappens, meist mit Hypertrophie der kontralateralen Seite, meist echonormales Grundmuster, Isthmus erhalten
- in 80 % der linke Lappen
- 3 x häufiger bei Frauen
- Zungengrundstruma
- Ist orthotop kein Schilddrüsengewebe abgrenzbar, soll dystopes Schilddrüsengewebe gesucht werden.
- Subakute Thyreoiditis de Quervain
- echonormale Grundstruktur, durchsetzt mit echoarmen, „wandernden“ Arealen
- Durchblutung initial vermindert, im Verlauf Normalisierung, teilweise passagere Hyperperfusion
- Sonografie schmerzhaft
- Häufig ist initial nur ein Schilddrüsenlappen betroffen, die Entzündung kann aber auf die gesamte Schilddrüse übergreifen.
- Hashimoto-Thyreoiditis
- initial echonormale Grundstruktur, durchsetzt mit multiplen, scharf abgegrenzten echoarmen Arealen („Schweizer Käse“)
- Im Verlauf diffus echoarmes Grundmuster, oft kaum von der Muskulatur abzugrenzen.
- positive Schilddrüsenantikörper (TPO-AK, TAK)
- latente, später manifeste Hypothyreose
- M. Basedow
- Schilddrüse meist vergrößert
- initial echonormal durchsetzt von scharf abgegrenzten echoarmen Arealen
- später diffus echoarm
- massiv erhöhte Durchblutung („Thyroid Inferno“)
- Normalisierung der Echostruktur bei Remission
- positive Schilddrüsenantikörper (TRAK, TPO-AK, TAK)
- hyperthyreot
- evtl. endokrine Orbitopathie
Knotige Veränderungen der Schilddrüse – Allgemeines
- Klinisch ist manchmal die Schilddrüse mit unebener und knotiger Oberfläche sichtbar/tastbar.
- Die klinische Untersuchung von Größe, Morphologie und Funktion ist jedoch sehr ungenau.1
- Bei bis zu 50 % der Patient*innen, bei denen ein solitärer Knoten tastbar ist oder eine diffus vergrößerte Schilddrüse vorliegt, werden in der sonografischen Untersuchung multiple Knoten nachgewiesen.2
- Knoten < 1 cm sind in der Regel nur sonografisch nachweisbar.
- Bestimmung der Schilddrüsengröße und Diagnose von Knoten
- Liegt bei einem euthyreoten Patient*innen eine klinisch und sonografisch diffuse Struma vor, die nicht oder nur langsam wächst, besteht in der Regel keine Indikation für eine weitere bildgebende Diagnostik.
- Befunde eines oder mehrerer kleiner Knoten mit einer Größe von weniger als 1 cm werden für gewöhnlich nicht eingehender untersucht. Davon ausgenommen sind Situationen, in denen der Verdacht auf ein Schilddrüsenkarzinom besteht. Knoten von unter 1 cm Größe können ggf. einmal im Jahr (oder seltener) sonografisch auf ihr Größenwachstum überprüft werden.
Malignitätskriterien
- Diagnose von „malignitätsverdächtigen“ Knoten, die eine weitere Abklärung mittels Feinnadelzytologie (FNZ) oder die histologische Abklärung erfordern.
- Sonografische Malignitätskriterien von Schilddrüsenknoten:3
- Echoarmut
- Mikrokalzifikationen
- unscharfe Begrenzung/kein Halo-Effekt
- intranoduläre Vaskularisation
- erhöhter Tiefendurchmesser
- Form und Lage quer zur Längsachse.
- Sonografische Befunde mit Malignitätskriterien gehen mit einer erhöhten Prävalenz von SD-Malignomen einher, jedoch ist die Spezifität jedes einzelnen Ultraschallparameters für die Malignitätsprädiktion gering.3
- Bei Nachweis mehrerer verdächtiger Ultraschallbefunde in einem SD-Knoten wird in der Literatur eine Sensitivität von 83–99 % und eine Spezifität von 56–85 % für das Vorliegen eines SD-Malignoms beschrieben.3
- Der positiv prädiktive Wert der Schilddrüsensonografie zur Knotenbeurteilung ist gering und erreicht in Kombination mehrerer Ultraschallparameter einen maximalen Wert von 39 %.4
- Das bedeutet, dass maximal 4 von 10 Knoten, die mehrere suspekte Sonokriterien aufweisen, tatsächlich maligne sind, während die anderen 6 von 10 nicht bösartig sind. Auch besteht zusätzlich das Problem der Überdiagnose.
Knotige Veränderungen der Schilddrüse – Befunddokumentation
- Folgende Punkte sollen beschrieben werden:
- Lage
- zentral/randständig
- kraniales, mittleres, kaudales Lappendrittel, Isthmus
- Halo
- gut abgrenzbar
- fehlend/unregelmäßig
- Begrenzung
- glatt
- irregulär
- Echogenität
- echogleich/echoreich/echoarm, homogen
- Kalk
- kleiner, grobschollig
- Mikroverkalkungen
- Blutfluss
- intranodulär niedrig/hoch
- peripher
- Lage
Knotige Veränderungen der Schilddrüse – Differenzialdiagnosen
- Oft vermehrte Durchblutung im Randbereich benigner Knoten (Halo)
- Ursachen knotiger Veränderungen der Schilddrüse: Kolloidknoten, Adenom, zystisch degeneriertes Adenom, Blutungszyste, funktionelle Autonomie, „kalter“ Knoten, Schilddrüsenkarzinom
- Seltenere Ursachen: Entzündungsherde bei Thyreoiditis, Lymphom, Nebenschilddrüsenadenom, Lipom, Neurinom, Lymphknoten, intrathyreoidale Metastase
Weitere Abklärung bei Spezialist*innen
- Szintigrafie
- Ist in der Regel bei der Diagnostik von euthyreoten Patient*innen mit kleinen Thyreoideaknoten oder diffuser Struma nicht indiziert.5
- Bei großer Struma ist eine Szintigrafie häufig nur dann sinnvoll, wenn eine Hyperthyreose vorliegt, oder bei euthyreoten Patient*innen, wenn die Radiojodbehandlung eine mögliche Behandlungsalternative ist.
- Bei Knoten mit einer Größe von mehr als 1 cm kann nach Abwägung aller Risiken (Strahlenbelastung, Überdiagnostik) und evtl. Vorteile (Detektion von heißen Arealen bei (subklinischer) Hyperthyreose) eine Szintigrafie erwogen werden.
- Die Szintigrafie liefert keinen Nachweis von Malignität.
- Bei einer Szintigrafie der Schilddrüse können anhand des Jod-Uptakes und des Verteilungsmusters kalte und heiße Knoten unterschieden werden.
- Kalte Knoten, die in der Sonografie nicht echofrei sind (Zysten) und suspekt erscheinen, können mit der Feinnadelaspirationszytologie (FNZ) resp. Feinnadelbiopsie (FNB) abgeklärt werden.
- Heiße Knoten sind jedoch nahezu immer benigne, meist liegt hier eine (ggf. subklinische) Hyperthyreose vor.
- Bei Nachweis einer SD-Autonomie kann auf eine Dignitätsabklärung des Knotens verzichtet werden, da autonome Adenome in aller Regel benigne Tumoren sind.
- Ist in der Regel bei der Diagnostik von euthyreoten Patient*innen mit kleinen Thyreoideaknoten oder diffuser Struma nicht indiziert.5
- Feinnadelzytologie oder -biopsie3
- Bei euthyreoten, szintigrafisch kalten Knoten > 1 cm, die auf der Basis von sonografischen Kriterien als malignitätsverdächtig gelten.
- Cave: Überdiagnostik – Mikrokarzinome, ohne klinische Relevanz!
- Knoten bei Patient*innen mit erhöhtem Malignitätsrisiko (externe Radiatio, positive Familienanamnese)
Beurteilung benachbarter Strukturen
- Bei der Schilddrüsensonografie werden auch evtl. vergrößerte Nebenschilddrüsen (Epithelkörperchen) diagnostiziert.
- Lymphknotensonografie
- Benigne Lymphknotenvergrößerungen sind häufig.
- elliptische Form, scharf begrenzt, Verhältnis Längs-/Querdurchmesser > 2,0
- echoarmes Grundmuster, echodichter Hilus zentral
- regelmäßige, nicht verstärkte Vaskularisation
- Malignitätskriterien
- plumpe, rundliche Form, Verhältnis Längs-/Querdurchmesser < 2,0
- Verlust von Hilus und Hilusdurchblutung
- inhomogenes Echomuster, manchmal zystisch
- Hypervaskularisation mit „chaotischen Gefäßen“
- unscharfe Begrenzung
- Verkalkungen
- multiple Lymphknoten
- im Abflussgebiet des Primärtumors gelegen
- Erfahrene Untersucher können ggf. mithilfe des Power-Doppler reaktive von neoplastischen Lymphknotenschwellungen unterscheiden.
- Benigne Lymphknotenvergrößerungen sind häufig.
Illustrationen
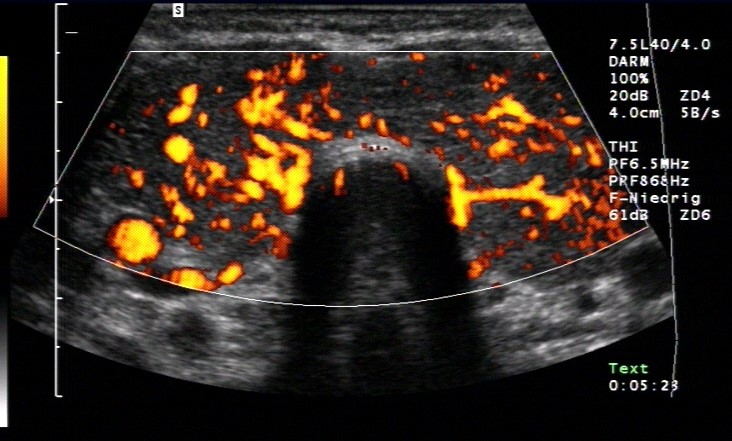
Morbus Basedow (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
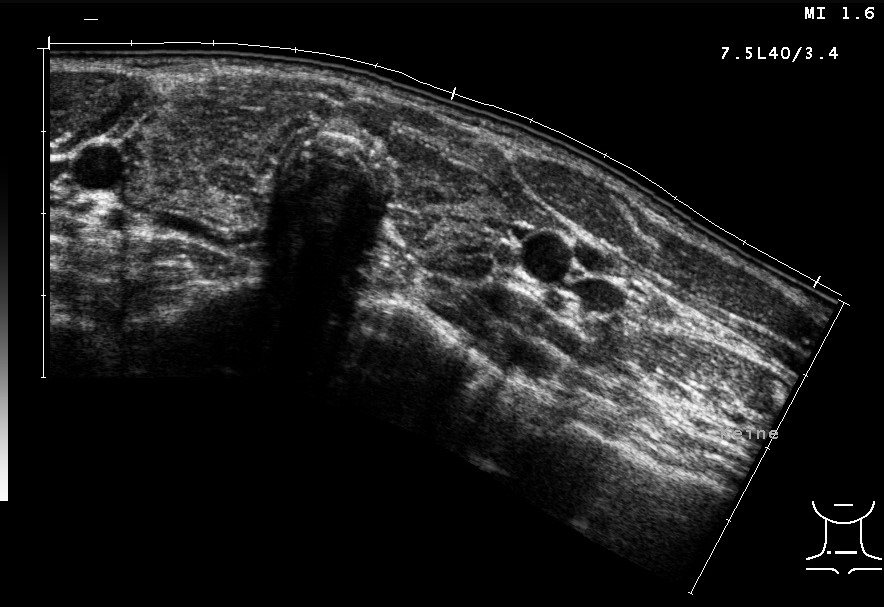
Hashimoto-Thyreoiditis (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
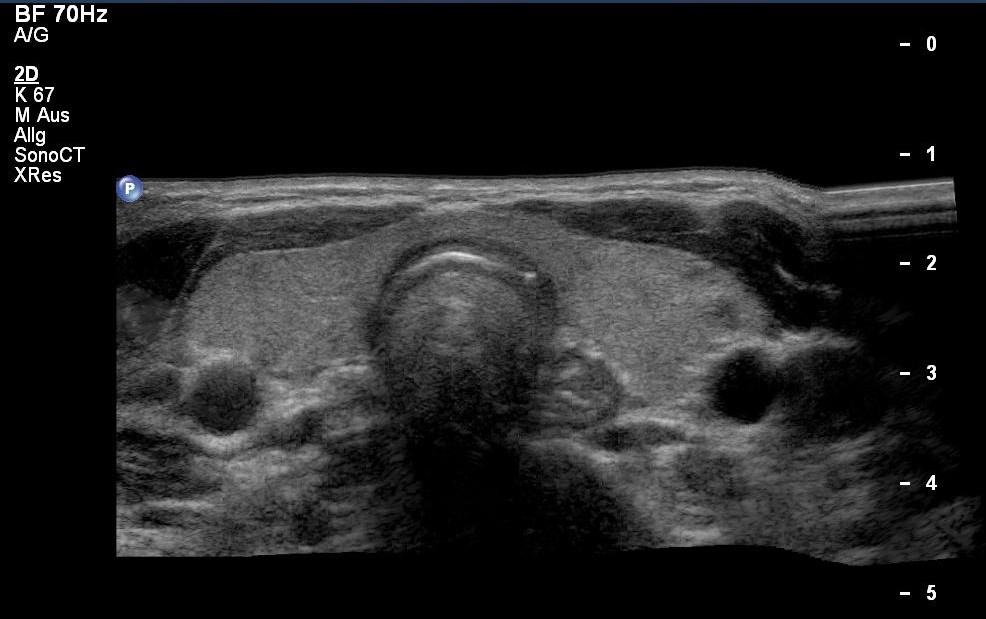
Normalbefund der Schilddrüse mit oberem Ösophagus in der Sonografie (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
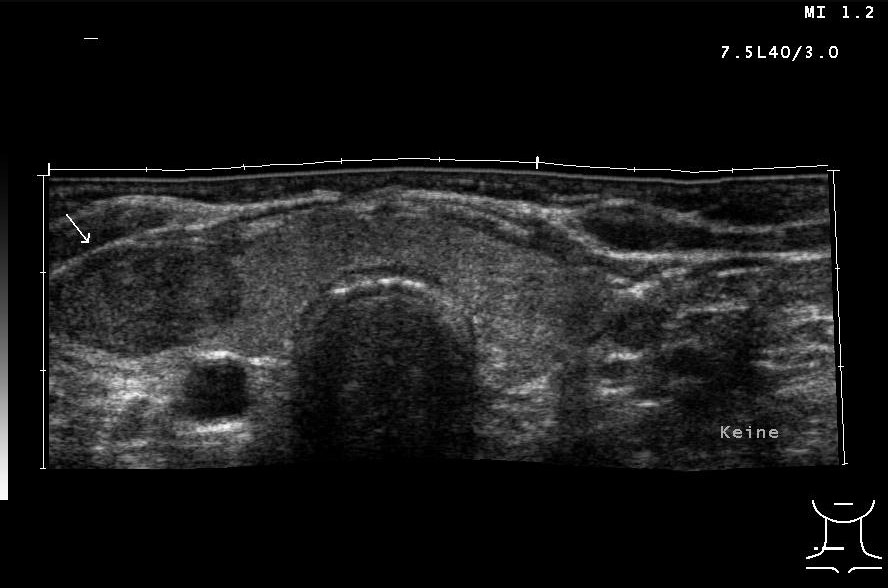
Solider Schilddrüsenknoten rechts in der Sonografie (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
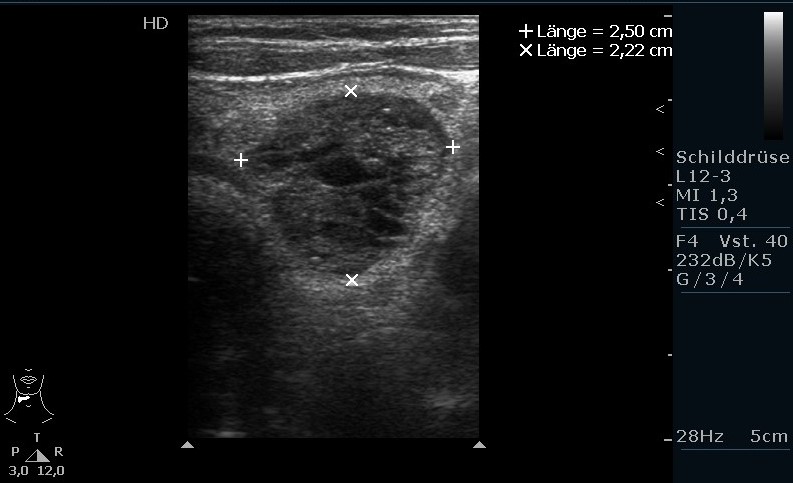
Struma multinodosa in der Sonografie, großer Knoten im linken SD-Lappen (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
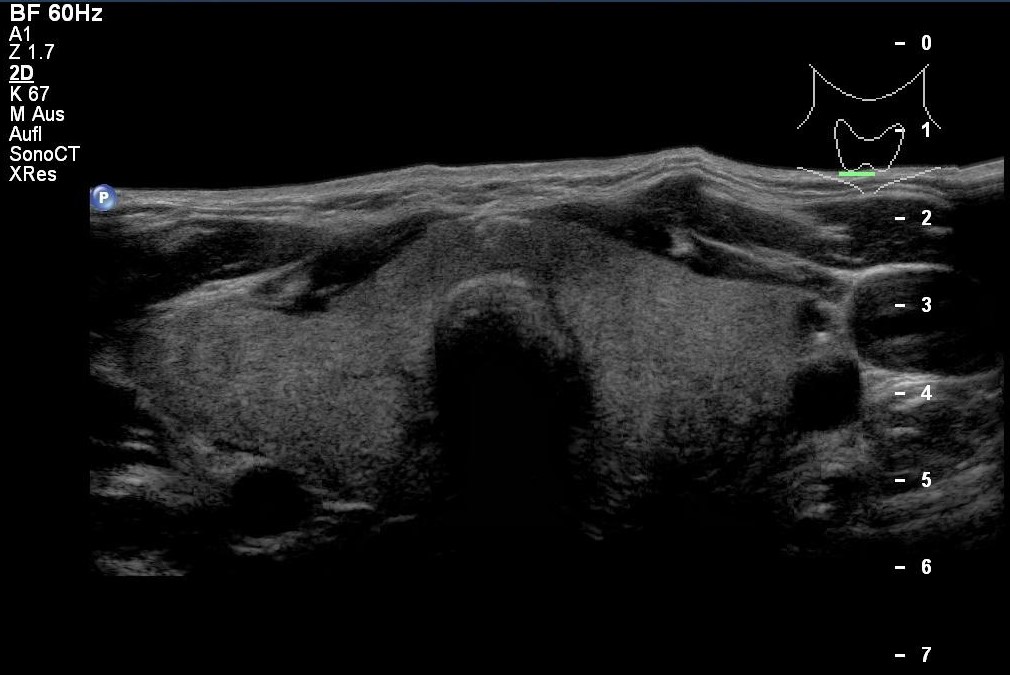
Struma diffusa in der Sonografie (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)

Schilddrüsenkarzinom in der Sonografie: echoarmer Knoten, kein Halo, Mikrokalzifikationen, inhomogen (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
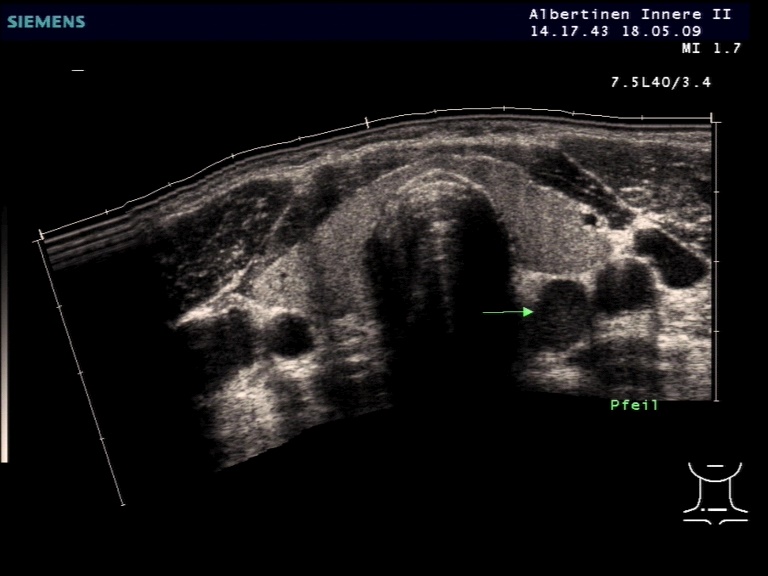
Nebenschilddrüse kaudal des Schilddrüsenlappens (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
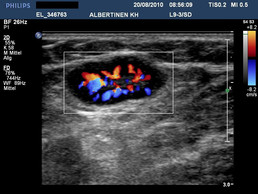
Reaktiver Lymphknoten (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
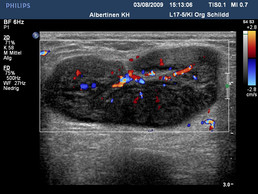
Maligne Lymphknoten (mit freundlicher Genehmigung von sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg)
Quellen
Literatur
- Jarløv AE, Nygaard B, Hegedüs L, Hartling SG, Hansen JM. Observer variation in the clinical and laboratory evaluation of patients with thyroid dysfunction and goiter. Thyroid 1998; 8: 393-8. pubmed.ncbi.nlm.nih.gov
- Hegedüs L. Thyroid ultrasound. Endocrinol Metab Clin North Am 2001; 30: 339-60. pubmed.ncbi.nlm.nih.gov
- Führer D, Bockisch A, Schmid KW: Euthyroid goiter with and without nodules—diagnosis and treatment. Dtsch Arztebl Int 2012; 109(29–30): 506–16. DOI: 10.3238/arztebl.2012.0506. www.aerzteblatt.de
- Papini E et al. Risk of Malignancy in Nonpalpable Thyroid Nodules: Predictive Value of Ultrasound and Color-Doppler Features. The Journal of Clinical Endocrinology & Metabolism, Volume 87, Issue 5, 1 May 2002, Pages 1941–1946, https://doi.org/10.1210/jcem.87.5.8504. academic.oup.com
- Knox MA. Thyroid nodules. Am Fam Physician 2013; 88: 193-6. search.aafp.org
Autorin
- Marlies Karsch-Völk, Dr. med., Fachärztin für Allgemeinmedizin, München