Zusammenfassung
- Definition:Unvollständiger Klappenschluss der Mitralklappe mit systolischem Rückfluss des Blutes in den linken Vorhof. Veränderungen, die zur Insuffizienz der Klappe führen, können den Klappenring, die Segel, die Sehnenfäden oder die Papillarmuskel betreffen. Primäre Mitralinsuffizienzen beruhen auf einer pathologischen Veränderung des Klappenapparates selbst, sekundäre auf einer Erkrankung des linken Ventrikels.
- Häufigkeit:Mitralklappeninsufizienz (nach Aortenklappenstenose) zweithäufigster behandlungsbedürftiger Klappenfehler. Degenerative Veränderungen inzwischen häufigste Ursache.
- Symptome:Leistungsschwäche, belastungsabhängige Atemnot, Palpitationen bei Vorhofflimmern.
- Befunde:Holosystolisches Herzgeräusch über dem Apex mit Ausstrahlung in die Axilla. Pulmonale Stauungszeichen. Im EKG evtl. p-mitrale, Vorhofflimmern. Laborchemisch evtl. BNP-Anstieg bei LV-Dysfunktion.
- Diagnostik:Verdachtsdiagnose durch Anamnese und klinischen Befund. Echokardiografie entscheidendes bildgebendes Verfahren für definitive Diagnosestellung und Schweregradbeurteilung.
- Therapie:Überwiegend operativ, heutzutage meistens Rekonstruktion der Klappe. Behandlung sekundärer Insuffizienzen bei KHK häufig im Rahmen einer koronaren Bypass-OP. Bei hohem Risiko einer Mitralklappen-OP kann im Einzelfall eine Katheterintervention mit Clipping der Mitralsegel eine Option sein.
Allgemeine Informationen
Definition
- Unvollständiger Klappenschluss der Mitralklappe mit systolischem Rückfluss des Blutes in den linken Vorhof
Häufigkeit
- Mitralklappeninsuffizienz (MI) nach der Aortenstenose zweithäufigste behandlungsbedürftige Klappenerkrankung in Europa1
- Prävalenz nach Ätiologie
- degenerative MI mittlerweile am häufigsten, die früher bedeutsame rheumatische Ätiologie ist heutzutage selten
- Prävalenz nach Alter
- Gesamtbevölkerung 0,6–1,7%
- >65-Jährige: 2,8%
- >75-Jährige: >7%
- Prävalenz nach Geschlecht
- Frauen und Männer gleichermaßen betroffen, bei Frauen allerdings öfetr nicht adäquat diagnostiziert und therapiert
Ätiologie und Pathogenese
- Einteilung der Ätiologien in zwei Gruppen: primäre und sekundäre MI
Primäre Mitralklappeninsuffizienz
- Umfasst alle Ätiologien mit intrinsischen Läsionen einer oder mehrerer Komponenten des Mitralapparates2
- Veränderungen können betreffen: 1. den Klappenring 2.die Segel 3. die Sehnenfäden (Aufhängung der Klappensegel) 4. die Papillarmuskel.
- Zahlreiche mögliche Ätiologien für eine primäre MI:
- degenerativ (häufigste Ursache einer primären MI)
- Prolaps3
- M. Barlow (Prolaps beider, myxomatös veränderter Segel)
- Verkalkungen des Klappenapparates
- infektiöse Endokarditis
- Perforation
- rupturierte Chordae
- rheumatisch
- traumatisch
- rupturierte Chordae
- Papillarmuskelabriss
- ischämisch
- rupturierter Papillarmuskel
- entzündlich (nicht-infektiös)
- Lupus erythematodes
- Löffler-Endokarditis (Hypereosinophiles Syndrom)
- kongenital
- Cleft im vorderen Mitralsegel
Sekundäre (funktionelle) Mitralklappeninsuffizienz
- Umfasst Ätiologien mit zugrunde liegender Erkrankung des linken Ventrikels, z.B.
- koronare Herzerkrankung
- Kardiomyopathien
- Die 2 wichtigsten Pathomechanismen der sekundären MI sind:
- Dilatation des Klappenrings und des Halteapparats mit Auseinanderziehen der Segel
- Einschränkung der Beweglichkeit der Klappensegel durch starken Zug auf Sehnenfäden/Papillarmuskeln
- Die Mitralklappensegel und -chordae selbst sind bei der sekundären MI primär meist strukturell intakt
Weitere Klassifikationen
- Neben der Einteilung in primäre und sekundäre Mitralklappeninsuffizienzen sind weitere Klassifikationen üblich:
- akut vs. chronisch
- ischämisch vs. nicht-ischämisch
- funktionelle Einteilung auf der Basis der Klappensegelbewegung (Carpentier-Klassifikation)4
- Carpentier I: normale Segelbeweglichkeit (z. B. bei Segelperforation)
- Carpentier II: erhöhte Segelbewglichkeit (z. B. bei Prolaps)
- Carpentier III: verminderte Segelbeweglichkeit (z. B. Retraktion nach Infarkt)
Pathophysiologie
- Systolischer Rückstrom vom linken Ventrikel in linken Vorhof
- Ausmaß des Rückstroms (Regurgitationsvolumen) abhängig von:
- effektiver Öffnungsfläche des Lecks
- systolischem Druck im Ventrikel
- Compliance des linken Vorhofs.
- Volumenüberlastung und dadurch Dilatation von linkem Vorhof und linkem Ventrikel
- im weiteren Verlauf linksventrikuläre Insuffizienz
- gehäuftes Auftreten von Vorhofflimmern durch linksatriale Belastung/Dilatation
- Vorhofflimmern nicht selten erstes klinisches Zeichen
- Erhöhung des pulmonalvenösen Drucks
- Lungenstauung/Lungenödem
- Entwicklung einer pulmonalen Hypertonie
- im weiteren Verlauf mit Rechtsherzinsuffizenz
Prädisponierende Faktoren
- Höheres Alter
- Koronare Herzerkrankung
- Kardiomyopathien
- Arterielle Hypertonie
- St. n. rheumatischem Fieber
- Fluorchinolone können das Risiko für Herzklappeninsuffizienzen erhöhen, vermutlich durch Kollagenabbau (Rote-Hand-Brief)
- Einsatz nur nach sorgfältiger Nutzen-Risiko-Abwägung insbesondere bei Patient*innen mit weiteren prädisponierenden Faktoren
ICPC-2
- K83 Herzklappenerkrankung
- K71 Rheumatisches Fieber/Herzerkrankung
ICD-10
- I05 Rheumatische Mitralklappenkrankheiten
- I05.1 Rheumatische Mitralklappeninsuffizienz
- I05.2 Mitralklappenstenose mit Insuffizienz
- I05.8 Sonstige Mitralklappenkrankheiten
- I05.9 Mitralklappenkrankheit, nicht näher bezeichnet
- I34 Nichtrheumatische Mitralklappenkrankheiten
- I34.0 Mitralklappeninsuffizienz
- I34.1 Mitralklappenprolaps
- I34.8 Sonstige nichtrheumatische Mitralklappenkrankheiten
- I34.9 Nichtrheumatische Mitralklappenkrankheit, nicht näher bezeichnet
Diagnostik
Diagnostische Kriterien
- Diagnose beruht auf:
- Symptomatik
- klinischem Befund
- Bildgebung (Echokardiografie).
Differenzialdiagnosen
Systolische Herzgeräusche
- Aortenklappenstenose
- Ventrikelseptumdefekt
- Trikuspidalklappeninsuffizienz
- Hypertrophe Kardiomyopathie
Anamnese
Akute Mitralklappeninsuffizienz
- Dramatisches Krankheitsbild, z. B. bei Papillarmuskelabriss
- Rasche Entwicklung eines kardiogenen Schocks mit Lungenödem und Low-Output
- Mechanische Kreislaufunterstützung und rasche operative Versorgung erforderlich
Chronische Mitralklappeninsuffizienz
- Patient*innen mit chronisch schwerer MI werden meist innerhalb von vier bis sechs Jahren symptomatisch
- Über einen längeren Zeitraum allmählich zunehmende Symptome
- Belastungs-Dyspnoe
- Leistungsschwäche
- Müdigkeit, Abgeschlagenheit
- Palpitationen (v. a. bei Vorhofflimmern)
- Symptomatik der chronischen MI entspricht somit weitgehend der Symptomatik der chronischen Herzinsuffizienz.
Klinische Untersuchung
- Nach lateral verlagerter, hebender Herzspitzenstoß
- Auskultation Herz (siehe auch Herzgeräusche bei Erwachsenen)
- bandförmiges Holosystlikum
- Punctum maximum Mitralpunkt
- Fortleitung in Axilla
- Lautstärke korreliert nicht mit Schwergrad!
- 3. Herzton
- bandförmiges Holosystlikum
- Evtl. unregelmäßige Herzaktion (bei Vorhofflimmern)
Auskultationsbefund Mitralinsuffizienz:
- Auskultation Lunge: Lungenstauung/Lungenödem
- Im späteren Verlauf bei Rechtsherzinsuffizienz:
- Halsvenenstauung
- peripere Ödeme
- Hepatomegalie.
Ergänzende Untersuchungen in der Hausarztpraxis
EKG
- Wenig spezifisch
- P-mitrale
- Unspezifische Erregungsrückbildungsstörungen (siehe auch EKG: Veränderungen von P-Welle, QRS-Komplex und ST-T-Segment)
- Evtl. Vorhofflimmern
Rö-Thorax
- Dilatation von linkem Vorhof und linkem Ventrikel
- Lungenstauung
Labor
- Erhöhung von BNP, NT-proBNP (bei Herzinsuffizienz)
Diagnostik bei Spezialist*innen
Echokardiografie
- Echokardiografie ist das mit Abstand wichtigste Bildgebungsverfahren
- Die echokardiografische Untersuchung bei Mitralinsuffizienz umfasst u.a. Beurteilung von:2
- Schweregrad
- Mechanismus (primär vs sekundär)
- Eignung für klappenerhaltende OP.
- Anwendung verschiedener echokardiografische Techniken :5-6
- Transthorakale Echokardiografie (TTE)
- 2D-Echokardiografie
- Größe von Ventrikeln und Vorhöfen
- Pumpfunktion der Ventrikel
- morphologische Beurteilung des Mitralklappenapparates
- Beurteilung der Klappenbeweglichkeit (Basis für die funktionelle Carpentier-Klassifikation)
- Messung des Diameters des Mitralklappenrings
- Doppler- und Farbdopplerechokardiografie
- Darstellung und semiquantitative Beurteilung des Regurgitationsjets
- Bestimmung der effektiven Regurgitationsfläche (wichtigster Parameter bei der Bestimmung des Schweregrades)
- Bestimmung des Regurgitationsvolumens
- 2D-Echokardiografie
- Transösophageale Echokardiografie (TEE)
- bei nicht ausreichender Aussagekraft der transthorakalen Untersuchung
- aufgrund der besseren Schallbedingungen bessere Beurteilung von Klappenpathologie und Insuffizienzmechanismus
- wichtig bei der Planung von chirurgischen und katheterinterventionellen Eingriffen
- 3D-Echokardiorafie
- bei der Mitralklappe v. a. 3D-TEE von Bedeutung
- räumliche Darstellung von Klappenmorphologie und -funktion, des MI-Mechanismus (z.B. bei Mitralklappenprolaps), des Regurgitationsjets
- Rekonstruktion des chirurgischen Blicks auf die Klappe
- Stressechokardiografie
- Beurteilung belastungsinduzierter Änderungen von:
- Schweregrad der MI
- linksventrikulärer Funktion
- pulmonal-arteriellem Druck.
- Beurteilung belastungsinduzierter Änderungen von:
Magnetresonanztomografie (MRT)
- Kein Routineverfahren in der Diagnostik von Mitralklappeninsuffizienzen
- Ergänzende Methode zur Beurteilung einer MI bei eingeschränkter echokardiographischer Bildqualität oder bei Befunddiskrepanz
- Viabilitätsbeurteilung des Myokards bei begleitender KHK und geplanter OP
Herzkatheteruntersuchung
- Für die Diagnostik der MI heute von untergeordneter Bedeutung
- Semiquantitative Darstellung der MI durch Kontrastmittelrückfluss in linken Vorhof
- Beurteilung von Größe und Funktion des linken Ventrikels
- Wichtig vor allem für die präoperative Koronardiagnostik
Indikation zur Überweisung
- Bei V. a. klinisch relevante Mitralklappeninsuffizienz
Therapie
Therapieziele
- Verbesserung der Prognose
- Verbesserung der Leistungsfähigkeit
- Symptomlinderung
Allgemeines zur Therapie
- Verschiedene Optionen für Eingriffe an der Mitralklappe:
Operative Verfahren
Klappenrekonstruktion/-ersatz
- Bei einer akut eintretenden schweren MI (z.B. bei Papillarmuskelabriss) besteht grundsätzlich eine OP-Indikation
- Paradigmenwechsel in der operativen Versorgung: während früher die Klappe vorwiegend ersetzt wurde, ist heutzutage die Klappenrekonstruktion vor allem bei der primären MI Mittel der Wahl2
- Isolierte Eingriffe an der Mitralklappe auch minimalinvasiv durchführbar,
Katheterinterventionelle Verfahren
TEER (Transcatheter Edge-to-Edge-Repair)
- Kathetergestütze Verfahren, bei denen - analog der früher verwendeten chirurgischen Alfieri-Naht - eine Verbindung zwischen anteriorem und posteriorem Segel geschaffen wird (dadruch Entstehung einer doppelten Öffnungsfläche)
- Durch technische Weiterentwicklungen konnten Wirksamkeit und Sicherheit in den vergangenen Jahren verbessert werden
Interventioneller Mitralklappenersatz
- Ein noch neues Vefahren ist der interventionelle Mitralklappenersatz, Option aktuell nur bei Patient*innen, die für eine Operation oder einen TEER nicht gut geeignet sind
Spezielle Therapie der primären und sekundären Mitralklappeninsuffizienz
Therapie der primären Mitralklappeninsuffizienz
Medikamentöse Therapie
- Bei chronischer primärer MI mit LV-Dysfunktion leitliniengerechte medikamentöse Herzinsuffizienztherapie2
- Bei erhaltener LV-Funktion gibt es keine Evidenz für den Nutzen einer nachlastsenkenden Behandlung2
Operative/interventionelle Therapie
- Rekonstruktion der Mitralklappe ist Goldstandard für Patient*innen mit primärer hochgradiger Mitralklappeninsuffizienz
- Operiert werden sollten symptomatische Patient*innen mit hochgradiger MI, aber auch asymptomatische Patient*innen mit echokardiografischer LV-Dysfunktion2
OP bzw. Intervention bei primärer MI
- Mitralklappenrekonstruktion sollte die bevorzugte OP-Technik sein, wenn ein dauerhaft gutes Ergebnis zu erwarten ist. (I/B)
- OP empfohlen bei symptomatischen Patient*innen, die operabel sind und kein hohes Risiko aufweisen. (I/B)
- OP empfohlen bei asymptomatischen Patient*innen mit LV-Dysfunktion (LVESD ≥ 40 mm und/oder LVEF ≤ 60 %). (I/B)
- OP sollte erwogen werden bei asymptomatischen Patient*innen mit erhaltener LV- Funktion (LVESD <40 mm and LVEF >60%) und MI-bedingtem Vorhofflimmern oder pulmonaler Hypertonie (systolischer Pulmonalarteriendruck in Ruhe > 50 mmHg). (IIa/B)
- Katheterintervention kann erwogen werden bei symptomatischen Patient*innen, die die notwendigen echokardiografischen Kriterien erfüllen und als inoperabel bzw. als Hochrisikopatient*innen durch das Herzteam beurteilt werden. (IIb/B)
Therapie der sekundären Mitralklappeninsuffizienz
Medikamentöse Therapie
- Erster und wichtigster Behandlungsschritt bei der sekundären MI ist eine optimale medikamentöse Herzinsuffizienztherapie, evtl. ergänzt durch eine kardiale Resynchronisationstherapie (CRT)7,8
- Wenn trotz optimaler Therapie die Symptome anhalten, sollten die Optionen für eine operative oder katheterinterventionelle Therapie evaluiert werden2
Operative/interventionelle Therapie
- Bei sekundärer MI ist der Vorteil der Rekonstruktion gegenüber dem Ersatz weniger deutlich als bei primärer MI
- In den vergangenen Jahren aber Fortschritte bei den Rekonstruktionstechniken von Klappe und klappenhaltendem Apparat,
- Bisherige Studien zur kathetergestützten TEER (Transcatheter Edge-to-Edge-Repair) haben widersprüchliche Ergebnisse gezeigt9-11
- Weitere Studien sind daher notwendig, um die Patient*innen zu identifizieren, die am meisten von dieser Technik profitieren2
OP bzw. Intervention bei sekundärer MI
Allgemeine Empfehlung
- Operation/Intervention nur empfohlen für Patient*innen mit schwerer MI, die trotz leitliniengerechter medikamentöser Behandlung (plus ggf. CRT) symptomatisch bleiben, Entscheidung durch Herz Team. (I/B)
Patient*innen mit KHK oder anderer behandlungsbedürftiger Herzerkrankungen
- Klappenchirurgie empfohlen bei Patient*innen mit Indikation zur koronaren Bypass-Operation oder anderer Herzchirurgie. (I/B)
- Bei symptomatischen Patient*innen, die nicht für eine Operation geeignet sind, sollte eine PCI (und/oder TAVI) mit anschliessender kathetergestützter Mitralklappenintervention (bei anhaltend schwerer MI) erwogen werden. (IIa/C)
Patient*innen ohne KHK oder andere behandlungsbedürftige Herzerkrankung
- Eine kathetergestütze Mitralklappenintervention sollte bei ausgewählten symptomatischen Patient*innen erwogen werden, die nicht zur Operation geeignet sind und die Kriterien für einen potentiel erfolgreichen Eingriff erfüllen. (IIb/C)
- Klappenchirurgie kann bei symptomatischen Patient*innen erwogen werden, die durch das Herz Team als für eine Operation geeignet beurteilt werden. (IIb/C).
Weitere Maßnahmen nach OP
Orale Antikoagulation
- Eine Antikoagulation mit Vit-K-Antagonist ist indiziert2
- dauerhaft nach Implantation einer mechanischen Prothese (INR 3–3,5)2
- 3 Monate nach Implantation einer Bioprothese oder nach Klappenrekonstruktion
Endokarditis-Prophylaxe
- Antibiotische Prophylaxe empfohlen bei Patient*innen mit12
- Klappenprothesen
- Klappenrekonstruktion unter Verwendung von prothetischem Material
Verlauf, Komplikationen und Prognose
Komplikationen
- Rezidiv der Mitralklappeninsuffizienz
- Progrediente Herzinsuffizienz
- Vorhofflimmern
- Embolische Ereignisse
- Infektiöse Endokarditis
Verlauf und Prognose
- Zum natürlichen Verlauf vs. OP/Intervention gibt es nur wenige wenige Daten
- Bei hochgradiger MI kardiale Ereignisrate von ca. 10 %/Jahr
- kardialer Tod
- Herzinsuffizienz
- Vorhofflimmern
- Prognostische Faktoren
- Alter
- Komorbiditäten
- klinische Symptomatik
- Schweregrad der MI
- bereits durchgeführte Behandlung
- Größe und Funktion des linken Ventrikels
- LA-Diameter > 40–50 mm
- pulmonale Hypertonie
- Vorhofflimmern
- erhöhte Herzinsuffizienz-Marker (BNP)
- Bei sekundärer MI perioperatives Risiko höher und Langzeitprognose schlechter als bei primärer MI
Verlaufskontrolle
- Regelmäßige klinische und echokardiografische Verlaufskontrollen
- Erste ambulante Echokardiografie ca. 3 Monate nach OP
- Im weiteren Verlauf einmal jährlich oder bei neuem klinischem Hinweis für Rezidiv
- INR-Kontrollen bei antikoagulierten Patient*innen
Patienteninformationen
Patienteninformationen in Deximed
Weitere Informationen
- Siehe Artikel Beurteilung der Fahreignung.
Illustrationen
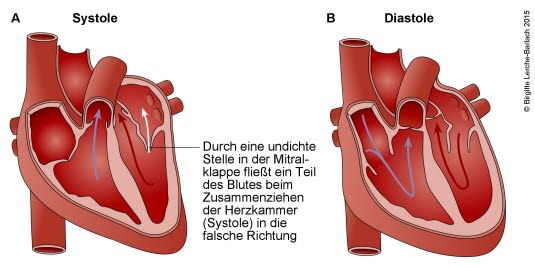
Mitralinsuffizienz
Geräusche
Mitralinsuffizienz:
Vorhofflimmern:
Quellen
Leitlinien
- European Society of Cardiology. Guidelines for the management of valvular heart disease. Stand 2021. www.escardio.org
- European Society of Cardiology. Guidelines for the diagnosis and treatment of acute and chronic heart failure. Stand 2021. www.escardio.org
- American Society of Echocardiography. Recommendations for Noninvasive Evaluation of Native Valvular Regurgitation. Stand 2017. www.asecho.org
- American Society of Echocardiography and Society of Cardiovascular Anesthesiologists. Guidelines for Performing a Comprehensive Transesophageal Echocardiographic Examination. Stand 2013. www.asecho.org
Literatur
- Iunga B, Baron G, b, Butchart E. A prospective survey of patients with valvular heart disease in Europe: The Euro Heart Survey on Valvular Heart Disease. Eur Heart J 2003; 24: 1231–1243. www.ncbi.nlm.nih.gov
- Vahanian A, Beyersdorf F, Praz F, et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J 2022; 43: 561-632. doi:10.1093/eurheartj/ehab395 DOI
- Hayek E, Gring CN, Griffin BP. Mitral valve prolapse. Lancet 2005; 365: 507-18. PubMed
- Pedrazzini G, Faletra F, Vassalli G. Mitral regurgitation. Swiss Med Wkly 2010; 140: 36-43. smw.ch
- Hahn R, MD, Abraham T, Adams M, et al. Guidelines for Performing a Comprehensive Transesophageal Echocardiographic Examination: Recommendations from the American Society of Echocardiography and the Society of Cardiovascular Anesthesiologists. J Am Soc Echocardiogr 2013; 26: 921-64. doi:10.1016/j.echo.2013.07.009 DOI
- Zoghbi W, Adams D, Bonow R, et al. Recommendations for Noninvasive Evaluation of Native Valvular Regurgitation. J Am Soc Echocardiogr 2017; 30: 303-371. doi:10.1016/j.echo.2017.01.007 DOI
- McDonagh T, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2021; 42: 3599-3726. doi:10.1093/eurheartj/ehab368 DOI
- Glikson M, Nielsen J, Kronborg M, et al. 2021 ESC Guidelines on cardiac pacing and cardiac resynchronization therapy. Eur Heart J 2021;00: 1-94. doi:10.1093/eurheartj/ehab364 DOI
- Obadia J, Messika-Zeitoun D, Leurent G, et al. Percutaneous Repair or Medical Treatment for Secondary Mitral Regurgitation. N Engl J Med 2018; 379: 2297-2306. doi:10.1056/NEJMoa1805374 DOI
- Stone G, Lindenfeld J, Abraham W, et al. Transcatheter Mitral-Valve Repair in Patients with Heart Failure. N Engl J Med 2018; 379: 2307-2318. doi:10.1056/NEJMoa1806640 DOI
- von Bardeleben R, Hobohm L, Kreidel F, et al. Incidence and in-hospital safety outcomes of patients undergoing percutaneous mitral valve edge-to-edge repair using MitraClip: five-year German national patient sample including 13,575 implants. Eurointervention 2019; 14: 1725-1732. doi:10.4244/EIJ-D-18-00961 DOI
- Habib G, Lancellotti P, Antunes M, et al. 2015 ESC Guidelines for the management of infective endocarditis. Eur Heart J 2015; 36: 3075–3123. doi:10.1093/eurheartj/ehv319 DOI
Autor*innen
- Michael Handke, Prof. Dr. med., Facharzt für Innere Medizin, Kardiologie und Intensivmedizin, Freiburg i. Br.
- Thomas M. Heim, Dr. med., Wissenschaftsjournalist, Freiburg