Zusammenfassung
- Definition:Eine bakterielle Meningitis bzw. Meningoenzephalitis ist eine schwerwiegende Infektion der Hirnhäute (Meningen) und des Hirngewebes (Enzephalon).
- Häufigkeit:Hohe regionale Variabilität. 1–3 Fälle pro 100.000 Einw. pro Jahr in Europa.
- Symptome:Klassische Symptome umfassen hohes Fieber, Kopfschmerzen, Übelkeit und Erbrechen und Meningismus; ggf. Bewusstseinsstörung, Verwirrtheit, epileptische Anfälle, Hirnnervenausfälle.
- Befunde:Meningismus, Fieber, reduzierter Allgemeinzustand, Vigilanzminderung, Hirnnervenausfälle, Sepsis, Schock, petechiales Hautexanthem als Hinweis auf Meningokokken.
- Diagnostik:Lumbalpunktion und Liquordiagnostik, Blutkulturen, Routinelabor, zytologischer oder kultureller Erregernachweis, zerebrale Bildgebung (CT/MRT), ggf. weitere Diagnostik.
- Therapie:Stationäre, ggf. intensivmedizinische Therapie. Frühzeitige, initial empirische Antibiotikatherapie entscheidend. Supportive Maßnahmen und Behandlung von Komplikationen. Erkrankung abhängig vom Erreger impfpräventabel.
Allgemeine Informationen
Definition
- Die bakterielle Meningitis bzw. Meningoenzephalitis ist eine akute, eitrige Entzündung der Hirnhäute (Meningen) sowie ggf. des Hirngewebes (Enzephalitis).1
- schwerwiegende Erkrankung mit hoher Letalität (15–20 %)
- Die häufigsten bakteriellen Erreger bei Erwachsenen sind Pneumokokken, Meningokokken und Listerien.
- effektive Impfungen gegen Pneumokokken und Meningokokken
- Klinische Leitsymptome sind Kopfschmerzen, Meningismus und Fieber.
- oft schwer beeinträchtigter Allgemeinzustand und Sepsis
- Notfalldiagnostik mit klinisch-neurologischer Untersuchung, Liquor- und Erregerdiagnostik sowie zerebraler Bildgebung
- Eine frühzeitige, ggf. empirische, antibiotische Therapie ist entscheidend für den Therapieerfolg.
Häufigkeit
- Eine bakterielle Meningitis ist seltener als virale Meningitiden.
- Hohe Variabilität der globalen Inzidenz nach Erreger und Region
- Inzidenz in Europa etwa 1–3/100.000 pro Jahr
- in Industrienationen fallende Inzidenz
- Inzidenz der invasiven Meningokokken-Infektionen in Europa 0,5–5/100.000 pro Jahr
- Meningitis durch Listerien
- jährliche Inzidenz ca. 0,5 Fälle pro 1 Mio. Einw.
- Meningitis durch Haemophilus influenzae:
- ca. 1–3 % aller bakteriellen Meningitiden
- Durch Einführung der Impfung ist die Häufigkeit der Erkrankung um mehr als 99 % gesunken.
Ätiologie und Pathogenese
Infektionswege
- Hämatogen
- vermutlich Haupteintrittspforte
- mehrstufiger Prozess mit Kolonisation (v. a. Respirationstrakt), Invasion und Replikation in der Blutbahn und Übertreten der Blut-Hirn-Schranke
- z. B. bei Pneumokokken-Pneumonie
- Direkt (per continuitatem)
- bei Sinusitis, Otitis, Mastoiditis
- seltener bei Liquorfisteln, z. B. nach Schädel-Hirn-Trauma
Erreger
- Streptococcus pneumoniae (Pneumokokken)
- Der Übertragungsweg ist am häufigsten eine von kolonisierten Schleimhäuten des Nasopharynx ausgehende Invasion der Blutbahnen und des ZNS.
- Eine interkurrente oder kürzlich aufgetretene Pharyngitis, Bronchitis oder Pneumonie kann die Schleimhaut anfällig machen.
- Eine rezeptorvermittelte Endozytose ermöglicht die Passage durch Epithelzellen und die Blut-Hirn-Schranke.
- Es kann zu einer direkten Invasion des ZNS über eine Sinusitis oder Otitis media kommen.
- Eine direkte Inokulation kann bei einem neurochirurgischen Eingriff, durch Traumata oder ein Liquorleck geschehen.
- Auch eine septische Embolisation von Mikroben von einem anderen Infektionsfokus (Endokarditis) aus ins ZNS kommt vor.
- Der Übertragungsweg ist am häufigsten eine von kolonisierten Schleimhäuten des Nasopharynx ausgehende Invasion der Blutbahnen und des ZNS.
- Neisseria meningitidis (Meningokokken)
- Die Übertragung erfolgt am häufigsten durch eine Invasion der Blutbahnen und des ZNS von kolonisierten Schleimhäuten des Nasopharynx aus.
- Haemophilus influenzae Typ B (Hib)
- Die Übertragung erfolgt am häufigsten durch eine Invasion der Blutbahnen und des ZNS von kolonisierten oder infizierten Schleimhäuten des Pharynx aus.
- Vor Einführung des Impfstoffes verursachte Haemophilus influenzae schwere Infektionen wie Epiglottitis, Meningitis, Pneumonie und Sepsis.
- Listeria monocytogenes
- Der genaue Übertragungsweg ist bisher noch unklar.
- atypische Manifestation als Hirnstammenzephalitis mit Hirnstammsyndrom und hoher Mortalität beschrieben
- Staphylokokken
- Die Übertragung erfolgt am häufigsten durch eine Bakteriämie, aber auch die direkte Inokulation im Falle von Traumata, Fremdkörpern und bei Eingriffen ist möglich.
- Sowohl Staph. aureus als auch andere Staphylokokken können sich sehr effektiv an der Oberfläche von Fremdkörpern festsetzen.
- Streptococcus agalactiae (beta-hämolysierende Streptokokken der Gruppe B)
- Am häufigsten sind Neugeborene einige Tage nach der Geburt betroffen. Die Übertragung erfolgt am häufigsten durch kolonisierte Schleimhäute im Urogenitalsystem der Mutter.
- Bis zu 30 % der Neugeborenen mit manifester bakterieller Meningitis weisen Zeichen einer gleichzeitigen Infektion der oberen Atemwege auf.
- Siehe Artikel B-Streptokokken in der Schwangerschaft.
- Gramnegative Stäbchenbakterien
- U. a. E. coli zählt ebenfalls zu den häufigeren Erregern der Neugeborenenmeningitis.
Häufigste Erreger nach Altersgruppe
- Neugeborene und Säuglinge < 6 Wochen
- beta-hämolysierende Streptokokken der Gruppe B: 50–60 %
- Enterobacteriaceae (z. B. E. coli, Klebsiella, Enterobacter, Proteus)
- Listeria monocytogenes: 0–3,5 %
- Säuglinge > 6 Wochen und Kinder
- Neisseria meningitidis (Meningokokken): 38–56 %
- Streptococcus pneumoniae (Pneumokokken): 34–46 %
- Haemophilus influenzae (bei nicht geimpften Kindern): 2–12 %
- Erwachsene
- Streptococcus pneumoniae (Pneumokokken): 37–59 %
- Neisseria meningitidis (Meningokokken): 24–43 %
- Listeria monocytogenes: 0,8–10 %
Prädisponierende Faktoren
- Risikofaktoren für eine bakterielle Meningitis
- Vorerkrankungen
- Alkoholabhängigkeit
- Operationen im Schädel-/HNO-/Kieferbereich
- Immunsuppression bzw. Immundefekt (z. B. Neutropenie, AIDS)
- Diabetes mellitus
- dentale Infektionen und Läsionen der Mundhöhle
- Endokarditis
- Sinusitis
- Otitis media
- Parotitis
- offenes Schädel-Hirn-Trauma
- erhöhte Trägerfrequenz von pathogenen Keimen im Pharynx
- Aufenthalt in Institutionen (Schule, Pflegeeinrichtungen usw.)
- Aufenthalt in Regionen mit endemischem Meningokokken-Vorkommen (Meningokokkengürtel)
- Kontakt mit einem Indexfall mit bakterieller Meningitis
- Rauchen
- Veränderung der Schleimhaut im Respirationstrakt
- erhöhtes Risiko für eine Bakteriämie
- Drogenmissbrauch mit Injektionen
- Vorerkrankungen
ICD-10
- Nach ICD-10-GM Version 2022
- G00: Bakterielle Meningitis, anderenorts nicht klassifiziert
- G00.0 Meningitis durch Haemophilus influenzae
- G00.1 Pneumokokkenmeningitis
- G00.2 Streptokokkenmeningitis
- G00.3 Staphylokokkenmeningitis
- G00.8 Sonstige bakterielle Meningitis
- G00.9 Bakterielle Meningitis, nicht näher bezeichnet
- G01: Meningitis bei andernorts klassifizierten bakteriellen Krankheiten. Meningitis (bei) (durch):
- Anthrax [Milzbrand] (A22.8+)
- Gonokokken (A54.8+)
- Leptospirose (A27.-+)
- Listerien (A32.1+)
- Lyme-Krankheit (A69.2+)
- Meningokokken (A39.0+)
- Neurosyphilis (A52.1+)
- Salmonelleninfektion (A02.2+)
- Syphilis, konnatal (A50.4+)
- Syphilis, sekundär (A51.4+)
- tuberkulös (A17.0+)
- Typhus abdominalis (A01.0+)
- G03.9 Meningitis, nicht näher bezeichnet
- G00: Bakterielle Meningitis, anderenorts nicht klassifiziert
Diagnostik
Diagnostische Kriterien
- Die bakterielle Meningitis ist ein medizinischer Notfall.
- schnelle Diagnostik und Therapieeinleitung erforderlich
- Klinische Symptomatik einer Meningitis bzw. Enzephalitis
- Entzündliche Veränderungen im Liquor
- granulozytäre Liquorpleozytose, Laktaterhöhung und Glukoseverminderung
- Diagnosesicherung durch Erregernachweis im Liquor oder Blut
Differenzialdiagnosen
- Bei Kopfschmerzen und Fieber
- Bei Kopfschmerzen und Meningismus
Anamnese
- Akuter Beginn und rasch progrediente Symptomatik
- meist < 24 Stunden zwischen Symptombeginn und Krankenhauseinweisung
- Hauptsymptome
- deutlich beeinträchtigter Allgemeinzustand
- Kopfschmerzen
- (hohes) Fieber
- Nackensteife (Meningismus)
- Übelkeit und Erbrechen
- Lichtscheu (Photophobie)
- Verwirrtheit
- Bewusstseinsstörung (Vigilanzminderung)
- Weitere Symptome
- epileptische Anfälle
- Hautveränderungen (petechiales Exanthem bei Meningokokken)
- Hirnnervenbeteiligung, z. B. Fazialisparese (ca. 10 %)
- fokal-neurologische Defizite, z. B. Sprach- und Sprechstörungen
- Hörminderung/-verlust, a. e. durch eitrige Labyrinthitis (10–20 %)
- Sepsis (v. a. bei Meningokokken)
- Atypische Präsentation ohne oder mit nur geringen Leitsymptomen insbesondere bei älteren Patient*innen
- Bei Neugeborenen und Säuglingen ebenfalls unspezifische Beschwerden wie Fieber, Hypothermie, Müdigkeit, Trinkschwäche, Erbrechen, Diarrhö, Krampfanfälle
Klinische Untersuchung
- Die klinischen Befunde sollten schnell erhoben werden, ohne unnötig Zeit zu verlieren.
- Vitalparameter (Herzfrequenz, Blutdruck, Temperatur, Atemfrequenz)
- Allgemeine körperliche Untersuchung
- Auskultation von Herz und Lunge
- Hautveränderungen
- makulopapulöses Exanthem, Petechien, Ekchymosen, Purpura, Hautnekrosen (v. a. bei Meningokokken, auch bei Streptokokken, Pneumokokken, Listerien, Hib)
- bei Meningokokken-Meningitis oft Herpes labialis (ausgedehnt)
- Racheninspektion (Pharyngitis, Tonsillitis)
- Otoskopie (eitriger Ausfluss? Otitis media?)
- Druckschmerz/Schwellung retroaurikulär (Mastoiditis)
- Neurologische Untersuchung
- Vigilanzminderung (Glasgow Coma Scale)
- Orientierung (Zeit, Ort, Person, Situation)
- Meningismus (schmerzhafte Nackensteifigkeit bei passiver Kopfneigung)
- weitere meningeale Reizzeichen
- Hirnnervenausfälle (v. a. III., VI., VII. und VIII. Hirnnerv)
- III, VI: Schielen und Doppelbilder
- VII: Fazialisparese
- VIII: Hörminderung/-verlust oder Schwindel
- Sprach- oder Sprechstörungen
- motorische oder sensible Defizite
- Möglichst frühzeitig HNO-ärztliche Untersuchung
- parameningealer Fokus, z. B. Mastoiditis, Sinusitis oder Otitis media
Ergänzende Untersuchungen im Krankenhaus
Vorgehen der Notfalldiagnostik und -therapie
- Bei bakterieller Meningitis Vorgehen abhängig vom klinischen Zustand
- Patient*innen ohne Bewusstseinsstörung bzw. fokal-neurologischem Defizit
- Lumbalpunktion und Liquordiagnostik (Kontraindikationen s. unten) sowie Blutkulturen
- frühe empirische Antibiotikatherapie und Glukokortikoide
- zerebrale Bildgebung
- Patient*innen mit Bewusstseinsstörung bzw. fokal-neurologischem Defizit
- Blutkulturen
- frühe empirische Antibiotikatherapie und Glukokortikoide
- zerebrale Bildgebung
- Lumbalpunktion und Liquordiagnostik (Kontraindikationen s. u.)
- Kontraindikationen für eine Lumbalpunktion
- erhöhter Hirndruck
- Blutungsneigung (z. B. Thrombozyten < 50.000/µl, INR > 1,8)
- Infektion im Verlauf des Punktionswegs
- Schwangerschaft
- Bildgebende Diagnostik
- Empfehlung zur zerebralen Bildgebung innerhalb von 24 Stunden nach Krankenhausaufnahme (CT oder MRT)
- oft notfallmäßige CT-Bildgebung, ggf. MRT im Verlauf
- Nachweis intrakranieller Komplikationen der Meningoenzephalitis
- z. B. Zeichen eines erhöhten intrakraniellen Drucks
- Hinweise auf einen entzündlichen Fokus oder eine Eintrittspforte
- Empfehlung zur zerebralen Bildgebung innerhalb von 24 Stunden nach Krankenhausaufnahme (CT oder MRT)
Indikationen zur Klinikeinweisung
- Bei Verdacht auf eine Meningitis oder Enzephalitis unverzügliche Krankenhauseinweisung
Therapie
Therapieziele
- Eine frühzeitige Therapie ist entscheidend für die Prognose.
- Letalen Verlauf verhindern.
- Infektion sanieren.
- Komplikationen (z. B. Sepsis) und Folgeschäden (z. B. Hörverlust) verhindern.
Allgemeines zur Therapie
- Präklinische Stabilisierung der Vitalparameter
- Patient*innen mit bakterieller Meningitis sollen in der Initialphase auf einer Intensivstation behandelt werden.
- erste Woche der Erkrankung als kritische Phase
- Komplikationen in etwa der Hälfte der Fälle
- Zur supportiven Therapie siehe auch Sepsisbehandlung.
Medikamentöse Therapie
- Frühzeitiger Therapiebeginn (unmittelbar nach Lumbalpunktion bzw. Blutkulturen),
- Bei Verdacht auf eine bakterielle Meningitis soll die Antibiose innerhalb von 30 min begonnen werden.
- ggf. Dexamethason 10 mg i. v.
- unmittelbar vor Gabe des Antibiotikums (oder zeitgleich)2
- bis zum Erregernachweis alle 6 Stunden wiederholen
- bei Nachweis von Pneumokokken: über 4 Tage fortführen
- bei Nachweis anderer Erreger: bereits begonnene Dexamethason-Therapie beenden
- ggf. empirische antibiotische Therapie
- z. B. bei Erwachsenen mit ambulant erworbener bakterieller Meningitis Ampicillin i. v. 6 x 2 g/d und Ceftriaxon i. v. 1 x 4 g/d
Antibiogrammgerechte Antibiotikatherapie
- Die Wahl der Antibiotika richtet sich nach dem Ergebnis der Resistenzprüfung (Antibiogramm).
- Die Wahl einer zielgerichteten Antibiotikabehandlung hängt vom Keim, der Resistenzbestimmung und der minimalen Hemmkonzentration (MHK) ab.
- Siehe Tabelle Dosierung einiger in der Therapie der bakteriellen Meningitis gebräuchlichen Antibiotika bei Erwachsenen.
Behandlungsdauer
- Bei einer bakteriellen Meningitis mit unbekanntem Erreger werden empirische Antibiotika über 10–14 Tage fortgesetzt.
- Behandlungsdauer je nach Erreger unterschiedlich:
- Bei fehlender klinischer Besserung innerhalb von 2 Tagen nach Beginn der Antibiotikatherapie sollen vor allem folgende Ursachen erwogen werden:
- Auftreten von intrakraniellen Komplikationen
- persistierender infektiöser Fokus (insbesondere ein nicht sanierter oder unzureichend operierter parameningealer Fokus, wie z. B. eine Mastoiditis, Sinusitis oder Otitis media)
- inadäquates Antibiotikaregime (z. B. unwirksames Antibiotikum oder zu niedrige Dosis).
Weitere Therapien
Antibiotika-Prophylaxe bei engen Kontaktpersonen
- Eine Entscheidung über eine Antibiotika-Prophylaxe und Impfung sollte mit dem zuständigen Gesundheitsamt abgesprochen werden.
- Eine Meningokokken-Erkrankung führt im Umfeld zu einem erhöhten Erkrankungsrisiko.
- Eine Antibiotika-Prophylaxe kann eine evtl. Trägerschaft vermeiden oder eine Infektion in der ersten Woche nach Erkrankungsbeginn bei Familienmitgliedern oder engen Kontakten verhindern.
- Eine Prophylaxe wird empfohlen für alle engen Kontaktpersonen und für das Pflegepersonal, das mit den respiratorischen Sekreten der Patient*innen in Kontakt kommt.
- Eine Prophylaxe wird so schnell wie möglich durchgeführt, die mikrobiologischen Ergebnisse werden nicht abgewartet. Sinnvoll ist sie max. bis 10 Tage nach dem letzten Kontakt mit der erkrankten Person.
- Siehe Tabelle Chemoprophylaxe der Meningokokken-Meningitis.
- Bei Meningitis mit Streptococcus pneumoniae (Pneumokokken)
- Die Pneumokokken-Impfung wird nur den Patient*innen empfohlen.
- Bei Meningitis mit Neisseria meningitidis (Meningokokken)
- Patient*innen mit Verdacht auf Meningokokken-Meningitis (z. B. petechiales Exanthem, gramnegative Kokken im Liquor) sollen sich bis 24 Stunden nach Beginn einer Antibiotikatherapie in Isolation begeben.
- Bereits bei begründetem Verdacht auf eine Meningokokken-Meningitis muss eine Meldung an das Gesundheitsamt erfolgen.
- Siehe Abschnitt Meldepflicht.
- postexpositionelle Prophylaxe
- Enge Kontaktpersonen (z. B. Haushaltsmitglieder) sollen vom Gesundheitsamt ausfindig gemacht und über das Risiko und mögliche Symptome einer Meningokokken-Erkrankung (z. B. Fieber, Schüttelfrost, Kopfschmerzen) aufgeklärt werden.
- Eine Chemoprophylaxe ist bei engen Kontakten mit dem Indexfall in den letzten 7 Tagen vor Erkrankungsbeginn indiziert.
- Beginn frühestmöglich nach Diagnosestellung (bis 10 Tage nach Exposition sinnvoll)
- verwendete Antibiotika: Rifampicin, Ciprofloxacin, Ceftriaxon
- Azitromycin als Einzeldosis von 500 mg ist ebenfalls wirksam, sollte aber wegen der bislang geringen Erfahrungswerte und zur Vermeidung von Resistenzen vor allem exponierten Schwangeren vorbehalten bleiben.
- Bei engen Kontaktpersonen sollte zusätzlich eine postexpositionelle Meningokokken-Impfung mit einem Impfstoff durchgeführt werden, der die entsprechende Serogruppe abdeckt.
- Dies gilt für die Serogruppen A, C, W, Y und B.
Maßnahmen bei einem Ausbruch
- Ein Ausbruch von Meningokokken-Erkrankungen ist definiert als als 2 oder mehr Erkrankungen der gleichen Serogruppe binnen 4 Wochen in einer Kindereinrichtung, Schulklasse, Spielgruppe oder einer Gemeinschaftseinrichtung.
- Bei einem Ausbruch erfolgt die Koordination der Maßnahmen durch das Gesundheitsamt.
- z. B. Koordination der Antibiotikaprophylaxe, Impfprophylaxe, Einschränkungen für Versammlungen, das Sozialleben, Kindergärten, Schulen, Arbeitsplätze usw.
Impfung/Prävention
Haemophilus influenzae Typ b (Hib)
- Grundimmunisierung
- reife Neugeborene
- Beginn der Grundimmunisierung im Alter von 2 Monaten
- Für die Sechsfach-Impfung, bei der gegen Diphtherie, Tetanus, Pertussis, Polio, Haemophilus influenzae Typ b und Hepatitis B immunisiert wird, wird ein 2+1-Schema mit Impfungen im Alter von 2, 4 und 11 Monaten empfohlen.
- Frühgeborene (vor der 37. Schwangerschaftswoche)
- aufgrund des noch nicht ausgereiften Immunsystems 3+1-Impfschema, mit 4 Impfstoffdosen im Alter von 2, 3, 4 und 11 Monaten
- reife Neugeborene
- Nachholimpfungen
- im 1. Lebensjahr
- Mindestabstand 2 Monate nach Erstimpfung, 6 Monate nach zweiter Dosis
- Ungeimpfte nach vollendetem 1. Lebensjahr
- nur noch eine Impfstoffdosis erforderlich
- im 1. Lebensjahr
- Nach der Einführung eines Impfstoffs ist die Inzidenz der Meningitis mit Haemophilus influenzae Typ B auf wenige Einzelfälle gesunken.
- Infektionen betreffen heute vor allem nichtgeimpfte Kinder.
Streptococcus pneumoniae (Pneumokokken)
- Siehe auch den Artikel zu Pneumokokken-Infektionen.
- Grundimmunisierung im Säuglingsalter (ab Alter von 2 Monaten)
- 2 Impfstoffdosen Pneumokokken-Konjugatimpfstoff im Abstand von 8 Wochen
- Bei Frühgeborenen 3 Impfstoffdosen ab dem chronologischen Alter von 2 Monaten im Abstand von jeweils 4 Wochen. Die Grundimmunisierung wird mit einer weiteren Dosis im Alter von 11–14 Monaten und mit einem Mindestabstand von 6 Monaten zur vorausgegangenen Impfung abgeschlossen.
- Nachholimpfungen
- im 1. Lebensjahr
- Mindestabstand 2 Monate nach Erstimpfung, 6 Monate nach 2. Dosis
- im 2. Lebensjahr
- Mindestabstand 8 Wochen nach Erstimpfung, keine 3. Dosis erforderlich
- im 1. Lebensjahr
- Standardimpfung für Senior*innen (Personen ≥ 60 Jahre)
- empfohlene einmalige Standardimpfung mit dem 23-valenten Polysaccharid-Impfstoff (PPSV23)
- Zusätzlich Indikationsimpfungen für Personen mit bestimmten Risikofaktoren für schwere Pneumokokken-Erkrankungen (siehe dort)
- Aufgrund der begrenzten Dauer des Impfschutzes Wiederholung der Impfung mit PPSV23 in allen Risikogruppen mit einem Mindestabstand von 6 Jahren
- Die Inzidenz der bakteriellen Meningitis nach der Einführung des Impfstoffs wurde um etwa 30 % reduziert, dabei war der stärkste Rückgang bei Kindern zu verzeichnen.
Neisseria meningitidis (Meningokokken)
- Meningokokken der Serogruppe B
- Evidenz für eine abschließende Entscheidung über eine generelle Impfempfehlung zur Meningokokken-B-Impfung noch nicht ausreichend
- Impfung bei Personen mit spezifischen Grundkrankheiten nach individueller Risikoabschätzung
- Meningokokken der Serogruppe C
- Empfehlung zur Impfung für alle Kinder im 2. Lebensjahr
- Eine fehlende Impfung soll bis zum 18. Geburtstag nachgeholt werden.
- Auffrischimpfung derzeit nicht empfohlen
- Impfung gegen Meningokokken der Serogruppen A, C, W und Y
- 4-valenter ACWY-Konjugatimpfstoff, zusätzlich zum Meningokokken-B-Impfstoff, empfohlen bei bestimmten Indikationen (z. B. Personen mit Immundefizienz, Reisende, exponiertes Laborpersonal)
Schutzimpfung bei Reisen
- Reisende in Länder mit epidemischem/hyperendemischen Vorkommen, besonders bei engem Kontakt zur einheimischen Bevölkerung (z. B. Entwicklungshelfer*innen, medizinisches Personal, bei Langzeitaufenthalt)
- für Pilger nach Mekka
- ACWY-Impfung muss von allen Pilgern ab dem 2. Lebensjahr bei der Einreise nach Saudi-Arabien nachgewiesen werden.
- Schüler*innen/Studierende vor Langzeitaufenthalten in Ländern mit empfohlener allgemeiner Impfung entsprechend den Empfehlungen der Zielländer
- WHO- und Länderhinweise beachten.
- für Pilger nach Mekka
- Wiederholte Epidemien von Meningokokken-Meningitis in einer zentralafrikanischen Region, dem sog. „Meningitisgürtel“1
Verlauf, Komplikationen und Prognose
Verlauf
- Meist abrupter Beginn und schnelle Verschlechterung der klinischen Symptome
- meist Krankenhauseinweisung innerhalb von 24 Stunden
- Stationäre, ggf. intensivmedizinische Therapie
- Schwere Erkrankung mit hoher Rate von Mortalität, Komplikationen und Spätfolgen
Komplikationen
Akutphase
- Etwa die Hälfte der erwachsenen Patient*innen entwickelt in der Akutphase der Erkrankung Komplikationen unterschiedlichen Schweregrades.
- die erste Woche der Erkrankung als kritische Zeit
- intensivstationäre Behandlung sinnvoll
Neurologische Komplikationen
- Hirnödem mit der Gefahr der Einklemmung (10–15 %)
- Zerebrovaskuläre Komplikationen (15–20 %)
- Arteriitis (Stenosen, Kaliberschwankungen), Vasospasmus, fokale kortikale Hyperperfusion, zerebrale Autoregulationsstörung
- ischämischer Schlaganfall
- septische Sinus- oder Hirnvenenthrombose
- Hydrozephalus (10–15 %)
- Vestibulokochleäre Beteiligung mit Hörstörungen, Vestibulopathie (10–20 %)
- Hirnnervenparesen (ca. 10 %)
- Zerebritis (Hirnphlegmone) (< 5 %)
- Epileptische Anfälle und sekundäre Epilepsie (2–15 %)
- Selten als Folge der Meningitis: Hirnabszess, subdurales Empyem
Extrakranielle Komplikationen
- Sepsis und septischer Schock
- Verbrauchsagulopathie (disseminierte intravasale Gerinnung)
- Adult Respiratory Distress Syndrome (ARDS)
- Arthritis (septisch und reaktiv)
- Elektrolytstörungen wie Hyponatriämie
- Syndrom der inadäquaten ADH-Sekretion (SIADH)
- Zerebrales Salzverlustsyndrom oder zentraler Diabetes insipidus
- Rhabdomyolyse
- Pankreatitis
- Septische einseitige (selten beidseitige) Endophthalmitis oder Panophthalmitis
- Spinale Komplikationen (z. B. Myelitis oder spinale Vaskulitis)
Waterhouse-Friderichsen-Syndrom
- Schwere Komplikation bei septischem Verlauf der bakteriellen Meningitis
- in 10–15 % der Meningokokken-Sepsis
- Beruht auf der Freisetzung von Endotoxinen.
- Syndrom aus:
- Sepsis und septischem Schock
- disseminierter intravasaler Gerinnung
- Petechien, Ekchymosen und flächige Nekrosen
- Einblutung in parenchymatöse Organe, v. a. Nebennierenrinde (akute Nebennierenrindeninsuffizienz).
Prognose
- Unbehandelt fast immer letaler Verlauf
- Die Mortalität ist abhängig vom Erreger der Meningitis.
- Pneumokokken-Meningitiden: 15–20 %
- Listerien-Meningitiden: 20–30 %
- Meningokokken-Meningitiden: 3–10 %
- Prognostische Faktoren
- Ein fortgeschrittenes Alter ist mit erhöhter Mortalität assoziiert.
- Bewusstlosigkeit (GCS < 8) und septischer Schock zum Diagnosezeitpunkt sind Indikatoren für eine schlechte Prognose.
- Bei Vorerkrankungen wie Alkoholismus, Leberzirrhose, malignen Erkrankungen, Immunsuppression, Diabetes mellitus oder chronischem Nierenversagen ist die Prognose schlechter.
- Residuen bzw. Folgeschäden
- neurologischen Residuen (Hörstörungen, neuropsychologische Auffälligkeiten, Hemiparese, epileptische Anfälle, seltener Ataxie, Hirnnervenparesen und Sehstörungen wie z. B. homonyme Hemianopsie) in 10–40 % der Fälle
- Bei Kindern ist ein residueller Hydrozephalus beschrieben.
Verlaufskontrolle
- Klinische Kontrollen nach überstandener bakterieller Meningitis sollten zusammen mit Untersuchungen hinsichtlich der Folgeschäden durchgeführt werden.
- Hörstörungen werden mit Audiometrie evaluiert.
- Bei Kindern mit Hydrozephalus sollten regelmäßige Kopfumfangsmessungen durchgeführt und Anzeichen von Drucksymptomen dokumentiert werden.
- Eine strukturelle Epilepsie als Spätfolge erfordert eine Beurteilung mittels EEG und ggf. eine antikonvulsive Therapie.
- Die Maßnahmen sollten bei Folgeschäden ergriffen werden, die man beeinflussen kann, z. B. neuropsychologische Folgeschäden wie Schlafstörungen.
Patienteninformationen
Patienteninformationen in Deximed
Illustrationen

Petechien bei Meningokokkensepsis
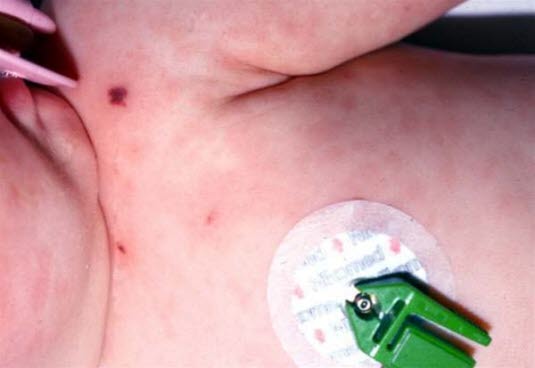
Nahaufnahmen von Petechien und Ekchymose
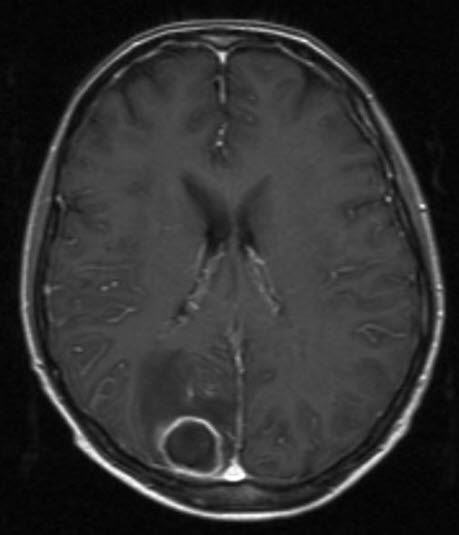
Hirnabszess
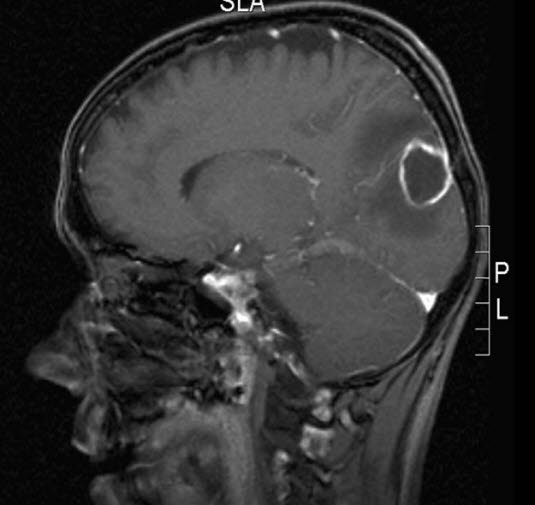
Hirnabszess
Falls Sie nach Krankheitszeichen auf dunkler Haut suchen, siehe Mind the Gap: hier im Besonderen das Bild Meningococceal disease.
Quellen
Literatur
- van de Beek D, Brouwer M, Hasbun R, Koedel U, Whitney CG, Wijdicks E. Community-acquired bacterial meningitis. Nat Rev Dis Primers. 2016 Nov 3;2:16074. doi: 10.1038/nrdp.2016.74 Review. PubMed PMID: 27808261 www.ncbi.nlm.nih.gov
- Brouwer MC, McIntyre P, Prasad K, van de Beek D. Corticosteroids for acute bacterial meningitis. Cochrane Database Syst Rev. 2015 Sep 12;(9):CD004405. doi: 10.1002/14651858.CD004405.pub5 Review. PubMed PMID: 26362566 PubMed Central PMCID: PMC6491272. pubmed.ncbi.nlm.nih.gov
Autor*innen
- Thomas M. Heim, Dr. med., Wissenschaftsjournalist, Freiburg
- Jonas Klaus, Arzt, Freiburg im Breisgau