Streszczenie
- Definicja: Ostre, szybko postępujące, bakteryjne zakażenie głębokich warstw tkanki podskórnej, szerzące się wzdłuż powięzi, prowadzące do martwicy zajętych tkanek. Cechuje się ciężkim, nierzadko septycznym przebiegiem oraz ekstremalnym bólem miejscowym.
- Epidemiologia: Zapadalność szacuje się na ok. 2 przypadki na 100 000 osób.
- Objawy: Ostry początek, wyjątkowo silny ból w okolicy zakażenia poprzedza wystąpienie objawów ogólnych. W dalszym przebiegu ogólnoustrojowe objawy zapalenia z gorączką, dreszczami i szybkim pogorszeniem ogólnego stanu fizycznego.
- Badanie fizykalne: Początkowo często brak miejscowych zmian patologicznych, widoczna martwica i pęcherze pojawiają się dopiero w późnych stadiach.
- Diagnostyka: Rozpoznanie na podstawie objawów klinicznych, w przypadku niepewności głębokie sondowanie aż do powięzi.
- Leczenie: Wczesna radykalna interwencja chirurgiczna i antybiotyki o szerokim spektrum działania.
Informacje ogólne
Definicja
- Zagrażające życiu bakteryjne zakażenie tkanek miękkich, któremu towarzyszy ekstremalny ból miejscowy.
- Początkowo często nieswoiste objawy bez wyraźnych zmian skórnych.
- Konieczne jest szybkie rozpoznanie i pilne radykalne leczenie chirurgiczne oraz odpowiednia antybiotykoterapia.
- Opóźnienie rozpoznania zwiększa śmiertelność.1
- Zakażenie szybko się rozprzestrzenia – ewolucja zmian w zajętych tkankach następuje w ciągu kilkunastu do kilkudziesięciu godzin.2
- Nawet u 50% chorych rozwija się wstrząs septyczny i/lub niewydolność oddechowa.
Epidemiologia
- Częstość występowania martwiczego zapalenia powięzi szacuje się na około 2 przypadki na 100 000 osób.
- Występowanie we wszystkich grupach wiekowych
- średnia wieku 54 lata.3
Klasyfikacja
- Na podstawie oznaczeń mikrobiologicznych zakażenie dzieli się na typ 1 i typ 2.4
- Typ 1
- często połączenie patogenów tlenowych i beztlenowych z tworzeniem gazów1
- najczęściej u starszych pacjentów z wielochorobowością
- głównie w pobliżu tułowia, okolicy odbytu i genitaliów.
- Typ 2
- najczęściej paciorkowce, a następnie MRSA1
- również u młodych, zdrowych pacjentów
- głównie na kończynach, głowie i szyi.
Patofizjologia
- Możliwe są zakażenia egzogenne lub endogenne przez drobnoustroje chorobotwórcze.
- Egzogenne (z powierzchownych warstw skóry do głębszych warstw tkanki podskórnej)1
- Patogeny dostają się do tkanek miękkich przez uszkodzenie skóry/zmianę skórną.
- Często przyczyną są błahe urazy, takie jak ukąszenia owadów, zadrapania czy otarcia skóry.5
- Dochodzi do uwalnianie egzotoksyn.
- Miejscowe uszkodzenie tkanki z obrzękiem i rumieniem.
- Agregacja leukocytów i płytek krwi prowadzi do okluzji naczyń włosowatych i uszkodzenia naczyń.
- Pojawiają się pęcherze i wybroczyny.
- Zstępowanie zakażenia do głębszych warstw tkanek i narastająca martwica.
- Endogenne (z głębokich do powierzchownych warstw tkanki)1
- Niewielkie, drobne zmiany w głębokich warstwach tkanek uruchamiają mechanizm naprawczy z napływem leukocytów i innych komórek.
- U pacjentów z immunosupresją, u których występuje przemijająca bakteriemia, czynniki chorobotwórcze docierają również do głębokich warstw tkanek.
- Uwolnienie egzotoksyn prowadzi do martwicy i uszkodzenia naczyń krwionośnych w głębokich warstwach tkanek.
- Martwica rozprzestrzenia się do warstw tkanek bliżej powierzchni, pęcherze i wybroczyny rozwijają się późno.
Czynniki predysponujące
- Zakażenia występują najczęściej u pacjentów z miejscowym lub ogólnoustrojowym niedoborem odporności.
- immunosupresja
- cukrzyca
- nadużywanie alkoholu
- nadużywanie narkotyków dożylnych
- zaburzenia krążenia obwodowego
- podeszły wiek
- marskość wątroby
- nadwaga
- miażdżyca
- niedożywienie
- niewydolność nerek.
- U około 1/4 chorych nie rozpoznaje się żadnego czynnika ryzyka.6
- Skórne wrota zakażenia można zidentyfikować u około 40% pacjentów.
ICD-10
- M72.6 Martwicze zapalenie powięzi.
Diagnostyka
Kryteria diagnostyczne
- Rozpoznanie kliniczne.
- Jedynym typowym wczesnym objawem jest ekstremalny ból miejscowy (niewspółmierny), spowodowany niedokrwieniem powięzi.
Diagnostyka różnicowa
- Róża
- powolna progresja i mniejsze skutki ogólnoustrojowe.
- Ropowica
- wyraźny obrzęk bez rozwoju martwicy, mniej bolesny.
- Zakrzepica żył głębokich
- obrzęk bez rozwoju martwicy w skórze, minimalne skutki ogólnoustrojowe.
- Zespół ciasnoty przedziałów powięziowych
- również silny ból, ale zazwyczaj tylko po ciężkim urazie.
- Inne zakażenia wywołane przez paciorkowce.
- Zgorzel Fourniera
- szczególna postać martwiczego zapalenia powięzi w okolicy narządów płciowych i pachwin.
Wywiad
- Ostry początek silnego bólu, który może wystąpić w dowolnym miejscu ciała.7
- Objawy zakażenia
- W ciągu 24 godzin w skórze pojawiają się zmiany zapalne: zaczerwienienie, ból, obrzęk i wzrost temperatury.5
- Zmiany skórne, takie jak rany (zadrapania) lub ukąszenia owadów.
- W zaawansowanym stadium uszkodzenie nerwów i pojawienie się niedoczulicy w obszarze objętym procesem chorobowym, może rozwinąć się obraz kliniczny z majaczeniem, odwodnieniem i początkiem niewydolności narządowej.
Badanie przedmiotowe
-
Poszukiwanie możliwych wrót zakażenia na skórze.
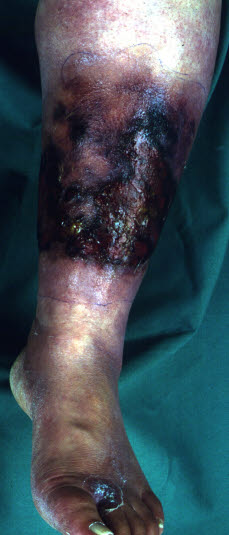 Martwicze zakażenie tkanek miękkich
Martwicze zakażenie tkanek miękkich - W metaanalizie 1463 przypadków ustalono następującą częstość występowania objawów8:
- obrzęk (81%)
- ból (79%)
- rumień (71%)
- nadmierne ucieplenie (44%)
- gorączka (40%)
- pęcherze (26%)
- martwica skóry (24%)
- niedociśnienie (21%)
- krepitacje (20%).
- W późnym stadium pojawiają się charakterystyczne żywe obszary martwicy skóry, niekiedy z pęcherzami, które mogą być sinoczarne z domieszką krwi.
- Oznaczanie zmian skórnych markerem w celu oceny ewentualnej progresji.
Badania uzupełniające
- Zalecane badania laboratoryjne
- Leukocytoza (>10 000/mcl) z neutrofilią i CRP powyżej 100 mg/l występują u niemal wszystkich pacjentów.
- Odsetek niedojrzałych neutrofili jest wysoki i sięga 40–50%.9
- Kinaza kreatynowa (CK)
- miarodajny wskaźnik zajęcia mięśni.10
- U pacjentów często występuje spadek hematokrytu oraz hiperglikemia, hipoalbuminemia, małopłytkowość, hipokalcemia i kwasica.5,11
Diagnostyka
- Szybka diagnostyka (badania dodatkowe) nie powinna opóźniać leczenia chirurgicznego.
- Badanie USG
- brzeg hipoechogeniczny jako oznaka rozpływnej martwicy powięzi.
- RTG przy podejrzeniu martwiczego zapalenia powięzi kończyn
- gaz wykrywalny w tkankach w 25% przypadków.8
- TK w celu oceny zaawansowania zmian zapalno-martwiczych, obecności gazu w tkankach oraz różnicowania z innymi zakażeniami skóry i tkanek miękkich.
- Posiewy krwi, wymazy i posiewy treści ropnej z pęcherzy lub sączących zmian skórnych oraz materiału biopsyjnego pobranego w trakcie zabiegu; materiał należy pobrać na posiew tlenowy i beztlenowy.
Diagnostyka chirurgiczna
- W niejasnych przypadkach, głębokie nacięcie diagnostyczne aż do powięzi.
Wskazania do skierowania
- Hospitalizacja w trybie pilnym w przypadku podejrzenia choroby.
Leczenie
Cele leczenia
- Ratowanie życia pacjentów!
- Chirurgiczna i antybiotykowa sanacja zakażeń.
- Ograniczenie uszkodzeń tkanki.
- Ewentualnie rekonstrukcja ubytków tkanki lub utraty funkcji.
Ogólne informacje o leczeniu
- Szybkie i radykalne chirurgiczne usunięcie tkanki martwiczej jest konieczne i ma ogromne znaczenie, opóźnienie leczenia chirurgicznego zwiększa ryzyko zgonu.7
- Ukierunkowana sanacja w ciągu pierwszych 6 do maksymalnie 12 godzin po przyjęciu wiąże się z istotnie lepszym rokowaniem.12
- Pierwsze radykalne opracowanie chirurgiczne powinno odbyć się jak najszybciej.
Leczenie chirurgiczne
- Szybkie i radykalne chirurgiczne usunięcie tkanki martwiczej.
- Planowe powtórne opracowanie chirurgiczne po około 24 godzinach (lub wcześniej, jeśli stan kliniczny pogarsza się) uwzględnia dynamikę martwiczych zakażeń skóry i tkanek miękkich oraz dostarcza informacji na temat kontroli miejscowego rozprzestrzeniania się zakażenia.
- Regularne opracowanie może być konieczne do czasu opanowania zakażenia.7
Intensywna farmakoterapia
- Intensywne leczenie ogólne
- Płyny, odżywianie, łagodzenie bólu.
- W związku z opracowaniem chirurgicznym często dochodzi do krwawień i może być wymagane przetaczanie krwi.13
- U większości pacjentów występuje hiperglikemia, która wymaga dożylnego leczenia insuliną.14
- Profilaktyka owrzodzeń przewodu pokarmowego wywołanych stresem u wybranych pacjentów.
- Ewentualnie szczepienie przeciwko tężcowi.
Antybiotyki
- Konieczna jest szybka antybiotykoterapia.15
- Empiryczna antybiotykoterapia o szerokim spektrum, obejmujacym typowe patogeny, tj. S. aureus (MRSA), lekooporne bakterie Gram-ujemne i beztlenowce.
- Zakażenia mieszane:
- piperacylina/tazobaktam lub imipenem lub meropenem, w przypadku podejrzenia zakażenia S. aureus z wankomycyną lub daptomycyną
- leczenie alternatywne - w przypadku przeciwwskazań do stosowania karbapenemów:
- cefepim z metronidazolem
- w przypadku alergii na beta-laktamy - ciprofloksacynę z metronidazolem
- dostosowanie terapii po identyfikacji patogenu.
Dalsze leczenie
- Tlenoterapia hiperbaryczna: należy rozważyć w szczególnie cięzkich przypadkach zakażeń bakteriami beztlenowymi.
Rehabilitacja i obserwacja
- Po fazie ostrej i leczeniu zakażenia często rozpoczyna się długi etap rehabilitacji z terapią zajęciową i fizjoterapią.
- Jeżeli doszło do poważnych uszkodzeń pierwotnych, przywrócenie sprawności może wymagać wtórnej rekonstrukcji.7
Przebieg, powikłania i rokowanie
Przebieg
- Rozwój martwicy w połączeniu z szybko postępującym zakażeniem w tkance podskórnej (ropowica), powięzi (zapalenie powięzi) oraz w pojedynczych przypadkach skóry (róża) i mięśni (zapalenie mięśni).
Powikłania
- Sepsa.
- Niewydolność nerek.
- Zespół wstrząsu toksycznego.
- Wstrząs.
- Uszkodzenie tkanki.
- Utrata sprawności.
- Zgon.
Rokowanie
- Śmiertelność 20–30%.
- Krótki okres od początku choroby do hospitalizacji oraz od przyjęcia do operacji zwiększa szanse na przeżycie.
- U 10–20% pacjentów z martwiczym zapaleniem powięzi kończyny dochodzi do amputacji.
- Czynniki pogarszające rokowanie
Informacje dla pacjentów
Informacje dla pacjentów w Medibas
Ilustracje
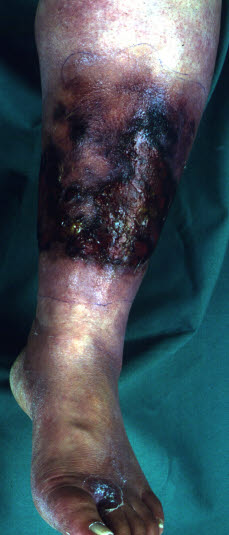
Rozwój martwicy prowadzi do przebarwień skóry, krepitacji, utraty czucia i nieprzyjemnego zapachu.
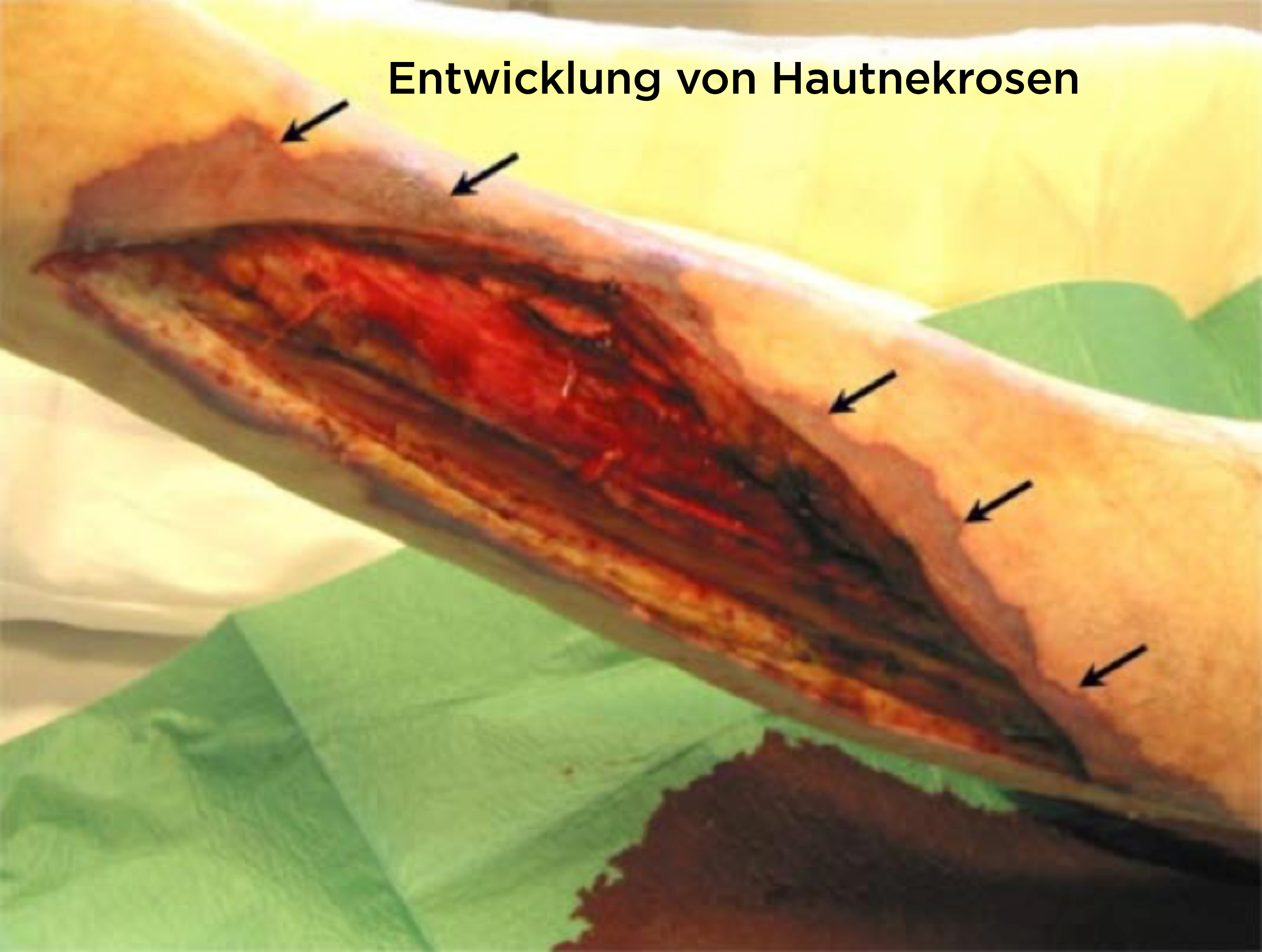
Progresja martwicy skóry (skóry właściwej) po usunięciu obszaru tkanki miękkiej na kończynie dolnej z powodu martwiczego zapalenia powięzi.
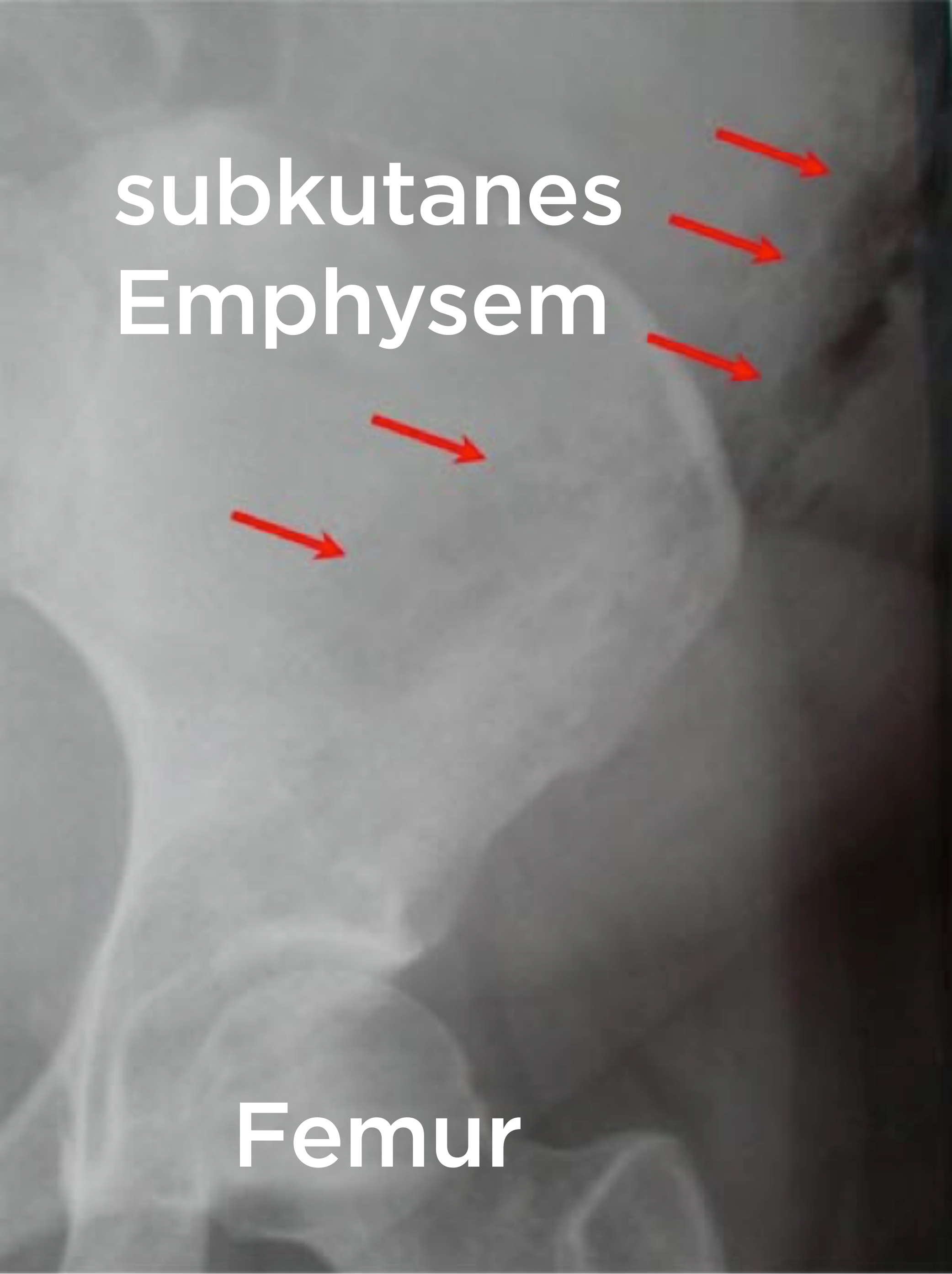
Odma podskórna w martwiczym zapaleniu powięzi.
Źródła
Piśmiennictwo
- Stevens DL, Bryant AE. Necrotizing Soft-Tissue Infections. NEJM 2017; 377: 2253-2265. www.ncbi.nlm.nih.gov
- Paty R, Smith A. Gangrene and Fournier's gangrene. Urol Clin North America 1992; 19: 149. pubmed.ncbi.nlm.nih.gov
- Cranendonk DR, van Vught LA, Wiewel MA, et al. Clinical Characteristics and Outcomes of Patients With Cellulitis Requiring Intensive Care. JAMA Dermatol 2017; 153(6): 578-82. www.ncbi.nlm.nih.gov
- Pasternack MS, Swartz MN. Cellulitis, necrotizing fasciitis, and subcutaneous tissue infections. Philadelphia: Elsevier, 2015.
- Singh G, Sinha SK, Adhikary S, Babu KS, Ray P, Khanna SK. Necrotising infections of soft tissues - a clinical profile. Eur J Surg 2002; 168: 366-71. PubMed
- Jung N, Eckmann C. Essentials in the management of necrotizing soft-tissue infections. Infection 2019; 47(4): 677-9. www.ncbi.nlm.nih.gov
- Hasham S, Matteucci P, Stanley PRW, Hart NB. Necrotising fasciitis. BMJ 2005; 330: 830-3. PubMed
- Goh T, Goh LG, Ang CH, et al. Early diagnosis of necrotizing fasciitis. Br J Surg 2014; 101(1): 119-25. www.ncbi.nlm.nih.gov
- Rea WJ, Wyrick WJ. Necrotizing fasciitis. Ann Surg 1970; 172: 957-65. PubMed
- Stevens DL, Tanner MH, Winship J. Reappearance of scarlet fever A among streptococci in the Rocky Mountain West: severe group A streptococcal infections associated with a toxic shock-like syndrom. N Engl J Med 1989; 321: 1-7. New England Journal of Medicine
- McHenry CR, Piotrowski JJ, Teprinic D, Malangoni MA. Determinants of mortality for necrotizing soft tissue infections. Ann Surg 1995; 221: 558-65. PubMed
- Hadeed GJ, Smith J, O'Keeffe T, et al. Early surgical intervention and its impact on patients presenting with necrotizing soft tissue infections: a single academic center experience.. J Emerg Trauma Shock 2016; 9(1): 22-27. www.ncbi.nlm.nih.gov
- Hackett SP, Stevens DL. Streptococcal toxic shock syndrome: Synthesis of tumour necrosis factor and interleukin-1 by monocytes stimulated with pyrogenic exotoxin A and streptolysin O. J Infect Dis 1992; 165: 879-85. PubMed
- Lin C, Yeh FL, Lin JT, Ma H, Hwang CH, Shen BH, Fang RH. Necrotizing Fasciitis of the Head and Neck: An Analysis of 47 Cases. Plast Reconstr Surg 2001; 107: 1684-93. PubMed
- Stevens DL, Bisno AL, Chambers HF, et al. Practice guidelines for the diagnosis and management of skin and soft tissue infections:2014 update by the infectious diseases society of America.. Clin Infect Dis 2014; 59(2): 59(2). www.ncbi.nlm.nih.gov
- Kao LS, Lew DF, Arab SN, et al. Local variations in the epidemiology, microbiology, and outcome of necrotizing soft-tissue infections: a multicenter study. Am J Surg 2011; 202(2): 139-45. www.ncbi.nlm.nih.gov
- Hadeed GJ, Smith J, O'Keeffe T, et al. Early surgical intervention and its impact on patients presenting with necrotizing soft tissue infections: A single academic center experience. J Emerg Trauma Shock 2016; 9(1): 22-27. www.ncbi.nlm.nih.gov
Autorzy
- Katarzyna Nessler (recenzent)
- Adam Windak (redaktor)
- Lino Witte (recenzent/redaktor)
