Komorowe zaburzenia rytmu serca i nagły zgon sercowy
Częstość występowania
- Nagły zgon sercowy to jedna z najczęstszych przyczyn zgonów, odpowiadająca za 50% wszystkich zgonów związanych z układem krążenia na całym świecie.
- 2/3 przypadków nagłego zgonu sercowego jest spowodowanych migotaniem komór.
- Roczna zapadalność: około 80/100 0001
- 34% przypadków w wieku 70-80 lat. 1
- Ryzyko nagłego zgonu sercowego jest wyższe u mężczyzn niż u kobiet.
- około 75% przypadków wśród mężczyzn.2-3
Etiologia i patogeneza
- Ryzyko nagłego zgonu sercowego rośnie wraz z wiekiem.4
- Główne przyczyny u młodszych osób:
- zaburzenia czynności kanałów jonowych
- kardiomiopatie
- zapalenie mięśnia sercowego
- anomalie naczyń wieńcowych
- główne przyczyny u starszych osób:
- choroba wieńcowa: ostry zespół wieńcowy, przewlekły zespół wieńcowy
- niewydolność serca o różnej etiologii
- zaburzenia dotyczące zastawek serca.
- Główne przyczyny u młodszych osób:
- Najczęstsza kaskada patofizjologiczna nagłego zgonu sercowego
- częstoskurcz komorowy przechodzący w migotanie komór i ostatecznie w asystolię.
- U 70–80% pacjentów występuje choroba wieńcowa.4
- Pierwsze zdarzenie jest często śmiertelne, tylko w 10–15% wcześniej wystąpiły arytmie.
- Identyfikacja przyczyny nagłego zgonu sercowego jest ważna dla oceny ryzyka w rodzinie.
Diagnostyka przy podejrzeniu lub udokumentowanych komorowych zaburzeniach rytmu serca4
- Metody nieinwazyjne
- 12-odprowadzeniowe badanie EKG
- badanie Holter EKG
- rejestrator zdarzeń lub implantowany rejestrator pętlowy
- w przypadku sporadycznych objawów
- próba wysiłkowa (próba kaszlowa)
- podejrzenie choroby wieńcowej
- w przypadku podejrzenia częstoskurczu komorowego wywołanego wysiłkiem fizycznym
- diagnostyka obrazowa
- echokardiografia przezklatkowa u wszystkich pacjentów
- rezonans magnetyczny serca: w obecnych wytycznych znacznie rozszerzono zakres stosowania RM.
- Diagnostyka genetyczna: w aktualnych wytycznych mocno wzrosło również znaczenie diagnostyki genetycznej — także jako elementu stratyfikacji ryzyka w odniesieniu do wskazań do wszczepienia kardiowertera-defibrylatora.
- Testy wywołania reakcji: np. test z ajmaliną w przypadku podejrzenia m.in. zespołu Brugadów
- przesiewowe badania toksykologiczne: przede wszystkim u młodych pacjentów po przeżyciu nagłego zgonu sercowego.
- Metody inwazyjne
- koronarografia w przypadku podejrzenia zaawansowanej choroby niedokrwiennej serca
- badanie elektrofizjologiczne u wybranych pacjentów.
Czynniki predysponujące
- Choroba wieńcowa.
- Zmniejszona czynność skurczowa lewej komory.
- Predyspozycje genetyczne.
Wskazania do implantacji wszczepialnego kardiowertera-defibrylatora
- Wszczepialny kardiowerter-defibrylator (ICD) umożliwia przerwanie częstoskurczu komorowego i migotania komór, a tym samym zapobiega nagłemu zgonowi sercowemu.5
- Działanie ICD jako rozrusznika serca polega również na leczeniu zaburzeń rytmu serca o charakterze bradykardii.6
- Profilaktyka wtórna po przebytym migotaniu komór lub niestabilnym hemodynamicznie częstoskurczu komorowym.
- Wskazanie do implantacji ICD w ramach profilaktyki pierwotnej prowadzi do zmniejszenia śmiertelności u pacjentów z grupy ryzyka.
- Ważnym kryterium zwiększonego ryzyka jest upośledzona funkcja lewej komory (EF ≤35%).
- Zmniejszenie śmiertelności zostało wykazane w przypadku:
- kardiomiopatii niedokrwiennej
- kardiomiopatii o podłożu innym niż niedokrwienie.
- Zmniejszenie śmiertelności zostało wykazane w przypadku:
- Jeśli wskazany jest ICD, to należy ocenić, czy pacjent mógłby odnieść korzyść z jednoczesnej CRT (terapii resynchronizującej serca) (system ICD-CRT).4
Wytyczne: wskazania do leczenia ICD4
Profilaktyka wtórna
- Implantacja ICD jest zalecana u pacjentów z udokumentowanym migotaniem komór lub niestabilnym hemodynamicznie częstoskurczem komorowym przy braku odwracalnych przyczyn.
Profilaktyka pierwotna
- Choroba niedokrwienna serca z obniżoną czynnością skurczową lewej komory
- Implantacja ICD jest zalecana u pacjentów z chorobą niedokrwienną serca, objawową niewydolnością serca (NYHA II–III) i LVEF ≤35% pomimo ≥3 miesięcy optymalnego leczenia farmakologicznego.
- Kardiomiopatia rozstrzeniowa, kardiomiopatia hipokinetyczna
- Implantację ICD należy rozważyć u pacjentów z kardiomiopatią, objawową niewydolnością serca (NYHA II–III) i LVEF ≤35% pomimo ≥3 miesięcy optymalnego leczenia farmakologicznego.
- Arytmogenna kardiomiopatia prawej komory (ARVC)
- Implantację ICD należy rozważyć u pacjentów z hemodynamicznie stabilnym utrwalonym monomorficznym częstoskurczem komorowym.
- Kardiomiopatia przerostowa
- Wszczepienie ICD należy rozważyć u pacjentów w wieku ≥16 lat i z szacowanym 5-letnim ryzykiem nagłego zgonu sercowego ≥6%.
Zastosowanie ICD
Ogólne informacje o leczeniu
-
Zasada leczenia
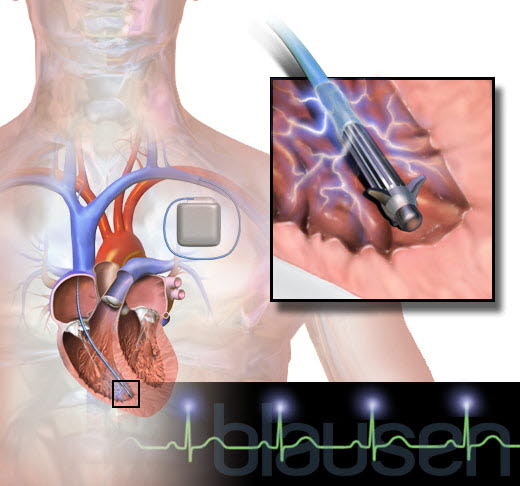 ICD: wszczepialny kardiowerter-defibrylator
ICD: wszczepialny kardiowerter-defibrylator- jednoczesna depolaryzacja komórek mięśnia sercowego przez impuls elektryczny, a tym samym zakończenie częstoskurczu komorowego lub migotania komór
- Elementy
- Podobnie jak rozrusznik serca, ICD składa się z urządzenia i co najmniej jednej elektrody (prawokomorowej z elektrodą [elektrodami] defibrylującą(-ymi) i elektrodą stymulującą/detekcyjną).
- Systemy dwujamowe mają dodatkowo elektrodę w prawym przedsionku.
- Systemy trójjamowe mają dodatkowo trzecią elektrodę w żyle wieńcowej do terapii resynchronizującej serca (ICD-CRT).
- Urządzenia ICD są nieco większe niż zwykłe rozruszniki serca.
- Implantacja
- wykonywana w znieczuleniu miejscowym i sedacji
- umieszczenie urządzenia zwykle poniżej lewego obojczyka
- W przypadku wszczepienia lewostronnie, występuje korzystniejsze ustawienie przepływu prądu dla skutecznej defibrylacji.
- Wprowadzenie elektrody przez żyłę podobojczykową lub żyłę odpromieniową
- do niedawna rutynowe testowanie skuteczności ICD poprzez wywoływanie migotania komór na zakończenie implantacji.
- Nowsze dane wskazują na równie dobrą skuteczność także bez testu śródoperacyjnego.7
Formy leczenia i opieki pooperacyjnej
- Stymulacja przeciwczęstoskurczowa
- po wykryciu częstoskurczu komorowego pierwsza próba przerwania za pomocą stymulacji przeciwczęstoskurczowej
- dwie formy stymulacji
- stymulacja typu burst: stały odstęp między stymulacjami
- stymulacja typu ramp: zmniejszający się odstęp między stymulacjami
- Skuteczna stymulacja przeciwczęstoskurczowa pozwala uniknąć konieczności wykonania obciążającej defibrylacji, która w przeciwnym razie byłaby konieczna dla pacjenta.
- Defibrylacja
- defibrylacja konieczna w przypadku wykrycia migotania komór lub nieskutecznej stymulacji przeciwczęstoskurczowej częstoskurczu komorowego
- najpierw naładowanie kondensatora
- czas trwania: około 7–10 sekund
- dostarczenie wyładowania dwufazowego o energii 30–40 J.
- Obserwacja kontrolna
- Po wstępnym ustawieniu, ICD są zwykle sprawdzane co 6 miesięcy.
Powikłania
Powikłania okołooperacyjne
- Odma opłucnowa.
- Krwiak opłucnej.
- Krwiak loży urządzenia.
- Zakażenie loży urządzenia.
- Zakrzepica.
- Przemieszczenie elektrody.
- Zapalenie osierdzia.
- Perforacja mięśnia sercowego.
Powikłania w dalszym przebiegu
- Powikłania i nieprawidłowe działanie urządzenia w dalszym przebiegu po wszczepieniu ICD są stosunkowo częste.
- Nieodpowiednie wyładowania (dostarczenie wyładowań bez obecności częstoskurczu komorowego)
- przyczyny
- błędna interpretacja częstoskurczu nadkomorowego przez algorytmy do wykrywania
- wady elektrody
- nadmierna czułość załamka T
- zakłócenia elektromagnetyczne
- 12-letnia zapadalność: 20%.8
- przyczyny
- Zakażenia
- 12-letnia zapadalność: 6%.8
- Usterki elektrody
- 12-letnia zapadalność: 17%.8
- Zaburzenia psychosomatyczne, zaburzenia lękowe,
- opieka w ramach konsultacji lub w grupach wsparcia o tematyce z zakresu arytmii
- ew. opieka psychokardiologiczna.
- Wielokrotne odpowiednie wyładowania („burza elektryczna”)
- odpowiednie leczenie za pomocą ICD ze wznowieniem zaburzeń rytmu serca w krótkim czasie
- stan nagły, natychmiastowe skierowanie do szpitala
- ew. leczenie przeciwarytmiczne amiodaronem
- sedacja, ewentualnie znieczulenie z intubacją i wentylacją mechaniczną.
Operacje niekardiologiczne
- Sygnały zakłócające spowodowane elektrokauteryzacją mogą wywołać nieodpowiednie impulsy ICD.
- Okołooperacyjna dezaktywacja funkcji terapii ICD
- Monitorowanie rytmu i gotowość do defibrylacji tak długo, jak terapia ICD jest dezaktywowana.
Badania RM
- Rezonans magnetyczny przez długi czas był uważany za absolutnie przeciwwskazany u pacjentów z ICD.
- Wiele systemów ICD dostępnych obecnie na rynku jest uważanych za „warunkowo bezpieczne w warunkach RM”.
- Przeprowadzenie badania powinno nastąpić dopiero po dokładnym rozważeniu korzyści i ryzyka.9
- Większa podatność uszkodzonego strukturalnie mięśnia sercowego per se
- wyższe ryzyko nieodwracalnego zaburzenia działania ICD niż w przypadku prostych rozruszników serca.
- Przeprogramowanie przed badaniem do specjalnego trybu RM, funkcja defibrylacji ICD jest dezaktywowana podczas badania.
Postępowanie pod koniec życia
- Celem powinno być uniknięcie bezcelowych lub niepożądanych terapii wyładowaniami.10
- W razie potrzeby dezaktywacja ICD10
- przez wykwalifikowany personel
- po odpowiedniej konsultacji z pacjentem
- w porozumieniu z prowadzącymi kardiologami/elektrofizjologami.
Informacje dla pacjentów
Informacje dla pacjentów w Medibas
Ilustracje

ICD: wszczepialny kardiowerter-defibrylator
Źródła
Wytyczne
- 2022 ESC Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death. www.escardio.org
- 2021 ESC Guidelines on cardiac pacing and cardiac resynchronization therapy. www.escardio.org
Piśmiennictwo
- Martens E, Sinner M, Siebermair J, et al. Incidence of sudden cardiac death in Germany: results from an emergency medical service registry in Lower Saxony. Europace 2014; 16: 1752-1758. doi:10.1093/europace/euu153 DOI
- Seidl K, Senges J. Worldwide utilization of implantable cardioverter/defibrillators now and in the future. Card Electrophysiol Rev 2003; 7: 5-13. PubMed
- Zipes DP, Wellens HJ. Sudden cardiac death. Circulation 1998; 98: 2334-51. pubmed.ncbi.nlm.nih.gov
- European Society of Cardiology: Guidelines for the management of patients with ventricular arrhythmias and the prevention of sudden cardiac death, Stand 2022. www.escardio.org
- Connolly SJ, Hallstrom AP, Cappato R, et al. Meta-analysis of the implantable cardioverter defibrillator secondary prevention trials. AVID, CASH and CIDS studies. Antiarrhythmics vs Implantable Defibrillator study. Cardiac Arrest Study Hamburg. Canadian Implantable Defibrillator Study. Eur Heart J 2000;21:2071–2078. doi:10.1053/euhj.2000.2476 DOI
- European Society of Cardiology. Guidelines on cardiac pacing and cardiac resynchronization therapy, Stand 2021. www.escardio.org
- Bänsch D, Bonnemeier H, Brandt J, et al. Intra-operative defibrillation testing and clinical shock efficacy in patients with implantable cardioverter-defibrillators: the NORDIC ICD randomized clinical trial. Eur Heart J 2015; 36: 2500-2507. doi:10.1093/eurheartj/ehv292 DOI
- van der Heijden A, Borleffs C, Buiten M, et al. The clinical course of patients with implantable cardioverter-defibrillators: Extended experience on clinical outcome, device replacements, and device-related complications.. Heart Rhythm 2015; 12: 1169-1176. doi:10.1016/j.hrthm.2015.02.035 DOI
- Bovenschulte H, Schlüter-Brust K, Liebig T. MRI in patients with pacemakers—overview and procedural management. Dtsch Arztebl Int 2012; 109: 270-75. doi:10.3238/arztebl.2012.0270 DOI
- Carlsson J, Paul N, Dann M, et al. The deactivation of implantable cardioverter-defibrillators:medical, ethical, practical, and legal considerations. Dtsch Arztebl Int 2012; 109: 535-541. doi:10.3238/arztebl.2012.0535 DOI
Autorzy
- Prof. dr hab. n. med. Jadwiga Nessler, (recenzent)
- Prof. dr hab. n. med. Adam Windak,(redaktor)
- Prof. dr med. Michael Handke, (recenzent)
