Streszczenie
- Definicja: Stan, w którym serce nie jest zdolne dostarczyć organizmowi wystarczającej ilości krwi ani tlenu, aby zapewnić stabilny metabolizm podczas wysiłku lub w spoczynku.
- Epidemiologia: Ogólna chorobowość 4%, silna zależność od wieku.
- Objawy: Zmniejszona wydolność fizyczna, duszność (wysiłkowa).
- Badanie fizykalne: Cechy zastoju w płucach, obrzęki nóg, poszerzenie żył szyjnych, arytmia, trzeci ton.
- Diagnostyka: Badania laboratoryjne (NTproBNP lub BNP), ekg, echokardiografia. Echokardiograficzny podział na niewydolność serca z obniżoną (HFrEF), łagodnie obniżoną (HFmrEF) i zachowaną (HFpEF) frakcją wyrzutową.
- Leczenie: Leczenie chorób podstawowych, skuteczne leczenie etiologii, chorób współistniejących zarówno sercowo-naczyniowych (CV), jak i innych niż CV. Farmakoterapia HFrEF: Podstawowe leczenie obejmuje jednoczasowe zastosowanie poczwórnej terapii obejmującej: inhibitory ACE (lub antagonistów receptora angiotensyny - tzw. sartanów lub bardziej rekomendowany sakubitryl/walsartan - ARNI), beta-blokery, antagonistów receptora mineralokortykoidowego (MRA) oraz inhibitory SGLT-2 (flozyny). Obecnie rekomenduje się włączanie wszystkich czterech wymienionych leków jednocześnie, w dawkach uzależnionych od wartości tętna, ciśnienia skurczowego oraz innych parametrów klinicznych. Farmakoterapia HFmrEF: inhibitory SGLT-2 jako podstawa leczenia oraz pozostałe leki jak w przypadku poprzednim, ale z niższym stopniem rekomendacji. Farmakoterapia HFpEF: inhibitory SGLT-2 to pierwsza terapia skutecznie poprawiająca rokowanie, . Diuretyki do objawowego leczenia obecności zastoju we wszystkich typach niewydolności serca. CRT i/lub ICD w określonych grupach jako terapie interwencyjne.
Informacje ogólne
Definicja1
- Przewlekłą niewydolność serca można zdefiniować klinicznie lub patofizjologicznie.
Definicja kliniczna
- Występowanie typowych objawów (np. duszności, zmniejszenia wydolności i/lub zatrzymania płynów lub ich redystrybucji) na tle zaburzeń czynnościowych serca.
Definicja patofizjologiczna
- Serce nie jest zdolne dostarczyć organizmowi wystarczającej ilości krwi ani tlenu, aby zapewnić stabilny metabolizm podczas wysiłku lub w spoczynku.
Klasyfikacje
- Przewlekłą niewydolność serca można klasyfikować według różnych kryteriów.
Klasyfikacja kliniczna (NYHA, New York Heart Association)
- Podział kliniczny na różne stopnie zaawansowania umożliwia oszacowanie rokowania, a także ma znaczenie przy wyborze odpowiedniego leczenia dla danego stadium.
- Najczęściej stosowaną klasyfikacją jest klasyfikacja NYHA.
- I stopień w skali NYHA:
- dysfunkcja serca bez ograniczeń w aktywności fizycznej
- zwykła aktywność fizyczna nie powoduje dolegliwości.
- II stopień w skali NYHA:
- niewielkie ograniczenie wydolności
- bez dolegliwości w spoczynku i przy niewielkim wysiłku
- większy wysiłek (np. chodzenie pod górę lub wchodzenie po schodach) powoduje duszność, wyczerpanie, arytmię lub dławicę piersiową.
- III stopień w skali NYHA:
- znaczne ograniczenie wydolności fizycznej
- bez dolegliwości w spoczynku
- niewielki wysiłek fizyczny (np. chodzenie po równym terenie) powoduje duszność, wyczerpanie, arytmię lub dławicę piersiową.
- IV stopień w skali NYHA:
- dolegliwości podczas każdego rodzaju aktywności fizycznej i w spoczynku
- pacjent leżący.
Klasyfikacja według frakcji wyrzutowej lewej komory serca
- Klasyfikacja ta ma znaczenie głównie przy wyborze terapii.
- Klasyczna farmakoterapia w niewydolności serca dotyczy pacjentów z obniżoną frakcją wyrzutową (EF), natomiast do niedawna nie była dostępna żadna farmakoterapia wpływająca na rokowanie u pacjentów z zachowaną EF.
- W przeszłości rozróżniano jedynie niewydolność serca z frakcją wyrzutową (EF - Ejection Fraction) obniżoną (HFrEF - Heart Failure with reduced Ejection Fraction) i zachowaną (HFpEF - Heart Failure with preserved Ejection Fraction); ostatnio wyodrębniono trzecią grupę z łagodnie obniżoną EF (HFmrEF - Heart Failure with mildly reduced Ejection Fraction) oraz dodatkowo z poprawą EF (HFimpEF - Heart Failure with improved Ejection Fraction ).
- Wybrane cechy wyróżniające populację pacjentów z zachowaną EF (HFpEF):
- starszy wiek
- częściej kobiety
- częstsze migotanie przedsionków
- częstsza przewlekła choroba nerek
- częstsze choroby współwystępujące o innym podłożu niż sercowo-naczyniowe.
- Niewydolność serca z obniżoną frakcją wyrzutową (HFrEF):
- LVEF ≤40%.
- Niewydolność serca z łagodnie obniżoną frakcją wyrzutową (HFmEF):
- LVEF 41–49%
- dalsze kryteria potwierdzające rozpoznanie:
- podwyższony poziom peptydów natriuretycznych (BNP >35 pg/ml i/lub NT-proBNP >125 pg/ml)
- zobiektywizowane echokardiograficznie zaburzenia strukturalne lub czynnościowe lewej komory serca.
- Niewydolność serca z zachowaną frakcją wyrzutową (HFpEF):
- LVEF ≥50%
- podwyższony poziom peptydów natriuretycznych (BNP >35 pg/ml i/lub NT-proBNP >125 pg/ml), zobiektywizowane echokardiograficznie zaburzenia strukturalne lub czynnościowe lewej komory serca.
- Niewydolność serca z poprawą EF (HFimpEF):
- HF z początkową LVEF ≤40% - zwiększenie o ≥10 punktów procentowych względem początkowej LVEF, w drugim pomiarze LVEF >40%.
Klasyfikacja w zależności od niewydolnego obszaru serca
- Niewydolność lewokomorowa.
- Niewydolność prawokomorowa.
- Globalna niewydolność serca.
Stadia niewydolności serca według ACC/AHA2
- Odzwierciedlają progresje choroby:
- A – „At risk for HF” (wysokie ryzyko). Osoby obciążone czynnikami ryzyka (np. nadciśnienie, cukrzyca, otyłość, choroba wieńcowa, czynniki genetyczne), bez zmian strukturalnych serca i bez objawów.
- B – „Pre‑HF” (wstępna faza). Osoby ze zmianami strukturalnymi serca (np. przerost, poszerzenie jam, zaburzenia kurczliwości, choroba zastawkowa) lub z biomarkerami uszkodzenia (np. podwyższone BNP), ale bez objawów niewydolności.
- C – „Symptomatic HF” (objawowa niewydolność serca). Osoby z chorobą strukturalną serca + obecnymi lub przebyłymi objawami niewydolności; typowe przypadki niewydolności serca.
- D – „Advanced HF” (zaawansowana niewydolność). Osoby z niewydolnością oporną na standardowe leczenie — pacjent ma nasilone objawy, często nawracające hospitalizacje, znaczące pogorszenie jakości życia.
Epidemiologia
- Zapadalność i chorobowość (Niemcy):3
- zapadalność w skali roku: 655 przypadków na 100 000 osób
- chorobowość: 4%.
- Chorobowość w Polsce:4
- u dorosłych 18–79 lat wynosi 2,4%–4,3%
- to odpowiada ok. 720 000–1 200 000 rozpoznanych przypadków w populacji Polski.
- Wiek:
- częstość występowania wzrasta z wiekiem
- 65–69 lat: 7%, 80–84 lata: 24%, ≥95 lat: 47%.
- Płeć:
- choroba znacznie częściej występuje u kobiet niż u mężczyzn.
- Typ niewydolności serca:
- na podstawie danych od pacjentów hospitalizowanych zakładano, że nie występują znaczące różnice w liczbie pacjentów z obniżoną i zachowaną EF
- najnowsze dane pochodzące od pacjentów ambulatoryjnych wskazują jednak, że przeważają pacjenci z obniżoną EF:
- HFrEF 60%, HFmEF 24%, HFpEF 16%.
Etiologia
Najczęstsze przyczyny
- Choroba wieńcowa: przewlekłe niedokrwienie, stan po zawale mięśnia sercowego, tętniak komory serca.
- Nadciśnienie tętnicze, nadciśnieniowa choroba serca.
Rzadsze przyczyny
- Kardiomiopatie o innym podłożu niż niedokrwienie:
- kardiomiopatia rozstrzeniowa: zakaźne (np. wirusowe), toksyczne (np. alkohol, kokaina, leki cytostatyczne), ciąża, choroby autoimmunologiczne (np. toczeń rumieniowaty, guzkowe zapalenie tętnic - PAN, idiopatyczne, itp.)
- kardiomiopatia przerostowa
- kardiomiopatia restrykcyjna: amyloidoza, sarkoidoza, hemochromatoza i inne choroby naciekowe.
- Arytmie:
- arytmie o charakterze tachykardii i bradykardii.
- Choroby zastawek serca.
- Wrodzone wady serca (np. ubytek przegrody międzyprzedsionkowej - ASD, ubytek przegrody międzykomorowej - VSD, itp.).
- Choroby osierdzia.
- Niewydolność przeciążeniowa — High Output Failure (niedokrwienie, tyreotoksykoza, przetoki tętniczo-żylne, itp.).
Patogeneza
- Niewydolność serca jako zespół kliniczny jest końcowym etapem różnych chorób przebiegających z uszkodzeniem serca.
- Różne etiologie mogą prowadzić do tego samego fenotypu klinicznego.
- Na początku dochodzi do uszkodzenia mięśnia sercowego, np. w wyniku przeciążenia ciśnieniowego lub objętościowego albo ubytków tkanki (obumarcie kardiomiocytów).
- Mechanizmy kompensacyjne krótkookresowo poprawiają rzut serca, ale w dłuższej perspektywie prowadzą do dalszego uszkodzenia komórek i objawów niewydolności serca.
- U pacjentów z obniżoną EF zmniejsza się przede wszystkim czynność skurczowa, a tym samym objętość wyrzutowa serca.
- U pacjentów z zachowaną EF patofizjologia jest bardziej złożona i nie jest do końca wyjaśniona: w kontekście chorób podstawowych, takich jak nadciśnienie tętnicze lub cukrzyca, dochodzi do zaburzeń zwłaszcza czynności rozkurczowej (dawniej często używano więc określenia „rozkurczowa niewydolność serca”).
Czynniki predysponujące
- W badaniach epidemiologicznych określono następujące najważniejsze czynniki predysponujące:
- nadciśnienie tętnicze
- choroba wieńcowa
- cukrzyca
- palenie papierosów
- nadużywanie alkoholu
- brak aktywności fizycznej
- otyłość.
ICD-10
- I50 Niewydolność serca.
- I50.0 Niewydolność serca zastoinowa.
- I50.1 Niewydolność serca lewokomorowa.
- I50.9 Niewydolność serca, nieokreślona.
- I11 Nadciśnieniowa choroba serca.
- I11.0 Choroba nadciśnieniowa z zajęciem serca, z (zastoinową) niewydolnością serca.
Diagnostyka
- Podejrzenie niewydolności serca opiera się na wywiadzie lekarskim i wynikach badań, ale poszczególne parametry kliniczne charakteryzują się albo ograniczoną czułością, albo ograniczoną swoistością.
- Patrz tabela Podejrzenie niewydolności serca, wrażliwość i swoistość różnych obserwacji klinicznych.pdf
- Im więcej jest objawów podmiotowych i przedmiotowych, tym bardziej prawdopodobna jest niewydolność serca.
- Postawienie ostatecznego rozpoznania wymaga na ogół diagnostyki uzupełniającej.
Ogólne informacje dotyczące diagnostyki
Diagnostyka
- Pacjentów z objawami niewydolności serca należy zbadać pod kątem typowych objawów klinicznych.
- W wywiadzie lekarskim należy zapytać oraz wziąć pod uwagę wcześniejsze i współistniejące choroby, narażenia (zawodowe), rzadkie przyczyny i predyspozycje rodzinne związane z niewydolnością serca.
- Jeśli po zebraniu wywiadu i badaniu fizykalnym nadal istnieje podejrzenie niewydolności serca, należy wyjaśnić je za pomocą diagnostyki laboratoryjnej i EKG (12 odprowadzeń).
- W ramach diagnostyki wykluczającej, jeżeli będzie konieczna, należy jak najwcześniej wykonać oznaczenie BNP lub NT-proBNP.
- U wszystkich pacjentów, u których po przeprowadzeniu podstawowej diagnostyki nadal podejrzewa się niewydolność serca, należy szybko wykonać przezklatkowe badanie echokardiograficzne (ECHO).
- U pacjentów z udokumentowaną przewlekłą niewydolnością serca należy ocenić i udokumentować aktualny stan funkcjonalny z wykorzystaniem klasyfikacji NYHA.
Dalsze procedury diagnostyczne
- Pacjentów z przewlekłą niewydolnością serca należy podczas konsultacji pytać o jakość życia związaną ze zdrowiem, zarówno po rozpoznaniu, jak i regularnie w przebiegu choroby.
- Pacjentów z przewlekłą niewydolnością serca należy podczas konsultacji pytać o stres psychospołeczny i współwystępujące choroby psychiczno-psychosomatyczne, zarówno po rozpoznaniu, jak i regularnie w przebiegu choroby.
- Dalszą, szczególnie skomplikowaną i inwazyjną diagnostykę powinni koordynować lekarze rodzinni i kardiolodzy.
- Należy wziąć pod uwagę indywidualne cele terapeutyczne, zwłaszcza w przypadku pacjentów w podeszłym wieku i/lub z chorobami wielonarządowymi, a także ewentualne obciążenia spowodowane działaniami diagnostycznymi.
- Chorych należy informować o dalszych działaniach diagnostycznych i możliwych następstwach terapeutycznych (np. operacji) i należy uzyskać ich akceptację. O dalszym postępowaniu należy decydować wspólnie z pacjentem.
Kryteria diagnostyczne
- Podejrzenie rozpoznania na podstawie objawów i wyników badania przedmiotowego.
- Potwierdzenie na podstawie:
- diagnostyki laboratoryjnej (NT-proBNP lub BNP)
- echokardiografii (zaburzenia czynnościowe i/lub strukturalne).
Diagnostyka różnicowa
- Choroby płuc (astma, POChP, choroby śródmiąższowe).
- Zatorowość płucna.
- Nadciśnienie płucne.
- Nadwaga z ogólnym osłabieniem.
- Obrzęki obwodowe spowodowane przewlekłą niewydolnością żylną lub obrzęki limfatyczne.
- Niewydolność nerek.
- Zaburzenie wątroby.
- Choroby tarczycy (niedoczynność tarczycy, nadczynność tarczycy).
- Niedokrwistość.
- Zaburzenia psychiczne.
Wywiad i badanie fizykalne
Objawy niewydolności serca
- Duszność:
- podczas wysiłku lub w spoczynku (NYHA), napadowa duszność nocna.
- Obniżenie wydolności:
- wyczerpanie niewspółmierne do wysiłku, ogólne osłabienie, zmęczenie.
- Zatrzymanie płynów:
- obrzęk obwodowy, uogólniony obrzęk (anasarca), szybki przyrost masy ciała.
- Suchy kaszel:
- zwłaszcza w nocy.
- Inne objawy:
- nykturia
- zawroty głowy
- kołatanie serca
- nudności, uczucie pełności, dolegliwości w jamie brzusznej
- u pacjentów w podeszłym wieku stany splątania niejasnego pochodzenia.
Objawy kliniczne
- Poszerzenie żył szyjnych (często nie występuje).
- Przesunięte w lewo uderzenie koniuszkowe (wysoce swoisty objaw, często nie występuje).
- Osłuchowo trzeci ton serca (wysoce swoisty objaw, często nie występuje).
- Mniej swoiste objawy:
- tachykardia
- szmery nad sercem
- rzężenia płucne utrzymujące się po kaszlu
- tachypnoe
- wysięk opłucnowy
- obrzęki obwodowe
- hepatomegalia.
Historia chorób i choroby współwystępujące, narażenia
- Choroba wieńcowa, choroba tętnic obwodowych (PAD), choroby naczyń mózgowych.
- Wady serca, kardiomiopatie.
- Nadciśnienie tętnicze.
- Cukrzyca.
- POChP.
- Zaburzenia oddychania podczas snu.
- Niewydolność nerek.
- Kolagenozy.
- Choroby spichrzeniowe (np. hemochromatoza).
- Choroby endokrynologiczne (niedoczynność/nadczynność tarczycy, guz chromochłonny).
- Depresja, zaburzenia lękowe.
- Predyspozycje rodzinne.
- Alkohol, narkotyki.
- Stan po radioterapii klatki piersiowej.
- Stan po kardiotoksycznej terapii onkologicznej.
Badania uzupełniające w praktyce lekarza rodzinnego
EKG
- Wartość EKG w diagnostyce przewlekłej niewydolności serca jest bardzo ograniczona.
- Zmiany w EKG nie potwierdzają podejrzenia niewydolności serca, a prawidłowe EKG nie wyklucza niewydolności serca.
- U pacjentów z prawidłowym zapisem EKG prawdopodobieństwo przewlekłej niewydolności serca wynosi 10–14%.1
- Niemniej jednak spoczynkowe EKG jest częścią podstawowej diagnostyki, ponieważ:
- Może stanowić wskazówkę co do etiologii (np. stan po zawale mięśnia sercowego).
- Może mieć konsekwencje terapeutyczne (np. migotanie przedsionków).
- Służy jako badanie wyjściowe do monitorowania zmian w przebiegu choroby.
- Najczęściej odnotowane są:
- stan po zawale mięśnia sercowego
- zmiany sugerujące przerost lewej komory
- zaburzenia rytmu (bradykardia, tachykardia, migotanie przedsionków)
- zaburzenia przewodzenia w sercu (bloki odnóg pęczka Hisa, bloki AV).
Badanie Holter EKG
- Przy podejrzeniu zaburzeń rytmu serca.
Badania laboratoryjne
- W przypadku podejrzenia niewydolności serca zalecane są następujące badania laboratoryjne:
- Peptydy natriuretyczne (NT-proBNP lub BNP) w celu wykluczenia lub potwierdzenia podejrzenia przewlekłej niewydolności serca.
- Prawidłowe wartości peptydów natriuretycznych w dużej mierze wykluczają niewydolność serca:
- NT-proBNP <125 pg/ml, BNP <35 pg/ml.
- Wartość diagnostyczną można dodatkowo zwiększyć, jeśli zastosuje się wartości progowe zależne od wieku; dla NT-proBNP są to:
- 75 lat: 250 pg/ml.
- Jeśli wartości NT-proBNP lub BNP są prawidłowe, dalsze badania diagnostyczne (np. echokardiografia) nie są konieczne.
- Prawidłowe wartości peptydów natriuretycznych w dużej mierze wykluczają niewydolność serca:
- Dalsze parametry laboratoryjne (profil można indywidualnie zawężać lub rozszerzać):
- morfologia krwi
- elektrolity w surowicy (Na, K)
- cukier we krwi, HbA1c
- lipidogram
- białko całkowite/albumina w surowicy
- kreatynina, eGFR, mocznik, UACR
- enzymy wątrobowe
- TSH
- CRP
- ferrytyna i wysycenie transferyny (zwłaszcza po rozpoznaniu przewlekłej niewydolności serca, ponieważ niedoboru żelaza może być wskazaniem do suplementacji)
- badanie moczu.
RTG klatki piersiowej
- Ewentualnie uwidocznienie powiększenia serca, zastoju w krążeniu płucnym, wysięku opłucnowego.
- Potwierdzenie lub wykluczenie patologii płucnych.
Badanie USG
- Średnica żyły głównej dolnej i zakres zapadania klatki piersiowej w trakcie wdechu do oceny statusu objętościowego.
Spirometria
- Wykrycie lub wykluczenie płucnej etiologii duszności.
Diagnostyka specjalistyczna
- Echokardiografia przezklatkowa:
- najważniejsza metoda obrazowa w diagnostyce przewlekłej niewydolności serca:
- wielkość i kurczliwość komór, w szczególności ocena frakcji wyrzutowej lewej komory (EF)
- pomiar grubości ścian serca (przerost lewej komory, przerost prawej komory)
- ocena zastawek serca
- uwidocznienie wrodzonej wady serca (np. ASD, VSD)
- ewentualnie ilościowa ocena nadciśnienia płucnego.
- najważniejsza metoda obrazowa w diagnostyce przewlekłej niewydolności serca:
- Echokardiografia wysiłkowa (stress ECHO):
- diagnostyka niedokrwienia przy podejrzeniu choroby wieńcowej.
- Echokardiografia przezprzełykowa:
- dokładniejsze uwidocznienie wad zastawek, wrodzonych wad serca.
- Tomografia komputerowa serca (TK serca):
- wykluczenie choroby wieńcowej ze zwężeniem.
- Obrazowanie metodą rezonansu magnetycznego (RM):
- ocena mięśnia sercowego (Zapalenie mięśnia sercowego? Niedokrwienie? Choroby spichrzeniowe?).
- Scyntygrafia mięśnia sercowego:
- diagnostyka niedokrwienia przy podejrzeniu choroby wieńcowej.
- Test 6-minutowego marszu:
- ocena wydolności
- kontrola skuteczności stosowanej terapii.
- Spiroergometria:
- różnicowanie etiologii sercowej i płucnej duszności
- wartość prognostyczna.
- Koronarografia i cewnikowanie lewej komory:
- potwierdzenie choroby wieńcowej
- ocena czynności lewej komory metodą wentrykulografii.
- Cewnikowanie prawej komory:
- złoty standard ilościowej oceny nadciśnienia płucnego.
- Biopsja endomiokardium:
- wykrywanie procesów zapalnych i naciekowych (wskazane tylko gdy wynik potencjalnie wpłynie na terapię).
- Próba wysiłkowa EKG:
- ocena wydolności, zaburzeń rytmu serca wywołanych wysiłkiem fizycznym
- obecnie o drugorzędnym znaczeniu w diagnostyce niedokrwienia (niska czułość i swoistość).
Algorytm diagnostyczny
- Pacjent z objawami niewydolności serca.
- Wywiad:
- historia chorób i choroby współwystępujące
- narażenia
- predyspozycje rodzinne.
- Badanie pod kątem objawów klinicznych.
- Jeśli w dalszym ciągu występuje podejrzenie niewydolności serca:
- NT-proBNP lub BNP, dodatkowe parametry laboratoryjne
- 12-odprowadzeniowe badanie EKG.
- Jeśli w dalszym ciągu występuje podejrzenie niewydolności serca:
- W przypadku potwierdzenia niewydolności serca konieczna może być dalsza diagnostyka:
- określenie stadium i etiologii
- rozpoznanie chorób współwystępujących
- ocena rokowania
- ocena jakości życia i diagnostyka psychospołeczna.
Wskazania do skierowania do specjalisty/szpitala
- Koordynacją działań diagnostycznych, terapeutycznych i rehabilitacyjnych zajmują się lekarze rodzinni we współpracy z kardiologami i innymi specjalistami.
- Specjalistyczne badania kardiologiczne należy oferować w ramach wstępnej diagnostyki, jak również w przebiegu choroby.
- W przypadku dekompensacji serca przyjęcie do szpitala.
Leczenie
Cele leczenia
- Poprawa rokowania.
- Zapobieganie hospitalizacji.
- Łagodzenie objawów.
- Zwiększenie wydolności i poprawa jakości życia.
Ogólne informacje o leczeniu
- Opcje leczenia niewydolności serca:
- leczenie przyczynowe choroby podstawowej (np. choroby wieńcowej)
- postępowanie niefarmakologiczne:
- zmiana stylu życia
- ćwiczenia fizyczne
- edukacja, w tym nauka samokontroli objawów
- farmakoterapia:
- leki poprawiające rokowanie
- leki poprawiające objawy
- terapia z użyciem urządzeń (np. terapia resynchronizująca serca — CRT).
- W planowaniu leczenia należy uwzględnić również aspekty psychospołeczne:
- współwystępujące choroby psychiczne i psychosomatyczne
- sprawność poznawczą
- środowisko społeczne
- psychospołeczne skutki działań terapeutycznych.
- W przypadku pacjentów z wieloma chorobami współwystępującymi, koncepcję leczenia należy ustalić z uwzględnieniem wartości i preferencji pacjenta, a także perspektywy lekarza prowadzącego.
- Lekarz i pacjent powinni wspólnie podejmować decyzje dotyczące celów i sposobu prowadzenia terapii.
Leczenie przyczynowe
- Należy leczyć chorobę będącą pierwotną przyczyną niewydolności serca, biorąc pod uwagę całościowy obraz.
- Przykładowe strategie terapii ukierunkowanej na przyczynę:
- terapia hipotensyjna w nadciśnieniu tętniczym
- rewaskularyzacja mięśnia sercowego w niedokrwieniu
- leczenie interwencyjne/chirurgiczne wad zastawkowych
- leczenie arytmii w postaci tachykardii lub bradykardii.
Postępowanie niefarmakologiczne
Aktywność fizyczna
- Pacjenci z niewydolnością serca mają niską tolerancję wysiłku fizycznego, ale unikanie ćwiczeń fizycznych tylko potęguje ten stan.
- Regularna aktywność fizyczna poprawia wydolność, jakość życia i rokowanie, a także zmniejsza liczbę hospitalizacji związanych z niewydolnością serca.
- Dotyczy to zwłaszcza pacjentów z obniżoną EF (HFrEF), w przypadku pacjentów z zachowaną EF (HFpEF) dowody są słabsze.
- Komponentem treningu są ćwiczenia wytrzymałościowe, a w przebiegu choroby — również dynamiczne ćwiczenia siłowe:
- trening wytrzymałościowy to np. nordic walking, jazda na rowerze, pływanie
- dynamiczny trening siłowy charakteryzuje się częstymi powtórzeniami z użyciem małych ciężarów.
- Konkretne uzgodnienia między lekarzem a pacjentem mogą poprawić przestrzeganie zaleceń i systematyczność.
Przykładowy plan treningowy
- Faza 1: tydzień 1–2 („lekki rozruch” — „Start Low”):
- ciągły trening wytrzymałościowy:
- zakres: 5–10 minut (stopniowo zwiększać intensywność)
- częstotliwość: codziennie, także kilka razy dziennie.
- ciągły trening wytrzymałościowy:
- Faza 2: tydzień 3–4 („tylko spokojnie” — „Go Slow”):
- ciągły trening wytrzymałościowy:
- zakres: 10–15 minut (stopniowo zwiększać intensywność)
- częstotliwość: codziennie, także 2 razy dziennie.
- ciągły trening wytrzymałościowy:
- Faza 3: tydzień 5–7:
- ciągły trening wytrzymałościowy:
- zakres: 15–20 minut (stopniowo zwiększać intensywność)
- częstotliwość: codziennie
- uzupełniająco: dynamiczny trening siłowy 2 razy w tygodniu.
- ciągły trening wytrzymałościowy:
- Faza 4: tydzień 8–12:
- ciągły trening wytrzymałościowy:
- zakres: 20–30 minut (stopniowo zwiększać intensywność)
- częstotliwość: 3–4 razy w tygodniu
- uzupełniająco: dynamiczny trening siłowy 2 razy w tygodniu
- alternatywnie łączenie treningu ciągłego i interwałowego
- ciągły trening wytrzymałościowy 3 razy w tygodniu (20–30 minut), trening interwałowy 1–2 razy w tygodniu (20 minut), 1 dzień przerwy po treningu interwałowym.
- ciągły trening wytrzymałościowy:
Styl życia
- Masa ciała:
- pacjenci z niewydolnością serca i nadwagą lub łagodną otyłością mają nieco lepsze rokowanie, dokładne korelacje są wciąż niejasne
- co do zasady, nie należy zatem tym pacjentom zalecać redukcji masy ciała
- pacjentom z przewlekłą niewydolnością serca należy zalecić codzienny pomiar i zapisywanie masy ciała oraz informowanie lekarza, jeśli wystąpi u nich nietypowy, szybki wzrost masy ciała
- u objawowych pacjentów z przewlekłą niewydolnością serca należy sprawdzić, czy są w stanie samodzielnie dostosować dawkę diuretyku w oparciu o masę ciała.
- Dieta:
- brak dowodów na korzyści wynikające z zastosowania określonej diety.
- Sól:
- ograniczenie soli było kiedyś zalecane ze względów teoretycznych, ale nie ma na to dowodów naukowych
- nie należy zatem zalecać ograniczenia spożycia soli.
- Nawodnienie:
- ogólne ograniczenie podaży płynów nie jest wskazane, ale należy unikać dużego spożycia (>3 l dziennie).
- podaż płynów powinna być dostosowana do zmian masy ciała oraz czynności nerek.
- Alkohol:
- nie należy przekraczać dawek alkoholu powszechnie uznawanych za bezpieczne; w przypadkach kardiomiopatii alkoholowej konieczna jest abstynencja.
- Używanie nikotyny:
- należy zalecać abstynencję nikotynową i zapoznać pacjenta z metodami ułatwiającymi zaprzestanie palenia papierosów.
Edukacja
- Zasadniczo pacjentów należy edukować, zarówno po rozpoznaniu, jak i regularnie w trakcie trwania choroby, jednak niezbędne struktury edukacyjne są dostępne tylko w ograniczonym zakresie.
- Uporządkowane działania edukacyjne mogą obejmować następujące elementy:
- wiedza o chorobie
- samodzielne zarządzanie chorobą
- aspekty psychospołeczne
- aktywność seksualna
- postępowanie niefarmakologiczne
- farmakoterapia
- terapia inwazyjna
- specjalne formy opieki
- środki pomocnicze
- prowadzenie pojazdów mechanicznych i podróżowanie
- opieka paliatywna.
Farmakoterapia w niewydolności serca z obniżoną frakcją wyrzutową (HFrEF, HFmrEF)
Informacje ogólne
- Pacjenci są często w podeszłym wieku i obciążeni wieloma chorobami, zaleca się zatem unikanie niedociśnienia i nagłych spadków ciśnienia:
- niższe dawki początkowe i
- powolne zwiększanie dawki.
- Dane z badań dotyczą głównie pacjentów z HFrEF, ale zalecenia dotyczące leczenia mogą mieć zastosowanie u pacjentów z HFmrEF, chociaż dowody są słabsze i dlatego poziom rekomendacji jest niższy.
- Leczenie bazuje na inhibitorach ACE (alternatywnie antagonistach receptora angiotensyny, „sartanach” lub ARNI - angiotensin receptor-nephrilysin inhibitor - sakubitril/walsartan), beta-blokerach i antagonistach receptora mineralokortykoidowego oraz inhibitorach SGLT-2.
- W przypadku utrzymywania się objawów lub w określonych powiązaniach klinicznych można rozważyć zastosowanie innych substancji.
Leki poprawiające rokowanie lub objawy
- Należy odróżnić substancje poprawiające rokowanie od środków działających jedynie objawowo.
- Leki wpływające na rokowanie:
- inhibitory ACE, antagoniści receptora angiotensyny (sartany)
- beta-blokery
- antagoniści receptora mineralokortykoidowego
- inhibitory SGLT-2
- sakubitril/walsartan
- ewentualnie iwabradyna.
- Leki wpływające na objawy:
- diuretyki
- naparstnica.
Linie leczenia (terapia krok po kroku)
Leczenie podstawowe
- Inhibitory ACE powinni przyjmować wszyscy pacjenci (z niewydolnością serca stopnia I–IV według NYHA, czyli również bezobjawowi pacjenci z dysfunkcją lewej komory).
- Inhibitory ACE należy preferować w stosunku do antagonistów receptora angiotensyny („sartanów”) przede wszystkim ze względu na lepsze dowody; te ostatnie są alternatywą zwłaszcza w przypadku nietolerancji (np. kaszlu wywołanego inhibitorem ACE).
- Sakubitril/walsartan powinien być rozważany jako zamiennik dla ACEi z uwagi na lepsze dowody kliniczne w odniesienie do redukcji zgonów i częstości hospitalizacji.
- UWAGA: należy zachować 36-godzinną przerwę między odstawieniem inhibitora ACE a rozpoczęciem stosowania sakubitrilu/walsartanu (w przeciwnym razie występuje ryzyko obrzęku naczynioruchowego)!
- Mechanizm działania sakubitrilu: hamowanie aktywności enzymu neprylizyny prowadzi do ograniczenia degradacji peptydów natriuretycznych, co skutkuje działaniem moczopędnym, natriuretycznym, rozszerzającym naczynia krwionośne i antyproliferacyjnym.
- Beta-blokery należy podawać wszystkim objawowym pacjentom (z niewydolnością serca stopnia II–IV według NYHA).
- Antagonistów receptora mineralokortykoidowego należy podawać, jeśli pacjenci pozostają objawowi pomimo zalecanej terapii inhibitorami ACE i beta-blokerami.
- Ważąc korzyści i ryzyko, można je podawać także u pacjentów z cukrzycą, niewydolnością nerek lub graniczną hiperkaliemią (ścisłe monitorowanie w fazie dostosowania dawki, potem co najmniej co 4 miesiące).
- Inhibitory SGLT-2 (niezależnie od występowania cukrzycy).
- Sakubitril/walsartan (jako zamienniki inhibitorów ACE) - patrz wyżej.
- Na podstawie kryteriów klinicznych (choroby współwystępujące, profil działań niepożądanych, doświadczenie osób leczących) lub utrzymywania się objawów klinicznych pomimo skojarzonej terapii, można zaproponować również inną substancję czynną/skojarzenie substancji czynnych.
Terapia uzupełniająca w przypadku nietolerancji beta-blokerów lub częstości akcji serca ≥75 uderzeń na minutę
- Iwabradyna:
- warunki wstępne: LVEF ≤35%, stabilny rytm zatokowy, częstość akcji serca w spoczynku ≥75na minutę pomimo dawki docelowej lub maksymalnej tolerowanej dawki beta-blokera, terapia inhibitorami ACE (lub antagonistami receptora angiotensyny/sartanami) i antagonistami receptora mineralokortykoidowego.
Poprawa objawów
- Diuretyki:
- w przypadku wystąpienia objawów retencji płynów należy podać leki moczopędne (preferowane są diuretyki pętlowe).
- Glikozydy nasercowe:
- lek rezerwowy w stadium III–IV pomimo optymalnej terapii
- przy przewlekłej chorobie nerek zmniejszenie dawki podtrzymującej digoksyny lub zamiana na digitoksynę.
Zmniejszenie liczby hospitalizacji po dekompensacji
- Vericiguat:
- lek niedawno dopuszczony do stosowania
- stymulator cyklazy guanylanowej
- może być rozważany u pacjentów po niedawnej dekompensacji krążenia przy terapii podstawowej w celu zmniejszenia ryzyka ponownej hospitalizacji.
Konsekwentne zwiększanie dawki
- Dawkę inhibitorów ACE należy zwiększać w odstępach dwutygodniowych do najwyższej dawki docelowej określonej w badaniach lub do maksymalnej tolerowanej dawki.
- Beta-blokery należy miareczkować do dawki docelowej lub maksymalnie tolerowanej:
- rozpoczęcie od małej dawki początkowej
- w odstępach co najmniej dwutygodniowych
- dostosowanie do tętna (cel: częstość akcji serca: 55–60 uderzeń na minutę)
- ukierunkowanie na objawy (cel: maksymalna kontrola objawów).
- Nawet jeśli niewydolność serca nasili się w przebiegu choroby (progresja do stadium III–IV), należy w miarę możliwości utrzymać beta-blokery.
Suplementacja żelaza
- U pacjentów z niewydolnością serca często stwierdza się niedobór żelaza.
- Uzupełnienie żelaza prowadzi do poprawy wydolności i jakości życia u pacjentów z HFrEF oraz zmniejszenia ryzyka ponownej hospitalizacji.
- Dotyczy to tylko dożylnego uzupełnienia żelaza, podawanie doustne okazało się nieskuteczne.
- Dlatego też należy rozważyć dożylną suplementację żelaza (karboksymaltoza żelazowa, derizmaltoza żelazowa) przy HFrEF i niedoborze żelaza (ferrytyna i wysycenie transferyny <20%).2,5
Farmakoterapia niewydolności serca z zachowaną frakcją wyrzutową (HFpEF)
- Do niedawna nie było żadnej terapii o potwierdzonej skuteczności pod względem poprawy rokowania u pacjentów z HFpEF.
- Terapia była więc ograniczona do:
- leczenia podstawowych chorób kardiologicznych i niekardiologicznych
- leczenia czynników ryzyka sercowo-naczyniowego
- leczenia moczopędnego w przypadku objawów przeciążenia płynami
- Aktualnie inhibitory SGLT-2 (empagliflozyna, dapagliflozyna) są pierwszą opcją leczenia HFpEF o korzystnym wpływie na rokowanie, z redukcją śmiertelności i hospitalizacji z przyczyn sercowo-naczyniowych.2,5
Leki o potencjalnym niekorzystnym wpływie na niewydolność serca
- Wskazania do stosowania leków, które mogą nasilić niewydolność serca, należy szczególnie krytyczne i regularnie weryfikować w trakcie leczenia. Zalicza się do nich:
- NLPZ:
- nieselektywne NLPZ
- selektywne inhibitory COX-2 (koksyby).
- Leki przeciwcukrzycowe:
- metformina (zwiększone ryzyko kwasicy mleczanowej przy zdekompensowanej niewydolności serca)
- inhibitory DPP4 (gliptyny): zwiększone ryzyko hospitalizacji podczas stosowania saksagliptyny.
- Leki przeciwarytmiczne:
- klasy I: flekainid, propafenon
- klasy III: dronedaron, sotalol.
- Leki hipotensyjne:
- antagoniści kanału wapniowego: werapamil, diltiazem, nifedypina
- agoniści receptorów alfa-2: moksonidyna
- leki rozszerzające naczynia obwodowe: dihydralazyna, minoksydyl.
- Leki przeciwpadaczkowe:
- karbamazepina
- pregabalina.
- Leki przeciwdepresyjne, leki przeciwpsychotyczne:
- trójpierścieniowe leki przeciwdepresyjne (TCA)
- citalopram, escitalopram (także fluoksetyna, wenlafaksyna i inne)
- lit
- klozapina.
- Leki urologiczne:
- blokery receptorów alfa-1 (doksazosyna, tamsulozyna, terazosyna).
Dawkowanie powszechnie stosowanych leków
- Zalecenia dotyczą przede wszystkim pacjentów z obniżoną frakcją wyrzutową lewej komory (HFrEF).
- Brak badań, które dotyczyłyby wyłącznie pacjentów z pośrednią frakcją wyrzutową (HFmrEF), ale zasadniczo można powielić schemat leczenia HFrEF.
Inhibitory ACE
- Ramipryl: dawka początkowa 1,25 mg 1 x na dobę, dawka docelowa 10 mg 1 x na dobę.
- Enalapryl: dawka początkowa 2,5 mg 1 x na dobę, dawka docelowa 20 mg 1 x na dobę.
- Lizynopryl: dawka początkowa 2,5 mg 1 x na dobę, dawka docelowa 20 mg 1 x na dobę.
- Perindopryl: dawka początkowa 2,5 mg 1 x na dobę, dawka docelowa 5 mg 1 x na dobę.
- Fozynopryl: dawka początkowa 10 mg 1 x na dobę, dawka docelowa 40 mg 1 x na dobę.
- Kaptopryl: dawka początkowa 6,25 mg 3 x na dobę, dawka docelowa 25–50 mg 3 x na dobę.
Antagoniści receptora angiotensyny („sartany”)
- Kandesartan: dawka początkowa 4 mg 1 x na dobę, dawka docelowa 32 mg 1 x na dobę.
- Losartan: dawka początkowa 12,5 mg 1 x na dobę, dawka docelowa 150 mg 1 x na dobę.
- Walsartan: dawka początkowa 40 mg 2 x na dobę, dawka docelowa 160 mg 2 x na dobę.
Beta-blokery
- Bursztynian metoprololu: dawka początkowa 23,75 mg 1 x na dobę, dawka docelowa 190 mg 1 x na dobę.
- Bisoprolol: dawka początkowa 1,25 mg 1 x na dobę, dawka docelowa 10 mg 1 x na dobę.
- Karwedilol: dawka początkowa 3,125 mg 2 x na dobę, dawka docelowa 25 mg 2 x na dobę.
- Nebiwolol: dawka początkowa 1,25 mg 1 x na dobę, dawka docelowa 10 mg 1 x na dobę.
Antagoniści receptora mineralokortykoidowego
- Eplerenon: 12,5–50 mg 1 x na dobę.
- Spironolakton: 12,5–50 mg 1 x na dobę.
Antagonista receptora angiotensyny II oraz inhibitor neprylizyny (ARNI)
- Sakubitril/walsartan: dawka początkowa 49/51 mg 2 x na dobę, zwiększać co 2–4 tygodnie do dawki docelowej 97/103 mg 2 x na dobę.
- UWAGA: Leczenie sakubitrilem/walsartanem można rozpocząć nie wcześniej niż 36 godzin po odstawieniu inhibitora ACE, w przeciwnym razie istnieje ryzyko obrzęku naczynioruchowego!
Inhibitory SGLT-2
- Dapagliflozyna: 10 mg 1 x na dobę.
- Empagliflozyna: 10 mg 1 x na dobę.
Diuretyki
- Dawkowanie diuretyków (pętlowych) w zależności od objawów i czynności nerek:
Inne substancje
- Iwabradyna:
- dawka początkowa 5 mg 2 x na dobę (u osób >70. roku życia można zacząć od dawki 2,5 mg 2 x na dobę), dawka docelowa 7,5 mg 2 x na dobę.
- Vericiguat:
- dawka początkowa 2,5 mg 1 x na dobę, dawka docelowa 10 mg 1 x na dobę.
- Preparaty naparstnicy:
- digitoksyna: dawka nasycająca zgodnie z charakterystyką produktu leczniczego, dawka docelowa 0,07–1,0 mg 1 x na dobę
- digoksyna: dawka nasycająca zgodnie z charakterystyką produktu leczniczego, dawka docelowa ok. 0,2–0,3 mg 1 raz na dobę (regularne kontrole stężenia, stężenie docelowe <1,2 ng/ml).
Terapia inwazyjna
Terapia resynchronizująca serca (CRT - cardiac resynchronization therapy)
- U około 1/3 pacjentów z HFrEF klasy III–IV wg NYHA występuje dyssynchronia kurczliwości serca (pogorszenie efektywności skurczu serca).
- W porównaniu z samą farmakoterapią, CRT w dyssynchronii prowadzi do poprawy rokowania i objawów:
- niższa śmiertelność
- mniejsza liczba hospitalizacji
- lepsza wydolność
- lepsza jakość życia.
- Najlepsza reakcja na CRT („responder”), jeżeli występuje:
- blok lewej odnogi pęczka Hisa (LBBB)
- szeroki zespół QRS
- u kobiet
- kardiomiopatia o innym podłożu niż niedokrwienie.
- CRT należy zaproponować objawowym pacjentom (NYHA II–IV), którzy spełniają następujące kryteria6:
- zmniejszona EF ≤35% pomimo optymalnej farmakoterapii
- rytm zatokowy
- blok lewej odnogi pęczka Hisa (LBBB)
- zespół QRS ≥130 ms.
- Jeśli spełnione są kryteria zarówno dla CRT, jak i ICD, można rozważyć zastosowanie układu CRT-ICD.
Wszczepialny kardiowerter-defibrylator (ICD - implantable cardioverter-defibrillator)
- ICD zapobiega nagłemu zgonowi sercowemu w arytmii komorowej poprzez wysłanie impulsu elektrycznego (lub stymulacji antytachyarytmicznej).
- ICD nie jest stosowany celem zapobiegania progresji niewydolności serca, w przypadku której może być wymagane zastosowanie układu CRT-ICD.
- Profilaktyka wtórna:
- ICD zaleca się po przebytym nagłym zgonie sercowym lub w przypadku utrzymującego się, stabilnego hemodynamicznie częstoskurczu komorowego.
- Profilaktyka pierwotna:
- ICD zaleca się pacjentom z kardiomiopatią niedokrwienną, którzy spełniają następujące kryteria:
- niewydolność serca klasy II–III według NYHA
- LVEF ≤35% pomimo optymalnej farmakoterapii
- oczekiwana dalsza długość życia >1 roku
- w kardiomiopatii o innym podłożu niż niedokrwienie — w tym wskazaniu dostępnych jest mniej pewnych dowodów, indywidualne wskazania przez specjalistów.
- ICD zaleca się pacjentom z kardiomiopatią niedokrwienną, którzy spełniają następujące kryteria:
Inne terapie inwazyjne
- Rewaskularyzacja mięśnia sercowego:
- decyzja o rewaskularyzacji mięśnia sercowego (operacja wszczepienia bypassów lub PCI) zależy od stwierdzenia niedokrwienia mięśnia sercowego.
- Wady zastawek:
- leczenie zgodne z wytycznymi niezależnie od stopnia niewydolności serca.
- Urządzenia wspomagające pracę serca/przeszczep serca:
- u pacjentów, u których mimo optymalnej terapii lekami i CRT/ICD występują ciężkie objawy, można rozważyć zastosowanie urządzenia wspomagającego pracę serca
- wskazanie to należy rozważyć odpowiednio wcześnie, zanim dojdzie do poważnych zaburzeń czynności narządu
- urządzenie wspomagające pracę serca może pomóc przeczekać czas do przeszczepu serca w schyłkowej niewydolności serca (bridge-to-transplant).
Leczenie uzupełniające/alternatywne
- Nie należy stosować innych suplementów leczniczych ani suplementów diety, np. wyciągu z głogu, koenzymu Q10, migdałecznika chebułowca, karnityny, kwasów tłuszczowych omega-3, tauryny, witamin (z wyjątkiem przypadków niedoboru).
Szczepienia
- Szczepienie przeciwko grypie należy wykonywać co roku.
- Należy przeprowadzić profilaktyczne szczepienia przeciwko pneumokokom.
- Szczepienie przeciwko COVID szczepionkami z mRNA jest bezpieczne dla pacjentów z przewlekłą niewydolnością serca.
Rehabilitacja
- W warunkach ambulatoryjnych należy skierować pacjenta na rehabilitację, jeżeli:
- choroba podstawowa ulega przewlekłemu nasileniu, a objawy (duszność, retencja płynów) są trudne do opanowania
- choroby współwystępujące, takie jak cukrzyca, nadciśnienie tętnicze lub niewydolność nerek przewlekle nasilają się i są trudne do ustabilizowania
- pacjent powinien rozpocząć terapię opartą na treningu, która początkowo wymaga monitorowania.
- istnieje szczególne zapotrzebowanie na edukację/interwencje w zakresie stylu życia
- pacjent wymaga pomocy psychokardiologicznej, aby nauczyć się radzić sobie z chorobą i/lub osiągnąć stabilizację psychiczną
- istnieje perspektywa ustabilizowania lub większego zaangażowania w życie społeczne i/lub zawodowe.
- O skierowaniu na rehabilitację i rodzaju rehabilitacji (ambulatoryjna czy stacjonarna) należy zdecydować na podstawie aspektów medycznych i psychospołecznych, a także preferencji pacjenta i dostępności odpowiednich placówek.
Opieka paliatywna
- Opieka paliatywna ma na celu zachowanie jak najlepszej jakości życia chorych i ich bliskich.
- Pacjentom z przewlekłą niewydolnością serca należy wcześnie zaproponować omówienie możliwych przebiegów choroby i scenariuszy kryzysowych.
- Elementami składowymi opieki paliatywnej są:
- wczesne wykrywanie objawów i obciążeń wskazujących na konieczność opieki paliatywnej
- wskazanie pożądanego postępowania
- w przypadku niezdolności do wyrażenia zgody — wyznaczenie osoby upoważnionej.
- Jeżeli pacjent umiera, należy zaprzestać lub nie rozpoczynać działań, które nie służą osiągnięciu celu, jakim jest jak najlepsza jakość życia.
Przebieg, powikłania i rokowanie
Powikłania
- Arytmia, nagły zgon sercowy.
- Wstrząs kardiogenny.
- Obrzęk płuc.
- Zdarzenia zakrzepowo-zatorowe.
Przebieg i rokowanie
Śmiertelność
- Przed rokiem 1990, a więc przed pojawieniem się nowoczesnej terapii niewydolności serca, śmiertelność 5-letnia wynosiła 60–70%.
- Jednak mimo znacznej redukcji wskaźników śmiertelności dzięki nowym metodom leczenia, śmiertelność 5-letnia jest nadal bardzo wysoka i wynosi 40–50%.7
- W zależności od ciężkości niewydolności serca śmiertelność jednoroczna wynosi:
- NYHA I: 5–10%
- NYHA II–III: 15–30%
- NYHA IV: 50%.
- W zaawansowanej niewydolności serca (NYHA IV) śmiertelność jest wyższa niż w większości nowotworów litych.
Hospitalizacja
- Chorzy z niewydolnością serca są hospitalizowani średnio 2 razy w roku.
- Około 1/4 pacjentów jest ponownie hospitalizowana w ciągu 30 dni od wypisu.
- Każda hospitalizacja pogarsza rokowanie, a z każdą hospitalizacją zmniejsza się czas do kolejnej rehospitalizacji.
Dalsze postępowanie
- Należy regularnie sprawdzać:
- wydolność funkcjonalną (klasa według NYHA)
- masę ciała i stan nawodnienia
- ciśnienie tętnicze, częstość akcji serca, rytm
- równowagę elektrolitową i czynność nerek
- leki
- funkcjonowanie w dniu codziennym, status psychospołeczny i jakość życia
- przestrzeganie zaleceń.
- Nie należy oznaczać peptydów natriuretycznych (NT-proNBP lub BNP) bez klinicznego podejrzenia pogorszenia stanu zdrowia.
- Pacjenci powinni codziennie mierzyć i dokumentować masę ciała, a jeśli w krótkim czasie ich masa ciała wzrośnie, powinni:
- skonsultować się z lekarzem prowadzącym lub
- samodzielnie dostosować dawkę diuretyku stosownie do wskazań.
- Wartości referencyjne dla potrzeby zwiększenia dawki leków moczopędnych:
- wzrost masy ciała o >1 kg w ciągu nocy lub
- wzrost masy ciała o >2 kg w ciągu 3 dni lub
- wzrost masy ciała o >2,5 kg w ciągu tygodnia.
Informacje dla pacjentów
Materiały edukacyjne dla pacjentów
Ilustracje
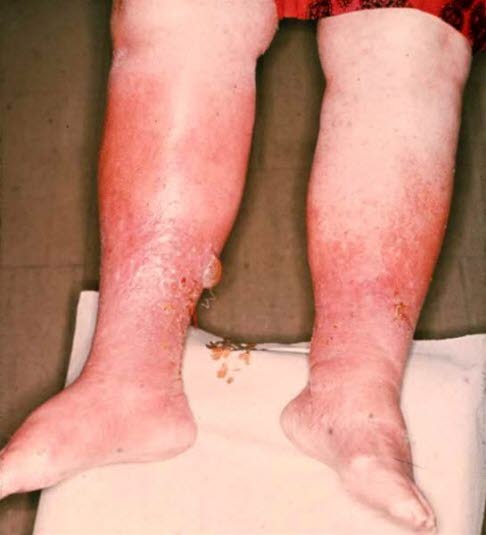
Obrzęki kończyn dolnych
Szmery w sercu: rytm galopujący
Źródła
Wytyczne
-
Chopra V, Khan MS, Abdelhamid M, et al. iCARDIO Alliance Global Implementation Guidelines on Heart Failure 2025. Heart Lung Circ. 2025 Jul;34(7):e55-e82. PubMed
- McDonagh TA, Metra M, Adamo M. et al. ESC Scientific Document Group. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2021; 42: 3599-726. PubMed
- McDonagh TA, Metra M, Adamo M i wsp.; ESC Scientific Document Group. 2023 Focused update of the 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2023 Oct 1;44(37): 3627-39. PubMed
- Nessler J, Windak A, Mastalerz-Migas A. et al. Zasady postepowania w niewydolności serca. Wytyczne Kolegium Lekarzy Rodzinnych w Polsce, Asocjacji Niewydolności Serca Polskiego Towarzystwa Kardiologicznego i Polskiego Towarzystwa Medycyny Rodzinnej. Lekarz Rodzinny, wydanie specjalne 1/2022. (dostęp 10.02.2024) klrwp.pl
- European Society of Cardiology (Europejskie Towarzystwo Kardiologiczne, ESC). Guidelines for the diagnosis and treatment of acute and chronic heart failure (Wytyczne dotyczące diagnostyki i leczenia ostrej i przewlekłej niewydolności serca.). Stan z 2021 roku. academic.oup.com
- European Society of Cardiology (Europejskie Towarzystwo Kardiologiczne, ESC). Guidelines on cardiac pacing and cardiac resynchronization therapy (Wytyczne stymulacji serca i terapii resynchronizującej serca). Stan z 2021 roku. academic.oup.com
- American College of Cardiology/American Heart Association (Amerykańskie Kolegium Kardiologiczne/Amerykańskie Stowarzyszenie Kardiologiczne). Guideline for the Management of Heart Failure (Wytyczne postępowania w niewydolności serca). Stan z 2022 roku. ahajournals.org
Piśmiennictwo
- McDonagh TA, Metra M, Adamo M, et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2021: ehab368. PMID: 34447992 PubMed
- American College of Cardiology/American Heart Association. Guideline for the Management of Heart Failure. Stand 2022. www.ahajournals.org
- Störk S, Handrock R, Jacob J, et al. Epidemiology of heart failure in Germany: a retrospective database study. Clin Res Cardiol 2017; 106: 913-22. PMID: 28748265 PubMed
- Puch-Walczak A, Bandosz P, Grodzicki T, et al. Prevalence of self‑reported heart failure in the adult Polish population: results of the NATPOL 2011 study. Pol Arch Intern Med. 2022 Apr 28;132(4):16184. pubmed.ncbi.nlm.nih.gov
- Anker SD, Butler J, Filippatos G, et al. Empagliflozin in Heart Failure with a Preserved Ejection Fraction. N Engl J Med 2021; 14; 385: 1451-61. pubmed.ncbi.nlm.nih.gov
- European Society of Cardiology. Guidelines on cardiac pacing and cardiac resynchronization therapy. Stand 2021. academic.oup.com
- Dumitru I. Heart Failure. Medscape, updated July 02,2022. emedicine.medscape.com
Opracowanie
- Prof. dr hab. med. Tomasz Tomasik, recenzent
- Sławomir Chlabicz (redaktor)
- Jadwiga Nessler (recenzent)
- Adam Windak (redaktor)
- Michael Handke (recenzent/redaktor)
