Czym jest choroba nowotworowa górnych dróg moczowych?
Definicja
Rak górnych dróg moczowych, nazywany inaczej rakiem przejściowokomórkowym, to nowotwór złośliwy wywodzący się z komórek błony śluzowej (nabłonka przejściowego, urotelium) górnych dróg moczowych.
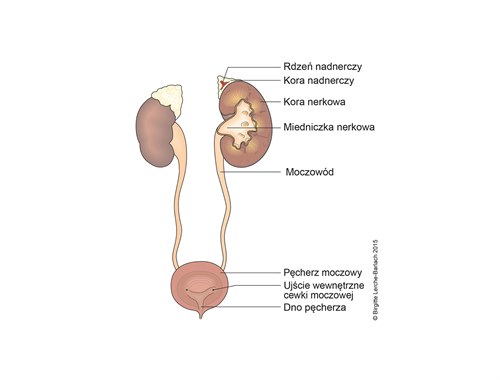
Urotelium wyściela wnętrze miedniczki nerkowej, moczowodu i pęcherza, aż do cewki moczowej.
Górne drogi moczowe składają się z dwóch miedniczek nerkowych (część nerki, w której zbiera się mocz) i dwóch moczowodów, którymi mocz z miedniczki nerkowej przedostaje się do pęcherza moczowego. Nerki znajdują się obustronnie w jamie brzusznej poniżej przepony. Pęcherz moczowy znajduje się w miednicy.
Guzy przejściowokomórkowe rosną brodawkowato, czyli przybierają postać małych wyrostków („brodawek”) i mogą wrastać bezpośrednio w miąższ nerki i przyległe do niej struktury lub rozprzestrzeniać się poprzez drobne naczynia krwionośne, przewody limfatyczne lub razem z moczem i tworzyć przerzuty w innych narządach.
Objawy
Objawami tych nowotworów są przede wszystkim krew w moczu (towarzyszy 80% przypadków) i dolegliwości bólowe zlokalizowane po bocznej stronie pleców lub w miednicy (ok. 20% osób dotkniętych uskarża się na bóle w boku).
U części pacjentów występują objawy i dolegliwości związane z zaawansowaną chorobą, takie jak utrata masy ciała, utrata apetytu, bóle kostne czy zatrzymanie wody w jamie brzusznej (wodobrzusze).
Należy wykluczyć inne choroby, które mogą powodować podobne objawy:
- Infekcja dróg moczowych u kobiet oraz mężczyzn
- Kamica nerkowa
- Rak nerki
- Zwężenie moczowodu.
Przyczyny
Największym czynnikiem ryzyka wystąpienia raka urotelialnego i przyczyną 70% przypadków tej choroby u mężczyzn i 40% przypadków u kobiet jest palenie tytoniu.
Do pozostałych czynników ryzyka należy przyjmowanie kwasów arystocholowych (często występujących w tradycyjnych lekach ziołowych pochodzących z Azji).
Osoby z zespołem Lyncha (dziedziczna forma raka jelita) również mają zwiększone ryzyko rozwoju nowotworów górnych dróg moczowych.
Częstotliwość występowania
- Liczba nowych zachorowań w ciągu roku wynosi 2 na 100 000 osób.
- Najczęściej chorują osoby ok. 70. roku życia.
- U mężczyzn do zachorowania dochodzi dwa do trzech razy częściej niż u kobiet.
Badania
W przypadku podejrzenia raka górnych dróg moczowych mocz bada się pod kątem śladowych ilości krwi niewidocznych gołym okiem (mikrohematuria) oraz wykonuje się badanie ultrasonograficzne pęcherza i nerek. Jeśli stwierdzone zostaną nieprawidłowości, wykonuje się diagnostykę obrazową, a badaniem z wyboru jest tomografia komputerowa nerek i dróg moczowych. Badanie przeprowadza się z użyciem środka kontrastującego lub bez niego (jest to substancja wstrzykiwana do krwiobiegu w celu ułatwienia dostrzeżenia dobrze unaczynionych zmian w trakcie diagnostyki obrazowej). Alternatywnie można wykonać obrazowanie metodą rezonansu magnetycznego.
Kolejną metodą diagnostyczną jest endoskopia pęcherza moczowego i moczowodu do wysokości miedniczki nerkowej. Podczas tego badania można pobrać próbkę tkanki z guza. Rozpoznanie jest stawiane na podstawie zbadania po mikroskopem (histopatologicznego) próbki tkanki (czyli biopsji) z nacieku raka.
Po przeprowadzeniu wszystkich koniecznych badań wskazywana jest odpowiednia metoda leczenia.
Postępowanie
Celem terapii w przypadku guza ograniczonego do jednego narządu jest całkowite wyleczenie. Jeśli nowotwór zdążył się rozprzestrzenić, leczenie będzie mieć na celu łagodzenie objawów choroby (leczenie paliatywne).
Forma leczenia zależy od stadium rozprzestrzenienia się choroby oraz stopnia agresywności nowotworu. Główne leczenie polega na chirurgicznym usunięciu nerki, moczowodu i niewielkiej części pęcherza moczowego w miejscu, w którym łączy się z moczowodem – po odpowiedniej stronie. W mniej zaawansowanych przypadkach choroby możliwe jest częściowe usunięcie guza, tak aby oszczędzić nerkę.
Leczenie endoskopowe
U niektórych pacjentów można przeprowadzić tzw. leczenie endoskopowe. Jest to operacja małoinwazyjna, czyli taka, w której ingerencja chirurgiczna ma znacznie mniejszy zakres, a guz usuwany jest za pomocą lasera. Jednak w przypadku tej formy leczenia rośnie prawdopodobieństwo nawrotu nowotworu.
Chemioterapia
Według badań, przeprowadzenie chemioterapii przed operacją daje dobre wyniki, zwłaszcza w przypadku nowotworów agresywnych, w ich przypadku udaje się w dużym stopniu ograniczyć ponowny wzrost guza. Chemioterapia wdrożona po operacji jest stosowana w celu leczenia obszarów, do których nowotwór już się rozprzestrzenił (przerzutów odległych).
Jako dodatkowe leczenie, można również rozważyć wstrzyknięcie miejscowo działających leków chemioterapeutycznych do pęcherza moczowego. Obniża się dzięki temu ryzyko pojawienia się nowotworów wtórnych (czyli nowotworów innego rodzaju niż guz pierwotny, które pojawiają się po upływie co najmniej dwóch miesięcy po zakończeniu terapii).
Terapia immunologiczna
Po chemioterapii może zostać wdrożona terapia immunologiczna. Aktywuje ona własne komórki odpornościowe organizmu, które są blokowane przez komórki nowotworowe. Immunoterapia znosi tę blokadę, dzięki czemu komórki odpornościowe mogą skuteczniej rozpoznawać i zwalczać komórki nowotworowe.
Radioterapia i zabieg chirurgiczny
Korzyści z radioterapii w raku górnych dróg moczowych są dyskusyjne. Niektóre badania wskazują na to, że radioterapia jest skuteczna jako leczenie dodatkowe obok zabiegu operacyjnego, a także jako leczenie paliatywne w przypadku nowotworów nieoperacyjnych.
U pacjentów w zaawansowanym wieku i w przypadku współwystępowania poważnych chorób towarzyszących, rozległa interwencja chirurgiczna może być zbyt dużym obciążeniem dla organizmu, dlatego plan leczenia (operacja, chemioterapia, radioterapia itd.), dobiera się indywidualnie. Interwencje te zazwyczaj służą jedynie złagodzeniu objawów, a nie leczeniu choroby.
Rokowania
W większości przypadków wymagana jest interwencja chirurgiczna o szerokim zakresie, aby zapobiec postępowaniu nowotworu. Rokowanie w przypadku raka urotelialnego górnych dróg moczowych w dużej mierze zależy od stopnia zaawansowania nowotworu (czyli tego, jak duży jest guz i ile narządów oraz węzłów chłonnych zajął).
Palenie tytoniu i zaawansowany wiek wiążą się z gorszymi rokowaniami.
W korzystnym przypadku, przy niewielkim rozmiarze guza i przy braku zajętych przez nowotwór węzłów chłonnych, przeżywalność 5-letnia wynosi około 86%.
Dodatkowe informacje
- Palenie szkodzi zdrowiu
- Rak urotelialny górnych dróg moczowych – informacje dla lekarzy
Autorka
- Susanna Allahwerde, specjalistka ds. medycyny ogólnej, Berlin
- Anna Zwierzchowska, lekarz rezydent, Kraków (edytor/recenzent)
Link lists
Authors
Previous authors
Updates
Gallery
Snomed
References
Based on professional document Guzy urotelialne górnych dróg moczowych. References are shown below.
- Siegel RL, Miller KD, Fuchs HE, Jemal A. Cancer Statistics, 2021. CA Cancer J Clin. 2021 Jan;71(1):7-33. pubmed.ncbi.nlm.nih.gov
- Cosentino M, Palou J, Gaya JM, et al. Upper urinary tract urothelial cell carcinoma: location as a predictive factor for concomitant bladder carcinoma. World J Urol. 2013 Feb;31(1):141-5. pubmed.ncbi.nlm.nih.gov
- Soria F, Shariat SF, Lerner SP, Fritsche HM, Rink M, Kassouf W, Spiess PE, Lotan Y, Ye D, Fernández MI, Kikuchi E, Chade DC, Babjuk M, Grollman AP, Thalmann GN. Epidemiology, diagnosis, preoperative evaluation and prognostic assessment of upper-tract urothelial carcinoma (UTUC). World J Urol. 2017 Mar;35(3):379-387. pubmed.ncbi.nlm.nih.gov
- Rouprêt M, Babjuk M, Burger M, et al. European Association of Urology Guidelines on Upper Urinary Tract Urothelial Carcinoma: 2020 Update. Eur Urol. 2021 Jan;79(1):62-79. pubmed.ncbi.nlm.nih.gov
- Xylinas E, Kluth LA, Rieken M, Lee RK, Elghouayel M, Ficarra V, Margulis V, Lotan Y, Rouprêt M, et al. Impact of smoking status and cumulative exposure on intravesical recurrence of upper tract urothelial carcinoma after radical nephroureterectomy. BJU Int. 2014 Jul;114(1):56-61. pubmed.ncbi.nlm.nih.gov
- Rink M, Xylinas E, Margulis V, Cha EK, Ehdaie B, Raman JD, Chun FK, Matsumoto K, Lotan Y, et a. Impact of smoking on oncologic outcomes of upper tract urothelial carcinoma after radical nephroureterectomy. Eur Urol. 2013 Jun;63(6):1082-90. pubmed.ncbi.nlm.nih.gov
- Ju JY, Mills AM, Mahadevan MS, et al. Universal Lynch Syndrome Screening Should be Performed in All Upper Tract Urothelial Carcinomas. Am J Surg Pathol. 2018 Nov;42(11):1549-1555. pubmed.ncbi.nlm.nih.gov
- Brierley, J.D., et al. TNM Classification of Malignant Tumours. 8th ed. 2016. www.uicc.org
- Cowan NC. CT urography for hematuria. Nat Rev Urol. 2012 Mar 13;9(4):218-26. pubmed.ncbi.nlm.nih.gov
- Margulis V, Shariat SF, Matin SF, et al. Outcomes of radical nephroureterectomy: a series from the Upper Tract Urothelial Carcinoma Collaboration. Cancer. 2009 Mar 15;115(6):1224-33. pubmed.ncbi.nlm.nih.gov
- Takahashi N, Glockner JF, Hartman RP, et al. Gadolinium enhanced magnetic resonance urography for upper urinary tract malignancy. J Urol. 2010 Apr;183(4):1330-65. pubmed.ncbi.nlm.nih.gov
- Millán-Rodríguez F, Palou J, de la Torre-Holguera P, Vayreda-Martija JM, Villavicencio-Mavrich H, Vicente-Rodríguez J. Conventional CT signs in staging transitional cell tumors of the upper urinary tract. Eur Urol. 1999 Apr;35(4):318-22. pubmed.ncbi.nlm.nih.gov
- Malm C, Grahn A, Jaremko G, Tribukait B, Brehmer M. Diagnostic accuracy of upper tract urothelial carcinoma: how samples are collected matters. Scand J Urol. 2017 Apr;51(2):137-145. pubmed.ncbi.nlm.nih.gov
- Witjes JA, Redorta JP, Jacqmin D, et al. Hexaminolevulinate-guided fluorescence cystoscopy in the diagnosis and follow-up of patients with non-muscle-invasive bladder cancer: review of the evidence and recommendations. Eur Urol. 2010 Apr;57(4):607-14. pubmed.ncbi.nlm.nih.gov
- Lee KS, Zeikus E, DeWolf WC, Rofsky NM, Pedrosa I. MR urography versus retrograde pyelography/ureteroscopy for the exclusion of upper urinary tract malignancy. Clin Radiol. 2010 Mar;65(3):185-92. pubmed.ncbi.nlm.nih.gov
- Seisen T, Peyronnet B, Dominguez-Escrig JL, et al. Oncologic Outcomes of Kidney-sparing Surgery Versus Radical Nephroureterectomy for Upper Tract Urothelial Carcinoma: A Systematic Review by the EAU Non-muscle Invasive Bladder Cancer Guidelines Panel. Eur Urol. 2016 Dec;70(6):1052-1068. pubmed.ncbi.nlm.nih.gov
- Raman J, Shore ND. Management of Low-grade Upper Tract Urothelial Carcinoma: An Unmet Need. Rev Urol. 2020;22(1):1-8. www.ncbi.nlm.nih.gov
- Clements MB, Krupski TL, Culp SH. Robotic-Assisted Surgery for Upper Tract Urothelial Carcinoma: A Comparative Survival Analysis. Ann Surg Oncol. 2018 Sep;25(9):2550-2562. pubmed.ncbi.nlm.nih.gov
- Dominguez-Escrig JL, Peyronnet B, Seisen T, Bruins HM, et al. Potential Benefit of Lymph Node Dissection During Radical Nephroureterectomy for Upper Tract Urothelial Carcinoma: A Systematic Review by the European Association of Urology Guidelines Panel on Non-muscle-invasive Bladder Cancer. Eur Urol Focus. 2019 Mar;5(2):224-241. pubmed.ncbi.nlm.nih.gov
- Baard J, Cormio L, Cavadas V, et al. Contemporary patterns of presentation, diagnostics and management of upper tract urothelial cancer in 101 centres: the Clinical Research Office of the Endourological Society Global upper tract urothelial carcinoma registry. Curr Opin Urol. 2021 Jul 1;31(4):354-362. pubmed.ncbi.nlm.nih.gov
- Cutress ML, Stewart GD, Wells-Cole S, Phipps S, et al. Long-term endoscopic management of upper tract urothelial carcinoma: 20-year single-centre experience. BJU Int. 2012 Dec;110(11):1608-17. pubmed.ncbi.nlm.nih.gov
- Remzi M, Schwentner C, Shariat S, Grubmüller B. Urothelkarzinom der Nieren und Harnleiter: Therapie. In: Die Urologie. Hrsg: Michel MS, Thüroff JW, Janetschek G, Wirth M. Springer-Verlag, 1. Aufl. 2016. 409-430.
- Gallioli A, Boissier R, Territo A, Vila Reyes H, et al. Adjuvant Single-Dose Upper Urinary Tract Instillation of Mitomycin C After Therapeutic Ureteroscopy for Upper Tract Urothelial Carcinoma: A Single-Centre Prospective Non-Randomized Trial. J Endourol. 2020 May;34(5):573-580. pubmed.ncbi.nlm.nih.gov
- Giannarini G, Kessler TM, Birkhäuser FD, et al. Antegrade perfusion with bacillus Calmette-Guérin in patients with non-muscle-invasive urothelial carcinoma of the upper urinary tract: who may benefit? Eur Urol. 2011 Nov;60(5):955-60. pubmed.ncbi.nlm.nih.gov
- Powles T, Csőszi T, Özgüroğlu M, et al. Pembrolizumab alone or combined with chemotherapy versus chemotherapy as first-line therapy for advanced urothelial carcinoma (KEYNOTE-361): a randomised, open-label, phase 3 trial. Lancet Oncol. 2021 Jul;22(7):931-945. pubmed.ncbi.nlm.nih.gov
- Huang YC, Chang YH, Chiu KH, Shindel AW, Lai CH. Adjuvant radiotherapy for locally advanced upper tract urothelial carcinoma. Sci Rep. 2016 Dec 2;6:38175. pubmed.ncbi.nlm.nih.gov
- Iwata T, Kimura S, Abufaraj M, Janisch F, et al. The role of adjuvant radiotherapy after surgery for upper and lower urinary tract urothelial carcinoma: A systematic review. Urol Oncol. 2019 Oct;37(10):659-671 pubmed.ncbi.nlm.nih.gov
- Abe T, Shinohara N, Harabayashi T, et al. Impact of multimodal treatment on survival in patients with metastatic urothelial cancer. Eur Urol. 2007 Oct;52(4):1106-13. pubmed.ncbi.nlm.nih.gov
- Rouprêt M, Babjuk M, Burger M, et al. EAU Guidelines on Upper Urinary Tract Urothelial Carcinoma. Limited Update 2022. https://uroweb.org/guidelines. Letzte Suche am 29.03.2022. uroweb.org
- Tomita Y, Yamamoto Y, Tsuchiya N, et al. Avelumab first-line maintenance plus best supportive care (BSC) vs BSC alone for advanced urothelial carcinoma: JAVELIN Bladder 100 Japanese subgroup analysis. Int J Clin Oncol. 2022 Feb;27(2):383-395. pubmed.ncbi.nlm.nih.gov
- Bellmunt J, de Wit R, Vaughn DJ, et al. Pembrolizumab as Second-Line Therapy for Advanced Urothelial Carcinoma. N Engl J Med. 2017 Mar 16;376(11):1015-1026. pubmed.ncbi.nlm.nih.gov
- Lemke E, Sahasrabudhe D, Guancial E, et al. The Role of Metastasectomy in Urothelial Carcinoma: Where Are We in 2020? Clin Genitourin Cancer. 2020 Aug;18(4):e478-e483. pubmed.ncbi.nlm.nih.gov
- Simsir A, Sarsik B, Cureklibatir I, Sen S, Gunaydin G, Cal C. Prognostic factors for upper urinary tract urothelial carcinomas: stage, grade, and smoking status. Int Urol Nephrol. 2011 Dec;43(4):1039-45. pubmed.ncbi.nlm.nih.gov
- Collà Ruvolo C, Nocera L, Stolzenbach LF, et al. Tumor Size Predicts Muscle-invasive and Non-organ-confined Disease in Upper Tract Urothelial Carcinoma at Radical Nephroureterectomy. Eur Urol Focus. 2021 Mar 15:S2405-4569(21)00060-2. pubmed.ncbi.nlm.nih.gov
- Guruli G, Konety BR. Transitional cell carcinoma, renal. eMedicine, July 27, 2006. emedicine.medscape.com
- Kirkali Z, Tuzel E. Transitional cell carcinoma of the ureter and renal pelvis. Crit Rev Oncol Hematol 2003; 47: 155-69. PubMed
- Michaelson MD, Kaufman DS, Oh WK. Transitional cell carcinoma of the upper uroepithelial tract. Clin Adv Hematol Oncol 2003; 1: 102-4. PubMed
- Chen CH, Grollman AP, Huang CY, et al. Additive Effects of Arsenic and Aristolochic Acid in Chemical Carcinogenesis of Upper Urinary Tract Urothelium. Cancer Epidemiol Biomarkers Prev. 2021 Feb;30(2):317-325. pubmed.ncbi.nlm.nih.gov
- Chen CH, Dickman KG, Moriya M, et al. Aristolochic acid-associated urothelial cancer in Taiwan. Proc Natl Acad Sci U S A. 2012 May 22;109(21):8241-6. pubmed.ncbi.nlm.nih.gov
- Cowan NC, Turney BW, Taylor NJ, McCarthy CL, Crew JP. Multidetector computed tomography urography for diagnosing upper urinary tract urothelial tumour. BJU Int. 2007 Jun;99(6):1363-70. pubmed.ncbi.nlm.nih.gov
- Janisch F, Shariat SF, Baltzer P, et al. Diagnostic performance of multidetector computed tomographic (MDCTU) in upper tract urothelial carcinoma (UTUC): a systematic review and meta-analysis. World J Urol. 2020 May;38(5):1165-1175. pubmed.ncbi.nlm.nih.gov
- Cornu JN, Rouprêt M, Carpentier X, Geavlete B, et al. Oncologic control obtained after exclusive flexible ureteroscopic management of upper urinary tract urothelial cell carcinoma. World J Urol. 2010 Apr;28(2):151-6. pubmed.ncbi.nlm.nih.gov
- Villa L, Cloutier J, Letendre J, Ploumidis A, et al. Early repeated ureteroscopy within 6-8 weeks after a primary endoscopic treatment in patients with upper tract urothelial cell carcinoma: preliminary findings. World J Urol. 2016 Sep;34(9):1201-6. pubmed.ncbi.nlm.nih.gov
- Matin SF, Margulis V, Kamat A, et al. Incidence of downstaging and complete remission after neoadjuvant chemotherapy for high-risk upper tract transitional cell carcinoma. Cancer. 2010 Jul 1;116(13):3127-34. pubmed.ncbi.nlm.nih.gov
- Margulis V, Puligandla M, Trabulsi EJ, et al. Phase II Trial of Neoadjuvant Systemic Chemotherapy Followed by Extirpative Surgery in Patients with High Grade Upper Tract Urothelial Carcinoma. J Urol. 2020 Apr;203(4):690-698. pubmed.ncbi.nlm.nih.gov
- Meng X, Chao B, Vijay V, Silver H, et al. High Response Rates to Neoadjuvant Chemotherapy in High-Grade Upper Tract Urothelial Carcinoma. Urology. 2019 Jul;129:146-152. pubmed.ncbi.nlm.nih.gov
- Tully KH, Krimphove Md MJ, Huynh MJ, et al. Differences in survival and impact of adjuvant chemotherapy in patients with variant histology of tumors of the renal pelvis. World J Urol. 2020 Sep;38(9):2227-2236. pubmed.ncbi.nlm.nih.gov
- Vassilakopoulou M, de la Motte Rouge T, Colin P, et al. Outcomes after adjuvant chemotherapy in the treatment of high-risk urothelial carcinoma of the upper urinary tract (UUT-UC): results from a large multicenter collaborative study. Cancer 2011; 117: 5500-8. doi:10.1002/cncr.26172 DOI
- Galsky MD, Mortazavi A, Milowsky MI, et al. Randomized Double-Blind Phase II Study of Maintenance Pembrolizumab Versus Placebo After First-Line Chemotherapy in Patients With Metastatic Urothelial Cancer. J Clin Oncol. 2020 Jun 1;38(16):1797-1806. pubmed.ncbi.nlm.nih.gov
- Balar AV, Galsky MD, Rosenberg JE, et al. Atezolizumab as first-line treatment in cisplatin-ineligible patients with locally advanced and metastatic urothelial carcinoma: a single-arm, multicentre, phase 2 trial. Lancet. 2017 Jan 7;389(10064):67-76. pubmed.ncbi.nlm.nih.gov
- Sharma P, Retz M, Siefker-Radtke A, et al. Nivolumab in metastatic urothelial carcinoma after platinum therapy (CheckMate 275): a multicentre, single-arm, phase 2 trial. Lancet Oncol. 2017 Mar;18(3):312-322. pubmed.ncbi.nlm.nih.gov
- Nazzani S, Preisser F, Mazzone E, et al. Survival Effect of Nephroureterectomy in Metastatic Upper Urinary Tract Urothelial Carcinoma. Clin Genitourin Cancer. 2019 Jun;17(3):e602-e611. pubmed.ncbi.nlm.nih.gov
- Lehmann J, Suttmann H, Albers P, et al. Surgery for metastatic urothelial carcinoma with curative intent: the German experience (AUO AB 30/05). Eur Urol. 2009 Jun;55(6):1293-9. pubmed.ncbi.nlm.nih.gov
- Brien JC, Shariat SF, Herman MP, et al. Preoperative hydronephrosis, ureteroscopic biopsy grade and urinary cytology can improve prediction of advanced upper tract urothelial carcinoma. J Urol. 2010 Jul;184(1):69-73 pubmed.ncbi.nlm.nih.gov
