Streszczenie
- Definicja: Jałowa martwica kości głowy kości udowej w dzieciństwie.
- Częstość występowania: Chorobowość wynosi ok. 11:100 000 dzieci, częściej występuje u chłopców.
- Objawy: Często niejasne z krótkotrwałymi, przejściowymi epizodami utykania i niewielkim bólem lub w ogóle bez objawów bólowych. Epizody występują głównie po obciążeniu i nasilają się z czasem, często promieniując do kolana.
- Badanie fizykalne: Utykanie i narastające ograniczenie ruchomości, szczególnie w zakresie odwodzenia i rotacji wewnętrznej.
- Diagnostyka: Główne postępowanie diagnostyczne polega na badaniu RTG i RM.
- Leczenie: Leczenie jest zachowawcze lub chirurgiczne, w zależności od czynników prognostycznych, takich jak wiek w momencie wystąpienia lub rozległość martwicy. Zasadą terapii jest optymalne wycentrowanie głowy kości udowej w panewce („uwięzienie“).
Informacje ogólne
Definicja
- Jałowa martwica kości głowy kości udowej w dzieciństwie, która ustępuje samoistnie w ciągu około 2–4 lat, ale może powodować nieodwracalne uszkodzenie stawu biodrowego w formie deformacji przedzwyrodnieniowej o różnym nasileniu.
- Synonimy: choroba Perthesa, Coxa plana.
- Istnieje kilka systemów klasyfikacji, w tym
- stopień zaawansowania radiologicznego według Waldenströma
- klasyfikacja Herringa oparta na ocenie bocznej kolumny nasady jako czynnika prognostycznego.
- Choroba została po raz pierwszy opisana niezależnie przez Legga, Calvégo i Perthesa w 1910 roku.
Klasyfikacja Herringa
- Wysokość bocznej 1/3 głowy kości udowej (zmniejszająca się z powodu martwicy)
- A: zachowana wysokość bocznej kolumny nasady
- B: wysokość bocznej kolumny nasady zmniejszona o <50%
- podtyp B/C: wysokość kolumny bocznej zmniejszona o 50%
- C: wysokość bocznej kolumny nasady zmniejszona o >50%
- Rokowanie w przypadku stadium A jest ogólnie uważane za korzystne, w przypadku stadium B nieprzewidywalne, a w przypadku stadium C niekorzystne.
Częstość występowania
- Stosunkowo częsta choroba stawu biodrowego w dzieciństwie.
- Występuje z częstością ok. 11:100 000 dzieci.
- Częściej u chłopców, w stosunku 4–5:1.
- Największa zapadalność w 5. i 6. roku życia.
- U 10% dzieci zajęta jest również druga kończyna dolna.1
- Wiek predylekcji wynosi 3‒12 lat.2
Anatomia
- Głowa kości udowej jest kulista i pokryta chrząstką stawową.
- Dołek głowy kości udowej to owalne, nie do końca wyśrodkowane zagłębienie, które służy jako mocowanie dla więzadła obłego.
- Głowa kości udowej (Caput femoris) jest zaopatrywana przez pierścień naczyniowy u podstawy szyjki kości udowej z gałęzi bocznych i przyśrodkowych tętnic okalających udo (Arteria circumflexa femoris). W mniejszym stopniu unaczynienie za pośrednictwem tętnic pośladkowych górnych i dolnych.
- Tętnica w więzadle obłym odpowiada za 1/3 dopływu krwi do głowy kości udowej u dzieci, podczas gdy u dorosłych jej udział jest niewielki.
Etiologia i patogeneza
- Zmniejszony przepływ krwi do głowy kości udowej powoduje jałową martwicę.3
- Przyczyna jest nieznana, ale wydaje się być wieloczynnikowa.
- Następujące czynniki mogą przyczyniać się do zmniejszenia przepływu krwi:
- zwiększona lepkość krwi przy np. zaburzeniach trombolizy
- nawracające zawały kości
- anomalie naczyniowe
- opóźnienie rozwoju szkieletu z opóźnionym kostnieniem
- Przy braku kostnienia przepływ krwi w naczyniach kości długich zmniejsza się wraz ze wzrostem masy ciała.
- zwiększona lepkość krwi przy np. zaburzeniach trombolizy
Patofizjologia
- Niedostateczne ukrwienie głowy kości udowej prowadzi do martwicy kości.
- W przypadku rewaskularyzacji głowy kości udowej najpierw dochodzi do resorpcji martwiczej kości, a trwający w czasie proces zastępowania nową tkanką zwiększa ryzyko, że głowa kości udowej ulegnie spłaszczeniu lub całkowitemu zapadnięciu.
- Skuteczność regeneracji zależy od wieku dziecka (im młodsze, tym lepiej), a także od wszelkich współistniejących infekcji, przylegania stawu oraz innych czynników mechanicznych i fizjologicznych.
- Leczenie ma na celu optymalizację tych czynników.
- Wyniki i przebieg procesu naprawy obejmującego rewaskularyzację i rekonstrukcję głowy kości udowej są różne.
- U niektórych pacjentów głowa kości udowej może zostać całkowicie odbudowana, ale u większości pozostaje spłaszczona.
- Stopień przylegania stawu po zakończeniu procesu naprawy jest najważniejszym czynnikiem prognostycznym przyszłego rozwoju choroby zwyrodnieniowej stawów.
- Typowy przebiegu etapów według klasyfikacji Waldenströma4:
- Stadium I: początkowe (martwica)
- Stadium II: sklerotyzacja
- Stadium III: fragmentacja (resorpcja)
- Stadium IV: odbudowa (reosyfikacja)
- Stadium V: gojenie.
Czynniki predysponujące
- Uraz z uszkodzeniem naczyń krwionośnych.
- Czynniki środowiskowe, które w przypadku predyspozycji genetycznych mogą zwiększać ryzyko wystąpienia choroby lub negatywnie wpływać na jej rokowanie5:
ICD-10
- M91 Młodzieńcza osteochondroza biodra i miednicy.
- M91.1 Osteochondroza młodzieńcza głowy kości udowej [choroba Legga-Calvégo-Perthesa].
- M 91.2 Miednica płaska.
Diagnostyka
Kryteria diagnostyczne
- Ból biodra związany z wysiłkiem fizycznym, często promieniujący do stawu kolanowego.
- Wszystkie niejasne wyniki dotyczące kolana i biodra w wieku predylekcyjnym są podejrzane i wymagają diagnostyki.
- W przypadku podejrzenia choroby Perthesa należy wykonać zdjęcie RTG miednicy w projekcji Lauensteina.
- We wczesnym stadium choroby wynik często jest ujemny, dlatego pomocne jest wykonanie RM.
Diagnostyka różnicowa
- Uwaga: objawy towarzyszące, takie jak złe samopoczucie, gorączka, utrata masy ciała lub niedokrwistość powinny wzbudzić podejrzenie choroby układowej!
- Przemijajaące zapalenie stawu biodrowego
- ustąpienie wysięku stawowego po kilku dniach.
- Dysplazja stawu biodrowego.
- Młodzieńcze idiopatyczne zapalenie stawów.
- Bakteryjne zapalenie stawów.
- Młodzieńcze złuszczenie głowy kości udowej.
- Zapalenie kości i szpiku.
- Nowotwór.
- Dysplazja Meyera (mnoga osteochondrodysplazja)
- symetryczne zmiany w badaniu radiologicznym
- ujemny wynik RM.
Wywiad lekarski
- Pacjenci mają zwykle od 4 do 10 lat. Najczęściej choroba występuje w 5. i 6. roku życia.
- Choroba często zaczyna się od krótkotrwałych, przejściowych epizodów utykania i niewielkiego bólu lub w ogóle nie daje objawów bólowych. Epizody te występują głównie po obciążeniu i z czasem ih częstotliwość wzrasta.
- Stopniowo utykanie staje się coraz bardziej wyraźne, a pacjenci skarżą się na ból w kolanie, pachwinie lub przedniej/zewnętrznej stronie uda.
- Zakres ruchu biodra może się zmniejszyć.
- Często objawy utrzymują się przez kilka tygodni zanim pacjent zasięgnie pomocy medycznej.
Badanie przedmiotowe
- Obserwacja — ocena:
- kondycji fizycznej (Nadwaga?)
- wzorca chodu (utykanie, późniejsze utykanie z powodu nierówności kończyn)
- atrofii mięśni.
- Palpacja
- ból przy ucisku w pachwinie
- nieprawidłowe ustawienie miednicy (anatomiczna lub czynnościowa rozbieżność długości kończyn dolnych)
- Badanie czynnościowe
- ruchomość stawów według metody badania zakresu ruchu (range of motion — ROM)
- ograniczony ruch, ból przy ruchu (najpierw ograniczona rotacja wewnętrzna i odwodzenie)
- dodatni wynik testu odwiedzenia
- Pacjent w pozycji na plecach.
- Kostkę badanej nogi umieszcza się na udzie drugiej nogi.
- Z góry ta pozycja nóg przypomina liczbę cztery.
- Kiedy wywiera się nacisk na staw kolanowy zgiętej nogi (wymuszając w ten sposób rotację zewnętrzną i odwodzenie), pojawia się ból.
- Objaw Trendelenburga
- opadanie miednicy po zajętej stronie przy staniu na jednej nodze z powodu niewydolności/zaniku odwodzicieli.
- Uwaga: zawsze należy badać obie strony, ponieważ u 10% dzieci zajęta jest również druga kończyna!
Badania uzupełniające w praktyce lekarza rodzinnego
Diagnostyka specjalistyczna
- Zdjęcia rentgenowskie są częścią standardowej diagnostyki
- Zdjęcie RTG miednicy w projekcji Lauensteina.
- Możliwość uwidocznienia różnych stadiów radiograficznych. Pierwsze zmiany są widoczne na zdjęciu rentgenowskim po 6–8 tygodniach.
- Wcześniej wykonane zdjęcia rentgenowskie często dają prawidłowe wyniki. Alternatywnie można zaobserwować niespecyficzny wzrost ilości płynu stawowego z nieznacznie poszerzoną jamą stawową10-11.
- W początkowej fazie widoczny jest nieregularny dół nasadowy i cienka przynasada w porównaniu do zdrowej strony. Rozjaśnienie podchrzęstne występuje stosunkowo szybko.
- W stadium sklerotyzacji widoczna jest sklerotyczna głowa kości.
- W stadium fragmentacji widoczny jest grudkowaty rozpad.
- Dopiero w stadium odbudowy, w którym następuje sukcesywne tworzenie się nowej kości, stopniowo uzyskuje się pogląd na stopień deformacji głowy kości.
- RM
- We wczesnych stadiach choroby wyższa czułość niż badanie rentgenowskie, a także większa dokładność w póxniejszych badaniach kontrolnych
- Dostarcza przydatnych informacji na temat położenia, kształtu i rozmiaru głowy kości udowej oraz otaczających ją tkanek miękkich.
- Zwykle wymaga sedacji lub znieczulenia ogólnego u młodszych dzieci.
- USG stawu biodrowego -wskazania:
- Diagnostyka różnicowa przemijającego zapalenia stawu biodrowego.
- Wysięk utrzymujący się >2 tygodni.
Wskazania do skierowania do specjalisty
- W każdym przypadku uzasadnionego podejrzenia choroby, nawet jeśli wczesne wyniki badań rentgenowskich są ujemne, należy skierować pacjenta do ortopedy.
Leczenie
Cele leczenia
- Celem leczenia jest uwolnienie od bólu i zapewnienie prawidłowej czynności stawu biodrowego w zaawansowanych stadiach choroby oraz regeneracja stawu.
Ogólne informacje o leczeniu
- Optymalne leczenie choroby Calvégo-Legga-Perthesa jest nadal przedmiotem dyskusji.
- Podstawową zasadą leczenia jest terapia odciążająca, pozwalająca na centralizację głowy kości udowej w panewce.
- Algorytm leczenia uwzględnia wiek, sprawność ruchową, radiologiczne nasilenie zmian w klasyfikacji Herringa i obecności ryzyka uszkodzenia głowy kości udowej.
- Dzieci w wieku <6 lat
- łagodna postać, stadium A lub B wg Herringa, dobra ruchomość → leczenie zachowawcze
- ciężka postać, stadium B/C lub C wg Herringa, słaba ruchomość → osteotomia międzykrętarzowa (intertrochanteric osteotomy — ITO)/osteotomia Saltera.
- Dzieci w wieku 6–10 lat
-
- centrowanie zachowane, stadium A lub B wg Herringa, dobra mobilność → leczenie zachowawcze
- utrata wycentrowania, stadium B/C lub C wg Herringa, słaba ruchomość → ITO/osteotomia Saltera
- Dzieci w wieku >10 lat
- centrowanie zachowane, ale z biodrem szpotawym i powiększeniem główki kości udowej → epifizjodeza krętacza/korygująca ITO/wydłużenie szyjki kości udowej
- utrata wycentrowania, krótka panewka, powiększenie główki kości udowej → potrójna osteotomia miednicy/ustawienie krętarza/wydłużenie szyjki kości udowej.
Leczenie zachowawcze
- Tylko w początkowym stadium
- bisfosfoniany hamujące resorpcję kości i wazoaktywne analogi prostacykliny jako leki wspomagające krążenie krwi
- Uwaga: bezpieczeństwo i skuteczność stosowania tych substancji u dzieci nie zostały potwierdzone. Jest to stosowanie poza wskazaniami rejestracyjnymi!
- Stosowanie tego leczenia farmakologicznego powinno być zatem ograniczone do wyspecjalizowanych ośrodków.
- bisfosfoniany hamujące resorpcję kości i wazoaktywne analogi prostacykliny jako leki wspomagające krążenie krwi
- Od stadium sklerotyzacji
- Poprawa ruchomości stawu biodrowego poprzez regularne ćwiczenia bez obciążania, takie jak fizjoterapia, pływanie, jazda na rowerze i kontrolowany trening mięśni.
- Zmniejszenie sił pionowych działających na staw poprzez częściowe odciążenie i zaprzestanie aktywności sportowych, które wiążą się z powtarzalnym obciążeniem stawu, takich jak bieganie, skakanie, przeskakiwanie itp.
- Objawowe leczenie bólu za pomocą leków przeciwbólowych, przeciwzapalnych i rozciąganie.
- Nie wykazano żadnego wpływu ortez i unieruchomień gipsowych na odciążanie stawu.
- Unieruchomienie w ortezie może skutkować zwiększeniem ciśnienienia wewnątrzstawowego.
Zalecenia dla pacjentów
- Ważne jest odciążenie chorej kończyny, zwłaszcza w przypadku bólu.
- Istostne jest także, aby dziecko regularnie uczęszczało na fizjoterapię w celu kontrolowania i utrzymania mobilności.
- Podczas odciążania dziecko powinno przyjąć pozycję, w której kość udowa jest odwiedziona i obrócona do wewnątrz, tak aby głowa kości udowej była dobrze osadzona w okrągłej części panewki.
Leczenie chirurgiczne
- Wykazano, że leczenie chirurgiczne z większym prawdopodobieństwem prowadzi do uzyskania kulistej, przylegającej nasady kości udowej u pacjentów w wieku 6 lat i starszych niż postępowanie zachowawcze.12-13
Zapobieganie
- Aby zapobiec rozwojowi choroby zwyrodnieniowej stawów w późniejszym okresie, pacjenci powinni być chronieni przed niepotrzebnymi obciążeniami i nie powinni podejmować pracy, która wymaga dużo chodzenia lub stania i podnoszenia ciężkich przedmiotów.
Przebieg, powikłania i rokowanie
Przebieg
- Martwica i rekonstrukcja głowy kości udowej trwają przez okres 2‒4 lat. Następnie choroba ustępuje z różnymi stopniami deformacji resztkowych.
- Choroba zazwyczaj przechodzi przez 5 etapów według Waldenströma:
- stadium początkowe
- stadium sklerotyzacji
- stadium fragmentacji
- stadium odbudowy
- stadium gojenia.
Powikłania
- Wtórna koksartroza.
- Wolne ciała wewnątrzstawowe.
Rokowanie
- Rokowanie krótkoterminowe i średnioterminowe (10‒20 lat) jest dobre u większości dzieci.
- Czynniki predykcyjne2
- Jeśli choroba zaczyna się wcześnie (przed ukończeniem 6. roku życia), rokowanie jest lepsze. Dotyczy to również przypadków martwicy obejmującej mniej niż 50% bocznej nasady kości udowej (A i B wg Herringa).
- Rokowanie jest nieco gorsze w przypadku dziewczynek niż chłopców.
- Rokowanie długoterminowe
- Choroba predysponuje do wtórnej choroby zwyrodnieniowej stawów.
- Rokowanie zależy w dużej mierze od stopnia przylegania stawu i zajęcia centrum nasady.
- U około 50% pacjentów rozwija się w przebiegu koksartroza, a druga połowa wykazuje powrót do pełnego zdrowia.14
Dalsze postępowanie
- Odpowiedzialność za leczenie w fazie aktywnej spoczywa na specjalistach.
- Na wczesnych etapach choroby zaleca się kontrolę ambulatoryjną co 3 miesiące, po wygojeniu i zakończeniu odbudowy głowy kości udowej co 6–12 miesięcy do zakończenia procesu wzrostu.
Informacje dla pacjentów
Informacje dla pacjentów w Medibas
Ilustracje
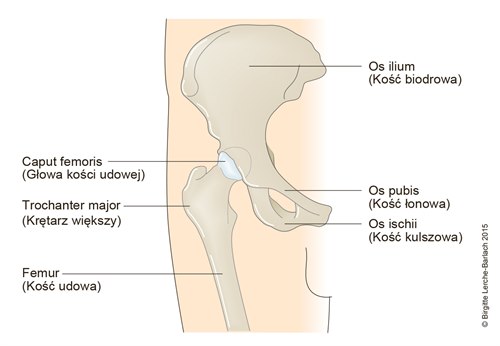
Udo, biodro i miednica
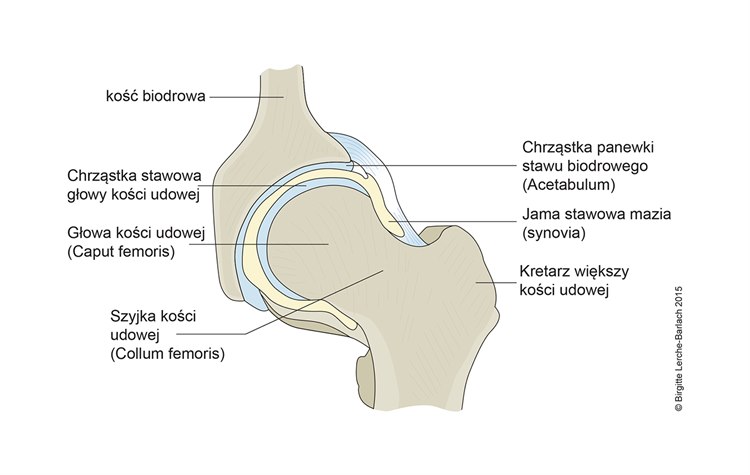
Staw biodrowy
Choroba Perthesa 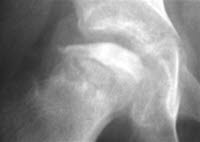

Choroba Calvégo-Legga-Perthesa, RTG
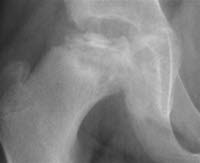
Choroba Calvégo-Legga-Perthesa, RTG
Źródła
Piśmiennictwo
- Guille JT, Lipton GE, Tsirikos AI, Bowen JR. Bilateral Legg-Calvé-Perthes disease: presentation and outcome. J Pediatr Orthop 2002; 22: 458-63. PubMed
- Wiig O, Terjesen T, Svenningsen S, et al. The epidemiology and aetiology of Perthes’ disease in Norway. A nationwide study of 425 patients. J Bone Joint Surg Br 2006; 88: 1217-23. PubMed
- Harris GD. Legg-Calve-Perthes disease. Medscape, last updated Feb 06, 2020. emedicine.medscape.com
- Waldenström H. Coxa plana, Osteochondritis deformans coxae. Zentralbl Chir 1920; 47: 5395. PubMed
- Pavone V, Chisari E, Vescio A, et al. Aetiology of Legg-Calvé-Perthes disease: a systematic review. World J Orthop 2019; 10(3): 145-65. www.ncbi.nlm.nih.gov
- Perry DC, Bruce CE, Pope D, et al. Perthes' disease of the hip: socioeconomic inequalities and the urban environment. Arch Dis Child 2012;97:1053-1057. PubMed
- Gordon JE, Schoenecker PL, Osland JD, et al. Smoking and socio-economic status in the etiology and severity of Legg-Calvé-Perthes' disease. J Pediatr Orthop B 2004;13:367-370. PubMed
- Bahmanyar S, Montgomery SM, Weiss RJ, et al. Maternal smoking during pregnancy and other prenatal and perinatal factors and the risk of Legg-Calvé-Perthes disease. Pediatrics 2008;122:459-464. europepmc.org
- Szepesi K, Posan E, Harsfalvi J, et al. The most severe forms of Perthes' disease associated with the homozygous Factor V Leiden mutation. J Bone Joint Surg Br 2004;86:426-429. PubMed
- Herring JA, Kim HT, Browne R. Legg-Calve-Perthes disease. Part II: Prospective multicenter study of the effect of treatment on outcome. J Bone Joint Surg Am 2004; 86: 2121-34. PubMed
- Herring JA, Kim HT, Browne R. Legg-Calve-Perthes disease. Part I: Classification of radiographs with use of the modified lateral pillar and Stulberg classifications. J Bone Joint Surg Am 2004; 86: 2103-20. PubMed
- Nguyen NA, Klein G, Dogbey G, et al. Operative versus nonoperative treatments for Legg-Calvé-Perthes disease: a meta-analysis. J Pediatr Orthop 2012;32:697-705. PubMed
- Saran N, Varghese R, Mulpuri K. Do femoral or salter innominate osteotomies improve femoral head sphericity in Legg-Calvé-Perthes disease? A meta-analysis. Clin Orthop Relat Res 2012;470:2383-2393. PubMed
- Heesakkers N, van Kempen R, Feith R, Hendriks J, Schreurs W. The long-term prognosis of Legg-Calvé-Perthes disease: a historical prospective study with a median follow-up of forty one years. Int Orthop. 2014 Nov 19. pubmed.ncbi.nlm.nih.gov
Autorzy
- Lek. Joanna Dąbrowska-Juszczak, (redaktor)
- Dr n. med. Lino Witte, (recenzent)
