Streszczenie
- Definicja: Idiopatyczne włóknienie płuc (idiopathic pulmonary fibrosis - IPF) jest szczególną, przewlekłą, postępującą, nieodwracalną postacią włóknienia płuc o niejasnej przyczynie. Choroba występuje głównie u starszych osób i ogranicza się do płuc. W badaniu radiologicznym daje ona obraz zwykłego śródmiąższowego zapalenia płuc (usual interstitial pneumonia –UIP).
- Epidemiologia: Chorobowość: 30–60 przypadków na 100 000 osób. W większości przypadków objawy występują po 50. roku życia. Stosunek liczby mężczyzn do liczby kobiet >2:1.
- Objawy: Duszność wysiłkowa oraz kaszel o postępującym przebiegu, zmęczenie.
- Badanie fizykalne: Palce pałeczkowate, trzeszczenia wdechowe u podstaw (sclerosiphonia). W zaawansowanych stadiach ewentualnie sinica, objawy prawokomorowej niewydolności serca.
- Diagnostyka: HRCT (high resolution computer tomography, tomografia komputerowa w wysokiej rozdzielczości) klatki piersiowej z uwidocznieniem wzorca UIP. Wykluczenie innych przyczyn śródmiąższowej choroby płuc.
- Leczenie: Leczenie obejmuje działania niefarmakologiczne oraz farmakoterapię przeciw włóknieniu. Przeszczep płuc jest jedyną metodą prowadzącą do wyleczenia.
Informacje ogólne
Definicja
- Definicja idiopatycznego włóknienia płuc (idiopathic pulmonary fibrosis – IPF) obejmuje następujące kryteria:1
- szczególna forma przewlekłego, postępującego, nieodwracalnego, zwłókniającego śródmiąższowego zapalenia płuc o nieznanej przyczynie
- występuje zazwyczaj u pacjentów w starszym wieku
- radiologiczny lub histopatologiczny wzorzec zwykłego śródmiąższowego zapalenia płuc (usual interstitial pneumonia – UIP).
- UIP jest określeniem zmian stwierdzanych w badaniu mikroskopowym wycinka płuca pobranego od chorych z klinicznym obrazem IPF
- Należy wykluczyć inne formy śródmiąższowego zapalenia płuc.
Epidemiologia
- Choroba rzadka, ale najczęstsza postać idiopatycznych śródmiąższowych zapaleń płuc
- W Europie roczna zapadalność wynosi 3–9 na 100 000 z tendencją wzrostową.
- szacuje się, że w Polsce roczna zapadalność na IFP wynosi 4,2–4,7 na 100 000.
- Chorobowość pomiędzy 30 a 60 na 100 000:
- wzrost częstości występowania z wiekiem.
- chorobowość u osób powyżej 70. roku życia nawet 10–krotnie wyższa.2
- w większości przypadków objawy występują po 50. roku życia.
- wzrost częstości występowania z wiekiem.
- Stosunek liczby mężczyzn do liczby kobiet >2:1.
- U większość pacjentów palenie tytoniu w wywiadzie.
Etiologia i patogeneza
Etiologia
- Zgodnie z definicją, etiologia IPF jest nieznana (idiopatyczna).
- Podłoże genetyczne stwierdza się nawet w 11% przypadków:
- rodzinne włóknienie płuc definiuje się jako występowanie śródmiąższowej choroby płuc u dwojga lub więcej członków tej samej rodziny
- dziedziczenie prawdopodobnie autosomalne dominujące ze zmniejszoną penetracją3
- objawy rodzinnego IPF występują w młodszym wieku niż postać sporadyczna.
Patogeneza
- Rozumienie patogenezy IPF w ostatnich latach uległo zmianie: obecnie przyjmuje się, że zamiast przewlekłej choroby zapalnej jest to przewlekła choroba zwłóknieniowa o złożonych mechanizmach.
- Zakłada się następujące mechanizmy patogenetyczne:
- punktem wyjścia jest zwiększony rozpad komórek nabłonka pęcherzyków płucnych.
- następnie występuje nieprawidłowo ukierunkowany proces gojenia z nadmierną, uporczywą proliferacją tkanki łącznej i bliznowaceniem.
- ostatnim etapem nieprawidłowo przebiegającego procesu gojenia jest rozwój torbieli o strukturze plastra miodu, wyściełanych komórkami nabłonka oskrzeli.
- Zmiany prowadzą do postępującej duszności i pogorszenia czynności płuc.
- W zależności od przebiegu, można rozróżnić cztery postaci:
- szybko postępującą
- z ostrym zaostrzeniem
- pośrednio postępującą
- wolno postępującą.
- Na objawy i przebieg choroby w sporadycznych przypadkach prawdopodobnie znaczący wpływ mają także predyspozycje genetyczne.
Czynniki predysponujące
- Palenie tytoniu jest jedynym udowodnionym egzogennym czynnikiem ryzyka.
- Inne możliwe czynniki ryzyka to:
- przewlekłe infekcje wirusowe (np. zapalenie wątroby, EBV)
- narażenie na pyły metali
- choroba refluksowa przełyku.
- Polimorfizmy i mutacje genetyczne są związane z IPF
ICD-10
- J84.1 Inne choroby tkanki śródmiąższowej płuc ze zwłóknieniem
Diagnostyka
- Rozpoznanie włóknienia płuc następuje średnio po około 2 latach od wystąpienia pierwszych objawów.
Kryteria diagnostyczne
- Do postawienia rozpoznania konieczne jest spełnienie kryteriów 1 i 2 lub 1 i 3
- wykluczenie śródmiąższowej choroby płuc o znanej przyczynie (np. spowodowanej przez choroby tkanki łącznej/inne choroby ogólnoustrojowe, narażenia na wziewne substancje szkodliwe, leki, itp.)
- obecność wzorca UIP w HRCT
- korelacja wyników HRCT i badań histopatologicznych
- Rozpoznanie IPF należy ustalić poprzez postępowanie interdyscyplinarne z udziałem pulmonologa, radiologa oraz ewentualnie histopatologa i reumatologa.
Diagnostyka różnicowa
- IPF należy odróżnić od innych chorób ze względu na odmienne leczenie i rokowanie.
- choroby z histopatologicznym lub radiologicznym wzorcem UIP
- włóknienie płuc związane z chorobami tkanki łącznej (w tym zapalenie stawów)
- pylica płuc, zwłaszcza azbestoza
- włóknienie płuc wywołane przez leki lub napromieniowanie
- przewlekła postać (stopień III) egzogennego alergicznego zapalenia pęcherzyków płucnych (AZPP)
- rzadkie przyczyny
- włóknienie płuc w dyskeratozie wrodzonej (dyskeratosis congenita)
- włóknienie płuc w zespole Hermanskiego–Pudlaka
- choroby z histopatologicznym lub radiologicznym wzorcem UIP
Wywiad
- Objawy:
- duszność
- wysiłkowa/w spoczynku?
- od kiedy?
- stopniowy początek?
- wolne/szybkie postępowanie objawów?
- suchy kaszel
- nasilenie przy wysiłku?
- nawracające infekcje dróg oddechowych?
- objawy ogólne: zmęczenie, znużenie, utrata masy ciała?
- trudności z zasypianiem i przesypianiem nocy, zmęczenie w ciągu dnia?
- duszność
- Leki (informacje na temat farmakologicznych czynników wyzwalających choroby układu oddechowego można znaleźć również na stronie pneumotox.com).
- Palenie tytoniu
- 60–70% pacjentów z IPF ma w wywiadzie palenie papierosów.
- Objawy choroby często utrzymują się również przez długi czas po zaprzestaniu palenia papierosów.
- Inne domowe lub zawodowe narażenia na wziewne substancje szkodliwe.
- Choroby tkanki łącznej/inne choroby autoimmunologiczne.
- Alergie.
- Dodatni wywiad rodzinny w kierunku idiopatycznego włóknienia płuc.
Badanie fizykalne
- Oglądanie:2
- palce pałeczkowate (ok. 20%)
- paznokcie zegarkowe (50–70%)
- w przypadkach zaawansowanych: duszność spoczynkowa, sinica, objawy prawokomorowej niewydolności serca.
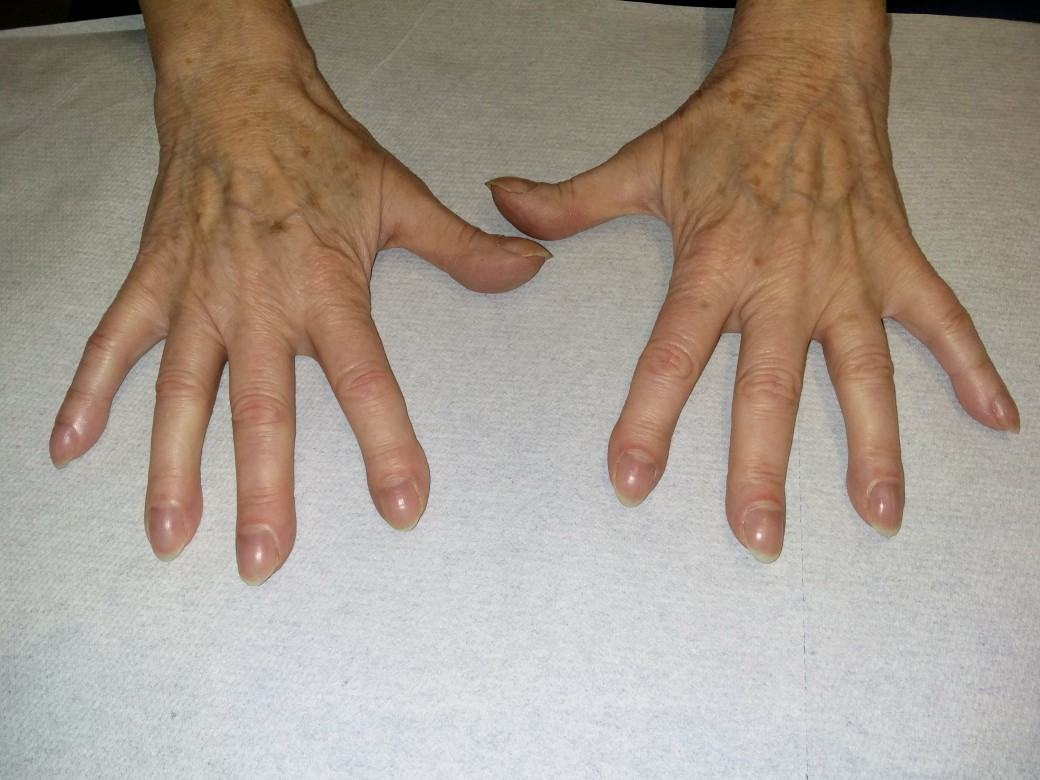 Palce pałeczkowate
Palce pałeczkowate
- Osłuchiwanie:
Badania uzupełniające
Badania laboratoryjne
- Brak swoistych wyników badań laboratoryjnych
- W celu wykluczenia/diagnostyki chorób tkanki łącznej można przeprowadzić badania przesiewowe:1
- OB, CRP, czynnik reumatoidalny (RF), anty–CCP
- wynik badania przeciwciał przeciwjądrowych i czynnika reumatoidalnego w IPF może być nieznacznie dodatni
- OB, CRP, czynnik reumatoidalny (RF), anty–CCP
- NT–proBNP (N-Terminal pro B–type Natriuretic Peptide), w przypadku podejrzenia nadciśnienia płucnego/prawokomorowej niewydolności serca
RTG klatki piersiowej
- Badanie rentgenowskie klatki piersiowej, zwłaszcza we wczesnych stadiach, może nie wykazywać zmian.
- Typowy obraz w RTG:4
- wyższe ustawienie obu kopuł przepony oraz zmniejszona powietrzność pól płucnych.
- zacienienia o typie siateczki widoczne w okolicach nadprzeponowych.
- w bardziej zaawansowanym stadium zacienienia sięgają coraz wyżej, ale zawsze są najbardziej nasilone w obwodowych częściach płuc, czyli pod opłucną
- zagęszczenia śródmiąższowe
- diagnostyka różnicowa za pomocą RTG klatki piersiowej nie jest jednak możliwa
Choroby współistniejące
- W przypadku pacjentów z IPF należy ocenić choroby współistniejące ze względu na ich wpływ na objawy, jakość życia, przebieg i rokowanie
- Do najczęstszych lub najbardziej istotnych chorób współistniejących należą:
- nadciśnienie płucne
- POChP/rozedma płuc
- rak płuca
- refluks żołądkowo–jelitowy (choroba refluksowa przełyku, GERD)
- choroba niedorwienna serca
- Innymi częstymi chorobami współistniejącymi są:
- cukrzyca
- obturacyjny bezdech senny
- nadciśnienie tętnicze i inne choroby sercowo-naczyniowe
- depresja
Diagnostyka specjalistyczna
Badania laboratoryjne
- W celu wykluczenia/stwierdzenia chorób tkanki łącznej można przeprowadzić badania przesiewowe:1
- przeciwciała przeciwjądrowe (antinuclear antibodies – ANA), przeciwciała przeciwko cytoplazmie neutrofilów (anti-neutrophil cytoplasmic antibodies –ANCA)
- wynik badania przeciwciał przeciwjądrowych – ANA w IPF może być nieznacznie dodatni.
- przeciwciała przeciwjądrowe (antinuclear antibodies – ANA), przeciwciała przeciwko cytoplazmie neutrofilów (anti-neutrophil cytoplasmic antibodies –ANCA)
TK klatki piersiowej wysokiej rozdzielczości (HRCT)
- HRCT jest rozstrzygającym badaniem obrazowym.
- Charakterystyczne zmiany:4
- zacienienia o wyglądzie siateczki oraz plastra miodu
- najbardziej nasilone w dolnych częściach płuc
- więcej z tyłu niż z przodu
- U wszystkich pacjentów z podejrzeniem IPF należy wykonać tomografię komputerową w technice wysokiej rozdzielczości bez podania kontrastu.
- Stwierdzenie cech UIP (zwykłego śródmiąższowego zapalenia płuc) jest kryterium diagnostycznym IPF.
- wzorzec zwykłego śródmiąższowego zapalenia płuc może jednak występować również w innych chorobach śródmiąższowych i w związku z tym nie jest patognomoniczny dla IPF
- Kryteria wzorca zwykłego śródmiąższowego zapalenia płuc (UIP)2
- zagęszczenia siateczkowate, zwłaszcza podopłucnowe i podstawne
- rozstrzenie oskrzeli z pociąganiem
- wzorzec plastra miodu
- torbielowate, wypełnione powietrzem obszary, typowo o średnicy 3–10 mm (do 25 mm)
- Kryteria wzorca UIP mogą zostać spełnione w różnym stopniu:
- definitywne zwykłe śródmiąższowe zapalenie płuc
- prawdopodobne zwykłe śródmiąższowe zapalenie płuc
- nieokreślone
- inne rozpoznanie.
- Jeżeli tomografia HRCT potwierdzi wzorzec UIP, w celu uniknięcia powikłań należy zrezygnować z biopsji płuca.1
Biopsja płuca
- U pacjentów bez potwierdzonego w HRCT wzorca UIP, można uzupełniająco wykonać biopsję płuca
- Ryzyko związane z biopsją może przewyższać korzyści, szczególnie w przypadku poważnych zaburzeń czynności płuc lub chorób współistniejących.
- Typowe cechy w badaniu mikroskopowym:4
- mozaikowatość zmian, czyli występowanie obszarów prawidłowego miąższu płuc na przemian z obszarami zmienionymi zapalnie, zaburzenie prawidłowej architektury płuca przez obszary plastra miodu oraz różnoczasowość zmian (obok siebie obszary „starych" zmian w postaci dokonanego włóknienia i „świeżych" w postaci skąpych nacieków zapalnych)
Płukanie oskrzelowo–pęcherzykowe (brochoalveolar lavage – BAL)
- U pacjentów bez jednoznacznego wzorca UIP w HRCT, zaleca się płukanie oskrzelowo-pęcherzykowe (BAL)1 - pomocne między innymi w różnicowaniu z egzogennym alergicznym zapaleniem pęcherzyków płucnych
Badania czynnościowe układu oddechowego
- Potwierdzenie i ilościowa ocena mechanicznego ograniczenia wentylacji oraz zaburzeń wymiany gazowej - spirometria, pletyzmografia oraz określenie pojemności dyfuzyjnej płuc.
- prawidłowy lub nieznacznie zmieniony wynik badań czynnościowych płuc (szczególnie spirometria) nie wyklucza IPF we wczesnych stadiach2
- W późniejszych stadiach typowe są:4
- cechy restrykcji - obniżenie pojemności życiowej – VC (vital capacity) i całkowitej pojemności płuc – TLC (total lung capacity)
- stosunek objętości wydechowej pierwszosekundowej (FEV1) do pojemności życiowej (VC), czyli wskaźnik FEV1/VC wyższy od spodziewanego
- Pomiar zdolności dyfuzyjnej dla tlenku węgla (DLCO) jest czułym wskaźnikiem zaburzeń czynnościowych w IPF, który jest nieprawidłowy wcześniej niż obserwowane zmiany w badaniu spirometrycznym.
Test 6–minutowego marszu
- Ocena wydolności.
- Znaczenie prognostyczne.
- Ewentualnie określenie wskazania do tlenoterapii.
Echokardiografia
- W przypadku podejrzenia nadciśnienia płucnego/prawokomorowej niewydolności serca.
Polisomnografia
- Zaburzenia snu i zaburzenia oddychania związane ze snem są u pacjentów z IPF bardzo częste.
- W związku z tym diagnostyka zaburzeń snu może zostać włączona do postępowania diagnostycznego.
Badania laboratoryjne
- Wskazane serologiczne badania przesiewowe wszystkich pacjentów z nowo rozpoznanym śródmiąższowym zapaleniem płuc, nawet jeśli nie występują inne objawy choroby tkanki łącznej/choroby ogólnoustrojowej:
- OB/CRP
- czynnik reumatoidalny (rheumatoid factor - RF)
- anty–CCP (anti–cyclic citrullinated peptides antibodies, przeciwciała przeciwko cyklicznemu cytrulinowanemu peptydowi)
- przeciwciała przeciwjądrowe (ANA) - w AOS
- ANCA – w AOS.
- Dalsza diagnostyka serologiczna w poszczególnych przypadkach (np. w kierunku zapalenia mięśni [myositis], zespołu Sjögrena, twardziny układowej).
Badanie genetyczne
- Testy genetyczne jako część standardowej diagnostyki klinicznej nie są obecnie zalecane.
Wskazania do skierowania do specjalisty
- W przypadku podejrzenia IPF pacjenta należy skierować do pulmonologa.
Leczenie
Cele leczenia
- Ograniczenie aktywności choroby.
- Wydłużenie czasu przeżycia.
Ogólne informacje o leczeniu
- Elementami terapii są:
- postępowanie niefarmakologiczne:
- zaprzestanie palenia
- normalizacja masy ciała
- aktywność fizyczna
- zapobieganie infekcjom (szczepienie przeciw grypie oraz pneumokokom)
- długoterminowa tlenoterapia
- wentylacja nieinwazyjna
- rehabilitacja pulmonologiczna
- farmakoterapia:
- pirfenidon i nintedanib spowalniają włóknienie i wydłużają średni czas przeżycia
- wskazania do terapii przeciwwłóknieniowej powinny być podejmowane przez zespół interdyscyplinarny.
- przeszczep płuc jako jedyna metoda prowadząca do wyleczenia.3
- postępowanie niefarmakologiczne:
Farmakoterapia
- Przed wprowadzeniem do leczenia leków hamujących włóknienie, stosowano leki immunosupresyjne, antagonistów receptora endoteliny, inhibitory fosfodiesterazy, acetylocysteinę5-6 - obecnie nie są one zalecane.
- Farmakoterapia opiera się obecnie na dwóch substancjach przeciwwłóknieniowych: pirfenidonie i nintedanibie (w Polsce dostępne wyłącznie w ramach programów lekowych)
- Pirfenidon:
- regulacja kaskad cytokin o działaniu profibrotycznym i prozapalnym, spowolnienie procesu chorobowego w badaniach klinicznych.7-8
- meta–analiza wyników trzech badań wykazała znaczące obniżenie śmiertelności z dowolnego powodu w grupie przyjmującej pirfenidon w porównaniu z grupą przyjmującą placebo.9
- przed rozpoczęciem leczenia należy oznaczyć stężenie transaminaz i bilirubiny oraz kontrolować raz w miesiącu przez pierwsze 6 miesięcy.
- w przypadku znacznego wzrostu stężenia aminotransferaz dostosowanie dawki lub przerwanie leczenia.
- Nintedanib
- wewnątrzkomórkowy inhibitor kinazy tyrozynowej.
- działa poprzez hamowanie transdukcji sygnału różnych czynników wzrostu (czynnik wzrostu śródbłonka naczyniowego [vascular endothelial growth factor –VEGF], czynnik wzrostu fibroblastów [fibroblast growth factor – FGF], płytkopochodny czynnik wzrostu [platelet derived growth factor – PDGF]).
- w porównaniu z placebo spowalnia proces chorobowy i wydłuża czas do pierwszego zaostrzenia.10-11
- należy zachować ostrożność w przypadku pacjentów ze zwiększonym ryzykiem sercowo–naczyniowym.
- U pacjentów objawowych zaleca się wdrożenie leczenia przeciwwłóknieniowego w momencie ustalenia rozpoznania.
- Jeśli jest dobrze tolerowane, należy stosować przez czas nieokreślony, w razie potrzeby do czasu przeszczepu płuc.
- Zamiana dwóch leków przeciwwłóknieniowych jest możliwa w przypadku wystąpienia niedających się kontrolować działań niepożądanych lub braku skuteczności.
- Leczenie skojarzone obecnie nie jest zalecane.
Przebieg, powikłania i rokowanie
Powikłania
- Ostre zaostrzenia IPF
- definiowane jako ostre, znaczne pogorszenie czynności układu oddechowego, zwykle w ciągu miesiąca
- brak skutecznego leczenia, bardzo niekorzystne rokowanie (śmiertelność >50%)
- Rozedma płuc
- Odma opłucnowa
- skumulowana zapadalność 8,5%, 12,5% lub 17,7% po 1, 2 i 3 latach.
- Nadciśnienie płucne
- do 1/3 pacjentów ma ciężkie nadciśnienie płucne
- Rak płuca
- zapadalność 5–48%, ryzyko raka płuc wzrasta wraz z czasem trwania choroby
- Zapalenie płuc
- Powikłania po biopsji płuca (m.in. krwotok, odma opłucnowa)
Przebieg
- Przebieg jest zróżnicowany i w związku z tym rokowanie trudne do jednoznacznego określenia
- rodzinne formy IPF często charakteryzują się wolniejszym postępem
- Możliwych jest wiele przebiegów choroby:
- przebieg stabilny
- powolny, równomierny postęp choroby (u większości pacjentów)
- szybka progresja
- nagłe ostre pogorszenie związane z powikłaniami, takimi jak zapalenie płuc lub z nieznanych przyczyn
- Różnice w przebiegu mogą być uwarunkowane złożoną interakcją płci pacjenta, jego wieku, czynników genetycznych i środowiskowych
- Progresję można ocenić poprzez okresowe badanie natężonej pojemności życiowej płuc (forced expiratory vital capacity – FVC):2
- pacjenci w stanie stabilnym z wahaniami <5%
- obniżenie FVC o 5–10% w ciągu 6–12 miesięcy wskazuje na istotną prognostycznie progresję
- obniżenie FVC >10% w ciągu 6 miesięcy jest związane ze znacznie podwyższoną śmiertelnością
Rokowanie
- Rokowanie złe - średni okres przeżycia po postawieniu rozpoznania: 3–5 lat3,12
- wskaźnik przeżycia 5-letniego: 20–40%
- IPF jest postacią włóknienia płuc o najgorszym rokowaniu
- Częstość zaostrzeń ok. 5–15% rocznie, z wysoką śmiertelnością2
- średni okres przeżywalności po ostrym zaostrzeniu: 3–4 miesiące
- Liczba chorób współistniejących bezpośrednio koreluje z rokowaniem
- konsekwentne leczenie chorób współistniejących może prowadzić do poprawy rokowania
Dalsze postępowanie
- Regularne kontrole zazwyczaj co 3–4 miesiące
- wskazana jest okresowa kontrola w poradni pulmonologicznej i/lub ośrodku referencyjnym leczenia chorób śródmiąższowych płuc.
- Rehabilitacja pulmonologiczna poprawia wydolność fizyczną, jakość życia i łagodzi objawy.13
- Do istotnych parametrów oceny przebiegu należą:
- jakość życia
- wydolność (test 6–minutowego marszu)
- badania czynnościowe płuc (spirometria/pletyzmografia)
- pojemność dyfuzyjna płuc
- diagnostyka obrazowa (HRCT)
Informacje dla pacjentów
Materiały edukacyjne dla pacjentów
Ilustracje

Palce pałeczkowate (dzięki uprzejmości dr n. med. Ericha Ramstöcka)
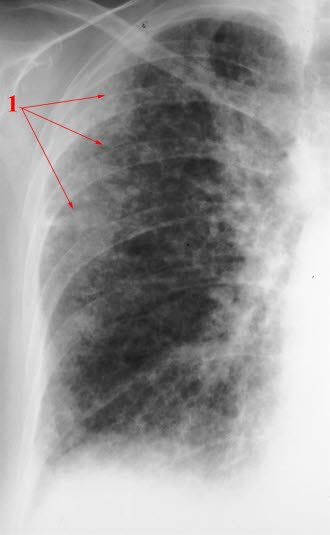
Włóknienie płuc, RTG: przepona ustawiona wysoko, widoczne rozsiane zmiany typu siateczki, najbardziej nasilone podopłucnowo (zaznaczone 1) oraz w dolnych partiach płuca
Źródła
Wytyczne
- American Thoracic Society, European Respiratory Society, Japanese Respiratory Society, Latin American Thoracic Society. Diagnosis of Idiopathic Pulmonary Fibrosis. Stan na 2018 r., www.atsjournals.org
- Piotrowski W,. Bestry I., Białas A., et al. Wytyczne Polskiego Towarzystwa Chorób Płuc dotyczące diagnostyki i leczenia idiopatycznego włóknienia płuc. Pneum Pol 2020, 1(1): 9-67, journals.viamedica.pl
Piśmiennictwo
- Raghu G., Remy-Jardin M., Myers J., et al. Diagnosis of Idiopathic Pulmonary Fibrosis. An Official ATS/ERS/JRS/ALAT Clinical Practice Guideline. Am J Respir Crit Care Med 2018; 198: e44-e68. doi:https10.1164/rccm.201807-1255ST, www.ncbi.nlm.nih.gov.
- Behr J. The diagnosis and treatment of idiopathic pulmonary fibrosis. Dtsch Arztebl Int 2015; 110: 875-81. doi:10.3238/arztebl.2013.0875, www.aerzteblatt.de.
- King Jr T.E., Pardo A., Selman M. Idiopathic pulmonary fibrosis. Seminar. Lancet 2011, 378: 1949-61, PubMed.
- Kuś J. Zwykłe śródmiąższowe zapalenie płuc, czyli samoistne włóknienie płuc. Postępy Nauk Medycznych 2011, 4: 260-6, www.czytelniamedyczna.pl.
- Zisman D.A., Schwartz M., Anstrom K.J., et al. A controlled trial of sildenafil in advanced idiopathic pulmonary fibrosis. N Engl J Med 2010, 363: 620-8, PubMed.
- Horton M.R., Santopietro V., Mathew L., et al. Thalidomide for the treatment of cough in idiopathic pulmonary fibrosis: a randomized trial. Ann Intern Med 2012, 157: 398-406, www.ncbi.nlm.nih.gov.
- Noble P.W., Albera C., Bradford W.Z., et al. Pirfenidone in patients with idiopathic pulmonary fibrosis (CAPACITY): two randomised trials. Lancet 2011, 377: 1760-9, PubMed.
- King TE, Bradford WZ, Castro-Bernardini S, et al. A phase 3 trial of pirfenidone in patients with idiopathic pulmonary fibrosis. N Engl J Med 2014. doi:10.1056/NEJMoa1402582 DOI
- Nathan S., Albera C., Bradford W. et al. Effect of pirfenidone on mortality: pooled analyses and meta-analyses of clinical trials in idiopathic pulmonary fibrosis. Lancet Respir Med 2017, 5: 33-41. doi:10.1016/S2213-2600(16)30326-5, DOI.
- Richeldi L., Costabel U., Selman M., et al. Efficacy of a tyrosine kinase inhibitor in idiopathic pulmonary fibrosis. N Engl J Med 2011, 365: 1079-87, New England Journal of Medicine.
- Richeldi L., du Bois R.M., Raghu G., et al. Efficacy and safety of nintedanib in idiopathic pulmonar fibrosis. N Engl J Med 2014. doi:10.1056/NEJMoa1402584, DOI.
- Ley B., Collard H.R., King T.E. Jr. Clinical course and prediction of survival in idiopathic pulmonary fibrosis. Am J Respir Crit Care Med 2011, 183: 431-40, PubMed.
- Cheng L., Tan B., Yin Y., et al. Short- and long-term effects of pulmonary rehabilitation for idiopathic pulmonary fibrosis: a systematic review and meta-analysis. Clin Rehabil. 2018, PMID: 29843523, www.ncbi.nlm.nih.gov.
- Raghu G., Weycker D., Edelsberg J., et al. Incidence and prevalence of idiopathic pulmonary fibrosis. Am J Respir Crit Care Med 2006; 174: 810-6, PubMed.
Opracowanie
- Natalia Jagiełła, (redaktor)
- Tomasz Tomasik (recenzent)
- Adam Windak (redaktor)
- Małgorzata Marczewska (recenzent/redaktor)
- Michael Handke (recenzent/redaktor)
