Streszczenie
- Definicja: Zwężenie pozaczaszkowej części tętnicy szyjnej wewnętrznej, spowodowane głównie miażdżycą.
- Epidemiologia: Chorobowość wzrasta wraz z wiekiem i wynosi ponad 5% u osób w wieku powyżej 65 lat oraz ponad 10% u osób w wieku powyżej 80 lat.
- Obraz kliniczny: Typowe objawy i powikłania to jednostronne niedokrwienie siatkówki (ślepota przejściowa), jednostronny niedowład, jednostronne zaburzenia czucia, zaburzenia mowy.
- Diagnostyka: Rozpoznanie za pomocą USG Duplex–Doppler, ewentualnie uzupełnione przez angiografię TK lub RM.
- Leczenie: Podstawą jest zmiana stylu życia i leczenie farmakologiczne ASA i statynami, a jeżeli występują, to również zwalczanie innych czynników ryzyka sercowo–naczyniowego. Rewaskularyzacja jest przydatna w przypadku zwężeń objawowych powyżej 50% i bezobjawowych powyżej 60%. Chirurgiczna tromboendarterektomia jest standardową procedurą, ale jako alternatywa w niektórych grupach pacjentów może być rozważane stentowanie tętnic szyjnych .
Informacje ogólne
Definicja
- Zwężenie pozaczaszkowej części tętnicy szyjnej wewnętrznej, spowodowane głównie miażdżycą.
- Do klasyfikacji zwężeń tętnic szyjnych stosuje się 2 główne kryteria:
- znaczenie kliniczne – bezobjawowe lub objawowe zwężenie tętnicy szyjnej.
- stopniowanie ciężkości za pomocą procedury obrazowania (głównie badania ultrasonograficznego z funkcją kolorowego Dopplera).
Epidemiologia
- Chorobowość zwężenia tętnicy szyjnej ≥50% (według NASCET) w populacji ogólnej: około 4%
- Chorobowość zwężeń wysokiego stopnia (≥70% według NASCET): około 1,7%.
- Stosunek liczby mężczyzn do liczby kobiet: około 2:1.1
- Najwyższa chorobowość u pacjentów z PAD (choroba tętnic obwodowych)3
- 28% ze zwężeniem tętnicy szyjnej powyżej 50%
- 14% ze zwężeniem tętnicy szyjnej powyżej 70%.
Etiologia i patogeneza
Etiologia
- Zdecydowanie najczęstszą etiologią (>90%) jest miażdżyca.
- Rzadszymi przyczynami są:
- zapalenie naczyń
- dysplazja włóknisto–mięśniowa
- rozwarstwienie
- angiopatia popromienna.
Patogeneza
- Zmiany miażdżycowe prowadzą do zwężenia światła pozaczaszkowej części tętnicy szyjnej wewnętrznej.
- Miejscem predylekcyjnym jest rozwidlenie tętnicy szyjnej wspólnej na tętnicę szyjną wewnętrzną i zewnętrzną.
- Oprócz czynników ryzyka miażdżycy, rolę w tworzeniu się blaszki miażdżycowej odgrywają warunki przepływu i geometria naczyń w rejonie rozwidlenia.4
- Najczęstszym mechanizmem udarów spowodowanych zwężeniem tętnicy szyjnej jest zator pochodzący ze zmian miażdżycowych.5
- Inne mechanizmy obejmują miejscową zakrzepicę lub niski przepływ związany ze zwężeniem.5
- W Europie około 15% przypadków niedokrwienia mózgu jest spowodowanych zwężeniem lub niedrożnością tętnicy szyjnej zewnątrzczaszkowej o ≥50%.
Ocena stopnia zwężenia i klasyfikacja
- W przeszłości stosowano różne definicje stopnia zwężenia; obecnie stopień zwężenia powinien być podawany zgodnie z (angiograficzną) definicją NASCET (North American Symptomatic Carotid Endarterectomy Trial).
- Stopień zwężenia (%) = (średnica światła naczynia dystalnie od zwężenia minus średnica światła naczynia w obszarze zwężenia)/średnica światła naczynia dystalnie do zwężenia x 100%.6
- Aby uniknąć nieporozumień, przy określaniu ilościowym należy zawsze podawać procedurę diagnostyczną i zastosowaną definicję zwężenia (najlepiej NASCET).1
- Klasyfikacja ciężkości na podstawie określonego stopnia zwężenia:
- niski stopień (<50% według NASCET)
- umiarkowany stopień (50‒69% według NASCET)
- wysoki stopień (70‒99% według NASCET).
- Wyniki wieloparametrycznych badań USG mogą i powinny być przenoszone przez osoby przeprowadzające badanie na stopnie zwężenia wg NASCET.
Czynniki predysponujące
- Czynniki ryzyka rozwoju zwężenia tętnicy szyjnej są podobne do czynników ryzyka choroby wieńcowej i PAD:4,6
- palenie tytoniu
- dyslipidemia
- nadciśnienie tętnicze
- cukrzyca
- otyłość
- brak aktywności fizycznej
- wiek
- wzrost stężenia CRP (przewlekły stan zapalny)
- płeć męska
- choroba naczyniowa w wywiadzie.
ICD–10
- I63.0 Zawał mózgu spowodowany przez zakrzep tętnic przedmózgowych.
- I63.1 Zawał mózgu spowodowany przez zator tętnic przedmózgowych.
- I63.2 Zawał mózgu spowodowany przez nieokreśloną niedrożność lub zwężenie tętnic przedmózgowych.
- I65.2 Niedrożność i zwężenie tętnicy szyjnej wewnętrznej.
- I67.2 Miażdżyca tętnic mózgowych.
Diagnostyka
Kryteria diagnostyczne
- Istotne zwężenie jest zwykle definiowane jako zwężenie ≥50%.
- Bezobjawowe zwężenia mogą być wykryte jedynie poprzez badania przesiewowe lub przypadkowo.
Rozróżnienie między zwężeniami objawowymi i bezobjawowymi
- Rozróżnianie objawowego i bezobjawowego zwężenia wymaga w pierwszej kolejności przeprowadzenie szczegółowego wywiadu i przedmiotowego badania neurologicznego.
- Objawowe zwężenie tętnicy szyjnej: jednostronny zawał mózgu, jednostronny przemijający atak niedokrwienny (TIA) lub jednostronne niedokrwienie siatkówki w ciągu ostatnich 6 miesięcy
- Zwężenie można również uznać za objawowe, jeśli w badaniu obrazowym wykazano jednostronne, klinicznie bezobjawowe niedokrwienie.
- Bezobjawowe zwężenie tętnicy szyjnej: brak objawów związanych ze zwężeniem w ciągu ostatnich 6 miesięcy.
- Objawowe zwężenie tętnicy szyjnej: jednostronny zawał mózgu, jednostronny przemijający atak niedokrwienny (TIA) lub jednostronne niedokrwienie siatkówki w ciągu ostatnich 6 miesięcy
Badania przesiewowe
-
U pacjentów z dwoma lub więcej czynnikami ryzyka sercowo-naczyniowego można rozważyć badanie przesiewowe w kierunku bezobjawowego zwężenia tętnicy szyjnej.
-
U pacjentów w stanie stabilnym przygotowywanych do CABG, u których w ciągu ostatnich 6 miesięcy wystąpił TIA lub udarem mózgu (bez rewaskularyzacji tętnicy szyjnej) należy rozważyć wykonanie ultrasonografia Duplex Doppler tętnicy szyjnej.
- Nie zaleca się przeprowadzania badań przesiewowych w populacji ogólnej.
- Badania przesiewowe populacji przy niskiej chorobowości generowałyby zbyt wiele wyników fałszywie dodatnich.7
Diagnostyka różnicowa
- Przemijający atak niedokrwienny (TIA) lub udar jako pierwszy objaw
- zatory proksymalne z serca (np. przy migotaniu przedsionków) lub aorty
- lakunarne zawały mózgu spowodowane niedrożnością małych naczyń krwionośnych
- krwotok mózgowy.
Diagnostyka
Wywiad – udar i TIA
- Patrz artykuł udar i TIA.
- Typowe objawy pozaczaszkowego zwężenia tętnicy szyjnej:1
- jednostronne niedokrwienie siatkówki (ślepota przejściowa)
- jednostronny niedowład
- jednostronne zaburzenia czucia
- zaburzenia mowy.
- Nietypowe objawy zwężenia tętnicy szyjnej:1
- zawroty głowy
- podwójne widzenie
- zaburzenia pamięci,
Badanie fizykalne
- Przedmiotowe badanie neurologiczne.
- Samo badanie przedmiotowe – zwłaszcza osłuchiwanie tętnicy szyjnej – ma niską czułość w wykrywaniu istotnego zwężenia tętnicy szyjnej.
- W pojedynczych przypadkach zwężenie tętnicy szyjnej można wykryć metodą osłuchową.
- Zasadniczo jednak osłuchiwanie nie jest odpowiednie do wykrywania/wykluczania zwężenia tętnicy szyjnej.
- Szmer przepływu nie dowodzi zwężenia wyższego stopnia, a brak szmeru przepływu nie wyklucza obecności zwężenia.
Badania uzupełniające w praktyce lekarza rodzinnego
- EKG
- migotanie przedsionków jako alternatywna (kardioemboliczna) przyczyna udaru.
- Pomiar ciśnienia tętniczego
- pomiar ciśnienia tętniczego w gabinecie, ewentualnie ambulatoryjny 24–godzinny pomiar ciśnienia tętniczego w diagnostyce nadciśnienia tętniczego (badania Holter dostępne w ramach Opieki Koordynowanej).
- Badania laboratoryjne:
- lipidogram: cholesterol całkowity, cholesterol LDL, cholesterol HDL, trójglicerydy
- glukoza, HbA1c
- CRP
- eGFR, kreatynina (przed diagnostyką inwazyjną/terapią z podaniem środka kontrastowego)
- TSH (przed diagnostyką inwazyjną/terapią z podaniem środka kontrastowego).
Diagnostyka specjalistyczna6
Badanie ultrasonograficzne (kolorowa ultrasonografia Duplex Doppler) – dostępne w POZ w ramach Opieki Koordynowanej
- Określenie stopnia zwężenia w zmianach tętnicy szyjnej powinno być wykonane za pomocą kolorowej ultrasonografii Duplex Doppler.
- Najważniejsza procedura z badań nieinwazyjnych:
- wolna od ryzyka
- szybko dostępna
- niedroga.
- Takie USG musi być wykonywane przez doświadczonych i wykwalifikowanych lekarzy.
- Ocena stopnia zwężenia pod kątem wielu parametrów
- Na podstawie 10 kryteriów ultrasonograficznych (5 głównych i 5 dodatkowych) oceniany jest stopień zwężenia, a odczyty ultrasonograficzne są przekształcane na stopnie ciężkości NASCET; metoda ECTS nie jest rekomedowana.
- Wyróżnia się następujące stopnie ciężkości (NASCET):
- blaszki miażdżycowe niezwężające (stopień zwężenia do 10%)
- zwężenie niskiego stopnia (20‒40%)
- umiarkowane zwężenie (50%)
- zwężenie średniego stopnia (60%)
- zwężenie wysokiego stopnia (70%)
- zwężenie bardzo wysokiego stopnia (80%)
- zwężenie najwyższego stopnia (90%)
- niedrożność (100%).
- Ze względu na wysoką dokładność diagnostyczną, badanie ultrasonograficzne jest również akceptowane jako podstawa planowania terapii przed interwencjami/operacjami.
- Jeśli diagnostyka ultrasonograficzna jest utrudniona lub istnieją wątpliwości co do klasyfikacji, należy dodatkowo wykonać angiografię TK lub angiografię RM.
Angiografia TK
- Morfologiczna prezentacja zwężenia.
- Dobre rozgraniczenie między światłem naczynia, tkankami miękkimi i strukturami kostnymi.
- Jeśli zwapnienie jest poważne, możliwe jest przeszacowanie stopnia zwężenia.
Angiografia RM
- Mniej zależne od osoby wykonującej badanie niż ultrasonografia.
- Podatność na artefakty niższa niż w przypadku angiografii TK.
- Tendencja do przeszacowania stopnia zwężenia.
Cyfrowa angiografia subtrakcyjna (digital subtraction angiography – DSA)
- Metoda referencyjna dla procedur nieinwazyjnych.8
- Nie należy wykonywać rutynowej diagnostyki DSA
- nieznaczne ryzyko powikłań (do 1%) nawet w przypadku czysto diagnostycznego, selektywnego DSA.
- DSA powinna być wykonywana tylko wtedy, gdy:
- brakuje jednoznacznych wyników procedur nieinwazyjnych
- należy spodziewać się konsekwencji terapeutycznych.
Przed planowaną interwencją/operacją
- Jeśli rozważana jest endarterektomia tętnicy szyjnej (carotid endarterectomy – CEA), ocena stopnia zwężenia określona na podstawie USG Duplex powinna zostać potwierdzona przez angiografię TK lub RM lub przez powtórne badanie ultrasonograficzne wykonane przez innego wykwalifikowanego lekarza.
- Jeśli rozważane jest stentowanie tętnic szyjnych (carotid artery stenting – CAS), badanie ultrasonograficzne powinno być uzupełnione angiografią TK lub RM w celu uzyskania dodatkowych informacji na temat łuku aorty, morfologii zwężenia oraz krążenia zewnątrzczaszkowego i wewnątrzczaszkowego.
Wskazania do hospitalizacji
- Do pacjentów z podejrzeniem ostrego udaru należy natychmiast wezwać pogotowie.
- Pacjenci z udarem powinni być leczeni w oddziałach udarowych.
- W przypadku pacjentów z TIA zaleca się również natychmiastową ocenę w ośrodku specjalizującym się w udarach.
Test FAST (Face, Arms, Speech, Time – twarz, ramiona, mowa, czas)
- W celu szybkiej oceny klinicznej czy występuje zaburzenie krążenia mózgowego, można zastosować test FAST.
- Face (twarz): czy ma miejsce porażenie twarzy?
- Poproś badaną osobę, aby się uśmiechnęła lub pokazała zęby.
- Sprawdź, czy nie pojawiła się asymetria.
- Arm (ramię): czy ma miejsce osłabienie ramion?
- Unieś ramiona badanej osoby do 90 stopni w pozycji siedzącej (45 stopni w pozycji leżącej), dłońmi do góry, poproś o przytrzymanie przez 5 sekund i opuszczenie rąk.
- Sprawdź, czy pacjent nie opuszcza ramion lub czy same nie opadają.
- Speech (mowa): czy ma miejsce upośledzenie mowy?
- Sprawdź, czy nie pojawiły się zaburzenia mowy.
- Spróbuj porozmawiać z badaną osobą.
- Zwróć uwagę na niewyraźną mowę.
- Zwróć uwagę na problemy ze znajdowaniem słów. Poproś badaną osobę o nazwanie widocznych przedmiotów, takich jak krzesło, stół, długopis. W przypadku zaburzeń widzenia należy dać osobie badanej znajomy przedmiot do ręki.
- Time (czas): jeśli przynajmniej 1 z wykonanych testów da wynik pozytywny, należy natychmiast wykonać połączenie alarmowe na pogotowie.
- Face (twarz): czy ma miejsce porażenie twarzy?
Leczenie
Cele leczenia
- Uniknięcie udaru/TIA.
- Zapobieganie/opóźnianie progresji zwężenia.
Ogólne informacje o leczeniu
- Leczenie zwężenia tętnicy szyjnej obejmuje następujące elementy:
- zmiana stylu życia
- profilaktyka pierwotna i wtórna lekami hamującymi agregację płytek i leczenie czynników ryzyka9
- podstawowa terapia zapobiegająca powikłaniom miażdżycowym z wykorzystaniem odpowiednich wytycznych i standardów (leczenie zaburzeń gospodarki lipidowej, nadciśnienia tętniczego oraz cukrzycy)
- pacjenci z bezobjawowym zwężeniem <60% prawdopodobnie odniosą większe korzyści z leczenia zachowawczego niż z rewaskularyzacji.1
- chirurgiczne (tromboendarterektomia) lub interwencyjne (stentowanie) leczenie zwężenia tętnicy szyjnej.10-15
Zmiana stylu życia
- Normalizacja masy ciała (redukcja nadwagi).
- Zmiana nawyków żywieniowych.
- Regularna aktywność fizyczna.
- Zaprzestanie palenia.
- Ograniczenie spożycia alkoholu.
Leczenie farmakologiczne
- Pacjenci ze zwężeniem tętnicy szyjnej powinni być leczeni farmakologicznie.
Hamowanie agregacji płytek krwi
- ASA 100 mg na dobę.
- Klopidogrel 75 mg na dobę w przypadku nietolerancji ASA.
Leczenie nadciśnienia tętniczego
- Inhibitory ACE lub antagoniści receptora angitensyny II (sartany) powinny być stosowane jako leki pierwszego rzutu w przypadku chorób naczyń obwodowych.16
- Informacje na temat leczenia nadciśnienia tętniczego opartego na wytycznych znajdują się również w artykule nadciśnienie tętnicze.
Statyny17
- Pacjentów z udokumentowaną chorobą sercowo–naczyniową na podłożu miażdżycy należy przydzielić do grupy bardzo wysokiego ryzyka sercowo–naczyniowego. Należy dążyć do osiągnięcia LDL–C <1,4 mmol/l (55 mg/dl) i zmniejszenia stężenia wyjściowego LDL–C o ≥50%, oraz nie–HDL–C <2,2 mmol/l (85 mg/dl).
- Statyny są zalecane u wszystkich pacjentów z chorobą naczyń obwodowych.16
- Zaleca się przepisywanie statyn w dużej, największej tolerowanej przez pacjenta dawce, w celu osiągnięcia celów terapeutycznych.
- Jeżeli przy stosowaniu statyny w największej tolerowanej dawce nie osiągnięto wartości docelowych, zaleca się połączenie statyny z ezetymibem.
- W prewencji wtórnej u pacjentów z grupy bardzo dużego ryzyka, u których nie osiągnięto celów leczenia mimo stosowania statyny w największej tolerowanej dawce w skojarzeniu z ezetymibem, zaleca się dołączenie inhibitora PCSK9.
- Jeśli schemat leczenia oparty na statynach nie jest tolerowany w żadnej dawce (nawet po próbie ponownego włączenia), należy zastosować leczenie ezetymibem, oraz, w razie potrzeby, dodanie do ezetymibu inhibitora PCSK9 i/lub kwasu bempediowego.
- Aby zapoznać się z wytycznymi dotyczącymi leczenia statynami, zobacz także artykuł hiperlipidemia.
Rewaskularyzacja
Informacje ogólne
- Wskazanie powinno być omówione interdyscyplinarnie.
- Rewaskularyzacja zwężenia tętnicy szyjnej może być technicznie wykonana poprzez chirurgiczną tromboendarterektomię (CEA) lub stentowanie tętnicy szyjnej (CAS).15
- Dane z badań porównujących obie procedury są niespójne.18-21
- Obecnie standardową procedurą rewaskularyzacji jest chirurgiczna tromboendarterektomia.
- Zabieg może być wykonany w znieczuleniu ogólnym lub miejscowym.
- Stentowanie tętnic szyjnych jest alternatywą dla niektórych grup pacjentów1
- podwyższone ryzyko operacji
- trudne warunki chirurgiczne.
- Warunkiem wstępnym stentowania tętnic szyjnych jest udokumentowany niski wskaźnik powikłań w ośrodku wykonującym zabieg (<3% dla zwężeń bezobjawowych, <6% dla zwężeń objawowych).1
Leczenie bezobjawowego zwężenia tętnicy szyjnej
(Wspomagające) leczenie zachowawcze
- Wszystkim pacjentom z bezobjawowym zwężeniem tętnicy szyjnej należy zalecić zróżnicowaną, zdrową dietę i aktywność fizyczną. Należy rzucić palenie.
- Wszyscy pacjenci z >50% bezobjawowym miażdżycowym zwężeniem tętnicy szyjnej powinni przyjmować 100 mg kwasu acetylosalicylowego (ASA) na dobę, jeśli ryzyko krwawienia jest niskie.
- W przypadku cukrzycy i/lub nadciśnienia tętniczego leczenie należy prowadzić zgodnie z wytycznymi.
- Wszyscy pacjenci z >50% bezobjawowym zwężeniem tętnicy szyjnej powinni przyjmować statyny w celu długoterminowej profilaktyki zdarzeń sercowo–naczyniowych (udar, zawał mięśnia sercowego, itp.).
- Pacjenci z bezobjawowym zwężeniem tętnicy szyjnej <60% powinni być leczeni zachowawczo, ponieważ nie odnoszą korzyści z leczenia inwazyjnego.
Leczenie chirurgiczne (CEA) i interwencyjne (CAS)
- W przypadku bezobjawowego zwężenia tętnicy szyjnej o 60‒99% można rozważyć CAS, jeśli nie ma zwiększonego ryzyka leczenia chirurgicznego.
- Okołozabiegowy wskaźnik udaru/śmiertelności powinien być jak najniższy w przypadku leczenia bezobjawowego zwężenia metodą CEA lub CAS. Częstotliwość występowania udaru/śmiertelność powinny być kontrolowane przez specjalistów neurologów i nie powinny przekraczać 2% podczas pobytu w szpitalu.
- Korzyści z CEA wykazano w przypadku zwężenia tętnicy szyjnej >60%.22
- Zmniejszenie 5–letniego ryzyka udaru z 11% do 5‒6% (NNT = 17‒20).23
- Mężczyźni odnoszą większe korzyści z leczenia zabiegowego niż kobiety.24
- Korzyści są większe u pacjentów w wieku poniżej 75. roku życia. 24
- Możliwe, że dodatkowe korzyści z zabiegu chirurgicznego są mniejsze w kontekście nowoczesnej farmakoterapii miażdżycy.1,25-26
- Należy również rozważyć CEA (można rozważyć CAS), zwłaszcza jeśli kryteria kliniczne lub wyniki badań obrazowych są związane ze zwiększonym ryzykiem niedokrwienia mózgu związanego z tętnicami szyjnymi w naturalnym przebiegu:
- przeciwstronny TIA lub zawał mózgu
- płeć męska
- klinicznie bezobjawowy jednostronny zawał mózgu (cTK, RM)
- szybka progresja stopnia zwężenia
- rozmiar blaszki miażdżycowej powyżej 80 mm2, blaszka miażdżycowa o niskim echu, krwawienie do blaszki miażdżycowej
- wykrycie mikrozatorowości przy użyciu przezczaszkowej ultrasonografii dopplerowskiej (transcranial Doppler – TCD)
- zmniejszona rezerwa naczynioruchowa (pojemność rezerwowa CO2).
- Jeśli rozważa się CEA lub CAS, oczekiwana długość życia powinna wynosić powyżej 5 lat, a wskaźnik powikłań okołozabiegowych poniżej 3%.
Leczenie objawowego zwężenia tętnicy szyjnej
(Wspomagające) leczenie zachowawcze
- Wszystkim pacjentom z objawowym zwężeniem tętnicy szyjnej należy zalecić zróżnicowaną dietę i aktywność fizyczną. Należy rzucić palenie.
- Pacjenci z objawowym zwężeniem tętnicy szyjnej powinni otrzymywać leki hamujące agregację płytek krwi (ASA 100 mg lub, w razie nietolerancji, klopidogrel 75 mg).
- U pacjentów zgłaszających się w ciągu 12 godzin od wystąpienia objawów z łagodnym zespołem neurologicznym (TIA z wysokim ryzykiem nawrotu, NIHSS ≤4), można rozważyć podwójną terapię hamującą agregację płytek przez 10‒21 dni za pomocą 100 mg ASA i 75 mg klopidogrelu po podaniu 300 mg dawki nasycającej klopidogrelu.
- Cukrzycę lub nadciśnienie tętnicze należy konsekwentnie leczyć zgodnie z wytycznymi.
- Pacjenci z objawowym zwężeniem tętnicy szyjnej <50% powinni być leczeni zachowawczo, ponieważ nie odnoszą korzyści z leczenia inwazyjnego.
Leczenie chirurgiczne (CEA) i interwencyjne (CAS)
- U pacjentów ze zwężeniem 70–99% po niedokrwieniu siatkówki, TIA lub małym udarze (minor stroke) należy przeprowadzić CEA.
- CEA powinna być wykonywana również u pacjentów z objawowym zwężeniem 50–69%, jeśli nie ma zwiększonego ryzyka zabiegu operacyjnego. Mężczyźni z niedawnymi objawami półkulowymi (niedokrwienie siatkówki, TIA, zawał mózgu mRS <3) najczęściej odnoszą korzyści z takiego leczenia.
- CAS można rozważyć u objawowych pacjentów ze zwężeniem tętnicy szyjnej 50–99% i normalnym ryzykiem operacyjnym.
- Częstość powikłań CEA i CAS przy objawowym zwężeniu tętnicy szyjnej powinna być kontrolowana przez specjalistę neurologa. Częstość udarów/śmiertelność w okresie okołozabiegowym udokumentowana podczas hospitalizacji powinna wynosić maksymalnie 4% dla wszystkich (wczesnych) planowych CEA lub CAS.
- Przy podejmowaniu decyzji o sposobie leczenia, oprócz czynników swoistych dla pacjenta i warunków anatomicznych, należy wziąć pod uwagę osobiste preferencje pacjenta. Warunkiem wstępnym są informacje i edukacja dostosowane do potrzeb danej osoby.
- Duże badania z randomizacją wykazały korzyści z CEA w porównaniu z leczeniem wyłącznie farmakologicznym.28-29
- Zakres korzyści z CEA zależy od stopnia zwężenia30-31
- Trwały efekt profilaktyczny tromboendarterektomii
- ryzyko jednostronnego udaru (>30 dni po operacji) to około 1% rocznie.
- Szczególnie duże korzyści odnotowuje się w następujących grupach pacjentów:
- płeć męska
- wiek powyżej 75 lat
- objawy półkulowe
- rosnąca wielochorobowość
- morfologicznie niestabilne/nieregularne zwężenia
- przeciwstronne zamknięcie tętnicy szyjnej.
- Czas wykonania CEA
- Korzyści są największe, jeśli CEA zostanie wykonana w ciągu 2 tygodni od wystąpienia objawów.32
- Wskaźnik powikłań okołooperacyjnych (udar/śmiertelność) w ośrodku wykonującym zabieg musi wynosić poniżej 6%.
- CAS można rozważyć jako alternatywę, jeśli wskaźnik powikłań również wynosi poniżej 6%.
- CAS jest korzystną opcją w szczególności u następujących pacjentów:1
- pacjenci chirurgiczni wysokiego ryzyka
- pacjenci ze zwężeniami w miejscach niedostępnych chirurgicznie
- z ponownymi zwężeniami po operacji
- ze zwężeniami radiogennymi
- ze zwężeniami tandemowymi ze zwężeniem wewnątrzczaszkowym lub wewnątrz klatki piersiowej wyższego stopnia
- z przeciwstronnym uszkodzeniem nerwu krtaniowego wstecznego.
- Przy podejmowaniu decyzji o formie leczenia (CEA lub CAS) powinny być również brane pod uwagę preferencje pacjenta.
Przebieg, powikłania i rokowanie
Powikłania
- Objawowe zwężenie tętnicy szyjnej wiąże się z wyższym ryzykiem udaru/zgonu w okresie okołozabiegowym niż zwężenie bezobjawowe.
- W przypadku bezobjawowych zwężeń częstość występowania udaru/zgonu w okresie okołozabiegowym wynosi około 2% (brak istotnej różnicy między tromboendarterektomią a stentowaniem).18
- Przy objawowych zwężeniach częstość występowania udaru/zgonu wynosi około 3% po tromboendarterektomii i 6% po stentowaniu tętnicy szyjnej.18
- Inne możliwe powikłania:
- niedokrwienie/zawał mięśnia sercowego
- Tromboendarterektomia wiąże się z nieznacznie wyższym ryzykiem zawału mięśnia sercowego.1
- miejscowe krwawienie
- Rozległe ponowne krwawienie wiąże się z wyższym ryzykiem udaru/zgonu.
- zakażenia ran
- uszkodzenia nerwów
- restenoza tętnicy szyjnej.
- niedokrwienie/zawał mięśnia sercowego
Przebieg i rokowanie
- Bezobjawowe zwężenia
- Po rewaskularyzacji (tromboendarterektomia lub stentowanie) w 4–letnim okresie, około 5% pacjentów doświadcza poważnego zdarzenia (zgon, udar lub zawał mięśnia sercowego).18
- Objawowe zwężenia
- Po rewaskularyzacji (tromboendarterektomia lub stentowanie) w 4–letnim okresie u około 8% pacjentów dochodzi do poważnego zdarzenia (zgon, udar lub zawał mięśnia sercowego).18
- Restenoza występuje zarówno po tromboendarterektomii, jak i stentowaniu tętnic szyjnych u około 6% pacjentów.
Dalsze postępowanie
- Pierwsza kontrola u pacjentów z bezobjawowym zwężeniem: 6 miesięcy po początkowym rozpoznaniu
- Zalecane coroczne badania kontrolne, jeśli wyniki pozostaną niezmienione.
- Po trombendarterektomii pierwsze badanie kontrolne należy przeprowadzić w ciągu 30 dni.
- Brak jasnych zaleceń dotyczących czasu badania po stentowaniu tętnic szyjnych.
- Do badań kontrolnych tętnicy szyjnej należy stosować metodę nieinwazyjną – zwykle jest to USG Duplex Doppler.
- Regularna kontrola czynników ryzyka sercowo–naczyniowego.
Informacje dla pacjentów
Edukacja pacjenta
- O korzyściach płynących z modyfikacji stylu życia w celu poprawy profilu ryzyka sercowo–naczyniowego.
- O sposobie działania profilaktyki lekowej.
- O zaletach i możliwych powikłaniach rewaskularyzacji.
Materiały edukacyjne dla pacjentów
Ilustracje
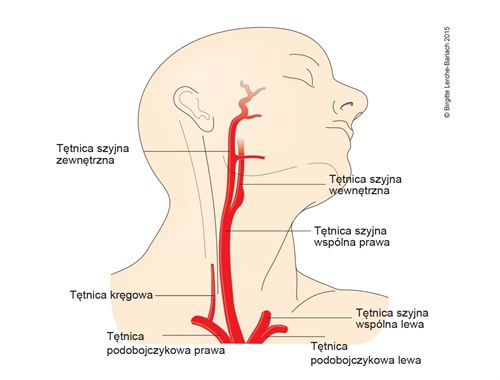
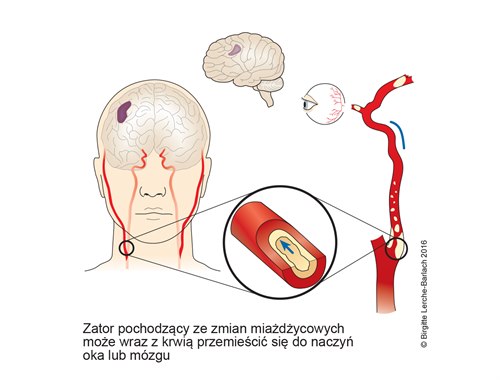
Źródła
Wytyczne
- European Society of Cardiology. 2024 ESC Guidelines of the management for peripheral arterial and aortic diseases, www.escardio.org
Piśmiennictwo
- Eckstein H., Kühnl A., Dörfler A., et al. Clinical Practice Guideline: The diagnosis, treatment and follow-up of extracranial carotid stenosis—a multidisciplinary German-Austrian guideline based on evidence and consensus, Dtsch Arztebl Int 2013, 110: 468-76, doi:10.3238/arztebl.2013.0468, DOI
- Benavente O., Moher D., Pham B. Carotid endarterectomy for asymptomatic carotid stenosis: a meta-analysis, BMJ 1998, 317: 1477-80, pubmed.ncbi.nlm.nih.gov
- Ahmed B., Al-Khaffaf H. Prevalence of significant asymptomatic carotid artery disease in patients with peripheral vascular disease. A meta-analysis, Eur J Vasc Endovasc Surg 2009, 37: 262-71, PubMed
- Prasad K. Pathophysiology and Medical Treatment of Carotid Artery Stenosis, Int J Angiol 2015, 24: 158-72, doi:10.1055/s-0035-1554911, DOI
- Hemingway J. Atherosclerotic Disease of the Carotid Artery. Medscape, aktualizacja: 04.10.2018, dostęp: 09.10.2018, emedicine.medscape.com
- Mazzolai L, Teixido-Tura G, Lanzi S, et al. 2024 ESC Guidelines for the management of peripheral arterial and aortic diseases. Eur Heart J. 2024 Sep 29;45(36):3538-3700. doi: 10.1093/eurheartj/ehae179. PMID: 39210722.
- Jonas D.E., Feltner C., Amick H.R., et al. Screening for asymptomatic carotid artery stenosis: A systematic review and meta-analysis for the U.S. Preventive Services Task Force, Ann Intern Med 2014, 161: 336-46, doi:10.7326/M14-0530, DOI
- Nederkoorn P.J., VanderGraaf Y., Hunink M.G.M. Duplex ultrasound and magnetic resonance angiography compared with digital subtraction angiography in carotid artery stenosis: a systematic review, Stroke 2003, 34: 1324-32, PubMed
- Goldstein L.B., Adams R., Alberts M.J., Appel L.J., Brass L.M., Bushnell C.D., et al. Primary prevention of ischemic stroke: a guideline from the American Heart Association/American Stroke Association Stroke Council: cosponsored by the Atherosclerotic Peripheral Vascular Disease Interdisciplinary Working Group; Cardiovascular Nursing Council; Clinical Cardiology Council; Nutrition, Physical Activity, and Metabolism Council; and the Quality of Care and Outcomes Research Interdisciplinary Working Group: the American Academy of Neurology affirms the value of this guideline, Stroke 2006, 37(6): 1583-633, pubmed.ncbi.nlm.nih.gov
- Mas J.L., Chatellier G., Beyssen B., et al, for the EVA-3S Investigators. Endarterectomy versus stenting in patients with symptomatic severe carotid stenosis, N Engl J Med 2006, 355: 1660-71, New England Journal of Medicine
- Meier P., Knapp G., Tamhane U., et al. Short term and intermediate term comparison of endarterectomy versus stenting for carotid artery stenosis: systematic review and meta-analysis of randomised controlled trials, BMJ 2010, 340: c467, BMJ (DOI)
- SPACE Collaborative Group; Ringleb P.A., Allenberg J., Bruckmann H., et al. 30 day results from the SPACE trial of stent-protected angioplasty versus carotid endarterectomy in symptomatic patients: a randomised non-inferiority trial, Lancet 2006, 368: 1239-47, PubMed
- Rerkasem K., Rothwell P.M. Carotid endarterectomy for symptomatic carotid stenosis, Cochrane Database of Systematic Reviews 2011, Issue 4. Art. No.: CD001081. DOI: 10.1002/14651858.CD001081.pub2, DOI
- Executive Committee for the Asymptomatic Carotid Atherosclerosis study: Endarterectomy for asymptomatic carotid artery stenosis, JAMA 1995, 273:1421, pubmed.ncbi.nlm.nih.gov
- Eckstein H., Tsantilas P., Kühnl A., et al. Surgical and endovascular treatment of extracranial carotid stenosis–a secondary analysis of statutory quality assurance data from 2009 to 2014, Dtsch Arztebl Int 2017, 114:729-36, DOI: 10.3238/arztebl.2017.0729, DOI
- Aboyans V., Ricco JB., Bartelink MEL., et al. 2017 ESC Guidelines on the Diagnosis and Treatment of Peripheral Arterial Diseases, in collaboration with the European Society for Vascular Surgery (ESVS), Eur Heart J 2018, 39:763-816. doi: 10.1093/eurheartj/ehx095, DOI
- Wytyczne ESC/EAS dotyczące postępowania w dyslipidemiach: jak dzięki leczeniu zaburzeń lipidowych obniżyć ryzyko sercowo‑naczyniowe (2019). Grupa Robocza do spraw leczenia dyslipidemii Europejskiego Towarzystwa Kardiologicznego (ESC) oraz Europejskiego Towarzystwa Badań nad Miażdżycą (EAS). Zeszyty edukacyjne. Kardiologia Polska,2020,3: 12-193, ptkardio.pl
- Brott T.G., Hobson R.W., Howard G., et al. Stenting versus endarterectomy for treatment of carotid-artery stenosis, N Engl J Med 2010, 362: e-pub, www.ncbi.nlm.nih.gov
- Lal B.K., Beach K.W., Roubin G.S., et al. Restenosis after carotid artery stenting and endarterectomy: a secondary analysis of CREST, a randomised controlled trial, Lancet Neurol 01.08.2012, pmid: PMID: 22857850, PubMed
- Bonati L.H., Lyrer P., Ederle J., et al. Percutaneous transluminal balloon angioplasty and stenting for carotid artery stenosis, Cochrane Database Syst Rev 12.09.2012, 9:CD000515, pubmed.ncbi.nlm.nih.gov
- Carotid Stenting Trialist' Collaboration. Short term outcome after stenting versus endarterectomy for symptomatic carotid stenosis: a preplanned meta-analysis of individual patient data, Lancet 2010, doi:10.1016/S0140-6736(10)61009-4, DOI
- Halliday A., Mansfield A., Marro J., et al. Prevention of disabling and fatal strokes by successful carotid endarterectomy in patients without recent neurological symptoms. Randomised controlled trial, Lancet 2004, 363: 1491-502, www.thelancet.com
- Halliday A., Harrison M., Hayter E., et al. 10-year stroke prevention after successful carotid endarterectomy for asymptomatic stenosis (ACST-1): a multicentre randomised trial, Lancet 2010, 376: 1074-84, www.ncbi.nlm.nih.gov
- Chambers B.R., Donnan G. Carotid endarterectomy for asymptomatic carotid stenosis, Cochrane Database of Systematic Reviews 2005, Issue 4. Art. No.: CD001923. DOI: 10.1002/14651858.CD001923.pub2, www.ncbi.nlm.nih.gov
- Kang S., Wu Y., Li X. Effects of statin therapy on the progression of carotid atherosclerosis: a systematic review and meta-analysis, Atherosclerosis 2004, 177(2): 433-42, PubMed
- Collins R., Armitage J., Parish S., et al. Effects of cholesterol-lowering with simvastatin on stroke and other major vascular events in 20536 people with cerebrovascular disease or other high-risk condition, Lancet 2004, 363: 757-63, PubMed
- Inzitari D., Eliasziw M., Gates P., et al. The causes and risk of stroke in patients with asymptomatic carotid artery stenosis, N Engl J Med 2000, 342: 1693-700, PubMed
- Barnett H.J.M., Taylor D.W., Eliasziw M., et al. Benefit of carotid endarterectomy in patients with symptomatic moderate or severe stenosis. North American Symptomatic Carotid Endarterectomy Trial Collaborators (NASCET). NEJM 1998, 339: 1415-25, www.nejm.org
- European Carotid Surgery Trialists' Collaborative Group. Randomised trial of endarterectomy for recently symptomatic carotid stenosis: final results of the MRC European Carotid Surgery Trial (ECST), Lancet 1998; 351: 1379-87, doi:10.1016/S0140-6736(97)09292-1, DOI
- Rerkasem K., Rothwell P.M. Carotid endarterectomy for symptomatic carotid stenosis, Cochrane Database of Systematic Reviews 2011, Issue 4. Art. No.: CD001081, pubmed.ncbi.nlm.nih.gov
- Rothwell P.M., Eliasziw M., Gutnikov S.A., et al. Analysis of pooled data from the randomised controlled trials of endarterectomy for symptomatic carotid stenosis, Lancet 2003, 361: 107-16, PubMed
- Rothwell P.M., Eliasziw M., Gutnikov S.A. et al. Carotid Endarterectomy Trialists Collaboration. Endarterectomy for symptomatic carotid stenosis in relation to clinical subgroups and timing of surgery, Lancet 2004, 363: 915-24, PubMed
Opracowanie
- Anna Fabian-Danielewska (recenzent)
- Tomasz Tomasik (redaktor)
- Adam Windak (redaktor)
- Michael Handke (recenzent/redaktor)
