Streszczenie
- Definicja: Astma to przewlekła, zapalna choroba dróg oddechowych, której towarzyszy nadreaktywność oskrzeli i odwracalna obturacja dróg oddechowych, prowadząca do napadów duszności, głównie wydechowej.
- Epidemiologia: Jedna z najczęstszych chorób przewlekłych, której częstość występowania w ciągu całego życia wynosi około 10%.
- Objawy: Zmienne, napadowe, o różnym nasileniu i często występujące w nocy: duszność, kaszel, uczucie ucisku w klatce piersiowej, świsty oddechowe (świszczący oddech). Napad często związany z czynnikiem wyzwalającym (np. alergeny, infekcje dróg oddechowych, wysiłek fizyczny).
- Badanie fizykalne: W okresie wolnym od objawów może nie budzić zastrzeżeń. Objawy niedrożności dróg oddechowych to wydłużony wydech, zmiany osłuchowe płuc (rozlane, obustronne świsty, furczenia), tachypnoe, praca dodatkowych mięśni oddechowych. W przypadku ciężkiej obturacji: wyczerpanie mięśni oddechowych, sinica, „cicha klatka piersiowa”.
- Rozpoznanie: Wywiad i badanie fizykalne. Badania czynnościowe płuc: dowody na (częściowo) odwracalną obturację dróg oddechowych (spirometria z próbą rozkurczową i w razie potrzeby z próbą prowokacji).
- Leczenie: Intensywność leczenia w zależności od stopnia kontroli astmy. Połączenie leków doraźnych (objawowych, przynoszących ulgę) i leków stosowanych długoterminowo (kontrolujących przebieg choroby). Postępowanie niefarmakologiczne obejmuje m.in. edukację pacjenta, regularną aktywność fizyczną, unikanie alergenów i fizjoterapię (oddechową).
Informacje ogólne
Definicja
- Astma jest heterogenną, przewlekłą chorobą zapalną dróg oddechowych, która charakteryzuje się nadreaktywnością oskrzeli i zmienną obturacją dróg oddechowych.
- objawy mają charakter napadowy i zmienne nasilenie, a są to: kaszel, duszność, świszczący oddech i ucisk w klatce piersiowej.
- ważną cechą choroby jest obturacja dróg oddechowych o zmiennym nasileniu.1
- Astmę można podzielić ze względu na etiologię:
- Astma alergiczna (zewnątrzpochodna)
- Zwykle rozpoczyna się w dzieciństwie.
- Związek z innymi chorobami alergicznymi/atopowymi, dodatni wywiad rodzinny.
- Czynnikami wyzwalającymi objawy są specyficzne alergeny.
- Zazwyczaj dobra odpowiedź na stosowanie glikokortykosteroidów wziewnych.
- Astma niealergiczna (wewnątrzpochodna)
- Częściej występuje u dorosłych.
- Czynnikami wyzwalającymi objawy są np. infekcje dróg oddechowych lub nietolerancja leków (często ASA lub NLPZ).
- Odpowiedź na glikokortykosteroidy wziewne jest często gorsza niż w astmie alergicznej.
- Astma alergiczna (zewnątrzpochodna)
- Dodatkowo mówi się o 3 fenotypach astmy: o późnym początku, z utrwaloną obturacją oskrzeli i współistniejącą z otyłością.2
- Obturacja dróg oddechowych w astmie wynika głównie z:
- skurczu mięśni gładkich oskrzeli
- obrzęku błony śluzowej w drogach oddechowych
- przebudowy ścian dróg oddechowych (remodeling)
- nagromadzenia wydzieliny w drogach oddechowych.
- Skurcz oskrzeli w przypadku nadreaktywności oskrzeli może być spowodowany przez różne czynniki wyzwalające:
- alergeny
- stres psychospołeczny3
- zakażenia układu oddechowego
- bodźce termiczne i chemiczne, dym i kurz
- wysiłek fizyczny
- leki.
- Nadreaktywność oskrzeli może występować również u osób zdrowych.3
- W ostrych napadach astmy lub jej zaostrzeniach dochodzi do przejściowego nasilenia objawów i pogorszenia czynności płuc.
- Nasilenie choroby jest bardzo zmienne i waha się od występowania okresowo łagodnych objawów do potencjalnie zagrażających życiu.
- Rozpoznanie astmy wymaga stwierdzenia objawów choroby oraz zmiennego stopnia obturacji oskrzeli w badaniach czynnościowych lub nadreaktywności oskrzeli.
- Leczenie zależy od stopnia kontroli astmy. Wyróżnia się 5 stopni intensywności leczenia według GINA.
- Istotnym elementem terapii jest również edukacja pacjenta i nauka prawidłowej inhalacji leku.
Definicja ciężkiej astmy
- Astma pozostaje niekontrolowana pomimo optymalnego leczenia o maksymalnej intensywności (stopień 4 i 5, trwające 3–6 miesięcy) oraz opanowywania czynników, mogących zaostrzać jej przebieg.
- Objawy nasilają się przy próbie zmniejszenia przyjmowanych leków.
- Spełnia kryteria astmy niekontrolowanej, gdy występują:
- ≥2 zaostrzenia wymagające zastosowania glikokortykosteroidów doustnych w ciągu ostatnich 12 miesięcy lub
- ≥1 zaostrzenie wymagające hospitalizacji lub wspomagania wentylacji w ciągu ostatnich 12 miesięcy lub
- niewystarczająca kontrola objawów, a także pogorszenie tolerancji wysiłku lub nocne wybudzenia związane z objawami astmy.3
Epidemiologia
- Epidemiologia astmy na świecie:
- Częstość występowania objawów astmy u dorosłych wynosi 6–7%.1
- Astma rozpoznawana jest częściej w zachodnich krajach uprzemysłowionych (częstość do 10%) niż w krajach rozwijających się (częstość 2–3%).1
- W ostatnich dekadach, mimo wzrostu występowania astmy w krajach zachodnich, liczba przyjęć do szpitala i zgonów uległa znacznemu zmniejszeniu.1,4
- Możliwe przyczyny wzrostu zachorowalności w ostatnich dekadach to:
- Wydaje się, że rosnąca od dawna częstość występowania astmy osiągnęła ostatnio w świecie zachodnim ustabilizowany poziom.7
- Częstość występowania w ciągu całego życia wynosi nieco poniżej 10%.
- Na astmę choruje około 10% dzieci.
- Częściej chłopcy niż dziewczynki.
- W dzieciństwie przeważa alergiczna postać astmy.
- Astma jest najczęstszą chorobą przewlekłą wieku dziecięcego.8
Etiologia i patogeneza
- Astma to choroba heterogenna o różnej patofizjologii.
- Na rozwój astmy ma wpływ wiele czynników genetycznych, środowiskowych i psychospołecznych.
- Warunki życia, takie jak dieta czy higiena, odgrywają prawdopodobnie znaczącą rolę. Stąd tak duże różnice w częstości występowania astmy między różnymi regionami świata.
Przyczyny astmy
- Czynniki genetyczne i epigenetyczne
- Istnieje złożona, wielogenowa, dziedziczna predyspozycja do zachorowania na astmę.
- Dotychczas zidentyfikowano wiele genów związanych ze zwiększonym ryzykiem wystąpienia astmy.9
- Czynniki genetyczne wydają się odgrywać ważną rolę, zwłaszcza w przypadku astmy rozpoznanej przed 12. rokiem życia.10
- Choroby atopowe, takie jak np. wyprysk atopowy u rodziców i rodzeństwa, zwiększają prawdopodobieństwo rozwoju atopii i astmy u dziecka.11
- Czynniki środowiskowe
- Zanieczyszczenie powietrza, np. spowodowane ruchem drogowym w miastach, wydaje się być związane z wyższym ryzykiem wystąpienia astmy.6
- Spaliny z silników Diesla zawierają wielopierścieniowe węglowodory aromatyczne (WWA), tlenek azotu (NO) i mikrocząsteczki. Badania pokazują, że ekspozycja na nie prowadzi do pogorszenia FEV1 i nasilenia stanu zapalnego dróg oddechowych.12
- Zanieczyszczenie i alergeny w pomieszczeniach, np. roztocza kurzu, dym lub alergeny zwierząt domowych, mogą przyczynić się do rozwoju astmy.13
- Czynnikami wyzwalającymi w środowisku pracy są alergeny zwierząt futerkowych, produktów rybnych, mąki i materiałów budowlanych, gazów oraz chemikaliów.
- Narażenie na dym papierosowy w czasie ciąży i we wczesnym dzieciństwie prowadzi do zwiększonego ryzyka zachorowania.
- Dzieciństwo spędzone na wsi w gospodarstwie rolnym (różnorodność mikroorganizmów) ma działanie ochronne.
- Za istotny czynnik rozwoju alergii uważa się uczulenie na roztocza kurzu i alergeny kota.8,15
- Kontakt ze zwierzętami
- Nie jest pewne, czy obecność zwierząt domowych ma działanie ochronne czy sprzyjające wystąpieniu alergii.
- Przykładowo aktualne niemieckie wytyczne dotyczące zapobiegania alergii zawierają następujące zalecenia:
- Osoby bez zwiększonego ryzyka wystąpienia alergii nie powinny wprowadzać ograniczeń związanych z posiadaniem zwierząt domowych.
- Rodziny ze zwiększonym ryzykiem wystąpienia alergii powinny unikać posiadania kotów.
- Posiadanie psa nie jest związane z większym ryzykiem wystąpienia alergii.
- Stały kontakt ze zwierzętami w pierwszych latach życia wydaje się być związany ze zmniejszonym ryzykiem wystąpienia astmy lub innych chorób atopowych.16
- Ekspozycja na alergeny kota może prowadzić do produkcji przeciwciał, nie powodując jednak uczulenia. Mogłoby to tłumaczyć zmniejszone ryzyko wystąpienia astmy.17
- Nawracające infekcje wirusowe górnych dróg oddechowych we wczesnym okresie życia
- Nie jest jasne, czy infekcje zwiększają ryzyko rozwoju astmy, czy też je zmniejszają (hipoteza higieniczna).
- W jednym z badań wykazano, że infekcje dróg oddechowych zmniejszają ryzyko wystąpienia astmy przed osiągnięciem wieku szkolnego.18
- Jednak infekcje wirusowe układu oddechowego, zwłaszcza zakażenie wirusem RSV i rinowirusami, odgrywają rolę zarówno w rozwoju, jak i w wywoływaniu ostrych ataków astmy.19
- Otyłość
- Nadwaga sprzyja rozwojowi choroby, wiąże się z cięższym przebiegiem i gorszą odpowiedzią na leczenie.20
- Związek z chorobami atopowymi21-24
- wyprysk atopowy (neurodermitis)
- alergiczny nieżyt nosa (katar sienny)
- alergiczne zapalenie spojówek
- pokrzywka.
- Leki
- Paracetamol i antybiotyki o szerokim spektrum działania, zarówno przyjmowane w ciąży jak i podawane w pierwszej fazie życia dziecka, powinny być stosowane tylko w przypadku wyraźnych wskazań.
- Według metaanalizy, narażenie na paracetamol we wczesnym okresie życia jest związane z ryzykiem rozwoju astmy.25
- Z kolei w prospektywnym badaniu kohortowym 620 dzieci z rodzinną historią alergii, nie stwierdzono związku między przyjmowaniem paracetamolu a ryzykiem rozwoju astmy.26
- Leczenie antybiotykami o szerokim spektrum działania w okresie rozwoju płodowego i wczesnego życia, może wiązać się ze zwiększoną częstością występowania astmy. Wciąż jednak brak jednoznacznych dowodów.
- Paracetamol i antybiotyki o szerokim spektrum działania, zarówno przyjmowane w ciąży jak i podawane w pierwszej fazie życia dziecka, powinny być stosowane tylko w przypadku wyraźnych wskazań.
Patogeneza
- Patogeneza astmy jest bardzo różnorodna.
- Podział postaci astmy na fenotypy wynika z założenia, że w niektórych grupach pacjentów występuje zarówno podobna patofizjologia astmy, jak i podobne cechy kliniczne.
- Wyróżnia się następujące postaci:
- Astma alergiczna (zewnątrzpochodna)
- Najczęstszy fenotyp astmy u dzieci (około 90% przypadków) i młodzieży.1
- Skłonność do atopii.
- Często dodatni wywiad rodzinny w kierunku chorób atopowych.
- Często z towarzyszącymi innymi chorobami atopowymi (atopowe zapalenie skóry, alergiczne zapalenie spojówek i alergiczny nieżyt nosa).
- Wykrywanie specyficznych IgE w surowicy.
- Przebieg sezonowy (np. w przypadku alergii na pyłki traw) lub całoroczny (np. alergia na roztocza kurzu domowego).
- Częściej występuje u dzieci.
- Astma niealergiczna (wewnątrzpochodna)
- Częściej występuje u dorosłych.
- Bez dowodów na alergiczne podłoże objawów.
- Czynnik wyzwalający to często infekcja dróg oddechowych.
- Inne szczególne postaci astmy (patrz niżej).
- Astma alergiczna (zewnątrzpochodna)
- Astma może wpływać na drogi oddechowe na różne sposoby, powodując:
- zmiany w błonie śluzowej
- zmiany w odpowiedzi immunologicznej
- zmiany w odpowiedzi nerwowo–mięśniowej/zmiana w regulacji nerwowej dróg oddechowych
- zmiany w zaopatrzeniu naczyniowym (wzmożona proliferacja naczyń).
- W drogach oddechowych u pacjentów chorujących na astmę występuje zwykle zwiększona ilość granulocytów kwasochłonnych, komórek tucznych, limfocytów T oraz mediatorów zapalnych i innych cytokin.
- Czynniki zapalne i wzrostowe prowadzą do przerostu i hiperplazji mięśni gładkich oskrzeli, co skutkuje ich obturacją.
- Zmieniona jest aktywność odruchowa i wrażliwość ściany oskrzeli, co przyczynia się do nadreaktywności oskrzeli.
Szczególne postaci astmy
- Podział ze względu na podłoże molekularne: astma związana z odpowiedzią immunologiczną typu Th2 (Th2 high) i bez tej odpowiedzi – Th2 low.
- Niektóre cytokiny, takie jak IL–5 i IL–13, mogą być uwalniane nie tylko przez alergenowo swoiste limfocyty Th pomocnicze, ale także przez alergenowo naturalne komórki limfoidalne typu 2 (ILC2), które produkują podobny profil cytokin jak limfocyty Th2.
- Określenie fenotypu może mieć kliniczne znaczenie dla predykcji odpowiedzi na leczenie wziewnymi glikokortykosteroidami lub niektórymi lekami biologicznymi.
- Kwestia, który biomarker (wydychany NO, periostyna) najlepiej identyfikuje ten typ astmy, pozostaje kontrowersyjna.
- Podział ze względu na rodzaj zapalenia w drogach oddechowych: astma eozynofilowa, neutrofilowa, ubogokomórkowa.
- W celu różnicowania konieczne jest wykonanie badania indukowanej plwociny oraz morfologii krwi z rozmazem.
- Przyjmuje się wartość progową poziomu eozynofili we krwi 150 eozynofili/mcl.
- W przypadku wartości >300/mcl konieczne jest wykluczenie zakażenia pasożytami, gdyż zastosowanie doustnych glikokortykosteroidów lub leków biologicznych mogłoby się potencjalnie przyczynić do uogólnienia zakażenia.
- W razie stwierdzenia hipereozynofilii >1500/mcl, w diagnostyce różnicowej należy brać pod uwagę rozpoznanie eozynofilowej ziarniniakowatości z zapaleniem naczyń.
- Pacjenci z astmą eozynofilową i nieeozynofilową różnią się znacząco pod względem odpowiedzi na wziewne glikokortykosteroidy.
- Klasyfikacja ta ma duże znaczenie we wskazaniach do terapii biologicznej: ponieważ wzrost liczby eozynofili zwiększa prawdopodobieństwo odpowiedzi na niektóre leki biologiczne (takie jak przeciwciało monoklonalne anty–IgE (omalizumab) lub przeciwciało monoklonalne przeciwko receptorowi dla IL–4 (dupilumab).
- Kaszlowy wariant astmy (Cough Variant Asthma)
- Główna dolegliwość to przewlekły, suchy kaszel spowodowany nieswoistą nadreaktywnością oskrzeli bez innych typowych objawów astmy.
- Badania czynnościowe płuc i badanie RTG klatki piersiowej są prawidłowe.
- U 1/3 pacjentów z kaszlowym wariantem astmy dochodzi do rozwoju astmy klasycznej, której może zapobiec wcześnie wdrożona terapia.
- Dla rozpoznania konieczne jest potwierdzenie zmiennej obturacji oskrzeli w spirometrii. W diagnostyce różnicowej należy brać pod uwagę eozynofilowe zapalenie oskrzeli (kaszel i eozynofilia w plwocinie indukowanej, przy prawidłowym wyniku spirometrii i reaktywności oskrzeli).27
- Kaszel jako jedyny objaw u dorosłych rzadko jest spowodowany astmą.2
- ,,Astma aspirynowa", choroba dróg oddechowych ulegająca zaosytrzeniu przez niesteroidowe leki przeciwzapalne (NSAIDs exacerbated respiratory disease – N–ERD)
- Nietolerancja inhibitorów cyklooksygenazy–1 (COX–1), takich jak kwas acetylosalicylowy (ASA) i niesteroidowe leki przeciwzapalne (NLPZ).
- Według różnych szacunków częstość występowania wynosi od 5,5% do 12,4% chorych na astmę.
- W klasycznej postaci, chorobie towarzyszą polipy nosa i przewlekłe zapalenie zatok (triada Samtera). Napadom astmy często towarzyszą podrażnienie spojówek, zaczerwienienie twarzy, wyciek wydzieliny z nosa.2
- Astma u chorych w podeszłym wieku
- Interpretacja wyników spirometrii bywa trudna, ze względu na zmieniającą się z wiekiem mechanikę oddychania (zmniejszenie sprężystości płuc, siły mięśni, stosunku FEV1/ FVC). Dodatkowo objawy choroby mogą być niedostatecznie zgłaszane przez chorych (gorsza percepcja, zaburzenia poznawcze).2
- U osób starszych różnicowanie astmy z POChP jest trudniejsze.
- Charakterystyczne cechy: podwyższone całkowite IgE, eozynofilia, nocne nasilenie objawów.
- Interpretacja wyników spirometrii bywa trudna, ze względu na zmieniającą się z wiekiem mechanikę oddychania (zmniejszenie sprężystości płuc, siły mięśni, stosunku FEV1/ FVC). Dodatkowo objawy choroby mogą być niedostatecznie zgłaszane przez chorych (gorsza percepcja, zaburzenia poznawcze).2
- Powysiłkowy skurcz oskrzeli
- Wcześniej nazywany „astmą wysiłkową”, jednak często występuje u osóby nie chorujących na astmę.
- Wysiłek fizyczny prowadzi do obturacji dróg oddechowych w ciągu 5–10 minut od jego zakończenia i ustępuje samoistnie w czasie 30–45 minut.1
- Uważa się, że przyczyną jest powtarzające się wysuszanie błon śluzowych, które sprzyja uwalnianiu mediatorów zapalnych przez eozynofile i mastocyty oraz aktywacji zakończeń nerwów czuciowych. Prowadzi to do przebudowy dróg oddechowych i rozwoju nadreaktywności oskrzeli.
- Występuje często podczas uprawiania sportów wytrzymałościowych (zwiększony wysiłek oddechowy). Częstość występowania powysiłkowego skurczu oskrzeli można zmniejszyć przez rozgrzewkę oraz stosując maski ogrzewające powietrze (w sportach zimowych).2
- Uwaga dla sportowców: leczenie beta–2–sympatykomimetykami podlega przepisom antydopingowym Światowej Agencji Antydopingowej (World Anti–Doping Agency – wada)!
Czynniki predysponujące
Czynniki wpływające na rozwój i ujawnienie astmy
- Predyspozycje genetyczne
- Dzieci z predyspozycjami genetycznymi (tzw. dzieci z grup ryzyka): w przypadku gdy przynajmniej 1 z rodziców lub rodzeństwa cierpi na zaburzenie atopowe, astmę.
- Narażenie na alergeny.
- Warunki środowiskowe, zanieczyszczenie środowiska.
- Wirusowe zakażenia układu oddechowego w dzieciństwie.
- Dym tytoniowy.
- Narażenie zawodowe.
- Stres psychospołeczny.
- Płeć żeńska (dorośli), męska (dzieci).
- Masa ciała.
- Ekspozycja na słońce (witamina D).
- Dieta.
- Leki.
Czynniki wyzwalające objawy
- Zobacz również artykuły napad astmatyczny u dorosłych oraz napad astmatyczny u dzieci i młodzieży.
- Istnieje wiele czynników, które mogą wywołać ostry napad astmatyczny:
- zakażenia dróg oddechowych, głównie wirusowe28
- alergeny
- narażenie na dym (tytoniowy), zanieczyszczenie powietrza, czynniki drażniące (aerozole)
- zimne powietrze
- pokarmy, konserwanty
- wysiłek fizyczny
- stres psychiczny, bardzo silne emocje (lęk)
- leki (np. beta–blokery lub ASA)
- metaanaliza wykazała, że kwas acetylosalicylowy jest czynnikiem wyzwalającym objawy u 7% dorosłych pacjentów z astmą i u 15% pacjentów z ciężką astmą.29
ICD–10
- J45 Astma oskrzelowa.
- J45.0 Astma oskrzelowa w głównej mierze z przyczyn alergicznych.
- J45.1 Astma oskrzelowa niealergiczna.
- J45.8 Astma oskrzelowa mieszana.
- J45.9 Astma oskrzelowa, nieokreślona.
- J46 Stan astmatyczny.
Diagnostyka
Kryteria diagnostyczne
- Rozpoznanie astmy opiera się na:
- szczegółowym wywiadzie z uwzględnieniem wywiadu rodzinnego
- wyniku badania fizykalnego
- badaniu czynnościowym płuc
- wykrycie zmiennej obturacji dróg oddechowych z udokumentowaną poprawą po krótko działającym beta–2–mimetyku
- wykrycie nadreaktywności oskrzeli.
- Początek objawów w wieku dorosłym nie przemawia przeciwko rozpoznaniu astmy.
- Często nie można postawić rozpoznania przy pierwszej wizycie: obserwacja przebiegu choroby i poprawy po leczeniu jest ważnym elementem diagnostyki.
- Najważniejszym rozpoznaniem różnicowym w wieku dorosłym jest przewlekła obturacyjna choroba płuc (POChP).
- Diagnostyka i leczenie astmy u osób starszych może być trudne, ze względu na choroby współistniejące, zmniejszoną percepcję objawów, akceptację duszności jako objawu starości.
Zaostrzenia
- Aby uzyskać informacje na temat rozpoznania i leczenia ostrego napadu astmatycznego, zobacz także:
Wytyczne: Diagnostyka30
4 filary rozpoznania astmy
- I: Wywiad.
- II: Zmienność obturacji dróg oddechowych z udokumentowaną poprawą po krótkodziałającym beta–2–mimetyku.
- III: Przewlekłe zapalenie dróg oddechowych.
- IV: Nadreaktywność oskrzeli.
Kryteria rozpoznania astmy
- Rozpoznanie astmy jest pewne w przypadku gdy:
- występują zmienne objawy ze strony układu oddechowego
- potwierdzono zmienny stopień ograniczenia wydechowego przepływu powietrza przez drogi oddechowe.
- Diagnozę astmy uznaje się za prawdopodobną w przypadku:
- typowego wywiadu i zmiennego charakteru objawów
- brak zmienności obturacji oskrzeli.
- Diagnozę uważa się za mało prawdopodobną w następujących przypadkach:
- nietypowe objawy
- brak poprawy obturacji po krótkodziałającym beta–2–mimetyku (SABA)
- brak obturacji
- brak nadreaktywności oskrzeli.
Wywiad
- Objawy klasyczne (o zmiennym nasileniu, często nie występują poza epizodami napadów i zaostrzeń):
- napadowa duszność (często nocna)
- świszczący oddech (świszczenie, świsty wydechowe)1
- ucisk w klatce piersiowej
- kaszel, zwykle suchy, bez odkrztuszania plwociny.
- Wywiad dotyczący astmy:
- czynniki wyzwalające
- np. bodźce oddechowe, pora dnia i roku, miejsce i aktywność
- u dzieci często wysiłek fizyczny (np. podczas zabawy)
- czynniki ryzyka
- np. atopia (egzema, nieżyt nosa) w wywiadzie osobniczym lub rodzinnym
- choroby współistniejące
- Przeciwko rozpoznaniu astmy przemawia:
- przewlekły kaszel z plwociną
- duszność wdechowa.
Badanie fizykalne
- Wyniki badania fizykalnego mogą nie budzić zastrzeżeń. W okresie objawowym choroby stwierdza się:
- objawy osłuchowe: świsty, furczenia, wydłużony wydech
- wysiłek oddechowy, duszność
- stridor wydechowy
- świszczący oddech
- zwiększoną częstość oddechów (tachypnoe)
- pracę dodatkowych mięśni oddechowych
- w ciężkim napadzie astmatycznym: brak objawów osłuchowych z powodu hiperinflacji („cicha klatka piersiowa”), sinica, spadek ciśnienia tętniczego, wyczerpanie, splątanie.
- U dzieci należy zwrócić dodatkową uwagę na:
- objawy atopii, np. wyprysk atopowy
- zaciąganie międzyżebrzy, dołków jarzmowych, nad– i podobojczykowych oraz przyczepów przepony jako oznak pracy dodatkowych mięśni oddechowych
- zwiększenie średnicy klatki piersiowej w wyniku hiperinflacji
- oznaki niedowagi i dystrofii u dziecka (zwiększony wysiłek oddechowy).
- Diagnostyka różnicowa (np. mukowiscydoza, niedobór odporności, pierwotna dyskineza rzęsek, itp.).
Badania czynnościowe płuc
- Aby potwierdzić rozpoznanie astmy, należy wykazać zmienną obturację dróg oddechowych w spirometrii z istotną poprawą po leku rozkurczającym oskrzela.
- Prawidłowe wyniki badań czynnościowych płuc nie wykluczają rozpoznania astmy.
Spirometria
- Wykonanie przynajmniej 3 manewrów forsownego wydechu (<8), przy spełnieniu kryteriów jakości i powtarzalności (różnice między 2 najlepszymi wynikami FVC i FEV1 nie przekraczają 150 ml).
- Obraz krzywej przepływ–objętość.
- Pomiar natężonej pojemności życiowej (forced vital capacity – FVC), natężonej objętości wydechowej pierwszosekundowej (forced expiratory volume in one second – FEV1) oraz stosunku FEV1/FVC (wskaźnik Tiffeneau).
- Zaburzenia wentylacji o typie obturacji
- zmniejszenie ilorazu FEV1 i FVC (wskaźnik Tiffeneau) poniżej dolnej granicy normy w populacji referencyjnej
- zmniejszenie FEV1 określa stopień nasilenia zaburzeń wentylacji.
- Ocena w odniesieniu do wartości referencyjnych dla danego wieku według Global Lung Initiative (GLI)30
- Wartość parametru jest prawidłowa, jeśli jest równa lub większa niż dolna granica normy (lower limit of normal – LNN) w populacji referencyjnej, czyli ≥5. centyl.
- Stosowane wcześniej arbitralne kryterium <0,7 nie uwzględniało wpływu wieku i prowadziło często do zbyt częstego rozpoznawania obturacji u osób w podeszłym wieku lub jej niedoszacowanie u osób młodych.2
- W wieku dorosłym klasyfikacja obturacji obejmuje 3 stopnie nasilenia (w astmie w zasadzie nie wyróżnia się stopni obturacji i nie klasyfikuje się na tej podstawie, gdyż początkowo obturacja jest odwracalna. Ten podział ma miejsce w POChP):
- Obturacja występuje, gdy FEV1/FVC < LLN.
- Łagodna obturacja: FEV1 ≥85% LLN (>60% wartości należnej).
- Umiarkowana obturacja: FEV1 55–84% LLN (40–60% wartości należnej).
- Ciężka obturacja: FEV1 <55% LLN (<40% wartości należnej).
- U dzieci brak podziału na stopnie nasilenia według FEV1/FVC jak u dorosłych.
- Zamiast tego podaje się wartości Z (odchylenia standardowe, o które mierzona wartość odbiega od średniej wartości należnej).
- Niskie FEV1 jest silnym predyktorem ryzyka zaostrzeń oraz utrwalonej obturacji, zwłaszcza jeśli wynosi <60% wartości należnej.
- Określenie wartości parametru FEV1 ma znaczenie także u chorych już leczonych lekami wziewnymi, w celu potwierdzenia rozpoznania astmy:
- Jeśli FEV1 wynosi >70% wartości należnej, a kontrola astmy jest utrzymana przez co najmniej 3 miesiące, można wziąć pod uwagę zmniejszenie dawki glikokortykosteroidów wziewnych (GKSw) o 25–50% lub odstawienie LABA i ponowną ocenę po 2–4 tygodniach, po czym do rozważenia wykonanie próby prowokacyjnej lub próby rozkurczowej.1
- Jeśli FEV1 wynosi <70% wartości należnej, wskazane jest zwiększenie intensywności leczenia i ponowną ocenę po 3 miesiącach. Jeśli to działanie nie przynosi efektu, należy wrócić do poprzedniego leczenia i skierować chorego na ponowną diagnostykę.27
Spirometryczna próba rozkurczowa
- U pacjentów z potwierdzoną obturacją dróg oddechowych zaleca się wykonanie próby rozkurczowej za pomocą krótkodziałających leków rozkurczających oskrzela (beta–mimetyków, short–acting beta–agonists – SABA).
- Za dodatni wynik próby rozkurczowej uznaje się wzrost wartości FEV1 o >12% oraz 200 ml (u dorosłych) w stosunku do wartości wyjściowych.
- Dodatnia próba rozkurczowa przemawia za rozpoznaniem astmy.
- Ujemna próba rozkurczowa nie wyklucza jednak astmy: w astmie ciężkiej lub z przebudową oskrzeli obturacja może być utrwalona.
- Prawidłowy wynik spirometrii nie wyklucza poprawy po leku rozkurczającym oskrzela, dlatego u pacjenta w trakcie pierwszorazowej diagnostyki wskazane jest wykonanie spirometrii z próbą rozkurczową (następnie można wykonywać spirometrię z próbą rozkurczową lub bez niej).2
- Według wytycznych ATS/ERS (2021) poprawę po przyjęciu leku uznaje się za istotną, jeżeli wartość FEV1 lub FVC zwiększy się o ≥10% wartości należnej.3
- Według wytycznych ATS/ERS (2021) poprawę po przyjęciu leku uznaje się za istotną, jeżeli wartość FEV1 lub FVC zwiększy się o ≥10% wartości należnej.3
- Spirometrię wykonuje się przed i 15 minut po inhalacji krótkodziałających beta–2–mimetyków.
- U dorosłych wziewne podanie SABA (np. do 400 mcg salbutamolu w 4 wdechach po 100 mcg z inhalatora ciśnieniowego)
- Alternatywnie krótkodziałający lek przeciwcholinergiczny (short–acting muscarinic antagonist – SAMA, bromek ipratropium w dawce 80 mcg [4 wdechy po 20 mcg]) i drugie badanie wykonać po 30 minutach (czas konieczny na pełne zadziałanie przyjętego leku).3
- Opcjonalnie powtórzenie spirometrii po inhalacji dużej dawki wziewnych glikokortykosteroidów (GKSw) podawanych 2 x dziennie przez co najmniej 4 tygodnie.
- U dzieci również wziewne podanie krótkodziałającego beta–2–mimetyku (SABA) do 4 dawek z inhalatora z dozownikiem (np. salbutamol 100 mcg).
- Ważne jest prawidłowe przygotowanie pacjenta do badania i odstawienie stosowanych leków wziewnych:
- SABA (fenoterol, salbutamol) na 6 godzin, LABA (formoterol i salmeterol) na 24 godziny, bardzo długo działające betamimetyki (indakaterol, wilanterol, olodaterol) na 36 godzin przed badaniem.
- SAMA (ipratropium) na 12 godzin, LAMA (tiotropium, umeklidynium na 3–7 dni, glikopironium, aklidynium – na 36–48 godzin przed badaniem.
Pomiar nadreaktywności – spirometryczna próba prowokacyjna (badanie specjalistyczne w ośrodku z udokumentowanym doświadczeniem)27
- Jeśli obraz kliniczny sugeruje astmę, co nie znalazło potwierdzenia w spirometrycznej próbie rozkurczowej, należy potwierdzić nadreaktywność oskrzeli w spirometrycznej próbie prowokacyjnej.
- Metody badania prowokacji:
- najczęściej stosowana w praktyce to nieswoista prowokacja wziewna z użyciem metacholiny
- standaryzowany wysiłek fizyczny (z użyciem bieżni, free running test zwłaszcza w przypadku małych dzieci lub – raczej mniej odpowiedniego – ergometru rowerowego)
- prowokacja zimnym powietrzem, wziewny mannitol.
- U dzieci z objawami podczas wysiłku fizycznego zaleca się wykonanie próby wysiłkowej w biegu.
- Ujemny wynik u chorego nieprzyjmującego wziewnych glikokortykosteroidów pozwala wykluczyć astmę.
- W razie wyniku dodatniego, należy pamiętać o możliwych rozpoznaniach różnicowych: dodatnia próba prowokacyjna występuje u chorych z alergicznym nieżytem nosa, POChP czy mukowiscydozą.27
Pletyzmografia całego ciała (badanie specjalistyczne)
- Pozwala na ocenę całkowitej ilości powietrza zawartej w płucach (hiperinflacja?) oraz oporu, jaki drogi oddechowe stawiają przepływającemu przez nie powietrzu.
- W sposób pośredni umożliwia ocenę stopnia obturacji (zwężenia) oskrzeli.
- Pomocna w przypadku wątpliwego wyniku spirometrii lub słabej współpracy.
- Szczególnie polecana w diagnostyce różnicowej pomiędzy astmą a POChP.
- W przeciwieństwie do spirometrii pozwala na ocenę hiperinflacji płuc.
- ERS nie zaleca wykonywania tego badania celem potwierdzenia rozpoznania astmy.3
Badanie transferu płucnego dla tlenku węgla (DLCO) (badanie specjalistyczne)
- Służy do ilościowej oceny procesu dyfuzji gazów przez barierę pęcherzykowo–włośniczkową.
- W astmie zwykle pozostaje bez zmian.
- Nie jest to badania pomocne w diagnostyce astmy– może być przydatne w diagnostyce różnicowej.
Pomiar szczytowego przepływu wydechowego (Peak Expiratory Flow – PEF) (w praktyce lekarza rodzinnego, ewentualnie pomiar własny)
- Rozpoznanie astmy nie powinno być stawiane wyłącznie na podstawie pomiaru szczytowego przepływu wydechowego (PEF), jeśli jest możliwość przeprowadzenia spirometrii oraz spirometrycznej próby rozkurczowej.3,27
- Należy monitorować PEF przez okres 1–2 tygodni.
- Zmienność dobową PEF >20% może potwierdzać rozpoznanie astmy.3
- Za prawidłową zmienność dobową PEF przyjmuje się <10% u dorosłych i <13% u dzieci.
- Zmienność dobową PEF >20% może potwierdzać rozpoznanie astmy.3
- Prawidłowa wartość PEF nie wyklucza obturacji i rozpoznania astmy!
- Domowy pomiar wartości PEF jest przydatny do oceny przebiegu choroby i oceny kontroli astmy.
- Nadmierna dobowa zmienność PEF u chorego z rozpoznaną astmą wskazuje na pogorszenie kontroli choroby.
- Ciągłe monitorowanie PEF zaleca się tylko u chorych z ciężką astmą lub z zaburzoną percepcją obturacji.27
- Badanie przydatne w rozpoznaniu astmy zawodowej.
- Ogólnie niezalecany u dzieci.
Dalsze badania
Stężenie tlenku azotu (FeNO) w powietrzu wydychanym
- Jedno z badań pomocniczych mogących potwierdzić rozpoznanie astmy.
- Zwykle zwiększone u nieleczonych chorych na astmę z zapaleniem eozynofilowym (Th high), ale może być też podwyższone u chorych z atopią, alergicznym nieżytem nosa czy egzemą.
- Zwiększone FeNO (>50 ppb) koreluje z dobrą odpowiedzią na leczenie GKSw.27
- Niski poziom FeNO nie wyklucza rozpoznania astmy. Niskie wartości są charakterystyczne dla astmy neutrofilowej.
- Niski poziom FeNO występuje u chorych leczonych GKSw, palących papierosy czy leczonych dupilumabem.
- Zalecana wartość graniczna (według American Thoracic Society) to FeNO <20 ppb dla dzieci (<25 ppb dla dorosłych).
- W przypadku podwyższonych wartości należy sprawdzić adherencję terapeutyczną, a w razie potrzeby zwiększyć dawkę GKSw.
Badanie rentgenowskie
- Brak wskazań w rutynowej diagnostyce.
- Zwykle obraz prawidłowy.
- W zaostrzeniu mogą występować cechy rozdęcia płuc i powikłania zaostrzenia (np. odma opłucnowa).2
- Zdjęcie RTG klatki piersiowej w 2 płaszczyznach pomocne w diagnostyce różnicowej objawów chorobowych (kaszel, plwocina i/lub duszność), w przypadku nietypowych objawów lub rozbieżnych wyników badań.
- W razie potrzeby można poszerzyć diagnostykę o badanie TK klatki piersiowej.
- U dzieci i młodzieży bardziej zalecane jest wykonywanie USG płuc.
Diagnostyka laboratoryjna
- W razie braku odpowiedzi na leczenie, częstych infekcji dróg oddechowych, nacieków płucnych lub w ciężkiej astmie, diagnostykę warto poszerzyć o dodatkowe badania laboratoryjne:
- Liczba leukocytów oraz CRP w przypadku podejrzenia zaostrzenia i/lub infekcji.
- Bezwzględna liczba eozynofili (eozynofile/mcl) jako marker eozynofilowego zapalenia dróg oddechowych i skuteczności terapii anty–IL–5.
- Całkowite IgE we krwi oraz IgE swoiste mogą ujawnić uczulający alergen u chorego na astmę alergiczną (wywiad lekarski!).
- Wartości powyżej 100 kU/l wskazują na alergiczną genezę astmy.
- Jeśli wartości wynoszą >1000 kU/l, a przebieg jest powikłany, należy wziąć pod uwagę inne rozpoznanie, np. zespół Churga–Straussa lub alergiczną aspergilozę oskrzelowo–płucną.
Diagnostyka alergologiczna krok po kroku
- Powinna być wykonywana u pacjentów z podejrzeniem astmy alergicznej.
- Diagnostyka krok po kroku:
- wywiad dotyczący alergii, w tym wywiad zawodowy
- alergiczne testy skórne (np. punktowe)
- oznaczanie IgE całkowite i swoiste
- w razie potrzeby próby prowokacyjne z alergenami
- diagnostyczne wyeliminowanie narażenia.
Weryfikacja rozpoznania
- Rozpoznanie astmy należy zweryfikować lub zakwestionować w przypadku:
- niewystarczającej kontroli pomimo leczenia zgodnego z wytycznymi
- nieuzyskania długotrwałej remisji, mimo uwzględnienia sezonowych czynników wyzwalających.
- Celem jest uniknięcie błędnego rozpoznania oraz niewłaściwego leczenia.
Kryteria ciężkiej astmy
- U dorosłych
- Astma pozostaje niekontrolowana mimo optymalnego leczenia o maksymalnej intensywności 4. lub 5. stopnia oraz opanowywania czynników współistniejących zaostrzających chorobę.
- Astma nasilająca się po zmniejszaniu dużych dawek leków.
- Potencjalne korzyści z włączenia leków biologicznych.
- Wymaga różnicowania z astmą trudną do leczenia: ze względu na czynniki wpływające na compliance, nieprawidłową inhalację leków lub współchorobowość (nieżyt nosa, otyłość).
- U dzieci i młodzieży
- Właściwe i odpowiednio prowadzone leczenie w celu uzyskania dobrej kontroli astmy.
- Utrzymująca się (>6 miesięcy) potrzeba dodatkowej terapii preparatem LAMA lub przeciwciałem monoklonalnym i/lub dużą dawką dobową GKSw.
Diagnostyka różnicowa
Dorośli
- Przewlekła obturacyjna choroba płuc (POChP).
- Przewlekłe zapalenie oskrzeli (uporczywy kaszel z plwociną).
- Zaburzenia oddychania, np. zespół hiperwentylacji.
- Rozstrzenie oskrzeli.
- Asthma cardiale (niewydolność serca).
- Mukowiscydoza (cystic fibrosis).
- Dysfunkcja strun głosowych (Vocal Cord Dysfunction – VCD).
- Aspiracja ciała obcego.
- Guz (krtań, tchawica, płuco).
- Hiperwentylacja.
- Otyłość.
- Zapalenie płuc.
- Krztusiec.
- Odma opłucnowa.
- Zatorowość płucna.
- Zwłóknienie płuc.
- Refluks żołądkowo–przełykowy.
- Gruźlica.
Dzieci i młodzież
- Wirusowe zapalenie oskrzeli.
- Zapalenie oskrzelików (wirus RS).
- Wrodzone wady serca.
- Wrodzone anomalie, np. tracheobronchomalacja.
- Aspiracja ciała obcego.
- Mukowiscydoza (cystic fibrosis).
- Podgłośniowe zapalenie krtani.
- Zapalenie nagłośni.
- Krztusiec.
- Cukrzycowa kwasica ketonowa.
- Zapalenie płuc.
- Odma opłucnowa.
- Hiperwentylacja.
- Dysfunkcja strun głosowych (Vocal Cord Dysfunction – VCD).
- Gruźlica.
Diagnostyka różnicowa astmy i POChP
- Patrz tabela różnicowanie astmy i POChP.
Wywiad
- Poza typowymi objawami chorobowymi, koniecznie należy uzupełnić wywiad o następujące informacje:
- Leki: szczegółowa historia przyjmowania leków
- ASA i NLPZ, a także beta–blokery mogą wpływać na ryzyko zaostrzeń astmy.
- Wywiad zawodowy
- W około 15% (9–25%) nowo rozpoznanych przypadków narażenie związane z pracą ma kluczowe znaczenie dla rozwoju choroby.31
- Astmę zawodową często poprzedzają objawy nieżytu nosa.32
- Zobacz też artykuł zawodowe alergiczne choroby układu oddechowego.
- Leki: szczegółowa historia przyjmowania leków
- W przypadku małych dzieci, w wywiadzie należy zwrócić uwagę na następujące kwestie:
Badanie fizykalne
- Patrz wyżej.
Badania uzupełniające w praktyce lekarza rodzinnego
Badania czynnościowe układu oddechowego
- Zaleca się przeprowadzenie badań czynnościowych płuc (zwykle spirometrii podstawowej, w miarę możliwości również próby rozkurczowej) w celu potwierdzenia rozpoznania i diagnostyki różnicowej.
- Powtarzanie badań czynnościowych płuc w celu określenia kontroli przebiegu choroby i skuteczności terapii.
- Więcej informacji na temat diagnostyki czynnościowej płuc znajdziesz wyżej.
Diagnostyka laboratoryjna
- Badania laboratoryjne nie są wymagane do rozpoznania, ale mogą być przydatne w diagnostyce różnicowej oraz w określeniu fenotypu astmy przed włączeniem leczenia biologicznego.
- Patrz wyżej.
- Bezwzględna liczba eozynofili (eozynofile/mcl)
- marker eozynofilowego zapalenia dróg oddechowych i skuteczności terapii anty–IL–5
- związek pomiędzy zwiększoną liczbą eozynofili (>400/mcl) a liczbą zaostrzeń, zmniejszoną kontrolą astmy i ryzykiem wystąpienia ostrych incydentów oddechowych.33
Diagnostyka specjalistyczna
- Więcej informacji na temat badań instrumentalnych zobacz wyżej.
- Informacje dotyczące diagnostyki alergologicznej metodą krok po kroku – zobacz wyżej.
Wskazania do diagnostyki specjalistycznej/hospitalizacji
- Wskazanie do skierowania do Poradni lub Oddziału Chorób Płuc:
- Wątpliwości dotyczące rozpoznania.
- Niewystarczająca kontrola astmy pomimo intensywnego leczenia i stosowania się pacjenta do zaleceń.
- Wcześniejsze leczenie w nagłych wypadkach.
- Wskazania do leczenia przeciwciałami monoklonalnymi.
- W razie potrzeby w przypadku chorób towarzyszących, które mają negatywny wpływ na kontrolę astmy (np. POChP, przewlekłe zapalenie zatok).
- Dzieci i młodzież, u których astma wymaga leczenia na 4. lub 5. stopniu intensywności terapii.
- Opieka w czasie ciąży:
- Konsultacja na początku ciąży odnośnie leczenia w celu osiągnięcia dobrej kontroli astmy podczas ciąży.
- Kobiety w ciąży z niedostateczną kontrolą astmy powinny być pod wspólną opieką współpracujących ze sobą pulmonologa i ginekologa.
- Wskazania do hospitalizacji:
- Ciężkie zakażenia dróg oddechowych i płuc.
- Kobiety ciężarne chorujące na astmę przy podejrzeniu zagrożenia dla nienarodzonego dziecka.
- W przypadku ciężkiego lub zagrażającego życiu napadu astmatycznego.
- Brak poprawy po 30–60 minutach od wstępnego leczenia łagodnego lub umiarkowanego napadu astmatycznego.
Leczenie
Cele leczenia
- Celem leczenia astmy jest osiągnięcie i utrzymanie kontroli objawów i normalnej aktywności życiowej przez długi okres czasu.
- Zminimalizowanie ryzyka:
- napadów astmatycznych i zaostrzeń astmy
- negatywnego wpływu na rozwój fizyczny, psychiczny i duchowy
- ograniczenia aktywności fizycznej i społecznej w życiu codziennym
- powikłań
- niepożądanych skutków leczenia.
- Poprawa jakości życia.
Ogólne informacje o leczeniu
Zasady leczenia astmy
- Na podstawie oceny kontroli objawów podejmowane są wszelkie decyzje terapeutyczne.3
- Zdefiniowano 3 stopnie kontroli astmy:
- 1. astma dobrze kontrolowana
- objawy dzienne ≤2 x na tydzień
- brak przebudzeń nocnych
- stosowanie leków doraźnych ≤2 x na tydzień (dotyczy SABA, nie dotyczy GKSw + formoterol jako lek doraźny)
- brak ograniczenia aktywności życiowej spowodowanego chorobą.
- 2. astma częściowo kontrolowana: spełnione 2 lub 3 z wyżej wymienionych kryteriów.
- 3. astma niekontrolowana: spełnione ≤1 z wyżej wymienionych kryteriów.
- Obserwacja przebiegu choroby na podstawie oceny w ciągu ostatnich 4 tygodni. Po interwencji terapeutycznej – powtórna ocena.
- 1. astma dobrze kontrolowana
- Do obiektywnej oceny nasilenia objawów choroby używa się Kwestionariusza Kontroli Astmy (ACQ), Testu Kontroli Astmy (ACT) lub kwestionariusza Asthma APGAR.2
- Unikanie czynników wyzwalających (np. narażenia na alergeny).
- Długotrwała i stopniowa farmakoterapia
- minimalizacja zużycia leków doraźnych poprzez efektywne, przewlekłe leczenie przeciwzapalne.
- Edukacja pacjentów i ich krewnych.
- W przypadku astmy alergicznej ewentualnie próba odczulania.
- Aby uzyskać informacje na temat leczenia u dzieci i młodzieży, zobacz też:
- Aby uzyskać informacje na temat terapii napadu astmatycznego, zobacz też:
Farmakoterapia
- Celem farmakoterapii jest uzyskanie dobrej kontroli objawów.
- Rozróżnia się leki stosowane doraźnie oraz leki stosowane długoterminowo, kontrolujące przebieg choroby.
- Leki doraźne stosowane są w stanach ostrych i w krótkim czasie zapewniają drożność oskrzeli.
- Do tej grupy należą: krótkodziałające beta–2–mimetyki (SABA), formoterol (działa szybko i długo), mała dawka GKSw w połączeniu z formoterolem (także u chorych stosujących to połączenie w terapii długotrwałej – MART (Maintenance and Reliever Therapy), krótkodziałające wziewne leki przeciwcholinergiczne (SAMA), a także glikokortykosteroidy doustne (GKSd) i inne leki stosowane przez krótki czas w celu opanowania zaostrzenia astmy.
- Długotrwała terapia ma na celu przede wszystkim zmniejszenie stanu zapalnego w drogach oddechowych, co zmniejsza objawy.
- Podstawę leczenia stanowią wziewne glikokortykosteroidy (GKSw), leki przeciwleukotrienowe oraz – zawsze w połączeniu z GKSw – długodziałające beta–2–mimetyki wziewne (LABA) lub długodziałające leki przeciwcholinergiczne (LAMA) i leki biologiczne, GKS doustne.
- Leki doraźne stosowane są w stanach ostrych i w krótkim czasie zapewniają drożność oskrzeli.
- Wybór leczenia, znajomość skutków ubocznych i techniki przyjmowania leków wziewnych są ważnymi elementami leczenia.
- Jest to kluczowe dla powodzenia terapii!
Stopniowa farmakoterapia u dorosłych
- Patrz tabela stopnie kontroli astmy u dorosłych.
- Patrz tabela schemat leczenia astmy krok po kroku.
- Rekomendacje GINA preferują podawanie GKSw w połączeniu z formoterolem zamiast SABA jako leku doraźnego.3
- Przemawia za tym możliwy wzrost ryzyka zaostrzeń przy monoterapii SABA oraz lepsza długoterminowa kontrola w efekcie stosowania GKSw.
- Patrz dawki kortykosteroidów wziewnych (GKSw) dla dorosłych.
Stopniowa farmakoterapia u dzieci i młodzieży
- Zobacz też artykuł astma u dzieci i młodzieży.
- Patrz tabela stopnie kontroli astmy u dzieci i młodzieży.
- Patrz tabela astma u dzieci i młodzieży, terapia krok po kroku.
- Patrz tabela ekwiwalentnych, dobowych dawek wziewnych kortykosteroidów (ICS) u dzieci i młodzieży.
Leczenie farmakologiczne w ostrym napadzie astmatycznym
- Zobacz artykuły:
Przegląd grup leków
- Leki stosowane w ostrym stanie (relievers):
- Preparat złożony, w jednym inhalatorze, zawierający małą dawkę glikokortykosteroidu wziewnego (GKSw) i formoterol – aktualnie preferowana opcja terapeutyczna. Takie podejście zmniejsza ryzyko ciężkiego zaostrzenia, przy podobnej jak w przypadku leczenia SABA kontroli objawów.27
- Może być stosowane na każdym stopniu leczenia, jako lek doraźny.
- U chorych leczonych w stopniu 3–5 – zarówno jako lek doraźny jak i kontrolujący przebieg choroby: (Single Inhaler) Maintenance And Reliever Therapy ((S)MART) – leczenie podtrzymujące i łagodzące objawy przy użyciu jednego inhalatora.
-
- Krótkodziałające beta–2–mimetyki (SABA): salbutamol, fenoterol
- Do rozważenia na 1. stopniu intensywności leczenia, doraźnie, każdorazowo z małą dawką GKSw.
- U chorych leczonych w stopniu 2–5, poza regularnie stosowanymi lekami kontrolującymi przebieg choroby, zawierającymi GKSw, stosuje się doraźnie SABA.
- Inne leki w ostrym napadzie astmatycznym
- krótkodziałające leki przeciwcholinergiczne (bromek ipratropium)
- parenteralne beta–2–sympatykomimetyki
- siarczan magnezu
- glikokortykosteroidy ogólnoustrojowe.
- Krótkodziałające beta–2–mimetyki (SABA): salbutamol, fenoterol
- Leki stosowane długoterminowo (controllers), leki kontrolujące przebieg choroby:
- glikokortykosteroidy wziewne (GKSw)
- np. budezonid, flutikazon
- długodziałające beta–2–mimetyki (LABA)
- np. formoterol, salmeterol
- długodziałające leki przeciwcholinergiczne (LAMA)
- antagoniści receptora leukotrienowego (LTRA)
- inne leki
- przeciwciała anty–IgE: omalizumab
- przeciwciała anty–IL–5: mepolizumab i reslizumab
- glikokortykosteroidy doustne (GKSd).
- glikokortykosteroidy wziewne (GKSw)
Wytyczne: Leczenie astmy30
Ogólne informacje o farmakoterapii
- Cele terapii:
- osiągnięcie optymalnej kontroli astmy
- unikanie zaostrzeń i napadów astmatycznych
- zmniejszenie nadreaktywności oskrzeli
- wyciszenie zapalenia dróg oddechowych związanego z astmą.
- Leczenie astmy ma na celu osiągnięcie i utrzymanie kontroli objawów zgodnie z zasadą „tyle, ile trzeba, ale jak najmniej”.
- Uzupełnienie farmakoterapii o metody niefarmakologiczne
- Ważne jest, aby pacjenci mieli jak największą wiedzę na temat swojej choroby i samodzielnego radzenia sobie z nią.
- Zbyt złożone schematy terapeutyczne mogą być przyczyną niestosowania się do zaleceń. Pacjentom należy przekazać pisemny plan leczenia, zawierający m.in. informacje na temat leków i sposobów ich przyjmowania oraz postępowania w razie nasilenia objawów.
- Ważne jest, aby pacjenci mieli jak największą wiedzę na temat swojej choroby i samodzielnego radzenia sobie z nią.
- Leki dzieli się na 2 klasy:
- Leki stosowane długoterminowo (controllers), kontrolujące przebieg choroby
- Leki te należy stosować przewlekle u dorosłych w przypadku konieczności korzystania z leków doraźnych częściej niż 2 razy w tygodniu.
- Glikortykosteroidy wziewne (GKSw) stanowią podstawę długoterminowego leczenia.
- GKSw w małych lub średnich dawkach i krótkotrwale w dużych dawkach, są bezpieczne.
- W celu zapobiegania grzybicy jamy ustnej i gardła, chrypce, należy zalecać płukanie jamy ustnej po inhalacji leku lub przyjmowanie GKSw w postaci proleku (cyklezonid).
- Długodziałające beta–2–mimetyki (LABA) lub długodziałające leki przeciwcholinergiczne (LAMA) zawsze powinny być stosowane w połączeniu z GKSw (nigdy w monoterapii).
- Leki doraźne (relievers)
- Połączenie małej dawki GKSw i formoterolu to preferowana opcja leczenia doraźnego. Może być stosowane także jako lek kontrolujący przebieg choroby, stosowany przewlekle.27
- Preparaty GKSw + LABA (inny niż formoterol) nie mogą być stosowane jako leki doraźne.
- Krótko działające beta–2–mimetyki (SABA) mogą być stosowane jako leki doraźne na każdym etapie terapii, koniecznie razem z GKSw (w stopniu 1. doraźnie w małej dawce, w kolejnych adekwatnie do stopnia w ramach leczenia przewlekłego GKSw).
- Różne formy podawania leków (wziewne, doustne, pozajelitowe):
- Preferowane preparaty wziewne.
- Wyższe stężenia miejscowe, szybszy początek działania i mniej ogólnoustrojowych efektów ubocznych.
- Preferowane preparaty wziewne.
- Pacjenci chorujący na astmę powinni być leczeni zgodnie ze schematem stopniowego przyjmowania leków.
- Decyzje terapeutyczne powinny być podejmowane na podstawie oceny stopnia kontroli astmy.
- Pomimo odpowiedniej terapii i przestrzegania zaleceń, w niektórych przypadkach nie udaje się osiągnąć dobrej kontroli choroby.
- W przypadku utrzymywania się objawów i zaostrzeń konieczna jest intensyfikacja terapii (patrz poniżej).
- Przed przejściem na wyższy stopień leczenia należy sprawdzić technikę inhalacji i przestrzeganie zaleceń przez pacjenta.
- Decyzje terapeutyczne powinny być podejmowane na podstawie oceny stopnia kontroli astmy.
- Leczenie astmy sezonowej powinno być dostosowane do narażenia na sezonowe alergeny.
Ocena przebiegu choroby: kontrola astmy
- Ocena kontroli astmy stanowi podstawę do oceny długoterminowego przebiegu choroby i podejmowania decyzji terapeutycznych.
- Kontrola astmy powinna być utrzymana przy zastosowaniu jak najmniejszej liczby leków przeciwastmatycznych w jak najniższej dawce.
- Podział na 3 stopnie uwzględnia dolegliwości, ograniczenia w życiu codziennym i leki używane doraźnie w ciągu ostatnich 4 tygodni:
- Astma dobrze kontrolowana:
- objawy dzienne ≤2 x na tydzień
- brak przebudzeń nocnych
- leki doraźne stosowane ≤2 x na tydzień
- brak ograniczeń aktywności życiowej spowodowanych chorobą.
- Astma częściowo kontrolowana: spełnione 2 lub 3 z wyżej wymienionych kryteriów.
- Astma niekontrolowana: spełnione ≤1 z wyżej wymienionych kryteriów.
- Astma dobrze kontrolowana:
- Do oceny nasilenia objawów choroby można używać Kwestionariusza Kontroli Astmy (ACQ), Testu Kontroli Astmy (ACT) lub kwestionariusza Asthma APGAR.
- Patrz tabela stopnie kontroli astmy u dorosłych.
- Patrz tabela stopnie kontroli astmy u dzieci i młodzieży.
Dostosowanie leczenia ukierunkowanego na kontrolę astmy
- Astma kontrolowana
- Do rozważenia zmniejszenie intensywności leczenia (patrz schemat stopniowy).
- Astma powinna być kontrolowana przez co najmniej 3 miesiące przed ewentualną modyfikacją terapii i zmniejszeniem jej intensywności.
- Nie dotyczy to pacjentów z astmą sezonową. W tym przypadku leczenie jest ukierunkowane na sezonową ekspozycję na pyłki, a zmniejszenie dawek leków jest możliwe już po krótszym czasie.
- Unikanie zbyt intensywnej farmakoterapii jest szczególnie istotne w dzieciństwie – jeśli astma pozostaje dobrze kontrolowana przez 2 miesiące, możliwa jest wcześniejsza deeskalacja leczenia.
- Należy ściśle monitorować stan pacjenta w przypadku po przerwaniu leczenia GKSw lub przeciwciałami monoklonalnymi.
- Astma częściowo kontrolowana lub niekontrolowana
- Sprawdzenie techniki inhalacji (pacjent powinien zademonstrować sposób inhalacji leku) i przestrzegania zaleceń terapeutycznych.
- Przegląd potrzeb edukacyjnych.
- Kontrola obecności alergenów w środowisku.
- Uwzględnienie chorób współistniejących i czynników obciążających.
- Weryfikacja rozpoznania astmy.
- Astma częściowo kontrolowana
- Należy rozważyć intensyfikację terapii (na podstawie schematu stopniowego).
- Astma niekontrolowana
- Zaleca się intensyfikację terapii (na podstawie schematu stopniowego).
- Obserwacja, ponowna wizyta (po intensyfikacji w ciągu 3 miesięcy).
Farmakoterapia krok po kroku
- U dorosłych pacjentów z astmą zalecana jest terapia podzielona na 5 stopni.
- W doborze farmakoterapii należy brać pod uwagę stopień nasilenia objawów oraz preferencje pacjenta.
- Leczenie początkowe u dorosłych:
- U wcześniej nieleczonych pacjentów z kryteriami częściowo kontrolowanej astmy:
- Rozpoczęcie terapii długoterminowej zwykle według stopnia 2.
- U wcześniej nieleczonych pacjentów z kryteriami niekontrolowanej astmy:
- Rozpoczęcie terapii długoterminowej co najmniej według stopnia 3.
- Aby uzyskać informacje na temat stopniowej farmakoterapii u dzieci, zobacz artykuł: astma u dzieci i młodzieży.
- Patrz tabela schemat leczenia astmy krok po kroku.
- Patrz tabela astma u dzieci i młodzieży, terapia krok po kroku.
Stopień 1. leczenia kontrolującego u dorosłych
- Leczenie pierwszego wyboru:
- Doraźne stosowanie preparatu złożonego zawierającego małą dawkę GKSw i formoterol.
- Leczenie alternatywne:
- Doraźnie stosowanie GKSw za każdym razem, gdy pacjent przyjmuje doraźnie SABA lub przyjmowanie doraźnie preparatu złożonego z GKSw i SABA (w Polsce niezarejestrowany).
- Według GINA istnieje zwiększone ryzyko zaostrzeń przy zastosowaniu samej terapii SABA: taka terapia do rozważenia tylko jeśli pacjent nie wyraża zgody na leczenie małą dawką GKSw i LABA, jeśli astma jest dobrze kontrolowana, bez obciążeń w wywiadzie.27
- Postępowanie niewskazane u młodzieży i dorosłych.
- Doraźnie stosowanie GKSw za każdym razem, gdy pacjent przyjmuje doraźnie SABA lub przyjmowanie doraźnie preparatu złożonego z GKSw i SABA (w Polsce niezarejestrowany).
Stopień 2. leczenia kontrolującego u dorosłych
- Leczenie pierwszego wyboru:
- Doraźne stosowanie preparatu złożonego zawierającego małą dawkę GKSw i formoterol.
- Leczenie alternatywne:
- Regularne stosowanie glikokortykosteroidu wziewnego GKSw w małej dawce:
- np. budezonid 200–400 mcg na dobę
- podawany jako pojedyncza dawka lub podzielony na 2 dawki dzienne.
- W razie potrzeby zastosowanie urządzeń wspomagających inhalację (komora inhalacyjna).
- W razie potrzeby leczenia doraźnego stosuje się SABA lub preparat złożony GKSw i SABA (w Polsce niezarejestrowany):
- np. salbutamol 1–2 dawki z inhalatora z dozownikiem (maksymalnie 10–12 dawek na dobę w przypadku dorosłych).
- Inne opcje:
- Antagonista receptora leukotrienowego: montelukast (LTRA) w monoterapii
- dawkowanie: 10 mg 1 x dziennie doustnie
- w przypadku wystąpienia działań niepożądanych po stosowaniu GKSw lub przeciwwskazań do stosowania GKSw lub preferencji pacjenta.
- Antagonista receptora leukotrienowego: montelukast (LTRA) w monoterapii
- Stosowanie GKSw w małej dawce doraźnie za każdym razem, kiedy chory przyjmuje SABA.
- Do rozważenia dołączenie immunoterapii alergenowej podjęzykowej:
- u pacjentów uczulonych na roztocza kurzu domowego, z alergicznym nieżytem nosa oraz z FEV1 >70% wartości należnej.
Stopień 3. leczenia kontrolującego u dorosłych
- Leczenie pierwszego wyboru:
- Doraźne oraz regularne stosowanie preparatu złożonego zawierającego małą dawkę GKSw i formoterol (Maintenance and Reliever Therapy – MART)
- np. budezonid lub beklometazon z formoterolem.
- Doraźne oraz regularne stosowanie preparatu złożonego zawierającego małą dawkę GKSw i formoterol (Maintenance and Reliever Therapy – MART)
- Leczenie alternatywne:
- Regularne przyjmowanie GKSw w małej dawce i LABA
- np. budezonid/formoterol, propionian flutikazonu/formoterol, beklometazon/formoterol
- zalecane stosowanie w formie preparatu złożonego (za pomocą jednego inhalatora).
- W razie potrzeby leczenia doraźnego stosuje się SABA lub preparat złożony GKSw i SABA (w Polsce niezarejestrowany).
- np. salbutamol 1–2 dawki z inhalatora z dozownikiem (maksymalnie 8 dawek na dobę w przypadku dorosłych).
- Regularne przyjmowanie GKSw w małej dawce i LABA
- Inne opcje leczenia:
- GKSw w średniej dawce
- do rozważenia dołączenie LTRA: montelukast 10 mg 1 x dziennie doustnie
- do rozważenia dołączenie immunoterapii alergenowej podjęzykowej:
- u pacjentów uczulonych na roztocza kurzu domowego, z alergicznym nieżytem nosa oraz z FEV1 >70% wartości należnej.
- GKSw w średniej dawce
Stopień 4. leczenia kontrolującego u dorosłych
- Leczenie pierwszego wyboru:
- regularne stosowanie preparatu złożonego zawierającego średnią dawkę GKSw i formoterol
- doraźne stosowanie preparatu złożonego zawierającego małą dawkę GKSw i formoterol
- np. budezonid lub beklometazon z formoterolem.
- Leczenie alternatywne:
- regularne przyjmowanie GKSw w średniej lub dużej dawce i LABA
- np. budezonid/formoterol, propionian flutikazonu/formoterol, beklometazon/formoterol
- zalecane stosowanie w formie preparatu złożonego
- w razie potrzeby leczenia doraźnego stosuje się SABA lub preparat złożony GKSw i SABA (w Polsce niezarejestrowany)
- np. salbutamol 1–2 dawki z inhalatora z dozownikiem (maksymalnie 8 dawek na dobę w przypadku dorosłych).
- regularne przyjmowanie GKSw w średniej lub dużej dawce i LABA
- Inne opcje leczenia:
- dołączenie LAMA lub LTRA: montelukast 10 mg 1 x dziennie doustnie
- GKSw w dużej dawce
- do rozważenia dołączenie immunoterapii alergenowej podjęzykowej:
- u pacjentów uczulonych na roztocza kurzu domowego, z alergicznym nieżytem nosa oraz z FEV1 >70% wartości należnej.
- Wyczerpanie wszystkich dostępnych opcji terapeutycznych przed eskalacją terapii do poziomu:
- np. połączenie GKSw w średnich lub dużych dawkach, LABA i LTRA
- np. połączenie GKSw w średnich lub dużych dawkach i LAMA.
Stopień 5. leczenia kontrolującego u dorosłych
- Wskazana wizyta u pulmonologa/alergologa z doświadczeniem w leczeniu ciężkiej astmy.
- Leczenie pierwszego wyboru:
- jak w stopniu 4, dodatkowo dołączenie LAMA: tiotropium (w inhalatorze miękkiej mgły) 5 mcg 1 x dziennie albo preparaty złożone zawierające 3 leki: GKSw, LABA i LAMA
- regularne stosowanie preparatu złożonego zawierającego średnią dawkę GKSw i formoterol
- doraźne stosowanie preparatu złożonego zawierającego małą dawkę GKSw i formoterol
- np. budesonid lub beklometazon z formoterolem.
- Leczenie alternatywne:
- regularne przyjmowanie GKSw w dużej dawce i formoterol lub inny LABA
- np. budezonid/formoterol, propionian flutikazonu/formoterol, beklometazon/formoterol
- długotrwałe stosowanie dużych dawek GKSw może spowodować ogólnoustrojowe działania niepożądane.
- regularne przyjmowanie GKSw w dużej dawce i formoterol lub inny LABA
- Ocena fenotypu astmy i kwalifikacja do leczenia biologicznego.
- Przeciwciała monoklonalne
- Stosowane tylko wtedy, gdy nie udaje się osiągnąć dobrej kontroli astmy po 3 miesiącach optymalnego leczenia w stopniu 4 lub 5.
- Wskazania i rozpoczęcie leczenia przez specjalistę pulmonologa doświadczonego w leczeniu ciężkiej astmy.
- W programach lekowych finansowanych przez NFZ dostępne są omalizumab, mepolizumab, benralizumab, dupilumab i tezepelumab.
- Początkowe utrzymanie leczenia przewlekłego (zmniejszenie po uzyskaniu odpowiedzi klinicznej pod ścisłą kontrolą).
- Monoklonalne przeciwciało anty–IgE (omalizumab)
- wskazania: ciężka niekontrolowana astma alergiczna
- dawkowanie: 150–600 mg podskórnie (w zależności od wyjściowego stężenia IgE w surowicy i od masy ciała), 1–4 wstrzyknięcia co 2–4 tygodnie
- ocena skuteczności po 4–6 miesiącach.
- Monoklonalne przeciwciało anty–IL5 (mepolizumab)
- wskazania: ciężka niekontrolowana astma eozynofilowa u osoby dorosłej, leczona co najmniej w stopniu 4
- Definicja astmy eozynofilowej: 2–krotne wykrycie ≥300 eozynofili/mcl krwi poza zaostrzeniami w ciągu ostatnich 2 lat.
- ocena efektów terapii po co najmniej 4 miesiącach.
- dawkowanie: 100 mg podskórnie 1 x na 4 tygodnie.
- wskazania: ciężka niekontrolowana astma eozynofilowa u osoby dorosłej, leczona co najmniej w stopniu 4
- Monoklonalne przeciwciało przeciw receptorowi dla IL–5 (benralizumab)
- wskazania: astma z eozynofilią, niekontrolowana pomimo leczenia stopnia 4. lub 5. u osoby dorosłej
- dawkowanie: 30 mg podskórnie co 4 tygodnie, po 3 miesiącach co 8 tygodni.
- Monoklonalne przeciwciało przeciw receptorowi dla IL4 (dupilumab)
- wskazania: astma z eozynofilią, niekontrolowana pomimo stosowania GKSw w dużej dawce z LABA lub wymagających stosowania GKS doustnego
- dawkowanie: pierwsza dawka: 400 lub 600 mg podskórnie, kolejne 200 albo 300 mg co 2 tygodnie.
-
- Monoklonalne przeciwciało przeciwko limfopoetynie zrębu grasicy (tezepelumab)
- wskazania: ciężka astma, niekontrolowana pomimo stosowania dużych dawek GKS
- dawkowanie: 210 mg podskórnie co 4 tygodnie.
- Monoklonalne przeciwciało przeciwko limfopoetynie zrębu grasicy (tezepelumab)
- Inne opcje leczenia:
- dołączenie azytromycyny lub LTRA
- w ostateczności glikokortykosteroid stosowany doustnie (GKSd)
- wskazanie w przypadku niewystarczającej kontroli astmy pomimo maksymalnej terapii skojarzonej i dodatkowego przeciwciała monoklonalnego
- przerywana lub stała terapia małymi dawkami (≤7,5 mg prednizonu lub równoważna)
- podawanie w najmniejszej skutecznej dawce
- ryzyko działań niepożądanych (wzrost ciśnienia tętniczego, cukrzyca, osteoporoza)
- dokładne wyjaśnienie i ocena przebiegu terapii
- profilaktyka osteoporozy przy długotrwałym leczeniu (≥3 miesiące).
Swoista immunoterapia alergenowa w astmie alergicznej (SIT)
- U chorych na astmę alergiczną należy rozważyć wskazanie do immunoterapii swoistej (allergen specific immunotherapy – SIT), jeśli komponent alergiczny objawów astmatycznych jest dobrze udokumentowany (udowodnione uczulenie swoiste i wyraźne objawy kliniczne po narażeniu na alergen).
- Wskazanie i dobór antygenów oraz formy podania ustalane są przez lekarza alergologa.
- Nie zastępuje standardowego leczenia wziewnego astmy!
- Wskazania bardziej restrykcyjne niż w przypadku alergicznego nieżytu nosa i spojówek.
- Dwie formy:
- Immunoterapia podskórna (SCIT)
- zmniejsza objawy astmy i zapotrzebowanie na leki
- większe ryzyko działań niepożądanych (w tym wstrząsu anafilaktycznego)
- mniejszy komfort pacjenta: długi czas leczenia, przedłużona obserwacja po przyjęciu dawki szczepionki.
- Immunoterapia podjęzykowa (SLIT)
- u dorosłych chorych
- ze współistniejącym alergicznym nieżytem nosa
- z uczuleniem na roztocze kurzu domowego
- FEV1 >70% wartości należnej
- zaostrzenia pomimo leczenia GKSw.
- u dorosłych chorych
- Przeciwwskazanie: astma niekontrolowana.
- Umiarkowana skuteczność, ale metoda bezpieczna dla chorych.
- Patrz artykuł swoista immunoterapia alergenowa (SIT).
MART (Maintenance and Reliever Therapy)
- GINA zaleca MART jako stosowanie preparatu złożonego z GKSw i formoterolu, zarówno w ramach terapii długoterminowej, podtrzymującej, jak i doraźnie (preparaty budezonid–formoterol oraz beklometazon–formoterol).
- Możliwe jest zastosowanie preparatów GKSw wraz z SABA innym niż formoterol LABA (nie jako terapia doraźna), jednak wówczas nie jako MART. Nadal często spotykany jest termin SMART (Single Maintenance and Reliever Therapy), który oznacza to samo co MART.2,27
Technika inhalacji i wybór systemu inhalacyjnego
- Korzystanie z systemów inhalacyjnych nadal obarczone jest dużym odsetkiem błędów.
- Jednym z powodów jest duża liczba różnych form aplikacji.
- Wybór systemu inhalacyjnego
- Dostosowanie do możliwości poznawczych i motorycznych pacjentów.
- Po uwzględnieniu preferencji pacjenta.
- W zależności od wieku chorego.
- W miarę możliwości 1 system inhalacyjny stosowany długoterminowo i doraźnie (tylko 1 typ inhalatora ciśnieniowego lub proszkowego).
- Unikanie zmiany systemu inhalacyjnego w trakcie leczenia (ryzyko błędów w obsłudze)
- po zmianie ponowna edukacja w zakresie techniki inhalacji.
- Szkolenie pacjentów w zakresie stosowania systemów inhalacyjnych3
- Sama informacja na ulotce dołączonej do opakowania zazwyczaj jest niewystarczająca.
- Demonstracja sposobu działania i ewentualnie instrukcje z obrazkami.
- Regularne sprawdzanie techniki inhalacji (zwłaszcza w przypadku niedostatecznej kontroli astmy).
- Ogólne zasady stosowania systemów inhalacyjnych:
- Przed inhalacją:
- głęboki wydech (wyjątek: nebulizator)
- przed użyciem należy wstrząsnąć inhalatorem z dozownikiem.
- Przed inhalacją:
- Podczas inhalacji – optymalny manewr oddechowy zależy od rodzaju systemu inhalacyjnego.
- inhalator ciśnieniowy (metered dose inhaler – MDI) i nebulizator: powolny i głęboki wdech
- inhalator suchego proszku (dry powder inhaler – DPI): wymuszony wdech z jak największym przepływem (nie nadaje się dla małych dzieci lub w przypadku napadu astmatycznego).
- Po inhalacji:
- pauza końcowo–wdechowa trwająca co najmniej 3, a najlepiej 5–10 sekund
- odstawienie urządzenia (unikanie wydechu do urządzenia).
- Urządzenia wspomagające inhalację (komora inhalacyjna)
- Możliwość stosowania od 1. roku życia.
- Zwiększenie depozycji leku w płucach o 15–20%.
- W długotrwałej terapii GKSw lepsza dostępność substancji czynnej z ograniczeniem działań niepożądanych.34
- Komory inhalacyjne często zastępują stosowanie nebulizatorów u dzieci do 4.–5. roku życia.35
- Technika inhalacji: powolny, głęboki wdech przez kilka oddechów.
- Najbardziej odpowiednie systemy inhalacyjne dla dzieci:
- Dzieci poniżej 5 lat
- preferowane inhalatory zawierające gaz nośnikowy z komorą inhalacyjną
- jak najwcześniejsze zastąpienie maski twarzowej ustnikiem (np. po ukończeniu przez dziecko 2. roku życia).
- Dzieci od 5 lat
- inhalator ciśnieniowy dozujący z komorą inhalacyjną i ustnikiem.
Leki stosowane w ostrym stanie3
- Patrz leczenie ostrego napadu astmatycznego.
- Krótko działający beta–2–mimetyk (SABA)
- Salbutamol: MDI 100 mcg (Aspulmo, Sabumalin, Ventolin), DPI 100 i 200 mcg (Buventol Easyhaler), DPI 200 mcg (Ventolin Dysk), roztwór do nebulizacji 1 i 2 mg/ml.
- Fenoterol: MDI 100 mcg (Berotec N 100).
- Jeśli stosowane pMDI – dołączyć komorę przedłużającą.
- Preparat złożony zawierający GKSw i formoterol
- Budezonid + formoterol: DPI 4,5 mcg/80 mcg, 4,5 mcg/160 mcg, 9 mcg/320 mcg (Airbufo Forspiro, Bufomix Easyhaler, DuoResp Spiromax, Symbicort Turbuhaler), MDI 4,5 mcg/160 mcg (Symbicort).
- Beklometazon + formoterol: MDI 6 mcg/100 mcg, 6 mcg/200 mcg (Formodual, Fostex), DPI 6 mcg/100 mcg (Fostex NEXThaler).
- Zwiększenie częstości przyjmowania, bez modyfikacji dawki.
- Krótkodziałające leki przeciwcholinergiczne (SAMA)
- Bromek ipratropium: MDI 20 mcg (Atrodil, Atrovent N, Ipravent Inhaler), roztwór do nebulizacji (0,25 mg/ml) (Atrovent).
- Zalecane w ciężkich i zagrażających życiu napadach astmatycznych oraz w przypadku niewystarczającego działania SABA.
- Mogą mieć lepsze działanie w połączeniu z SABA niż podawane oddzielnie.36
- Glikokortykosteroidy doustne (GKSd)
- Prednizon 40–50 mg (Encorton) lub prednizolon (Encortolon, Predasol) lub metyloprednizolon (Medrol, Meprelon, Metypred) doustnie.
- Wczesne zastosowanie doustnych kortykosteroidów zmniejsza prawdopodobieństwo hospitalizacji.37
- Nie zastępują stosowania GKSw – należy wdrożyć jak najszybciej!
- Stosowanie doustne równie skuteczne jak dożylne.
- Tlenoterapia
- W ostrym napadzie astmatycznym zaleca się podawanie tlenu z małą szybkością przepływu.
- Cel: saturacja na poziomie co najmniej 95%.
- Siarczan magnezu
- Dożylne podawanie siarczanu magnezu jest zalecane w przypadku ciężkich napadów astmatycznych ze słabą odpowiedzią na leczenie oraz w przypadku ataków zagrażających życiu.38
- 1,0–2,0 g w ciągu 20 minut (Inj. Magnesii Sulfurici Polpharma) najlepiej w nebulizacji z salbutamolem (skuteczniejsza niż z 0,9% NaCl).2
- Teofilina
- Liczba przepisywanych recept na ten lek zmniejszyła się w ostatnich latach.
- Nie należy stosować:
- niski zakres terapeutyczny, możliwość wystąpienia działań niepożądanych
- dostępne alternatywne metody terapii.
- Stosowanie tylko w sytuacjach zagrożenia życia i przy braku odpowiedzi na początkową terapię
- oznaczanie poziomu w surowicy po pierwszym podaniu.
Leczenie długoterminowe, kontrolujące przebieg choroby3
- Glikokortykosteroidy wziewne (GKSw)
- beklometazon: MDI 100 i 200 mcg (Soprobec)
- flutikazon: MDI 50, 125 i 250 mg (Flixotide, Flurhinal), DPI 50, 100, 125, 250 i 500mcg (Flixotide Dysk, Flutixon), zaw. do nebulizacji 0,25 i 1 mg/ml (Flixotide)
- budezonid: MDI 200 mcg (Budiair, Ribuspir), DPI 100, 200 i 400 mcg (Budesonide Easyhaler, Budezonid Lek-AM, Miflonide Breezhaler, Pulmicort Turbuhaler), zaw. do nebulizacji 0,125, 0,25 i 0,5 mg/ml (BDS N, Benodil, Budixon Neb, Nebbud, Pulmicort)
- najskuteczniejsze dostępne leki do stosowania na stałe.3
- Patrz tabela porównawcza dawek kortykosteroidów wziewnych (GKSw) dla dorosłych.
- Patrz tabela ekwiwalentnych, dobowych dawek wziewnych kortykosteroidów (ICS) u dzieci i młodzieży.
- Do udowodnionych efektów należą:
- ograniczenie zapalenia błony śluzowej w drogach oddechowych
- zmniejszenie nadreaktywności oskrzeli
- poprawa czynności płuc
- mniejsza częstotliwość objawów astmy, rzadsze i łagodniejsze zaostrzenia
- zmniejszenie liczby przyjęć do szpitala i zgonów
- zmniejszenie ilości leków doraźnych.
- Działania niepożądane
- Mogą wystąpić miejscowe działania niepożądane (pleśniawki jamy ustnej, dysfonia).
- Zaleca się, aby po zastosowaniu leku pacjenci przepłukali jamę ustną wodą.
- W razie potrzeby należy zastosować komorę inhalacyjną, aby zmniejszyć gromadzenie leku w jamie ustnej i gardle.34,39
- Regularne stosowanie może prowadzić do zahamowania wzrostu u dzieci.
- Do udowodnionych efektów należą:
- Długodziałające beta–2–mimetyki (LABA)
- Formoterol: MDI 12 mcg (Atimos), DPI 4,5, 9 i 12 mcg (Foradil, Forastmin, Formoferol Easyhaler, Oxis Turbuhaler, Oxodil PPH, Zafiron).
- Salmeterol: MDI 25 mcg (Pulveril, Serevent), DPI 50 mcg (Pulmoterol, Serevent Dysk).
- LABA nie powinny być stosowane jako monoterapia, a jedynie razem z GKSw.40-43
- W przypadku samodzielnego podawania prowadzą do pogorszenia stanu i zwiększenia liczby zaostrzeń.
- Preparat złożony z formoterolu i budezonidu (GKSw) w stałych dawkach zarówno jako leczenie długoterminowe, jak i jako lek doraźny zmniejsza liczbę zaostrzeń.
- Takie zastosowanie GKSw i formoterolu w stałej kombinacji nazywane jest ([Single Inhaler] Maintenance and Reliever Therapy – MART).
- Kombinacja małych dawek GKSw i LABA jest najskuteczniejszym i najbezpieczniejszym sposobem zapobiegania i ograniczania zaostrzeń.44
- Mniej zaostrzeń w przypadku terapii skojarzonej niż w przypadku stosowania samych GKSw.45
- Antagoniści receptora leukotrienowego (LTRA):
- Montelukast: 10 mg 1 x dziennie doustnie (Asmenol, Astmodil, Milukante, Monkasta).
- Stosowany tylko w leczeniu łagodnej i umiarkowanej astmy.
- Montelukast może być stosowany jako monoterapia u dzieci w wieku 2–14 lat na drugim poziomie terapii.
- U dorosłych pacjentów dodanie LABA do GKSw jest bardziej skuteczne niż LTRA, zwłaszcza biorąc pod uwagę czynność płuc.46
- FDA ostrzega przed zwiększonym ryzykiem neuropsychiatrycznych działań niepożądanych i zaleca ścisłe stosowanie się do wskazań.47
- Długodziałające leki przeciwcholinergiczne (LAMA):
- Tiotropium: SMI (inhalator miękkiej mgły) (Spiriva Respimat) 2,5 mcg.
- Leki z grupy LAMA nie powinny być stosowane jako monoterapia, a w razie potrzeby jako leki dodatkowe u chorych leczonych w stopniu 4–5.
- Przeciwciała anty–IgE: omalizumab
- W Polsce możliwość leczenia w ramach programu lekowego finansowanego przez NFZ u chorych z ciężką postacią astmy alergicznej IgE–zależnej.50
- Zatwierdzony u dzieci od 6. roku życia, młodzieży i dorosłych na najwyższym stopniu leczenia.
- Dawkowanie: 150–600 mg 1–4 wstrzyknięcia podskórnie co 2–4 tygodnie (w zależności od stężenia IgE w surowicy i od wagi).
- Przeciwciało monoklonalne wiąże się z krążącymi w organizmie przeciwciałami typu IgE.
- Może być stosowany w przypadku ciężkiej astmy, która jest niekontrolowana pomimo optymalnego leczenia.
- Omalizumab zmniejszył liczbę i ciężkość zaostrzeń u pacjentów już leczonych GKSw i LABA.
- Duże koszty leczenia.
- Przeciwciała anty–IL5: mepolizumab, benralizumab i resilizumab (niedostępny w Polsce)
- Dla dorosłych pacjentów na 5. stopniu leczenia z ciężką astmą eozynofilową.
- Przeciwciała anty–IL5 stosowane jako terapia dodatkowa, zmniejszają liczbę zaostrzeń u pacjentów z ciężką, źle kontrolowaną astmą eozynofilową o około 50%.51
- Dawkowanie – 1 wstrzyknięcie co 4 tygodnie:
- mepolizumab 100 mg podskórnie
- reslizumab 3 mg/kg m.c. dożylnie
-
-
- benralizumab (przeciwciało przeciw receptorowi dla IL5) 30 mg podskórnie.
-
- Przeciwciała przeciwko limfopoetynie zrębu grasicy: tezepelumab
- dawkowanie: 210 mg 1 wstrzyknięcie podskórne co 4 tygodnie.
- Glikokortykosteroidy doustne (GKSd)
- Tylko jako dodatkowa opcja terapii w stopniu 5. ze względu na możliwe ciężkie działania niepożądane.
- Wskazane tylko wtedy, gdy kontrola astmy jest niewystarczająca pomimo łącznego stosowania różnych metod terapii z poprzedniego etapu oraz dodatkowo przeciwciał monoklonalnych.
- Zaprzestanie terapii glikokortykosteroidami, zwłaszcza podawanymi systemowo >3 tygodni, niesie ze sobą ryzyko wystąpienia niedoczynności kory nadnerczy.52
- Immunoterapia swoista (allergen specific immunotherapy – SIT)
- Patrz wyżej.
Przegląd kontroli astmy i dostosowanie terapii
- Patrz wyżej.
Metody niefarmakologiczne
- Leczenie farmakologiczne astmy powinno być uzupełnione o metody niefarmakologiczne.3
- Celem jest między innymi wzmocnienie umiejętności radzenia sobie z chorobą i samokontroli.
- Do metod niefarmakologicznych należą:
- edukacja pacjentów
- fizjoterapia i fizjoterapia układu oddechowego
- aktywność fizyczna
- unikanie ekspozycji na alergeny lub inne czynniki wyzwalające
- redukcja masy ciała w razie nadwagi i otyłości
- zaprzestanie palenia
- ewentualne doradztwo społeczne i zawodowe
- wsparcie ze strony rodziny i społeczności.
Edukacja pacjenta
- Wszystkim leczonym przewlekle pacjentom z astmą należy zalecić i umożliwić udział w zorganizowanym programie edukacji behawioralnej.
- W przypadku dzieci i młodzieży należy w miarę możliwości zaangażować rodziców.
- Należy zapewnić regularne szkolenia uzupełniające.
- Udowodnione działanie:
- poprawa kontroli astmy z mniejszą liczbą napadów astmatycznych
- poprawa jakości życia
- zmniejszenie liczby dni hospitalizacji, niezdolności do pracy i nieobecności w szkole
- aktywny udział pacjentów (w przypadku dzieci i młodzieży także ich rodzin) w procesie radzenia sobie z chorobą.
- Treść programów edukacyjnych:
- patofizjologia i czynniki wyzwalające chorobę
- zasady leczenia
- techniki inhalacji
- przestrzeganie schematu leczenia
- indywidualny plan działania w przypadku astmy lub plan samokontroli53
- np. dziennik objawów, domowe pomiary PEF
- zdolność do samokontroli.
Unikanie czynników wyzwalających
- W miarę możliwości należy unikać zidentyfikowanych czynników wyzwalających, np. zimnego powietrza czy zanieczyszczeń powietrza.
- Unikanie alergenów
- Istotny element leczenia astmy alergicznej.
- W przypadku udowodnionej alergii na zwierzęta z objawami przy ekspozycji, należy dążyć do unikania bezpośredniego i pośredniego kontaktu ze zwierzętami.
- Niestosowanie leków potencjalnie wywołujących napady (ASA, NLPZ lub beta–blokery).
- Dostosowanie środowiska zawodowego, jeśli istnieje związek z objawami astmy.
- Adaptacja środowiska domowego
- unikanie wilgoci w pomieszczeniach i rozwoju pleśni
- środki zmniejszające ekspozycję na alergeny, np. specjalne pokrowce na łóżka chroniące przed roztoczami kurzu domowego lub filtry powietrza
- antyroztoczowe pokrowce na materac mogą przyczynić się do zmniejszenia ilości alergenów.
Fizjoterapia
- Fizjoterapia oddechowa
- Mobilizacja mięśni oddechowych oraz nauka i wzmocnienie fizjologicznych wzorców oddechowych.
- Powinna być oferowana wszystkim pacjentom, u których współwystępuje astma i zaburzenia oddychania.
- Powinna być zalecana pacjentom z astmą i lękiem wywołanym przez duszność.
- Celem jest kontrolowanie duszności, kaszlu i niepokoju.
- Trening oddechowy połączony z treningiem relaksacyjnym lub metodami biofeedback może również prowadzić do zmniejszenia objawów i poprawy jakości życia.54
- Z doświadczenia klinicznego wynika, że ćwiczenia oddechowe są korzystne, ale ich efekt nie jest jednoznacznie potwierdzony.55
Aktywność fizyczna
- Wszystkim pacjentom z astmą należy zalecić trening fizyczny (np. sporty szkolne, grupy ćwiczeń płuc).
- Objawy wywołane wysiłkiem fizycznym są często wyrazem niedostatecznej kontroli astmy.
- W razie potrzeby intensyfikacja terapii długoterminowej zgodnie z zasadami terapii stopniowej.
- Efekty regularnej aktywności fizycznej to:56
- zmniejszenie objawów astmy
- poprawa odporności
- poprawa jakości życia
- zmniejszenie zachorowalności
- uniknięcie stygmatyzacji.
- Redukcja masy ciała przy nadwadze ma pozytywny wpływ na przebieg choroby.
- Redukcja masy ciała jest zalecana w przypadku astmy i otyłości.
- Regularny trening fizyczny poprawia funkcjonowanie serca i maksymalny pobór tlenu; jednak badania wykazały, że czynność płuc prawdopodobnie pozostaje bez zmian.57
Zaprzestanie palenia tytoniu
- Zaprzestanie palenia
- Wszystkim pacjentom z astmą należy zalecić zaprzestania palenia tytoniu.
- Pacjenci, którzy chcą rzucić palenie, powinni uzyskać od lekarza stosowną poradę w tym zakresie.
- Zaoferowanie pomocy niefarmakologicznej i farmakologicznej.
- Pacjenci powinni mieć możliwość życia w środowisku wolnym od dymu tytoniowego.
Rehabilitacja
- Powinna być oferowana pacjentom, u których pomimo odpowiedniej opieki ambulatoryjnej występują uciążliwe fizyczne, społeczne lub psychiczne konsekwencje choroby.
- Konsekwencje choroby utrudniają możliwości wykonywania normalnych czynności lub uczestniczenia w normalnym życiu zawodowym i prywatnym.
- Działania rehabilitacyjne należy rozważyć zwłaszcza po leczeniu szpitalnym napadów astmatycznych. Podejście wielokierunkowe obejmuje między innymi:
- spersonalizowaną diagnostykę
- badanie czynników wyzwalających i narażenia na alergeny
- optymalizację leczenia
- edukację pacjenta
- fizjoterapię i terapię treningową
- poradnictwo psychologiczne i psychoterapię
- zaprzestanie palenia
- konsultacje dietetyczne
- doradztwo zawodowe.
Astma i choroby współistniejące
- Nieżyt nosa
- Astma związana jest z przewlekłymi chorobami zapalnymi górnych dróg oddechowych.
- Niektórzy autorzy uważają, że choroby zapalne o takiej samej patogenezie w górnych i dolnych drogach oddechowych, stanowią jednolity obraz kliniczny (hipoteza united airways).
- Przewlekłe choroby zapalne górnych dróg oddechowych powinny być rzetelnie diagnozowane i leczone, aby zapobiec rozwojowi lub pogorszeniu kontroli astmy oskrzelowej.
- Refluks
- Refluks żołądkowo–przełykowy występuje znacznie częściej u chorych na astmę niż w populacji ogólnej.
- Pacjenci z objawami zgłaszali wpływ na jakość życia, ale choroba refluksowa wydawała się nie mieć wpływu na objawy astmy.58
- Objawowa choroba refluksowa powinna być leczona zgodnie z obowiązującymi wytycznymi.
- Choroby psychiczne
- Należy uwzględnić sytuację psychologiczną i środowisko społeczne w leczeniu i ocenie przebiegu choroby.
- Upośledzenie psychospołeczne spowodowane astmą jest powszechne i niedostatecznie diagnozowane w życiu prywatnym i zawodowym pacjentów.
- Może utrudniać leczenie i samokontrolę.
- Astmie często towarzyszą zaburzenia lękowe i depresja.
- U dzieci i młodzieży rozwój fizyczny, umysłowy i edukacyjny może być zaburzony przez współistniejące choroby psychiczne.
- Leczenie psychospołeczne i psychoterapeutyczne stanowią często część rehabilitacji pneumologicznej.59
Niekonwencjonalne i alternatywne metody leczenia
- Pacjentów (a w przypadku dzieci – ich rodziców) należy zapytać, czy stosują niekonwencjonalne metody leczenia astmy. Jeśli tak, należy poinformować o ryzyku dla zdrowia ze względu na brak dowodów skuteczności takiej terapii i zdecydowanie zalecić kontynuowanie leczenia o udowodnionej skuteczności.
- W związku z niewystarczającą ilością danych, nie można wydać wiarygodnej opinii na temat poniższych metod:
- akupunktura60
- homeopatia
- chiropraktyka61
- suplementy diety (olej rybny, ograniczenie soli, podawanie witaminy C, suplementacja lub ograniczenie minerałów)
- hipnoza lub techniki relaksacyjne.
- W indywidualnych przypadkach: poprawa subiektywnego samopoczucia lub czynności płuc
- jonizatory powietrza w pomieszczeniu (air Ionizers)
-
- nie należy ich stosować w terapii astmy
- kontrola wilgotności
- speleoterapia
- tradycyjna medycyna chińska (TCM)
- fitoterapia
- mieszanki ziołowe mogą zawierać składniki, które pozytywnie wpływają na astmę.
- Termoplastyka oskrzeli
- Eksperymentalna metoda leczenia stosowana w ramach badań klinicznych u najciężej chorych.
- Procedura bronchoskopowa w alternatywnym leczeniu astmy: przeprowadzana w wyspecjalizowanych ośrodkach.
- Drogi oddechowe są poddawane działaniu ciepła poprzez leczenie impulsami o częstotliwości radiowej.
- Wytyczne klasyfikują dowody dotyczące skuteczności i długoterminowego efektu jako niewystarczające.
- Według GINA do rozważenia jako dodatkowe leczenie w ciężkich przypadkach.3
- U pacjentów z niekontrolowaną astmą i częstymi zaostrzeniami należy oznaczyć poziom witaminy D i w razie potrzeby ją suplementować.
- U niektórych pacjentów z niskim poziomem witaminy D i częstymi napadami astmatycznymi wymagających leczenia systemowymi glikokortykosteroidami, może wystąpić korzystny efekt ze zmniejszeniem liczby zaostrzeń.
- Nie ma danych na temat poważnych działań niepożądanych.
Astma w ciąży
- Pacjentki w wieku rozrodczym chorujące na astmę, powinny uzyskać informacje od swojego lekarza rodzinnego na temat znaczenia dobrej kontroli choroby w momencie zajścia w ciążę.
- Kobiety z dobrze kontrolowaną astmą są mniej narażone na powikłania ciążowe i porodowe.
- Niekontrolowana astma stanowi zagrożenia dla zdrowia matki i płodu.62
- Zwiększone ryzyko stanu przedrzucawkowego, cukrzycy ciążowej, odklejenia łożyska, łożyska przodującego oraz przedwczesnego porodu.
- Kobiety w ciąży z niedostateczną kontrolą astmy powinny być pod wspólną opieką współpracujących ze sobą pulmonologów i ginekologów.
- Rozpoznanie astmy nie stanowi wskazania do cięcia cesarskiego i nie powinno być wykorzystywana jako jego uzasadnienie.
- Badania kontrolne w ciąży powinny obejmować również ocenę kontroli astmy.
- Kobiety palące papierosy powinny być informowane o zagrożeniach wynikających z palenia tytoniu dla ich własnego zdrowia i zdrowia nienarodzonego dziecka. Zawsze należy proponować metody wspomagania zaprzestania palenia.
- Farmakoterapia w czasie ciąży
- Farmakoterapia, która jest niezbędna do utrzymania kontroli nad astmą, jest często modyfikowana, ograniczana lub przerywana przez pacjentki lub lekarzy z obawy przed działaniami niepożądanymi.
- Zmniejszenie lub odstawienie leków wiąże się z ryzykiem pogorszenia kontroli astmy. Wynikające z tego ryzyko dla przebiegu ciąży jest uważane za poważniejsze niż potencjalne działania niepożądane leków.
- Napad astmatyczny w ciąży
- U pacjentek w ciąży z napadem astmatycznym należy wcześnie rozpocząć leczenie tlenem (docelowa saturacja: >95%) i monitorowanie płodu.
- Indukcja porodu i leczenie poporodowej atonii macicy
- Jeśli indukcja porodu lub leczenie poporodowej atonii macicy podejmowane są za pomocą leków, u kobiet z astmą jako lek pierwszego wyboru należy zastosować oksytocynę.
Astma związana z pracą zawodową
- Znanych jest ponad 550 różnych czynników powodujących astmę zawodową.
- Istnieją 2 postaci astmy zawodowej:
- postać alergiczna (IgE–zależna)
- postać wywołana przez czynniki drażniące.
- Zawodowe czynniki wyzwalające mają wpływ na rozwój choroby u 9–25% pacjentów chorujących na astmę.
- Wywiad zawodowy jest ważnym elementem diagnostyki astmy u dorosłych.
- Zalecane są regularne badania lekarskie w ramach medycyny pracy dla pracowników z grupy ryzyka (nadzór).
- Najważniejszym sposobem leczenia astmy zawodowej jest konsekwentne unikanie czynników, które ją wywołują.
- Może się to wiązać z koniecznością zmiany pracy lub nawet przekwalifikowania się.
- Zobacz artykuł zawodowe alergiczne choroby układu oddechowego.
Zapobieganie
Ogólne
- Zobacz też artykuł zapobieganie alergii.
- Profilaktyka w astmie
- Działania interwencyjne w ramach profilaktyki pierwotnej astmy, powinny być rozpoczęte możliwie jak najwcześniej, najlepiej jeszcze w czasie ciąży.
- Działania te obejmują ograniczenie biernego narażenia na dym tytoniowy oraz wzmocnienie naturalnych czynników ochronnych (które w wyniku rozwoju współczesnej cywilizacji uległy osłabieniu).
- Zalecenia prewencyjne
- Noworodki powinny być karmione wyłącznie piersią przez 4 miesiące.
- Po 4. miesiącu życia należy wprowadzić pokarmy uzupełniające – nie należy tego opóźniać.
- Dzieci zagrożone alergią nie powinny posiadać zwierząt futerkowych ani pierzastych. Posiadanie kota jest niewskazane.
- Należy unikać dużej wilgotności i braku wentylacji w pomieszczeniach, lotnych związków organicznych (np. formaldehydu), czynnego i biernego narażenia na dym tytoniowy i spaliny pojazdów mechanicznych.
- Niemowlęta i dzieci z grupy zwiększonego ryzyka wystąpienia astmy powinny być szczepione zgodnie z ogólnymi zaleceniami.
- Nadwaga i otyłość wiążą się ze zwiększoną częstością występowania astmy.
- Opinie/stwierdzenia bez silnych dowodów naukowych
- Nie ma dowodów na to, że stosowanie częściowo lub ekstensywnie hydrolizowanych preparatów dla niemowląt jest korzystne w zapobieganiu astmie.
- Nie są wymagane żadne ograniczenia związane z dietą matki w okresie ciąży i laktacji.
- Dzieci bez ryzyka alergii nie muszą rezygnować z posiadania zwierząt domowych.
- Zwalczanie roztoczy kurzu domowego nie jest zalecane w profilaktyce pierwotnej, ale jest wskazane w profilaktyce wtórnej i trzeciorzędowej.
- Posiadanie większej liczby starszego rodzeństwa, uczęszczanie do przedszkola, dorastanie na wsi w gospodarstwie rolnym ze zwierzętami i zakażenia pasożytnicze mają ujemny związek z występowaniem astmy.
- Aktywne unikanie dymu tytoniowego i ścisłe unikanie środowiskowego dymu tytoniowego (Environmental Tobacco Smoke – ETS) jest najważniejszym działaniem profilaktycznym w czasie ciąży.
- Telemedycyna
- Teleporady mogą mieć duże znaczenie w opiece nad pacjentami z astmą, chociaż dotychczasowe dowody są niewystarczające, aby wprowadzić zalecenia dotyczące takich interwencji.
- Przykładem mogą być systemy przypominania SMS, aplikacje na smartfony i tablety lub interwencje oparte na grach dla młodzieży.
Immunoterapia swoista (SIT)
- Nie zastępuje farmakoterapii astmy, ale może być stosowana we wczesnym okresie leczenia astmy alergicznej.
- Swoista immunoterapia alergenowa (SIT, odczulanie) zmniejsza objawy astmy, zapotrzebowanie na leki i swoistą nadreaktywność oskrzeli.63
- Wskazania do działania zapobiegawczego
- U pacjentów z alergicznym nieżytem nosa immunoterapia podskórna zmniejsza nasilenie objawów astmy (zmiana stopnia leczenia) do 7 lat po zakończeniu 3–letniej terapii.64
- Wśród dzieci z alergicznym nieżytem nosa leczonych tą metodą, po 3 latach tylko u połowy z nich rozwinęła się astma w porównaniu z grupą kontrolną.65
Szczepienia
- Astma, podobnie jak inne choroby przewlekłe, zwiększa ryzyko zachorowania na grypę oraz zakażenia pneumokokowe.
- Pacjentom z astmą należy zatem regularnie proponować zalecane szczepienia przeciw grypie, pneumokokom, RSV, COVID-19 i krztuścowi
Przebieg, powikłania i rokowanie
Przebieg
- Zapalenie dróg oddechowych powoduje nawracające epizody duszności, ucisku w klatce piersiowej i kaszlu.
- Przebieg choroby może być bardzo zmienny, zwłaszcza jeśli występuje sezonowy komponent alergiczny.
- Liczba hospitalizacji z powodu zaostrzeń i napadów astmatycznych wykazuje tendencję spadkową (efekt długotrwałej terapii GKSw).
- Dzieci, u których objawy astmy występują w związku z wirusowymi infekcjami górnych dróg oddechowych, zwykle lepiej funkcjonują latem ze względu na rzadsze infekcje.
Powikłania
- Ciężki i zagrażający życiu ostry napad astmatyczny.
- Przejście w postać mieszaną z przewlekłą obturacyjną chorobą płuc – nakładanie astmy i POChP (asthma–COPD overlap – ACO).
- Wtórna niewydolność kory nadnerczy52
- Należy ją wykluczyć u pacjentów przyjmujących przez dłuższy czas duże dawki glikokortykosteroidów wziewnych (zwłaszcza flutikazonu) lub glikokortykosteroidów doustnych.
- Znaki ostrzegawcze to utrata wagi, zmęczenie, nudności i wymioty.
- Zwiększone ryzyko zachorowania na grypę oraz zakażenia pneumokokowe.
- Wskazane szczepienia zgodnie z ogólnymi zaleceniami.
Zwiększone ryzyko śmiertelności w przypadku napadu astmatycznego
- Na zwiększone ryzyko śmiertelności w przypadku ciężkiego napadu astmatycznego wskazują następujące czynniki:
- nieprzestrzeganie zaleceń terapeutycznych
- nadmierne stosowanie beta–2–sympatykomimetyków
- terapia glikokortykosteroidami doustnymi
- ciężki napad astmatyczny (near-fatal asthma) w wywiadzie
- intubacja z wentylacją mechaniczną podczas wcześniejszego napadu astmatycznego
- leczenie szpitalne z powodu zaostrzenia astmy w ciągu ostatniego roku.
Rokowanie
- U dużej części dzieci i młodzieży z astmą objawy ustępują w ciągu życia.
- W okresie dojrzewania objawy ulegają poprawie, zwłaszcza u chłopców.8
- U 30–50% dzieci objawy astmy ustępują w okresie dojrzewania, jednak choroba może nawracać w wieku dorosłym.
- U starszych dzieci objawy mają tendencję do zmniejszania się wraz z wiekiem, ale często występują jeszcze w dorosłym życiu.66
- Czynnikami predykcyjnymi uporczywej astmy są atopia, gorsza czynność płuc i nadreaktywność oskrzeli.
- U niektórych dorosłych pacjentów, zwłaszcza palaczy, z czasem może dojść do nieodwracalnych zmian w drogach oddechowych z utrwaleniem obturacji i przejściem w POChP.
- Wiek w momencie wystąpienia choroby
- Rokowanie wydaje się być związane z wiekiem w chwili rozpoznania choroby. W szczególności późny początek choroby w wieku dorosłym, zwiększa ryzyko ciężkiego przebiegu, pogorszenia czynności płuc i występowania zaostrzeń.2
- Wpływ na życie społeczne i zawodowe w astmie dziecięcej jest niewielki.66
Dalsze postępowanie
- Stały nadzór i ocena kliniczna
- Zapewnienie długoterminowej kontroli astmy i wybór najniższego skutecznego stopnia leczenia.
- Informacje na temat dostosowania terapii stopniowej znajdują się w sekcji farmakoterapia krok po kroku.
- Dalsza kontrola jest wskazana nawet w przypadku astmy kontrolowanej, ponieważ przebieg choroby bywa zmienny.
- Zapewnienie długoterminowej kontroli astmy i wybór najniższego skutecznego stopnia leczenia.
- Monitorowanie wzrostu u dzieci i młodzieży z wykorzystaniem siatki centylowej podczas długotrwałej terapii GKS.
- Szczepienia.
- Podczas każdej wizyty kontrolnej należy ocenić:
- występowanie objawów astmy w ciągu dnia, w nocy oraz podczas aktywności fizycznej
- częstotliwość stosowania leków doraźnych
- ograniczenia aktywności życia codziennego
- stosowanie się do zaleceń terapeutycznych i technikę inhalacji
- częstotliwość występowania oraz czynniki wyzwalające zaostrzenia
- skuteczność i tolerancję farmakoterapii.
Informacje dla pacjentów
Edukacja pacjenta
- Samokontrola, również w przypadku ostrych objawów:
- indywidualny plan działania w przypadku astmy lub plan samokontroli
- w razie potrzeby pomiary PEF i wpisy do dzienniczka.
- Zalecenie edukacji pacjentów i ich bliskich w ramach szkoły astmy.
- Udzielanie wskazówek dotyczących prawidłowej techniki inhalacji.
- Możliwość wsparcia ze strony organizacji samopomocy pacjentów.
Materiały edukacyjne dla pacjentów
Astma
- Astma.
- Napad astmatyczny u dorosłych.
- Astma wysiłkowa.
- Dlaczego warto rzucić palenie i jak to zrobić?
Astma u dzieci i młodzieży
Ilustracje
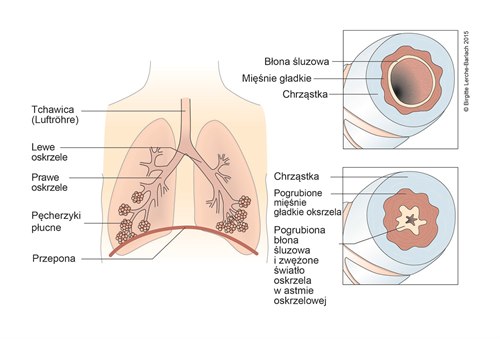
Drogi oddechowe i zmiany w astmie
Źródła
Wytyczne
- Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention 2024. ginasthma.org.
Piśmiennictwo
- GBD 2015 Chronic Respiratory Disease Collaborators. Global, regional, and national deaths, prevalence, disability-adjusted life years, and years lived with disability for chronic obstructive pulmonary disease and asthma, 1990-2015: a systematic analysis for the Global Burden of Disease Study 2015, Lancet Respir Med. 2017 Sep, 5(9): 691-706, doi: 10.1016/S2213-2600(17)30293-X, Epub 16.08.2017, PubMed PMID: 28822787, www.ncbi.nlm.nih.gov
- Lange P., Çolak Y., Ingebrigtsen T.S., Vestbo J., Marott J.L. Long term prognosis of asthma, chronic obstructive pulmonary disease, and asthma-chronic obstructive pulmonary disease overlap in the Copenhagen City Heart study: a prospective population-based analysis, Lancet Respir Med. 2016 Jun, 4(6): 454-62,. doi: 10.1016/S2213-2600(16)00098-9, Epub 6.04.2016, PubMed PMID: 27061878, www.ncbi.nlm.nih.gov
- Global Initiative for Asthma,. Global Strategy for Asthma Management and Prevention 2025 ginasthma.org
- Moorman J.E., Akinbami L.J., Bailey C.M., Zahran H.S., King M.E., Johnson C.A., Liu X. National surveillance of asthma: United States, 2001-2010, Vital Health Stat 3. 2012 Nov, (35):1-58, PubMed PMID: 24252609, www.ncbi.nlm.nih.gov
- Ramsey C.D., Celedón J.C. The hygiene hypothesis and asthma, Curr Opin Pulm Med., 2005 Jan, 11(1): 14-20, Review. PubMed PMID: 15591883, www.ncbi.nlm.nih.gov
- Kelly F.J., Fussell J.C. Air pollution and airway disease, Clin Exp Allergy, 2011 Aug, 41(8): 1059-71, doi: 10.1111/j.1365 2222.2011.03776.x Epub 30.05.2011, Review. PubMed PMID: 21623970, www.ncbi.nlm.nih.gov
- Sears M.R. Trends in the prevalence of asthma. Chest. 2014 Feb. 145(2): 219-25., doi: 10.1378/chest.13-2059, PubMed PMID: 24493506, www.ncbi.nlm.nih.gov
- Gibson G.J., Loddenkemper R., Sibille Y. et al. (Hrsg) (2013) The European lung white book. Respiratory health and disease in Europe. European Respiratory Society, Sheffield, www.ncbi.nlm.nih.gov
- Halapi, E.; Bjornsdottir, US (January 2009). "Overview on the current status of asthma genetics". The clinical respiratory journal. 3 (1): 2–7, doi:10.1111/j.1752-699X.2008.00119.x PMID 20298365, www.ncbi.nlm.nih.gov
- Dietert R.R. Maternal and childhood asthma: risk factors, interactions, and ramifications, Reprod Toxicol. 2011 Sep, 32(2): 198-204, doi: 10.1016/j.reprotox.2011.04.007 Epub 2011 May 6, Review. PubMed PMID: 21575714, www.ncbi.nlm.nih.gov
- Upton M.N., McConnachie A., McSharry C., Hart C.L., et al. Intergenerational 20 year trends in the prevalence of asthma and hay fever in adults: the Midspan family study surveys of parents and offspring, BMJ 2000, 321: 88-92, www.ncbi.nlm.nih.gov
- McCreanor J., Cullinan P., Nieuwenhuijsen M.J., et al. Respiratory effects of exposure to diesel traffic in persons with asthma, NEJM 2007; 357: 2348-58, www.nejm.org
- Ahluwalia S.K., Matsui E.C. The indoor environment and its effects on childhood asthma, Curr Opin Allergy Clin Immunol. 2011 Apr, 11(2): 137-43,. doi: 10.1097/ACI.0b013e3283445921, Review. PubMed PMID: 21301330, www.ncbi.nlm.nih.gov
- Mackay D., Haw S., Ayres J.G., et al. Smoke-free legislation and hospitalizations for childhood asthma, N Engl J Med 2010, 363: 1139-45, www.nejm.org
- Lau S., Illi S., Sommerfeld C., Niggeman B., et al. Early exposure to house dust mite and cat allergens and development of childhood asthma: a cohort study, Lancet 2000, 356: 1392-7, www.ncbi.nlm.nih.gov
- Riedler J., Braun-Fahrländer C., Eder W., Schreuer M., et al. Exposure to farming in early life and development of asthma and allergy: a cross-sectional survey, Lancet 2001, 358: 1129-33, www.ncbi.nlm.nih.gov
- Platts-Mills T., Vaughan J., Squillace S., Woodfolk J., Sporik J. Sensitisation, asthma, and a modified Th2 response in children exposed to cat allergen: a population-based cross-sectional study, Lancet 2001, 357: 752-6, www.ncbi.nlm.nih.gov
- Illi S., von Mutius E., Lau S., Bergmann R., Niggemann B., Sommerfeld C., Wahn U. Early childhood infectious diseases and the development of asthma up to school age: a birth cohort study, BMJ 2001, 322: 390-5, www.ncbi.nlm.nih.gov
- Clark C.E., Coote J.M., Silver D.A.T., Halpin D.M.G. Asthma after childhood pneumonia: six year follow up study, BMJ 2000, 320: 1514-6, www.bmj.com
- Beuther D.A. Obesity and asthma. Clin Chest Med. 2009 Sep, 30(3): 479-88, viii. doi: 10.1016/j.ccm.2009.05.002Review PubMed PMID:19700046, www.ncbi.nlm.nih.gov
- van der Hulst A.E., Klip H., Brand P.L.. Risk of developing asthma in young children with atopic eczema: A systematic review, J Allergy Clin Immunol 2007, 120: 565-9, www.ncbi.nlm.nih.gov
- Bergmann R.L., Edenharter G., Bergmann K.E., Forster J., Bauer C.P., Wahn V., et al. Atopic dermatitis in early infancy predicts allergic airway disease at 5 years, Clin Exp Allergy 1998, 28: 965-70, www.ncbi.nlm.nih.gov
- Russell G., Ninan T.K. Respiratory symptoms and atopy in Aberdeen school children: evidence from two surveys 25 years apart, BMJ 1992, 304: 873-5, www.ncbi.nlm.nih.gov
- Goksör E., Loid P., Alm B., et al.. The allergic march comprises the coexistence of related patterns of allergic disease not just the progressive development of one disease, Acta Paediatr 2016 Dec, 105(12): 1472-9, pmid:27381249, www.ncbi.nlm.nih.gov
- Etminan M., Sadatsafavi M., Jafari S., et al. Acetaminophen use and the risk of asthma in children and adults: a sytematic review and metaanalysis, Chest 2009,136: 1316-23, www.ncbi.nlm.nih.gov
- Lowe A.J., Carlin J.B., Bennett C.M., et al. Paracetamol use in early life and asthma: prospective birth cohort study, BMJ 2010, 341: c4616, dx.doi.org
- Venkatesan P. 2023 GINA report for asthma, Lancet Respir Med 2023, 11(7): 589, www.thelancet.com
- Hershenson M.B. Rhinovirus-Induced Exacerbations of Asthma and COPD. Scientifica (Cairo), 2013, 2013: 405876. doi: 10.1155/2013/405876 Epub 2013 Feb 21, Review. PubMed PMID: 24278777 PMID:24278777, www.ncbi.nlm.nih.gov
- Rajan P., Wineinger N.E., Stevenson D.D., White A.A. Prevalence of aspirin-exacerbated respiratory disease among asthmatic patients: A meta-analysis of the literature, J Allergy Clin Immunol 2015, 135: 676-81, doi:10.1016/j.jaci.2014.08.020, DOI
- Global Initiative for Asthma. Pocket Guide for Asthma Management and Prevention, Stand 2020, ginasthma.org
- Eagan T.M., Gulsvik A., Eide G.E., et al. Occupational airborne exposure and the incidence of respiratory symptoms and asthma, Am J Respir Crit Care Med 2002, 1665: 933-8, www.ncbi.nlm.nih.gov
- EAACI Task Force on Occupational Rhinitis, Moscato G., Vandenplas O., Gerth Van Wijk R., Malo J.L., Quirce S., Walusiak J., Castano R., De Groot H., Folletti I., Gautrin D., Yacoub M.R., Perfetti L., Siracusa A. Occupational rhinitis. Allergy. 2008 Aug, 63(8): 969-80, doi: 10.1111/j.1398-9995.2008.01801.x PubMed PMID: 18691299, www.ncbi.nlm.nih.gov
- Price D.B., Rigazio A., Campbell J.D., et al. Blood eosinophil count and prospective annual asthma disease burden: A UK cohort study, Lancet Respir Med 2015, 3(11): 849-58, pubmed.ncbi.nlm.nih.gov
- Leach C.L., Colice G.L. A pilot study to assess lung deposition of HFA-beclomethasone and CFC-beclomethasone from a pressurized metered dose inhaler with and without add-on spacers and using varying breathhold times, J Aerosol Med Pulm Drug Deliv. 2010 Dec, 23(6): 355-6, doi: 10.1089/jamp.2009.0783 Epub 24.06.2020, PubMed PMID: 20575669, www.ncbi.nlm.nih.gov
- Cates C.J., Welsh E.J., Rowe B.H. Holding chambers versus nebulisers for beta-agonist treatment of acute asthma, Cochrane Database Syst Rev 2013, 9: CD000052. PMID: 24037768, PubMed
- Rodrigo G.J., Castro-Rodriguez J.A. Anticholinergics in the treatment of children and adults with acute asthma: a systematic review with meta-analysis, Thorax 2005, 60: 740-6, PubMed
- Rowe B.H., Spooner C., Ducharme F.M., Bretzlaff J.A., Bota G.W. Early emergency department treatment of acute asthma with systemic corticosteroids, CochranenDatabase Syst Rev. 2001, (1):CD002178. Review. PubMed PMID: 11279756, www.ncbi.nlm.nih.gov
- Currie G.P., Devereux G.S., Lee D.K.C., Ayres J.G. Recent developments in asthma management, BMJ 2005; 330: 585-9, www.ncbi.nlm.nih.gov
- Brozek J.L., Kraft M., Krishnan J.A., et al. Long-acting beta2-agonist step-off in patients with controlled asthma: systematic review with meta-analysis, Arch Intern Med 2012: 1-11, pmid:22928176, PubMed
- Walters E.H., Gibson P.G., Lasserson T.J., Walters J.A.E. Long-acting beta2-agonists for chronic asthma in adults and children where background therapy contains varied or no inhaled corticosteroid, Cochrane Database of Systematic Reviews 2007, Issue 1. Art. No.: CD001385, Cochrane (DOI)
- Salpeter S.R., Buckley N.S., Ormiston T.M., Salpeter E.E. Meta-analysis: effect of long-acting beta-agonists on severe asthma exacerbations and asthma-related deaths, Ann Intern Med. 2006, 144: 904-12, PubMed
- Salpeter S.R., Wall A.J., Buckley N.S. Long-acting beta-agonists with and without inhaled corticostreoids and catastrophic asthma events, Am J Med 2010, 123: 322-8, PubMed
- Cates C.J., Jaeschke R., Schmidt S., et al. Regular treatment with formoterol and inhaled steroids for chronic asthma: serious adverse events. Cochrane Database Syst Rev 2013, 6: CD006924, pmid:23744625, PubMed
- Loymans R.J., Gemperli A., Cohen J., et al. Comparative effectiveness of long term drug treatment strategies to prevent asthma exacerbations: network meta-analysis, BMJ. 2014 May 13, 348:g3009. doi: 10.1136/bmj.g3009, DOI
- Busse W.W., Bateman E.D., Caplan A.L., et al. Combined Analysis of Asthma Safety Trials of Long-Acting β2-Agonists, N Engl J Med 2018, 378(26): 2497-505, pmid:29949492, www.nejm.org
- Chauhan B.F., Ducharme F.M. Addition to inhaled corticosteroids of long-acting beta2-agonists versus anti-leukotrienes for chronic asthma, Cochrane Database Syst Rev. 24.01.2014, 1:CD003137, Cochrane (DOI)
- FDA. Press Announcements. FDA Requires Stronger Warning About Risk of Neuropsychiatric Events Associated with Asthma and Allergy Medication Singulair and Generic Montelukast, March 2020, www.fda.gov
- Peterrs S.P., Kunselman S.J., Icitovic N., et al. Tiotropium bromide step-up therapy for adults with uncontrolled asthma, N Eng J Med 2010, doi:10.1056/NEJMoa1008770, DOI
- Kerstjens H.A., Engel M., Dahl R., et al. Tiotropium in asthma poorly controlled with standard combination therapy, N Engl J Med., 2.09.2012, pmid:22938706, PubMed
- Program lekowy B.44. Leczenie chorych z ciężką postacią astmy (ICD-10: J45, J82), dostęp: 21.04.2024, www.gov.pl
- Farne H.A., Wilson A., Powell C., Bax L., Milan S.J. Anti-IL5 therapies for asthma. Cochrane Database of Systematic Reviews 2017, Issue 9. Art: No.: CD010834. pmid:10.1002/14651858.CD010834.pub3, Cochrane (DOI)
- Sannarangappa V., Jalleh R. Inhaled Corticosteroids and Secondary Adrenal Insufficiency, The Open Respiratory Medicine Journal 2014, 8: 93-100, doi: 10.2174/1874306401408010093, www.ncbi.nlm.nih.gov
- Reddel H.K., Barnes D.J. Pharmacological strategies for self-management of asthma exacerbations, Eur Respir J 2006, 28: 182-99, PubMed
- Lehrer P.M., Vaschillo E., Vaschillo B., Lu S.E., Scardella A., Siddique M., Habib R.H. Biofeedback treatment for asthma, Chest. 2004 Aug, 126(2): 352-61, PubMed PMID:15302717, www.ncbi.nlm.nih.gov
- Freitas D.A., Holloway E.A., Bruno S.S., et al. Breathing exercises for adults with asthma, Cochrane Database Syst Rev. 1.10.2013, 10:CD001277, pubmed.ncbi.nlm.nih.gov
- Eichenberger P.A., Diener S.N., Kofmehl R., et al. Effects of exercise training on airway hyperreactivity in asthma: a systematic review and meta-analysis, Sports Med. 2013, 43(11): 1157-70, doi: 10.1007/s40279-013-0077-2, www.ncbi.nlm.nih.gov
- Carson K.V., Chandratilleke M.G., Picot J., Brinn M.P., Esterman A.J., Smith B.J. Physical training for asthma, Cochrane Database Syst Rev., 30.09.2013, (9):CD001116. doi: 10.1002/14651858.CD001116.pub4 Review. PubMed PMID: 24085631, www.ncbi.nlm.nih.gov
- DiMango E., Holbrook J.T., Simpson E., et al. Effects of asymptomatic proximal and distal gastroesophageal reflux on asthma severity, Am J Respir Crit Care Med 2009, 180: 8090-16, www.ncbi.nlm.nih.gov
- Ahnert J., Löffler S., Müller J., Vogel H. [Systematic literature review on interventions in rehabilitation for children and adolescents with asthma bronchiale]. Rehabilitation (Stuttg). 2010 Jun, 49(3): 147-59, doi:10.1055/s-0030-1254081, Epub 2010 Jun 8. Review. German, PubMed PMID: 20533145, www.ncbi.nlm.nih.gov
- McCarney R.W., Brinkhaus B.G., Lasserson T.J., Linde K. Acupuncture for chronic asthma, Cochrane Database of Systematic Reviews 2003, 3: CD000008, Cochrane (DOI)
- Hondras M.A., Linde K., Jones A.P. Manual therapy for asthma (Cochrane Review). In: The Cochrane Library, Issue 4 2002, Oxford: Update Software, pubmed.ncbi.nlm.nih.gov
- Nelson-Piercy C. Asthma in pregnancy. Thorax 2001, 56: 325-8, doi: 10.1136/thorax.56.4.325, thorax.bmj.com
- Abramson M.J., Puy R.M., Weiner J.M. Injection allergen immunotherapy for asthma, Cochrane Database of Systematic Reviews 2010, Issue 8. Art. No.: CD001186. Cochrane (DOI)
- Jacobsen L., Niggemann B., Dreborg S., Ferdousi H.A., Halken S., Høst A., Koivikko A., Norberg L.A., Valovirta E., Wahn U., Möller C.; (The PAT investigator group). Specific immunotherapy has long-term preventive effect of seasonal and perennial asthma: 10-year follow-up on the PAT study. Allergy. 2007 Aug, 62(8): 943-8, PubMed PMID: 17620073, www.ncbi.nlm.nih.gov
- Möller C., Derborg S., Ferdousi HA, et al. Pollen immunotherapy reduces the development of asthma in children with seasonal rhinoconjunctivitis (the PAT-study). J ALlergy Clin Immunol 2002; 109: 251-6. PubMed
- Kjellman B, Gustafsson PM. Children with asthma followed up for 21 years; severity improved, but patients seldom grow out of asthma by adulthood. Läkartidningen 2000; 97: 4572-7. www.ncbi.nlm.nih.gov
- Wytyczne konsultanta krajowego alergologii, konsultanta krajowego medycyny rodzinnej oraz prezydenta Polskiego Towarzystwa Alergologicznego dotyczące diagnostyki i leczenia astmy u dorosłych w POZ, z uwzględnieniem opieki koordynowanej z dnia 16 lutego 2024, dostęp: 21.04.2024, koordynowana.nfz.gov.pl
- Wolf F.M., Guevara J.P., Grum C.M., Clark N.M., Cates C.J. Educational interventions for asthma in children, Cochrane review, Cochrane Database Syst Rev 2004, (4): CD000326, dx.doi.org
- Guevara J.P., Wolf F.M., Grum C.M., Clark N.M. Effects of educational interventions for self management of asthma in children and adolescents: systematic review and meta-analysis, BMJ 2003; 326: 1308-9, pubmed.ncbi.nlm.nih.gov
- Gøtzsche P.C., Johansen H.K. House dust mite control measures for asthma. Cochrane Database of Systematic Reviews 2008, Issue 2. Art. No.: CD001187, Cochrane (DOI)
- Woodcock A., Forster L., Matthews E., et al. Control of exposure to mite allergen and allergen-impermeable bed covers for adults with asthma, N Engl J Med 2003, 349: 225-36, PubMed
- Mutius E., Vercelli D. Farm living: effects on childhood asthma and allergy, Nat Rev Immunol. 2010 Dec, 10(12): 861-8, doi: 10.1038/nri2871 Epub 2010 Nov 9, Review. PubMed PMID: 21060319, www.ncbi.nlm.nih.gov
- Warner J.O., ETAC Study Group. Early treatment of the atopic child. A double-blinded, randomized, placebo-controlled trial of cetirizine in preventing the onset of asthma in children with atopic dermatitis: 18 months' treatment and 18 months' posttreatment follow-up, J Allergy Clin Immunol 2001, 108: 929-37, www.ncbi.nlm.nih.gov
- Örtqvist A.K., Lundholm C., Kieler H., et al. Antibiotics in fetal and early life and subsequent childhood asthma: nationwide population based study with sibling analysis, BMJ 2014, 349: g6979, dx.doi.org
- Zhang L., Prietsch S.O.M., Ducharme F.M. Inhaled corticosteroids in children with persistent asthma: effects on growth, Cochrane Database of Systematic Reviews 2014, Issue 7. Art. No.: CD009471. DOI: 10.1002/14651858.CD009471.pub2 www.ncbi.nlm.nih.gov
- Jones A., Fay J.K., Burr M.L., Stone M., Hood K., Roberts G. Inhaled corticosteroid effects on bone metabolism in asthma and mild chronic obstructive pulmonary disease, Cochrane Database of Systematic Reviews 2002, Issue 1. Art. No.: CD003537, Cochrane (DOI)
- Normansell R., Walker S., Milan S.J., et al. Omalizumab for asthma in adults and children, Cochrane Database Syst Rev 2014, 1: CD003559, pmid:24414989, PubMed
- Norman G., Faria R., Paton F., et al. Omalizumab for the treatment of severe persistent allergic asthma: a systematic review and economic evaluation, Health Technol Assess 2013, 17: 1-342, pmid:24267198, PubMed
Opracowanie
- Prof. dr hab. Sławomir Chlabicz, (redaktor/recenzent)
- Natalia Jagiełła (redaktor)
- Elżbieta Kryj–Radziszewska (recenzent)
- Adam Windak (redaktor)
- Lino Witte (recenzent/redaktor)
- Marlies Karsch–Völk (recenzent/redaktor)
- Monika Lenz (recenzent/redaktor)
- Jonas Klaus (recenzent/redaktor)
