Streszczenie
- Definicja: Łagodny rozrost gruczołu krokowego (benign prostatic hyperplasia – BPH) to patologiczne zwiększenie liczby komórek gruczołu krokowego, które nie wykazują żadnych innych zmian chorobowych; BPH może być związany z objawami ze strony dolnych dróg moczowych.
- Epidemiologia: BPH występuje u 10% wszystkich mężczyzn w 40. roku życia i u 70–80% mężczyzn powyżej 60. roku życia, często przebiega bezobjawowo.
- Objawy: Typowe objawy to osłabienie strumienia moczu i duża częstotliwość mikcji. W około połowie przypadków pokrywają się z zespołem objawów nadreaktywności pęcherza. Są to dolegliwości, które według badań epidemiologicznych dotyczą około 13% dorosłej populacji – zarówno kobiet, jak i mężczyzn – i nasilają się wraz z wiekiem.
- Badanie fizykalne: Palpacyjnie (w badaniu per rectum) zwykle powiększony, elastyczny, dobrze odgraniczony, symetryczny, niebolesny gruczoł krokowy.
- Diagnostyka: Ultrasonograficzna ocena wielkości gruczołu krokowego i pomiar objętości zalegającego moczu po mikcji. Ewentualnie pomiary urodynamiczne. Badanie ogólne moczu i badania czynności nerek, ewentualnie oznaczenie PSA, tomografia komputerowa lub cystoskopia.
- Leczenie: Należy leczyć objawy, które wpływają na jakość życia, i zapobiegać powikłaniom. Podejście wyczekujące z monitorowaniem podaży płynów i mikcji (dzienniczek mikcji) u pacjentów bez wskazań chirurgicznych i z mniej uciążliwymi dolegliwościami. W pozostałych przypadkach stosuje się monoterapię lub terapię skojarzoną lekami, a w razie konieczności leczenie chirurgiczne, najczęściej z dostępu przezcewkowego.
Informacje ogólne
Definicja
- Łagodny rozrost gruczołu krokowego
- Oznacza zmianę histologiczną, która jest przyczyną powiększenia gruczołu krokowego.
- W rozroście (hiperplazji) powiększenie narządu wynika z proliferacji komórek, w przeciwieństwie do hipertrofii, która wynika z powiększenia komórek.
- Może prowadzić do niedrożności dróg moczowych.
- Oznacza zmianę histologiczną, która jest przyczyną powiększenia gruczołu krokowego.
- Łagodna niedrożność gruczołu krokowego
- Jest to stan kliniczny charakteryzujący się utrudnionym przepływem moczu przez cewkę moczową na odcinku, który przebiega przez gruczoł krokowy.
- Prawidłowe wymiary gruczołu krokowego wynoszą do 4 cm × 3 cm × 2 cm, a objętość 25 ml.
- Łagodnemu rozrostowi prostaty mogą, ale nie muszą, towarzyszyć objawy dyzuryczne, określane wspólnym mianem „objawy dolnych dróg moczowych” czyli LUTS (Lower Urinary Tract Symptoms).
Epidemiologia
- Histologicznie łagodny rozrost gruczołu krokowego (BPH) występuje u:
- 10% mężczyzn w wieku 40 lat
- 50% mężczyzn w wieku 50 lat
- 70–80% mężczyzn powyżej 60. roku życia.
- BPH z umiarkowanymi lub ciężkimi objawami (ocena w skali IPSS >7) dotyczy:
- około 20% mężczyzn między 50. a 60. rokiem życia
- około 40% mężczyzn w wieku powyżej 70 lat.
- Około 25% mężczyzn z objawowym BPH wymaga leczenia w celu poprawy odpływu moczu.
Etiologia i patogeneza
- Hiperplazja prostaty jest prawdopodobnie spowodowana związanymi z wiekiem zmianami w produkcji hormonów i zmianami stosunku androgenów do estrogenów w organizmie.
- Powstawanie testosteronu i jego metabolitu, dihydrotestosteronu, jest niezbędnym warunkiem rozwoju BPH.1
- Mężczyźni, którzy nie produkują testosteronu, nie chorują na BPH.
- Poziom testosteronu w surowicy nie koreluje z zapadalnością na BPH ani przebiegiem BPH.
- Możliwe, że dihydrotestosteron, który powstaje w gruczole krokowym z testosteronu, odgrywa główną rolę w rozwoju BPH.
- Patomechanizm na poziomie endokrynologicznym nie został jeszcze w pełni wyjaśniony.
- Powstawanie testosteronu i jego metabolitu, dihydrotestosteronu, jest niezbędnym warunkiem rozwoju BPH.1
- Objawy wynikają z zaburzeń we współdziałaniu pęcherza moczowego, szyi pęcherza, gruczołu krokowego i cewki moczowej w wyniku łagodnego powiększenia gruczołu krokowego.
- Nie ma silnej korelacji między objawami a wielkością gruczołu krokowego.
- W miarę narastania niedrożności pęcherz może jeszcze przez jakiś czas kompensować zwiększony opór poprzez zwiększenie nacisku mięśnia wypieracza.
- Następnie pęcherz traci tę zdolność, dochodzi do zalegania moczu i utrudnionego odpływu, a w skrajnym przypadkach zatrzymania moczu. Niedrożność może sprzyjać zakażeniom układu moczowego.
- Utrudnienie odpływu moczu na tle BPH może przyspieszać narastanie dysfunkcji pęcherza moczowego związanej z wiekiem.
- U niektórych pacjentów nadreaktywność mięśnia wypieracza przyczynia się do zwiększenia częstotliwości mikcji.2
- Nadreaktywność mięśnia wypieracza często występuje u pacjentów z pęcherzem nadreaktywnym (overactive bladder – OAB), może towarzyszyć obturacyjnej dysfunkcji oddawania moczu.
- Fakt, że OAB występuje równie często u mężczyzn i kobiet, potwierdza teorię, że jego przyczyną są procesy starzenia dotyczące pęcherza i ewentualnie centralnego systemu nerwowego, zwłaszcza że zwężenie drogi odpływu moczu z pęcherza moczowego jest niezwykle rzadkie u kobiet.
Czynniki predysponujące
- Podeszły wiek.
- Otyłość.
- Cukrzyca.3
- Spożywanie dużej ilości alkoholu.
- Brak aktywności fizycznej.
- Produkcja androgenów (patrz wyżej).
ICD–10
- N40 Rozrost gruczołu krokowego.
- N40.1 Rozrost gruczolakowłóknisty (gruczołu krokowego).
- N40.3 Powiększenie (łagodne) (gruczołu krokowego).
- N40.6 Przerost (łagodny) (gruczołu krokowego).
Diagnostyka
Kryteria diagnostyczne
- Typowe objawy:
- słaby strumień moczu
- częste oddawanie moczu
- nokturia
- naglące parcie na mocz
- nietrzymanie moczu
- rozpryskiwanie moczu
- strumień przerywany
- utrudnione rozpoczęcie mikcji
- wykapywanie moczu pod koniec mikcji
- uczucie niekompletnego opróżnienia pęcherza.
- Częste objawy w badaniu przedmiotowym
- palpacyjnie w badaniu per rectum powiększony gruczoł krokowy.
- Przydatne informacje dodatkowe
- mocz zalegający
- urodynamika.
Okresy w rozwoju BPH
Cztery okresy w przebiegu choroby:
- I okres – bezobjawowy: powiększenie stercza; przepływ cewkowy prawidłowy; bez objawów klinicznych
- II okres – podrażnienia: opór powodowany przeszkodą podpęcherzową, kompensowany przez mięsień wypieracz pęcherza moczowego; przepływ cewkowy miernie upośledzony; w USG bez zalegania moczu; objawy - dominuje częstomocz oraz parcie naglące
- III okres – kompensacji: narasta przeszkoda podpęcherzowa, mięśniówka pęcherza po okresie przerostu zanika; niedoczynność mięśnia; zaleganie moczu w pęcherzu, utrudniony odpływ moczu
- IV okres – dekompensacji: zanik mięśniówki i rozwijająca się atonia pęcherza, znaczne zaleganie moczu; rozwijają się powikłania i objawy nimi spowodowane (np. kamica, przewlekła choroba nerek).7
Diagnostyka różnicowa
Przeszkody w odpływie moczu
- Rak prostaty.
- Przewlekłe zapalenie gruczołu krokowego.
- Niedrożność szyi pęcherza moczowego.
- Zwężenie cewki moczowej.
Choroby pęcherza moczowego
- Zakażenie układu moczowego.
- Niestabilność mięśnia wypieracza.
- Zmniejszona kurczliwość pęcherza moczowego.
- Rak pęcherza moczowego.
- Kamica nerek.
- Uchyłki.
- W przypadku nadreaktywności pęcherza moczowego:
- zaburzenia neurologiczne
- zaburzenia endokrynologiczne (np. cukrzyca)
- czynniki psychiczne
- niewydolność serca z nykturią
- leki (np. diuretyki).
Wywiad
- Rodzaj, umiejscowienie, nasilenie, początek i czas trwania dolegliwości.
- Wpływ na jakość życia.
- Oznaki zwężenia drogi odpływu moczu:
- trudności z rozpoczęciem mikcji (opóźniony początek mikcji)
- słaby strumień moczu
- przedłużone mikcje
- uczucie niepełnego opróżnienia pęcherza
- przerywany strumień moczu (przerywane mikcje)
- parcie na mocz
- popuszczanie ostatnich kropli
- pieczenie lub ból przy oddawaniu moczu
- ostre zatrzymanie moczu w wywiadzie.
- Objawy ze strony pęcherza moczowego
- silne, naglące parcie na mocz, konieczność natychmiastowego oddania moczu,
- częste oddawanie moczu
- oddawanie małej ilości moczu
- nocne mikcje (nokturia)
- ból skojarzony z wypełnianiem się pęcherza moczowego
- nietrzymanie moczu.
- Ewentualnie ostre zatrzymanie moczu.
- Źródłem cennych informacji może być dzienniczek mikcji.
- Kwestionariusz IPSS (International Prostate Symptom Score) również dostarcza informacji anamnestycznych o charakterze diagnostycznym.
- Inne ważne informacje:
- gorączka
- dyzuria
- krwiomocz
- bóle sugerujące kamień w drogach moczowych
- wcześniejsza inwazyjna diagnostyka lub terapia układu moczowego
- somatyczne i psychiczne choroby poprzedzające lub współistniejące
- rak prostaty lub rak pęcherza moczowego w rodzinie.
Jak należy interpretować wyniki IPSS?
- Wynik poniżej 8: łagodne objawy.
- Wynik 8–19: umiarkowane objawy.
- Wynik powyżej 19: nasilone objawy.
- Sama wartość IPSS nie jest wystarczająca do określenia niezbędnych działań terapeutycznych. Decydujące znaczenie ma m.in. to, czy istnieją wskazania do zabiegu chirurgicznego i jak bardzo dolegliwości obniżają jakość życia pacjenta.
Badanie fizykalne
- Badanie per rectum
- Powiększenie gruczołu krokowego: jeśli przy palpacji odbytnicy nie można wyczuć górnej granicy gruczołu krokowego, objętość gruczołu zwykle przekracza 50 ml.
- Ograniczenia badania: różne wyniki w zależności od diagnosty, niska czułość i niska wartość predykcyjna w rozpoznaniu raka prostaty.6
- Czułość wyników badania palpacyjnego w przypadku raka prostaty wynosi tylko 30–50%, ale swoistość jest wyższa.
- Typowy wynik badania prostaty w łagodnym powiększeniu gruczołu krokowego:
- symetrycznie powiększony
- zwarta, elastyczna konsystencja
- równa powierzchnia
- wyraźne odgraniczenie narządu
- brak bolesności
- możliwość przesunięcia błony śluzowej odbytnicy.
- Zatrzymanie moczu
- wykrywalne przez opukiwanie, ewentualnie również przez palpację
- duża ilość zalegającego moczu może dawać mylne wrażenie powiększonej prostaty.
- badanie ultrasonograficzne (zastój w pęcherzu moczowym i nerkach?).
Badania uzupełniające w gabinecie lekarza rodzinnego
- Badanie ogólne moczu
- Nie należy przypisywać wszystkich patologicznych wyników badań moczu wyłącznie BPH, ale należy je dalej wyjaśniać.
- Kreatynina w surowicy.
- Pomiar zalegającego moczu (ultrasonografia) w następujących przypadkach:2
- nasilone objawy
- podejrzenie przewlekłego zatrzymania moczu
- bardzo słaby strumień.
- Pomiar czasu mikcji
- jeśli podejrzewa się zmniejszony przepływ moczu: powtórzenie testu kilka razy w domu.
- Dzienniczek mikcji.
Swoisty antygen gruczołu krokowego (PSA)
- PSA (Prostate Specific Antigen) jest bardzo czułym, ale mało swoistym biomarkerem raka prostaty. Podwyższona wartość PSA może wskazywać również na BPH. Rak prostaty może być przyczyną zatrzymania moczu.
- Dodatkowy 1 g tkanki prostaty zwiększa stężenie PSA o maksymalnie 0,15 ng/ml, natomiast tkanka raka prostaty uwalnia około 10 do 30 razy więcej PSA. Ze względu na znaczne różnice w ilości tkanki w BPH (wiele gramów) i raku prostaty (kilka gramów) wartości progowe (wartości prawidłowe) nie różnicują raka prostaty i BPH.
- PSA jest dobrym predyktorem do monitorowania terapii BPH finasterydem.
- Badanie na obecność PSA może być wskazany w indywidualnych przypadkach u mężczyzn, których objawy sugerują chorobę gruczołu krokowego (i których przewidywana dalsza długość życia wynosi co najmniej 10 lat).Pacjenta należy jednak dokładnie poinformować o niepewności diagnostycznej wyników badania.
- PSA i biopsja gruczołu krokowego są wskazane, jeśli wyniki palpacji wzbudzają podejrzenie raka prostaty.
- Mężczyznom, których bracia i/lub ojcowie chorowali na nowotwór prostaty, należy uświadomić, że są narażeni na ponad 2–krotnie zwiększone ryzyko zachorowania na raka prostaty w ciągu całego życia.
- W praktyce lekarzy rodzinnych zaleca się następujące postępowanie przy oznaczaniu wartości PSA:
- Mężczyźni, którzy z własnej woli proszą o wykonanie badania w kierunku wczesnego wykrywania – z oznaczeniem wartości PSA lub bez – powinni zostać poinformowani o zaletach i wadach tego postępowania.
- Mężczyzn w ramach badania w kierunku wczesnego wykrywania nie należy aktywnie namawiać do oznaczania wartości PSA.
- Przedstawić korzyści i zagrożenia (nadwykrywalność i niepotrzebne leczenie)
- wyjaśnić znaczenie dodatnich i ujemnych wyników badań
- dowody na korzyści wynikające z badania per rectum nie są wystarczające, aby móc zalecać to badanie wszystkim pacjentom.
- Wartości prawidłowe są zależne od wieku.
- Prawdopodobieństwo raka prostaty jest różne w zależności od wyniku badania:
- 9–17% przy PSA: <4 ng/ml
- 20–45% przy PSA: 4–10 ng/ml
- 30–75% przy PSA >10 ng/ml.
- Umiarkowanie podwyższona wartość PSA może być fałszywie dodatnia, zwłaszcza w skojarzeniu z zakażeniem układu moczowego. W tym przypadku test na obecność PSA należy powtórzyć po wyleczeniu zakażenia.
- Więcej informacji na temat korzyści wynikających z badań przesiewowych PSA można znaleźć w artykułach podwyższona wartość PSA oraz rak prostaty.
Diagnostyka u urologa
- Nie jest zwykle konieczna w pierwotnym wyjaśnianiu niepowikłanego BPH.
- W zależności od dominujących objawów i wyników ewentualnie:
- urografia TK
- badanie ultrasonograficzne
- w razie potrzeby transrektalne, do pomiaru objętości gruczołu krokowego oraz do prowadzenia igły podczas biopsji gruczołu krokowego
- cystoskopia
- urodynamika (pomiar ciśnienia i przepływu)
- zwężenie drogi odpływu moczu w dolnym odcinku układu moczowego wykrywa się poprzez jednoczesny pomiar ciśnienia w pęcherzu, ciśnienia w jamie brzusznej i przepływu moczu
- RM (uzupełniająco).
Wskazania do skierowania do specjalisty
- Skierowanie do specjalisty w następujących przypadkach:
- nasilone objawy
- niejasne lub nietypowe objawy lub wyniki badań
- podejrzenie raka prostaty
- częste zakażenia układu moczowego
- hematuria
- podejrzenie zwężenia cewki moczowej
- podejrzenie zaburzeń neurologicznych (np. neurogenny pęcherz moczowy w stwardnieniu rozsianym lub polineuropatii)
- objawy uboczne zastosowanego leczenia.
- Skierowanie w przypadku podejrzenia nowotworu prostaty:
- wyczuwalne zmiany w gruczole krokowym w badaniu per rectum (asymetryczny, twardy, guzki)
- PSA >4 ng/ml lub wzrost PSA >0,75 ng/ml przez rok u pacjentów z przewidywaną dalszą długością życia powyżej 10 lat
- rzeczywiste podwyższenie wartości PSA podczas leczenia inhibitorem 5–alfa–reduktazy (inhibitory 5–alfa–reduktazy obniżają poziom PSA).
- Natychmiastowe skierowanie w przypadku następujących objawów:
- znaczna ilość zalegającego moczu: >300 ml lub całkowite zatrzymanie moczu z koniecznością założenia cewnika
- wodonercze
- upośledzona czynność nerek (podwyższona kreatynina w surowicy).
Lista kontrolna przy skierowaniu do specjalisty
Łagodny zespół gruczołu krokowego
- Cel skierowania
- Diagnostyka i ewentualnie leczenie zaburzeń mikcji.
- Diagnostyka i ewentualnie biopsja z powodu podwyższonej wartości PSA.
- Hematuria (cystoskopia?).
- Wywiad lekarski
- Początek i czas trwania?
- Dolegliwości związane z mikcją?
- Trudności w oddawaniu moczu?
- Silne nagłe parcie na mocz?
- Nocne dolegliwości?
- Wyciek moczu?
- Krwiomocz?
- Krew w spermie?
- Zatrzymanie moczu?
- Próba terapii?
- Inne istotne choroby?
- Leki?
- Badanie fizykalne
- Stan ogólny pacjenta.
- BMI.
- Badanie per rectum: powiększona prostata, stwardnienie?
- Badanie uzupełniające
- Badanie ogólne moczu.
- PSA.
- Hb, parametry stanu zapalnego (morfologia, CRP, OB), badania czynnościowe wątroby (gamma–GT, ALP, AST, ALT, bilirubina, ChE, INR, PTT), kreatynina.
- TK dróg moczowych, alternatywnie badanie ultrasonograficzne.
Leczenie
Cele leczenia
- Łagodzenie dolegliwości, które wpływają negatywnie na jakość życia.
- Zapobieganie powikłaniom.
- Możliwe strategie to:
- informacja i poradnictwo, z dalszym postępowaniem lub bez
- leczenie farmakologiczne
- leczenie inwazyjne.
Leczenie łagodnego rozrostu gruczołu krokowego
Informacje ogólne
- W przypadku następujących objawów/wyników badań laboratoryjnych nie należy rozważać leczenia wyłącznie zachowawczego (bezwzględne wskazania do zabiegu chirurgicznego):
- nawracające zatrzymanie moczu
- nawracające zakażenia układu moczowego
- nawracający krwiomocz makroskopowy, którego nie można opanować zachowawczo
- złogi w pęcherzu moczowym
- poszerzenie górnego odcinka układu moczowego, upośledzona czynność nerek lub niewydolność nerek z powodu zwężenia drogi odpływu moczu z pęcherza moczowego (bladder outlet obstruction – BOO).
- Przy braku bezwzględnych wskazań do operacji leczenie należy ukierunkować na subiektywne dolegliwości pacjenta.
- Podejście oparte na uważnej obserwacji (watchful waiting)
- Należy rozważyć u pacjentów, którzy odczuwają nieznaczny dyskomfort i/lub mogą początkowo wdrożyć zmiany stylu życia w celu złagodzenia objawów.
- Należy je stosować w sposób dopasowany do ryzyka
- Nieodpowiednie w przypadku zwiększonego ryzyka progresji.
- Nie ma wpływu na naturalny przebieg BOO.
- Rozpoczęcie leczenia w momencie, gdy pacjent cierpi
- Ewentualnie operacja przy klinicznie istotnym BOO.
- Leczenie zachowawcze:
- brak istotnego klinicznie BOO
- przeciwwskazania do zabiegu operacyjnego
- brak zgody pacjenta na operację.
- Jeśli wskazane jest leczenie zachowawcze, odpowiednie są następujące opcje farmakoterapii (substancje czynne i zalecane dawki – patrz kolejne sekcje):
- Łagodne powiększenie gruczołu krokowego (objętość gruczołu krokowego powyżej 30–40 ml)
- monoterapia inhibitorami 5–alfa reduktazy (terapia długoterminowa, minimum 1 rok) lub
- alfa1–bloker + inhibitor 5–alfa reduktazy
- gdy nacisk kładzie się na leczenie objawowe, a nie na ograniczenie progresji BPS: monoterapia alfa1–blokerem lub inhibitorem PDE–5 (Inhibitory fosfodiesterazy).
- Gruczoł krokowy niepowiększony (objętość prostaty poniżej 30–40 ml)
- alfa1–bloker i/lub lek antymuskarynowy (monoterapia lub terapia skojarzona) lub
- inhibitor PDE–5.
- Łagodne powiększenie gruczołu krokowego (objętość gruczołu krokowego powyżej 30–40 ml)
- Jeśli leczenie zachowawcze jest nieskuteczne, można rozważyć zabieg chirurgiczny.
- Patrz algorytm leczenie łagodnego zespołu gruczołu krokowego.
Zalecenia dla pacjentów
- Regulacja spożycia płynów (łączna ilość około 1500 ml na dobę).
- Spożycie płynów równomierne rozłożone w ciągu dnia, unikanie nadmiernego spożycia płynów wieczorem i przed niektórymi czynnościami.
- Silnie ograniczone spożycie płynów może jednak prowadzić do nasilenia dyskomfortu w pęcherzu moczowym wynikającego z podrażnienia („objawy magazynowania”).
- Ograniczenie lub unikanie moczopędnego i drażniącego działania kawy, alkoholu i ostrych przypraw spożywanych w nadmiernych ilościach.
- Sprawdzenie lub unikanie stosowania leków moczopędnych wieczorem, ewentualnie zmiana leków.
- Usuwanie („wymasowywanie”) zalegającego moczu z cewki moczowej po mikcji w celu zapobieżenia kropelkowemu wyciekaniu moczu po mikcji.
- Można spróbować ponownie oddać mocz, aby w przewlekłym zaleganiu zmniejszyć objętość zalegającego moczu, ograniczyć skłonność do zakażeń lub zniwelować wykrytą niestabilność mięśnia wypieracza.
- Pacjent powinien zawsze przeznaczać odpowiednią ilość czasu na wizyty w toalecie.
- Kiedy pacjent poczuje, że pęcherz opróżnił się całkowicie, powinien odczekać jeszcze kilka minut i ponownie spróbować oddać mocz.
- Jeśli w wyniku kolejnej mikcji ponownie wypłynie mocz, należy jeszcze raz powtórzyć cały proces.
- Trening pęcherza.
Farmakoterapia
Fitoterapia
- Obecnie nie można sformułować żadnych jednoznacznych, ogólnych zaleceń dotyczących stosowania fitoterapeutyków w BPH.
- Fitoterapeutyki, których wyższość nad placebo wykazano w badaniach, można rozważać u pacjentów z łagodnymi do umiarkowanych objawami i dyskomfortem, jeżeli pacjent nie chce przejmować preparatów chemicznych.
- Dotychczas w żadnym badaniu nie stwierdzono wpływu fitoterapeutyków na progresję BPH (np. zmniejszenie częstości występowania ostrego zatrzymania moczu lub konieczności interwencji chirurgicznych/z użyciem narzędzi).
- Nieglikozydowe beta–sitosterole wpływają na poprawę LUTS i parametry urodynamiczne. Brakuje jednak danych na temat ich długoterminowej skuteczności i bezpieczeństwa, a także skuteczności w zakresie ryzyka powikłań.
- Dowody na skuteczność wyciągów z korzenia pokrzywy, pyłku kwiatowego, pestek dyni czy kory śliwy afrykańskiej na objawy BPH pochodzą w przeważającej mierze z badań o niskiej jakości i dlatego wymagają weryfikacji.
Alfa–1–blokery (antagoniści receptorów alfa–1)
- Blokują wywołany przez pobudzenie receptorów alfa-adrenergicznych skurcz mięśni gładkich gruczołu krokowego i szyi pęcherza moczowego.
- Prowadzą do szybkiego zmniejszenia objawów i zahamowania progresji objawowej.
- Wszystkie dostępne alfa–1–blokery są równie skuteczne w odpowiednich dawkach i zmniejszają wynik oceny IPSS o 1–4 punkty w porównaniu z placebo.
- Istotne obniżenie IPSS występuje już po 1 tygodniu od rozpoczęcia leczenia.
- Efekty długoterminowe zależą od objętości gruczołu krokowego w momencie rozpoczęcia terapii.
- Istnieją dowody, że alfa–1–blokery są mniej skuteczne w dłuższej perspektywie u pacjentów z łagodnym powiększeniem gruczołu krokowego (>30 ml).
- Nie mają wpływu na wielkość prostaty.
- Mają niewielki wpływ na BOO.
- Nie przeciwdziałają długotrwałemu (>1 roku) ostremu zatrzymaniu moczu ani konieczności operacji gruczołu krokowego.
- Profile działań niepożądanych poszczególnych alfa–1–blokerów są różne.
- Możliwe działania niepożądane:
- zmęczenie i osłabienie
- zawroty głowy
- ból głowy
- biegunka
- obrzęk błony śluzowej nosa
- objawy grypopodobne
- zaburzenia hipotoniczne
- omdlenia.
- Zwiększone ryzyko wystąpienia zawrotów głowy, zaburzeń hipotonicznych lub omdleń obserwowano zwłaszcza w przypadku doksazosyny i terazosyny (ryzyko względne 3,71–5,53), rzadziej w przypadku silodosyny lub tamsulozyny (uroselektywne alfa1–blokery).
- Wpływ na ciśnienie tętnicze jest wyraźniejszy u osób z nadciśnieniem niż u osób z ciśnieniem tętniczym w normie.
- Wykazano, że alfa–1–blokery pierwotnie stosowane w leczeniu nadciśnienia tętniczego (doksazosyna, terazosyna) są gorzej tolerowane niż alfa–1–blokery opracowane pierwotnie do leczenia BPS (alfuzosyna, silodosyna, tamsulozyna).
- Jednoczesne przyjmowanie leków moczopędnych, beta–blokerów, inhibitorów ACE lub antagonistów kanału wapniowego w terapii nadciśnienia tętniczego w połączeniu z alfa–1–blokerami, zwłaszcza z doksazosyną lub terazosyną, może prowadzić do zwiększenia działań niepożądanych ze strony układu sercowo–naczyniowego.
- Nie łączyć z inhibitorami PDE5 (patrz poniżej)!
- Uwaga: hipotonia ortostatyczna!
- U pacjentów z BPH leczonych alfa–1–blokerami przeciwwskazane jest jednoczesne podawanie innych alfa–1–blokerów w leczeniu nadciśnienia tętniczego.
- Informować pacjentów o działaniu obniżającym ciśnienie tętnicze!
- W szczególności w odniesieniu do silodosyny wykazano zwiększoną częstość występowania zaburzeń ejakulacji (nieprawidłowy wytrysk ze zmniejszeniem objętości ejakulatu).
- Preparaty o opóźnionym uwalnianiu substancji czynnej (preparaty retard) wykazują zasadniczo lepszą tolerancję w porównaniu z preparatami o szybkim uwalnianiu.
- Wszystkie powyższe działania niepożądane są zasadniczo odwracalne po odstawieniu alfa–1–blokera.
- Substancje czynne i zalecane dzienne dawkowanie:
- alfuzosyna o szybkim uwalnianiu 3 x 2,5 mg
- alfuzosyna o przedłużonym uwalnianiu 2 x 5 mg lub 1 x 10 mg
- doksazosyna bez przedłużonego uwalniania 1 x 2–8 mg
- doksazosyna o przedłużonym uwalnianiu 1 x 4–8 mg
- sylodosyna 1 x 4–8 mg
- tamsulozyna o przedłuzonym/zmodyfikowanym ualanianiu 1 x 0,4 mg
- terazosyna 1 x 5–10 mg.
Inhibitory 5–alfa–reduktazy
- Blokują metabolizm testosteronu do dihydrotestosteronu.
- Następuje indukcja apoptozy komórek nabłonka gruczołu krokowego, co prowadzi do zmniejszenia rozmiaru o 18–28% i zmniejszenia o połowę wartości PSA w surowicy po okresie leczenia trwającym 6–12 miesięcy.
- Są odpowiednie do zmniejszenia objawów i zahamowania progresji u pacjentów z BPH i objętością gruczołu krokowego 30–40 ml lub większą, tj. do uniknięcia ostrego zatrzymania moczu lub operacji.
- Istotne zmniejszenie objawów występuje dopiero po kilku miesiącach.
- Leczenie jest zalecane jako terapia długoterminowa (powyżej 1 roku).
- Finasteryd ma niewielki wpływ na BOO.
- Nie ma danych dotyczących wpływu innych inhibitorów 5–alfa–reduktazy na BOO.
- Możliwe działania niepożądane:
- zaburzenia ejakulacji (2,4% w porównaniu z 0,7% przy stosowaniu placebo)
- utrata libido (4,6% w porównaniu z 2,6 %)
- zaburzenia erekcji (7,1% w porównaniu z 3,8 %)
- ginekomastia (1,6% w porównaniu z 0,5 %)
- zwiększone ryzyko rozwoju cukrzycy w porównaniu z lekami blokującymi receptory alfa–1 (76 w porównaniu z 60 przypadkami na 10 000 pacjentów).8
- Reakcje niepożądane zwykle ustępują w przebiegu leczenia.
- Możliwe, że finasteryd zmniejsza ryzyko raka prostaty
- częściowo sprzeczne dane
- najwyraźniej brak wpływu na śmiertelność.
- Substancje czynne i zalecane dzienne dawkowanie:
- dutasteryd 1 x 0,5 mg
- finasteryd 1 x 5 mg.
Antagoniści receptora muskarynowego
- Statystycznie istotnie zmniejszają objawy zalegania moczu (naglące parcie na mocz, częstomocz, nietrzymanie moczu z parcia naglącego) w 12–tygodniowych badaniach.
- Mogą być stosowane w leczeniu naglącego parcia na mocz, nietrzymania moczu z parcia naglącego i zwiększonej częstotliwości mikcji (nadreaktywności pęcherza moczowego) u mężczyzn bez BOO.
- Obecnie nie można ich zalecać w przypadku innych objawów BPH oraz w leczeniu BOO.
- W badaniach suchość ust występowała istotnie częściej w przypadku antagonistów receptorów muskarynowych niż w przypadku placebo. Wszystkie inne reakcje niepożądane związane z antagonistami receptorów muskarynowych nie występowały częściej niż w przypadku placebo.
- Substancje czynne i zalecane dzienne dawkowanie:
- oksybutynina 1 x 7,5–15 mg
- solifenacyna 1–10 mg
- tolterodyna 2 x 1–2 mg
- tolterodyna o przedłużonym uwalnianiu 1 x 4 mg.
Inhibitory fosfodiesterazy (inhibitory PDE5)
- Działają poprzez rozkurcz mięśni gładkich, m. in. w gruczole krokowym.
- Poprawiają objawy u mężczyzn z umiarkowanymi i ciężkimi objawami ze strony dolnych dróg moczowych z zaburzeniami erekcji lub bez nich.
- W przypadku tadalafilu w dawce 5 mg/d istnieją dowody wskazujące, że następuje poprawa nie tylko parametrów subiektywnych (IPSS), ale także obiektywnych (Qmax).
- Nie mają wpływu na BOO (dane tylko dla tadalafilu).
- Nie łączyć z alfa–1 blokerami!
- Uwaga: hipotonia ortostatyczna!
- Więcej na temat bezpieczeństwa i tolerancji można znaleźć w artykule zaburzenia erekcji.
- Substancje czynne (niezatwierdzone do leczenia BPH i związanych z nim objawów):
Połączenie alfa–1–blokera i inhibitora 5–alfa reduktazy
- Uzupełniający się mechanizm działania obu substancji może w większym stopniu wpływać na łagodzenie objawów.9
- Stosowanie łączne leków z tych grup powinno być zalecane jako leczenie pierwszego rzutu u pacjentów z umiarkowanym lub ciężkim dyskomfortem przy mikcji.
- Ocena ryzyka progresji opiera się przede wszystkim na objętości gruczołu krokowego.
- Przewaga terapii skojarzonej nad monoterapią alfa–1–blokerami zwiększa się wraz z objętością gruczołu krokowego.
- Klinicznie istotny próg: 30–40 ml.
- Zalecane wyłącznie jako długoterminowe podejście terapeutyczne (>1 roku).
- Złagodzenie objawów może utrzymywać się do 12 miesięcy po odstawieniu alfa–1–blokera.
- Wpływ na BOO nie jest znany, ale prawdopodobnie będzie równie niewielki ze względu na ograniczony mechanizm działania poszczególnych substancji.
- Częstość występowania reakcji niepożądanych jest umiarkowana pomimo addytywnego działania poszczególnych substancji.
- Przykładowe dawkowanie:
- dutasteryd 0,5 mg + tamsulozyna 0,4 mg/d (dostępne w preparacie łączonym)
- finasteryd 5 mg + tamsulozyna 0,4 mg/d.
Połączenie blokera alfa–1 i antagonisty receptora muskarynowego10
- Korzystnie wpływa na poprawę objawów zalegania moczu w pęcherzu i przewyższa pod tym względem monoterapię alfa–1-blokerami.
- Działa niezależnie od objętości gruczołu krokowego i PSA.
- Pod wpływem leczenia resztkowa objętość moczu nieznacznie wzrasta. Jednak ryzyko (ostrego) zatrzymania moczu i konieczności cewnikowania pęcherza moczowego nie jest zwiększone.
- Niewielki wpływ na BOO.
- Suchość ust występuje częściej niż w przypadku monoterapii alfa–1–blokerem.
- Wszystkie dotychczasowe dane i wyniki badań odnoszą się do maksymalnego czasu trwania terapii wynoszącego 3 miesiące.
- Przykładowe dawkowanie:10
- tolterodyna o przedłużonym uwalnianiu 4 mg + tamsulozyna 0,4 mg/d
- oksybutynina 10 mg + tamsulozyna 0,4 mg/d
- solifenacyna 5 mg + tamsulozyna 0,4 mg/d
- tolterodyna o przedłużonym uwalnianiu 4 mg + doksazosyna 4 mg/d.
Procedury instrumentalne/operacyjne
- Standardem postępowania są następujące procedury:
- resekcja przezcewkowa (TURP)
- otwarta enukleacja gruczolaka
- elektroporacja przezcewkowa (TUEVRP)
- przezcewkowe nacięcie gruczołu krokowego (TUIP)
- resekcja prostaty laserem holmowym (HoLRP)
- enukleacja prostaty laserem holmowym (HoLEP).
- Procedury niezalecane:
- śródmiąższowa koagulacja laserowa (ILK)
- ablacja gruczołu krokowego laserem holmowym (HoLAP)
- nacięcie szyi pęcherza laserem holmowym (HoBNI)
- przezcewkowa ablacja igłowa (TUNA)
- laseroterapia hybrydowa
- zogniskowana terapia ultradźwiękowa o wysokiej intensywności przy BPS (HIFU)
- termoterapia wywołana wodą (WIT)
- ablacja laserem tulowym
- przezcewkowa ablacja etanolem gruczołu krokowego (TEAP).
Przebieg, powikłania i rokowanie
Przebieg
- BPH zwykle rozwija się powoli, ale objawy mogą znacznie obniżyć jakość życia.
- Nieleczony BPH ma zmienny przebieg; w około 50% występuje stopniowe pogorszenie objawów i szybkości przepływu moczu.
- U 30% objawy nie ulegają zmianie.
- 20% doświadcza spontanicznej poprawy objawów.
Powikłania
- Kamienie w pęcherzu moczowym.
- Uchyłek pęcherza moczowego.
- Zakażenia układu moczowego.
- Wodonercze.
- Obniżona czynność nerek.
- Ostre zatrzymanie moczu u 1–2% mężczyzn z objawami rocznie.
Rokowanie
- Łagodne powiększenie gruczołu krokowego rzadko jest stanem zagrażającym życiu, nawet jeśli występują objawy.
- Operacji poddaje się 15–25% mężczyzn po 75. roku życia.
Dalsze postępowanie
- Ocena odpowiedzi na leczenie.
- Ocena reakcji niepożądanych.
- Kwestionariusz IPSS.
- Badanie palpacyjne gruczołu krokowego.
- Badanie ogólne moczu, ewentualnie bakteriologiczne.
- Ewentualnie PSA.
- Ewentualnie ocena zalegania moczu.
- Ewentualnie urodynamika.
- Ewentualnie czynność nerek.
Wytyczne: Leczenie i dalsze postępowanie u mężczyzn z nieneurogennymi LUTS, w tym z łagodną niedrożnością w rozroście gruczołu krokowego11
- Zalecenia dotyczące dalszej obserwacji pacjentów poddanych różnym metodom leczenia zachowawczego i/lub operacyjnego opierają się na danych empirycznych i na rozważaniach teoretycznychl; brakuje badań dostarczających dowody naukowe.
- Należy prowadzić obserwację wszystkich pacjentów, którzy otrzymali leczenie zachowawcze i/lub chirurgiczne, a okreśony odstęp między poradami dostosowany jest do metody zastosowanego leczenia.
- Pacjenci, których zakwalifikowano do dalszej obserwacji, powinni być ponownie przebadani po 6 miesiącach, a następnie co roku.
- Warunek: brak pogorszenia objawów lub wystąpienia bezwzględnych wskazań do zabiegu operacyjnego.
- Pacjenci otrzymujący alfa–1-blokery lub antagonistów receptora muskarynowego powinni być ponownie poddani ocenie pod kątem odpowiedzi na leczenie po 4–6 tygodniach od rozpoczęcia terapii. Podobne postępowanie wskazane jest w przypadku zastosowania połączeń alfa–1–blokerów z inhibitorami 5–alfa reduktazy lub antagonistami receptorów muskarynowych.
- Jeśli pacjenci odczuwają złagodzenie objawów bez niepokojących reakcji niepożądanych, można kontynuować leczenie.
- Dalsze postępowanie należy przeprowadzić po 6 miesiącach, a następnie raz w roku.
- Warunek: brak pogorszenia objawów lub wystąpienia bezwzględnych wskazań do zabiegu operacyjnego.
- U pacjentów otrzymujących inhibitory 5–alfa–reduktazy
- Odpowiedź na leczenie i wszelkie reakcje niepożądane należy ocenić po 12 tygodniach i ponownie po 6 miesiącach.
- Należy wykonywać regularne badania PSA, o ile oczekiwana długość życia wynosi ponad 10 lat, diagnostyka przesiewowa jest pożądana przez pacjenta, a rozpoznanie raka prostaty zmieniłoby podejście terapeutyczne.
- Należy oznaczyć wartość PSA wyjściową i po 6 miesiącach od rozpoczęcia leczenia.
- W przypadku leczenia inhibitorem 5-alfa-reduktazy należy wyjaśnić każdy potwierdzony wzrost PSA.
- Po zabiegu instrumentalnym/operacyjnym na gruczole krokowym odpowiedź na leczenie i ewentualne reakcje niepożądane należy ocenić po 4–6 tygodniach od usunięcia cewnika.
Informacje dla pacjentów
Edukacja pacjenta
- O prawidłowych wzorcach mikcji.
- O alternatywnych metodach leczenia:
- leki: możliwości i reakcje niepożądane
- zabieg operacyjny: możliwości i powikłania.
- Mężczyźni, którzy zgłaszają problemy z oddawaniem moczu, powinni mieć wykonany pomiar PSA. Należy poinformować pacjenta o możliwych konsekwencjach, takich jak biopsje i ewentualnie leczenie radykalne w przypadku wykrycia raka prostaty.
Materiały edukacyjne dla pacjentów
Ilustracje
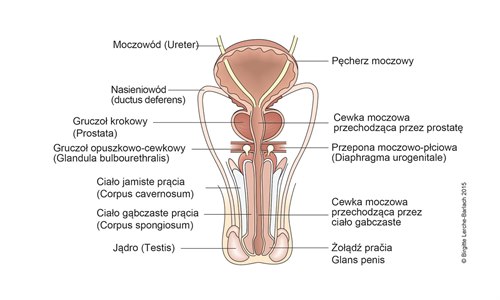
Układ moczowy i męskie narządy płciowe
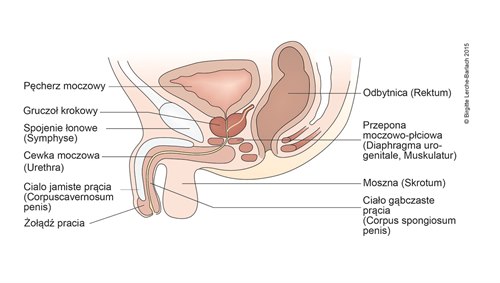
Męskie narządy płciowe w przekroju strzałkowym, wyniki prawidłowe
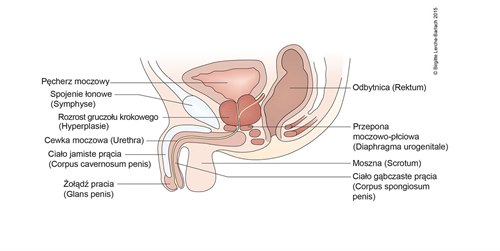
Męskie narządy płciowe, rozrost gruczołu krokowego
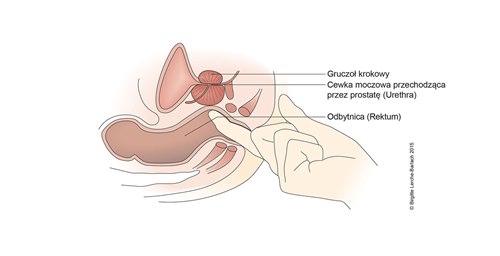
Badanie gruczołu krokowego (badanie per rectum)
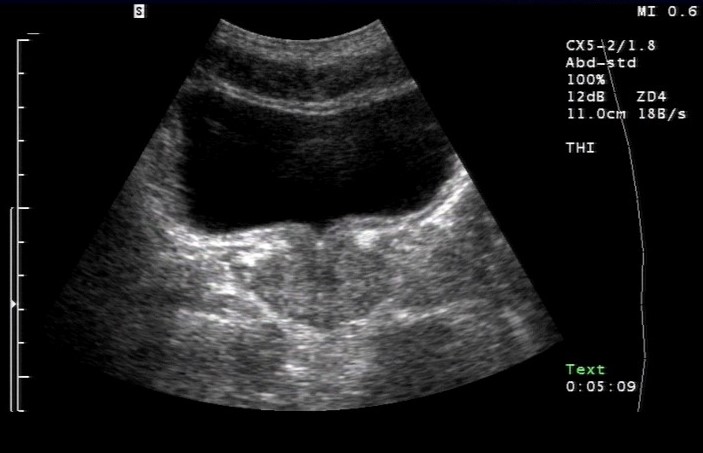
Badanie USG: gruczoł krokowy, prawidłowy (dzięki uprzejmości sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg).
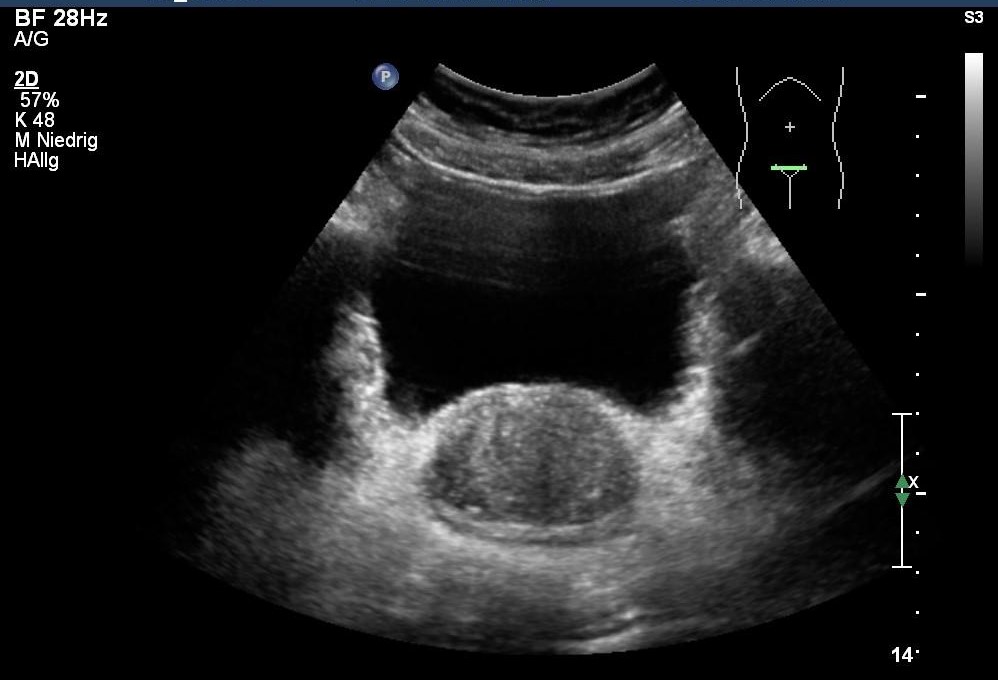
Badanie USG: Rozrost gruczołu krokowego (dzięki uprzejmości sonographiebilder.de ©Albertinen-Diakoniewerk e. V., Hamburg).
Źródła
Piśmiennictwo
- van der Sluis T.M., Vis A.N., van Moorselaar R.J. et al. Intraprostatic testosterone and dihydrotestosterone. Part I: concentrations and methods of determination in men with benign prostatic hyperplasia and prostate cancer, BJU Int 2012, 109: 176-82, PMID: 21992222, PubMed
- Sarma A.V., Wei J.T. Benign prostatic hyperplasia and lower urinary tract symptoms, N Engl J Med 2012, 367: 248-57, New England Journal of Medicine
- Sarma A.V., St Stauver J.L., Hollingsworth J.M., et al. Diabetes treatment and progression of benign prostatic hyperplasia in community-dwelling black and white men, Urology 2012, 79: 102-8, PubMed
- Gratzke C., Bachmann A., Descazeaud A. et al. EAU Guidelines on the Assessment of Non-neurogenic Male Lower Urinary Tract Symptoms including Benign Prostatic Obstruction, Eur Urol 2015, 67: 1099-109, PMID: 25613154, pubmed.ncbi.nlm.nih.gov
- Pearson R., Williams P.M. Common questions about the diagnosis and management of benign prostatic hyperplasia, Am Fam Physician., 01.12.2014, 90(11): 769-74, PMID: 25611711, PubMed
- McVary K.T., Roehrborn C.G., Avins A.L., et al. Update on AUA guideline on the management of benign prostatic hyperplasia, J Urol. 2011, 185(5): 1793-803, PMID: 21420124, PubMed
- 7.Tomasik Tomasz, Łagodny rozrost stercza. W: Repozytorium medycyny rodzinnej 2023. Windak Adam, Chlabicz Sławomir (red.), 2023, Kraków, ZiZ Centrum Edukacji : Fundacja Zdrowia Publicznego, s.181-188, ISBN 978-83-945938-1-0.
- Wei L., Lai E.C-C., Kao-Yang Y-H., et al. CCBY Open access Research Incidence of type 2 diabetes mellitus in men receiving steroid 5α-reductase inhibitors: population based cohort study, BMJ 2019, 365: l1204, doi:10.1136/bmj.l1204, www.bmj.com
- Fullhase C., Chapple C., Cornu J.N., et al. Systematic review of combination drug therapy for non-neurogenic male lower urinary tract symptoms, Eur Urol 2013, 64: 228-43, PMID: 23375241, PubMed
- Filson C.P., Hollingsworth J.M., Clemens J.Q., Wei J.T. The efficacy and safety of combined therapy with α-blockers and anticholinergics for men with benign prostatic hyperplasia: a meta-analysis, J Urol 2013, 190: 2153-60, pmid:23727412, PubMed
- Cornu JN, Gacci M, Hashim H et al. EAU Guidelines on Non-Neurogenic Male Lower Urinary Tract Symptoms (LUTS). European Association of Urology 2024. uroweb.org
- Thompson I.M. Jr, Goodman P.J., Tangen C.M., et al. Long-term survival of participants in the prostate cancer prevention trial, N EnglJ Med 2013, 360: 603-10, pmid:23944298 PubMed
- Robinson D., Garmo H., Bill-Axelson A., et al. Use of a 5α-reductase inhibitors for lower urinary tract symptoms and risk of prostate cancer in Swedish men: natiowide, population based case-control study, BMJ 2013, 346: f3406, BMJ (DOI)
Opracowanie
- Tomasz Tomasik (recenzent)
- Paweł Lewek (recenzent)
- Tomasz Tomasik (redaktor)
- Thomas M. Heim (recenzent/redaktor)
