Streszczenie
- Definicja: Choroba zakaźna wywołana poprzez pierwotniaki z rodzaju Leishmania przenoszone przez ukąszenie much piaskowych.
- Częstość występowania: Na całym świecie szacunkowo około 12 milionów chorych.
- Objawy: W leiszmaniozie trzewnej zły stan ogólny, w leiszmaniozie skórnej tylko objawy miejscowe.
- Badanie fizykalne: W leiszmaniozie trzewnej gorączka i hepatosplenomegalia. W leiszmaniozie skórnej zaczerwieniona grudka lub guzek z owrzodzeniem o uniesionych brzegach (ang. oriental bump) w miejscu ukąszenia, ewentualnie dodatkowe zmiany na błonie śluzowej jakmy ustnej, gardła i/lub nosa w śluzówkowo-skórnej postaci choroby.
- Diagnostyka: Bezpośrednie wykrywanie patogenów w badaniu histopatologicznym lub PCR z krwi.
- Leczenie: W przypadku postaci trzewnej lub śluzówkowo-skórnej zawsze stosuje się terapię ogólnoustrojową; w przypadku niepowikłanych zmian skórnych możliwa jest również terapia miejscowa.
Informacje ogólne
Definicja
- Choroba zakaźna wywoływana przez pierwotniaki z rodzaju Leishmania.
- Incydentalne przypadki w Europie.
- Klasyfikacja według lokalizacji objawów:
- Leiszmanioza trzewna (kala azar).
- Określenie kala azar pochodzi z języka hindi i oznacza „czarna skóra”.
- Możliwa hiperpigmentacja skóry w postaciach o ciężkim przebiegu.
- Leiszmanioza skórna (wrzód o uniesionych brzegach (ang. oriental bump).
- Leiszmanioza śluzówkowo-skórna (zajęcie błon śluzowych jamy ustnej, gardła i nosa).
- Leiszmanioza trzewna (kala azar).
Epidemiologia
- Częstość występowania
- Na całym świecie ok. 12 milionów chorych, liczba zgonów wynosi rocznie około 20 000–30 000.1
- Na świecie rocznie występuje ok. 50 000 do 90 000 nowych przypadków leiszmaniozy trzewnej, z których jedynie 25-45% jest zgłaszanych do WHO.1
- Jest uznawana za jedną z najbardziej „zaniedbanych chorób” biorąc pod uwagę jej występowanie w bardzo biednych regionach świata oraz nakłady finansowe na badania nad nowymi metodami diagnostyki, leczenia i zapobiegania.
- Rozkład geograficzny
- Endemiczne występowanie w ponad 60 krajach świata.
- Leiszmanioza skórna
- Leiszmanioza trzewna
- 90% wszystkich przypadków odnotowuje się w Brazylii, Etiopii, Indiach, Kenii, Somalii, Sudanie i Sudanie Południowym.3
- Leiszmanioza skórno-śluzówkowa
- Ponad 90% przypadków występuje w Boliwii, Brazylii, Etiopii i Peru.
Etiologia i patogeneza
- Zoonoza przenoszona przez ukąszenia much piaskowych (ponad 90 gatunków może przenosić pasożyty Leishmania).1
- Muchy (1–3 mm) są aktywne głównie o zmierzchu i w nocy.
- Człowiek jest jedynie przypadkowym żywicielem; do żywicieli pośrednich należą np. gryzonie i psy.
- W południowo-zachodniej części Europy zarażonych jest około 10% wszystkich psów.4
- Leiszmanioza trzewna jest również przenoszona z człowieka na człowieka (pre- lub perinatalnie z matki na dziecko lub horyzontalnie od dawców krwi i narządów).
- Istnieje ponad 20 różnych gatunków Leishmania:
- Główne dwa gatunki Leishmania wywołujące leiszmaniozę trzewną (Visceral leshimaniasis - VL) to spokrewnione Leishmania donovani i Leishmania infantum (synonim Leishmania chagasi).
- Częstymi patogenami wywołującymi leiszmaniozę skórną są L. tropica (Chiny, Indie, region śródziemnomorski) i L. mexicana (Ameryka Północna, Południowa i Środkowa).5
Patogeneza6
- Po ukąszeniu przez samicę muchy piaskowej, Leishmania w postaci wiciowej (promastigota) docierają do tkanki podskórnej.
- Wnikają one do miejscowych komórek gospodarza, np. granulocytów obojętnochłonnych lub są przez nie fagocytowane.
- W makrofagach ocalałe promastigota przekształcają się w formy bezwiciowe (amastigota), które z kolei zarażają kolejne makrofagi w otaczających tkankach lub odległych obszarach organizmu.
- U podatnych pacjentów prowadzi to do miejscowego lub ogólnoustrojowego stanu zapalnego, który w przypadku obniżonej odporności skutkuje rozwojem choroby.
- Okres wylęgania wynosi od kilku tygodni do kilku miesięcy.
- Choroba postępuje powoli, zatem związek z przebytą podróżą lub ukąszeniem przez muchę nie zawsze jest oczywisty w momencie pojawienia się objawów klinicznych.
Zakażenie utajone
- U pacjentów z upośledzeniem odporności (np. zakażonych HIV) reaktywacja może nastąpić nawet kilkadziesiąt lat po zakażeniu.
Czynniki predysponujące
- Podróżni po pobycie na obszarach endemicznych, migranci, osoby ubiegające się o azyl, uchodźcy z obszarów endemicznych.
- Osoby zakażone HIV i inni pacjenci z niedoborami odporności.
ICD-10
- B55 Leiszmanioza.
- B55.0 Leiszmanioza trzewna.
- B55.1 Leiszmanioza skórna.
- B55.2 Leiszmanioza skóry i błon śluzowych.
- B55.9 Leiszmanioza, nieokreślona.
Diagnostyka
Kiedy należy rozpocząć diagnostykę w kierunku leiszmaniozy trzewnej?
- U każdej osoby, która pochodzi z obszarów endemicznych lub przebywała na obszarze endemicznym oraz podróżowała do lub wróciła z takiego obszaru w ciągu ostatnich tygodni do miesięcy (w skrajnych przypadkach również w odstępie od 10 dni do kilku lat) oraz występują u niej:
- gorączka
- lub hepatosplenomegalia
- lub niedokrwistość, leukopenia lub trombocytopenia (lub pancytopenia)
- lub nowo powstała hiperpigmentacja skóry
- lub (rzadko) podwyższony poziom ferrytyny o niejasnej przyczynie
- lub zespół hemofagocytozy o niejasnej przyczynie
- lub hipergammaglobulinemia
- albo
- rozpoznane zakażenie HIV oraz niejasny obraz kliniczny.
Kryteria diagnostyczne
- Złotym standardem jest bezpośrednie wykrywanie pasożytów lub wykrywanie swoistego dla Leishmania kwasu nukleinowego metodą PCR z krwi obwodowej.
Diagnostyka różnicowa
Leiszmanioza trzewna
- Białaczka.
- Chłoniak.
- Choroby reumatologiczne
- zapalenie wielostawowe, reumatoidalne zapalenie stawów (RA), toczeń rumieniowaty (SLE), zapalenie skórno-mięśniowe, zapalenie naczyń.
- Gruźlica.
- Bruceloza.
- Malaria.
- Dur plamisty.
- Schistosomatoza.
- Infekcyjne zapalenie wsierdzia.
- Marskość wątroby.
Leiszmanioza skórna
- Rumień lub piodermia nadżerkowo-owrzodzeniowa (Staph. aureus).
- Pierwotna gruźlica skóry.
- Gruźlica brodawkowata skóry.
- Mykobakteriozy atypowe (owrzodzenie Buruli, ziarniniak basenowy).
- Trąd.
- Trichofitoza głęboka lub zapalna grzybica krostkowa (wywołana przez grzyby odzwierzęce i glebowe).
- Kiła.
- Nowotwory skóry.
Wywiad lekarski
Leiszmanioza trzewna
- Do zarażenia dochodzi poprzez ukąszenie muchy piaskowej.
- Okres wylęgania: zwykle od 2 tygodni do 8 miesięcy.
- Początkowo występują epizody gorączki, czasami nawet 2 razy na dobę, oraz nasilające się wyraźne pogorszenie ogólnego stanu fizycznego ze zmęczeniem oraz utratą masy ciała.
- Czasami zanim ujawnią się ogólnoustrojowe objawy choroby, w miejscu ukąszenia można zaobserwować nieowrzodzony guzek.
Leiszmanioza skórna
- Okres wylęgania: 2 tygodnie do kilku miesięcy.
- Rozwój typowej zmiany skórnej w miejscu ukąszenia (patrz sekcja Badanie przedmiotowe).
- Objawy ogólnoustrojowe występują rzadko, jednak na początku może pojawić się krótkotrwała, niewysoka gorączka.
- Po kilku miesiącach zmiany goją się samoistnie, tkanka ziarninowa tworzy się od środka do krawędzi rany, ostatecznie pokrywając całą ranę.
Leiszmanioza śluzówkowo-skórna
- Początkowo w miejscu ukąszenia pojawiają się klasyczne zmiany skórne.
- W przebiegu choroby rozprzestrzenianie się Leishmania z ognisk skórnych na błony śluzowe.
- Obecne owrzodzenia jamy ustnej i nosowej.
Badanie przedmiotowe
Leiszmanioza trzewna
- Objawy główne: gorączka, hepatosplenomegalia i pancytopenia.
- Uogólnione powiększenie węzłów chłonnych.
- W pojedynczych przypadkach hiperpigmentacja skóry, szczególnie na dłoniach, stopach, brzuchu i czole (kala-azar).
- Następstwa pancytopenii, np. wybroczyny i samoistne krwotoki.
Leiszmanioza skórna
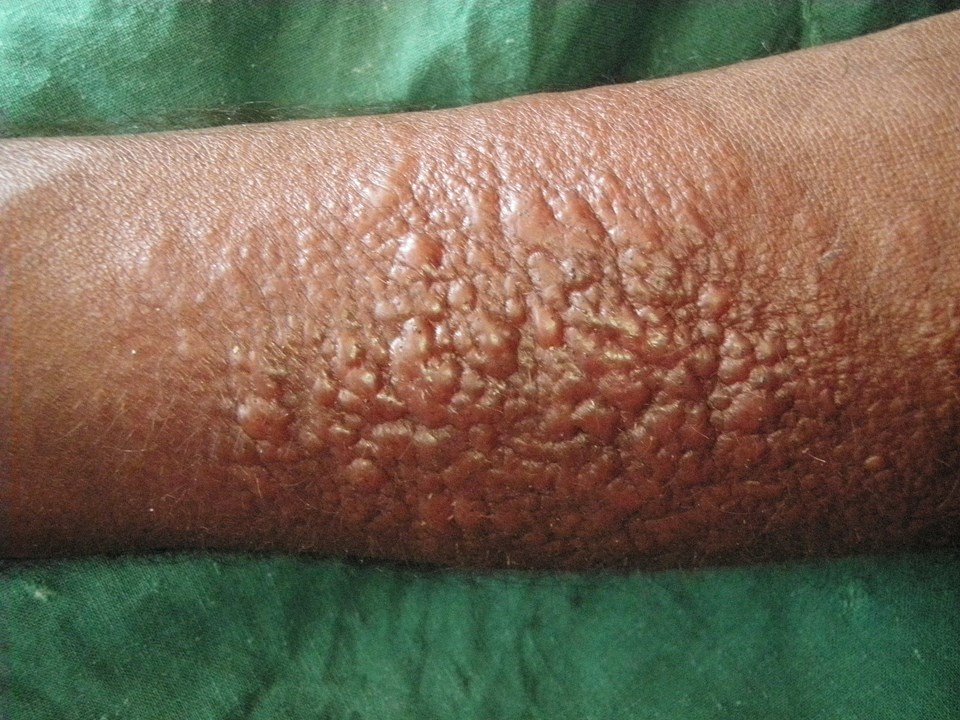
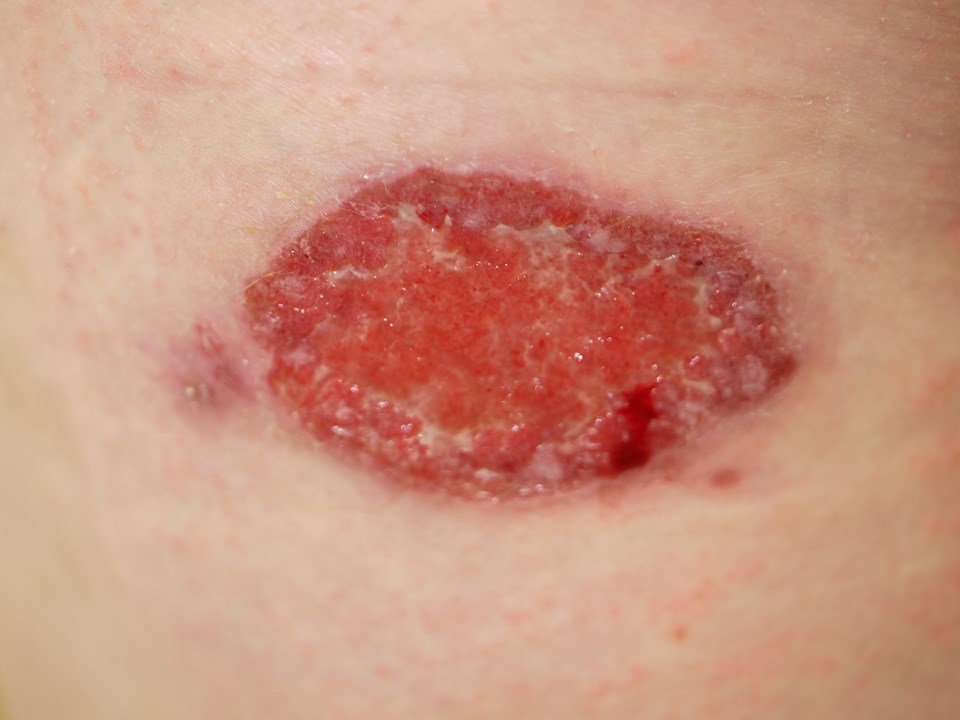
- Po zarażeniu pojawia się czerwona grudka, następnie guzek, który zwykle ulega owrzodzeniu.
- Owrzodzenie ma nieregularne, lekko uniesione, niekiedy nadmiernie zrogowaciałe brzegi i często jest pokryte strupem.
- Czasami pojawiają się kolejne owrzodzenia w bezpośrednim sąsiedztwie (autoinokulacja) lub na innych odsłoniętych częściach ciała (zakażenie wieloogniskowe).
- Zmiany zwykle występują na odkrytych okolicach skóry.
Leiszmanioza śluzówkowo-skórna
- Oprócz objawów skórnych występują zmiany w błonie śluzowej nosa i jamy ustnej.
Badania obowiązkowe
Bardzo specjalistyczne wykonywane są w nielicznych, dedykowanych ośrodkach (w Polsce Instytut Medycyny Morskiej i Tropikalnej w Gdyni).
Leiszmanioza trzewna
- Aspiracja szpiku kostnego, badanie próbki w specjalistycznym laboratorium
- barwienie rozmazów barwnikiem Giemsy, Wrighta lub Leishmana, mikroskopowe wykrywanie patogenów.
- Jeśli badanie mikroskopowe jest ujemne (lub już w pierwszym etapie):
- wykrywanie materiału genetycznego Leishmania (PCR).
- Wykrywanie patogenów (mikroskopowo, PCR) możliwe jest również z biopsji lub punkcji z węzłów chłonnych, wątroby lub śledziony.
- wykrywanie materiału genetycznego Leishmania (PCR).
- W przypadku rozpoznania leiszmaniozy trzewnej należy określić stopień zajęcia narządów i wykryć ewentualne wtórne zakażenia
- morfologia krwi z rozmazem (niedokrwistość, leukopenia, trombocytopenia)
- CRP i/lub OB (aby ukierunkować dalsze postępowanie)
- osoczowy układ krzepnięcia (obniżony czas protrombinowy)
- AST, ALT, GGTP, bilirubina, kreatynina w surowicy lub cystatyna C, elektrolity
- elektroforeza białek (albuminy obniżone, globuliny podwyższone)
- USG jamy brzusznej (hepatomegalia, możliwe drastyczne powiększenie śledziony)
- RTG klatki piersiowej (wykluczenie współwystępującej gruźlicy)
- test na HIV (za zgodą pacjenta).
Leiszmanioza skórna
- W diagnostyce wykorzystuje się jest materiał bogatokomórkowy, który należy uzyskać możliwie bezkrwawo. Badania wykonywane są w ośrodkach specjalistycznych.
- Dostępne są następujące opcje:
- Biopsja
- Pobrać biopsję sztancową (np. przy użyciu sztancy 4 mm) z brzegu zmiany.
- Zeskrobiny skórne
- Za pomocą skalpela lub ostrej łyżeczki usuwa się możliwie bezkrwawo tkankę ze środka i brzegu owrzodzenia.
- Wymaz z próbki pobranej przez nacięcie skóry (Slit Skin Smear — SSS).
- Aspirat.
- Biopsja
- Biopsje mają tę zaletę, że uzyskuje się materiał wystarczający do równoległego wykonania kilku metod diagnostycznych, w tym diagnostyki różnicowej (histologia, dalsze badania mikrobiologiczne metodą posiewu lub mikrobiologii molekularnej), a czułość jest odpowiednio wysoka.
Wskazania do skierowania do hospitalizacji
- W każdym przypadku podejrzenia leiszmaniozy — niezwłoczne skierowanie do szpitala.
Leczenie
Cele leczenia
- Przeżycie pacjenta (leiszmanioza trzewna).
- Gojenie zmian skórnych z jednoczesnym zapobieganiem wtórnym zakażeniom lub szpecącym bliznom.
Ogólne informacje o leczeniu
Powinno być prowadzona w specjalistycznych ośrodkach leczenia chorób tropikalnych.
Leiszmanioza trzewna
- Leczeniem pierwszego wyboru jest liposomalna amfoterycyna B.
- Dawka całkowita wynosi 20 mg/kg m.c., podzielona na co najmniej 5 dawek pojedynczych.
- Każdorazowo dawka dożylna 3–4 mg/kg m.c. przez 10–21 dni (np. 3–4 mg/kg m.c. na dobę w dniach 0, 1, 2, 3, 4 i 10).
- Miltefozyna jest lekiem drugiego wyboru, np. w przypadku uczulenia na liposomalną amfoterycynę B.
- Dawka dzienna 1,5–2,5 mg/kg m.c. doustnie, maksymalnie 150 mg 1 raz na dobę, czas trwania leczenia: 28 dni.
- Kapsułki należy przyjmować wraz z posiłkiem.
Leiszmanioza śluzówkowo-skórna i skórna
- Przed rozpoczęciem terapii należy dążyć do różnicowej identyfikacji gatunków ze względu na toksyczność i zależną od gatunku skuteczność stosowanych leków.
- W przypadku zmian prostych możliwe jest leczenie miejscowe lub oczekiwanie na samoistne wygojenie.
- Wskazania do terapii ogólnoustrojowej
- zmiany złożone (patrz sekcja Badanie przedmiotowe)
- postać śluzówkowo-skórna
- nawracające, rozsiane lub rozproszone zmiany skórne.
Zapobieganie
- Kontrola populacji much piaskowych na obszarach endemicznych.1
- Profilaktyka ekspozycji: podczas podróży na tereny endemiczne należy stosować indywidualną ochronę przed ukąszeniami owadów: okrywanie ciała odzieżą wierzchnią, repelenty, moskitiery o drobnych oczkach (najlepiej nasączone środkami owadobójczymi).
Monitorowanie leczenia
- W trakcie terapii liposomalną amfoterycyną B
- morfologia krwi z rozmazem, parametry czynności nerek i elektrolity 2 razy w tygodniu
- przerwanie terapii w przypadku hipokaliemii <3,2 mmol/l, wzrostu stężenia kreatyniny lub cystatyny C >50% wartości wyjściowej (badanie cystatyny C niedostępne w POZ), istotnych zmian w morfologii krwi.
- W trakcie terapii miltefozyną
- parametry czynności wątroby i nerek co tydzień
- przerwanie terapii w przypadku podwyższenia stężenia kreatyniny lub cystatyny C >50% wartości wyjściowej, podwyższenia stężenia transaminaz do poziomu przekraczającego trzykrotność górnej wartości normy
- Natychmiast przerwać stosowanie preparatu w przypadku wystąpienia objawów ze strony oczu.
Badania kontrolne
- Regularne badania kontrolne należy wykonywać co 3 miesiące przez okres 2 lat.
- Wielkość śledziony, morfologia krwi, albuminy w surowicy i OB są czułymi parametrami nawrotu choroby.
- PCR z krwi należy wykonywać co 3 miesiące w trakcie obserwacji.
- Kolejna punkcja lędźwiowa nie jest konieczna w obserwacji.
Informacje dla pacjentów
- Pacjentów należy poinformować o konieczności ponownego zgłoszenia się do lekarza w przypadku nawrotu gorączki, powiększenia węzłów chłonnych lub niewyjaśnionych innych objawów.
Przebieg, powikłania i rokowanie
Przebieg
- W farmakoterapii leiszmaniozy trzewnej u pacjentów zwykle gorączka obniża się w ciągu 1 tygodnia, a parametry kliniczne i laboratoryjne ulegają poprawie w ciągu 2 tygodni.
- Większość nawrotów obserwuje się w ciągu 6 miesięcy, ale w pojedynczych przypadkach także później.
Powikłania
- Nieleczona leiszmanioza trzewna charakteryzuje się wysoką śmiertelnością z powodu wtórnych zakażeń przebiegających z sepsą, krwotokami i wyniszczeniem.5
- Leiszmanioza skórna po kala-azar
- Utrzymywanie się patogenów w skórze pomimo leczenia.
- Plamisto-grudkowa wysypka rozpoczynająca się wokół ust i rozprzestrzeniająca się na tułów.
- Leiszmanioza skórna po kala-azar
- Leiszmanioza skórna może prowadzić do ropnych powikłań, takich jak w zapaleniu naczyń chłonnych lub róży, a także do szpecących blizn.
- Leiszmanioza śluzówkowo-skórna może prowadzić do powikłań w wyniku uszkodzenia tkanek miękkich i chrząstek nosa, warg, jamy ustnej i gardła.
- Często dochodzi do wtórnego zakażenia bakteryjnego.
- Zmiany okaleczające twarzy, np. deformacja nosa.5
Rokowanie
- Leiszmanioza skórna zwykle ustępuje samoistnie w ciągu 3–6 miesięcy, ale często pozostawia blizny.5
- Bardzo dobra odpowiedź na farmakoterapię, potem często gojenie bez blizn.5
- Po wystąpieniu objawów klinicznych nieleczona leiszmanioza trzewna prowadzi do postępującej utraty masy ciała; zwykle w ciągu 2 lat dochodzi do śmierci chorego z powodu sepsy spowodowanej zakażeniem bakteryjnym, ostrej niedokrwistości, niewydolności wątroby lub krwotoku.
- Dzięki wczesnemu rozpoznaniu i leczeniu śmiertelność obniża się do około 5%.5
Informacje dla pacjentów
Informacje dla pacjentów w Medibas
Ilustracje
Źródła
Piśmiennictwo
- World Health Organization. Fact sheet: leishmaniasis (ostatni dostęp 02.2024). www.who.int
- Alvar J, Vélez ID, Bern C, et al; WHO Leishmaniasis Control Team. Leishmaniasis worldwide and global estimates of its incidence. PLoS One. 2012;7:e35671. journals.plos.org
- Burza S, Croft SL, Boelaert M. Leishmaniasis. Lancet 2018; 392(10151): 951-70. www.ncbi.nlm.nih.gov
- Franco AO, Davies CR, Mylne A, et al. Predicting the distribution of canine leishmaniasis in western Europe based on environmental variables. Parasitology 2010; 138(14): 1878-91. www.ncbi.nlm.nih.gov
- Stark CG. Leishmaniasis. Medscape, last updated Feb 18, 2020. emedicine.medscape.com
- Belkaid Y, Mendez S, Lira R, Kadambi N, Milon G and Sacks D. A natural model of Leishmania major infection reveals a prolonged "silent" phase of parasite amplification in the skin before the onset of lesion formation and immunity. J Immunol 2000; 165: 969-77. PubMed
Autorzy
- Joanna Dąbrowska-Juszczak (redaktor)
- Anna Grzeszczuk (recenzent)
- Sławomir Chlabicz (redaktor)
- Lino Witte (recenzent/redaktor)
- Birgit Wengenmayer (recenzent/redaktor)
