Streszczenie
- Definicja: Choroba tętnic obwodowych (peripheral arterial disease — PAD) to stan, który polega na ograniczeniu przepływu krwi w tętnicach zaopatrujących kończyny. Może to być ograniczenie częściowe (w wyniku zwężenia naczynia) lub całkowite (okluzja naczynia). Najczęściej (95%) na podłożu miażdżycy.
- Epidemiologia: Częstość występowania na świecie 1,52%, a u osób powyżej 80. roku życia 15%. Stosunek pacjentów bezobjawowych do objawowych wynosi ok. 4:1.
- Objawy: Typowym objawem jest ból przy wysiłku z ograniczeniem dystansu, który może przejść chory i poprawą w spoczynku (chromanie przestankowe). W zależności od lokalizacji zmian naczyniowych objawy mogą występować w obrębie pośladka, uda, łydki lub stopy.
- Badanie fizykalne: Osłabione tętno obwodowe, szmer naczyniowy nad zwężonym naczyniem, zaburzenia troficzne skóry; dodatni test Ratschowa.
- Diagnostyka: Potwierdzenie rozpoznania poprzez obliczenie wskaźnika kostka-ramię (ankle-brachial index — ABI) <0,9. Uzupełniająco TBI, TCPO2 oraz USG dopplerowskie w diagnostyce lokalizacji zwężenia.
- Leczenie: Leczenie czynników ryzyka i hamowanie agregacji płytek krwi, nadzorowana aktywność fizyczna (supervised exercise training - SET). W przypadku bólu o dużym nasileniu lub krytycznego niedokrwienia kończyn należy wykonać przeskórną rewaskularyzację wewnątrznaczyniową lub zabieg operacyjny.
Informacje ogólne
Definicja
- Choroba tętnic obwodowych (PAD) to stan, w którym dochodzi do ograniczenia przepływu krwi w tętnicach zaopatrujących kończyny lub, rzadziej, w aorcie.
- Może to być ograniczenie częściowe (w wyniku zwężenia) lub całkowite (okluzja).
Znaczenie problemu dla lekarzy rodzinnych
- Stosunkowo wysoka częstość występowania PAD w podstawowej opiece zdrowotnej.1
- Częstość występowania i znaczenie PAD są niekiedy bagatelizowane przez lekarzy i pacjentów.2
- Niedoszacowanie częstości występowania, z powodu występowania typowych objawów tylko u co 4. pacjenta
- u chorych z owrzodzeniami na kończynach, przy braku dolegliwości bólowych wywołanych wysiłkiem z powodu ograniczenia ruchu z innych przyczyn (np. choroba zwyrodnieniowa stawów, niewydolność serca lub choroba płuc), można podejrzewać bezobjawową PAD („maskowaną”) na podstawie badania fizykalnego i diagnostyki wstępnej (ocena tętna na kończynach, ABI, TBI).3
- Pacjenci z PAD są niedostatecznie leczeni pod względem czynników ryzyka i chorób towarzyszących.
- Śmiertelność z przyczyn sercowo-naczyniowych jest zwiększona nawet u bezobjawowych pacjentów i odnoszą oni korzyści z działań prewencyjnych.
Klasyfikacja PAD
- Na podstawie prostej klasyfikacji klinicznej, można wyróżnić trzy postacie kliniczne schorzenia:
- bezobjawowa PAD
- objawowa (chromanie przestankowe)
- przewlekle niedokrwienie/zagrażająca martwica.
- W celu lepszego szczegółówego sklasyfikowania stopnia zaawansowania choroby, powszechnie wykorzystuje się klasyfikację wg Fontaine'a; w krajach anglosaskich i na świecie częściej stosuje się klasyfikację według Rutherforda.
Tabela: Choroba tętnic obwodowych - klasyfikacje na podstawie objawów klinicznych (ESC 2024)3
| Postaci kliniczne PAD | Klasyfikacja Fontaine'a | Klasyfikacja Rutheforda | ||
| Bezobjawowa | I | Brak objawów | 0 | Brak objawów |
| Objawowa (związana z wysiłkiem) | IIa | Łagodne chromanie (>200 m) | 1 | Chromanie łagodne |
| IIb | Umiarkowane chromanie (<200 m) | 2 | Chromanie umiarkowane | |
| 3 | Chromanie ciężkie | |||
| Przewlekłe niedokrwienie/zagrażająca martwica | III | Ból w spoczynku | 4 | Ból w spoczynku |
| IV | Owrzodzenie niedokrwienne lub martwica | 5 | Niewielkie uszkodzenie tkanek | |
| 6 | Duże uszkodzenie tkanek | |||
Epidemiologia
- PAD jest chorobą powszechnie występującą na świecie
- dotyczy 113 milionów osób w wieku >40. roku życia3
- Częstość występowania na świecie wynosi 1,52% i wzrasta wraz z wiekiem3:
- u osób w wieku >80 lat wynosi 14,9% 3
- Kobiety chorują częściej niż mężczyźni:
- 18% (K) vs. 10,5% (M) w tej samej grupie wiekowej3
- Proporcja pacjentów bezobjawowych do objawowych nie zależy od wieku i wynosi ok. 4:1
- U ok. 3% hospitalizowanych pacjentów stwierdza się PAD4
Etiologia i patogeneza
Etiologia
- Miażdżyca tętnic odpowiada za >95% przypadków PAD
- Rzadsze przyczyny zmian prowadzących do zwężenia/zamknięcia tętnicy:
- zapalenie naczyń
- wrodzone lub nabyte malformacje naczyniowe
- dysplazja włóknisto-mięśniowa
- zatorowość obwodowa
- zwyrodnienie torbielowate przydanki
- zespoły ucisku (compression syndrome)
- guz naczyniowy
- kępki żółte rzekome (pseudoxanthoma elasticum)
- uraz lub uszkodzenie popromienne
Patogeneza
- Początkowo powstawanie zmian miażdżycowych przy nadal wystarczającej perfuzji w spoczynku i podczas wysiłku
- Wraz z narastaniem zwężenia dochodzi do rozwoju niedokrwienia obciążeniowego - klinicznie objawiającego się jako chromanie przestankowe
- Chromanie przestankowe charakteryzuje się somatycznym bólem głębokim, jego patogenezę wyjaśniają następujące hipotezy:
- zaburzenia odżywienia komórek (niedobór tlenu i substancji odżywczych)
- zaburzenia wydalania (niedostateczne wypłukiwanie produktów przemiany materii)
- przyczyna bólu związana jest z mechaniką mięśni (przedłużona faza relaksacji)
- wzrost ciśnienia w loży powięziowej
- Zjawisko „rozchodzenia”: ok. 1–2 minuty po rozpoczęciu obciążenia poprawia się wypłukiwanie mediatorów bólu poprzez wykorzystanie naczyń włosowatych, w których nie ma perfuzji w spoczynku
- Progresja PAD nadmiernie obciąża mechanizmy kompensacyjne i prowadzi do przewlekłego krytycznego niedokrwienia kończyn z bólem w spoczynku, a w końcu do martwicy
Czynniki ryzyka
- Najważniejsze klasyczne czynniki predysponujące do rozwoju PAD, z których każdy jest istotnie i niezależnie związany ze zwiększonym ryzykiem wystąpienia choroby:
- modyfikowalne3
- palenie tytoniu
- odpowiada za połowę objawowych przypadków PAD
- ryzyko wzrasta wraz z intensywnością stosowania nikotyny3
- ryzyko względne 5,6 (palenie ≥35 lat) wystąpienia PAD wymagającego hospitalizacji
- cukrzyca
- drugi najważniejszy czynnik ryzyka
- ryzyko względne zwiększone 2–4-krotnie
- wzrost HbA1c o 1% zwiększa ryzyko PAD o ok. 28%
- nie udało się wykazać odpowiedniego zmniejszenia ryzyka w przypadku zmniejszenia HbA1c spowodowanego stosowaniem leków
- zmniejszona sprawność chodu i mobilność oraz 5-krotnie zwiększone ryzyko amputacji u pacjentów z PAD i cukrzycą w porównaniu do pacjentów bez cukrzycy3
- hiperlipidemia
- wysokie stężenie cholesterolu całkowitego i cholesterolu LDL są niezależnymi czynnikami ryzyka PAD
- inne czynniki ryzyka to:
- zmniejszone stężenie cholesterolu HDL
- wysoki poziom trójglicerydów
- lipoproteina A
- nadciśnienie tętnicze:
- ryzyko względne zwiększone 2-krotnie
- wzrost ciśnienia skurczowego o 20 mmHg wiąże się z 63% wzrostem ryzyka.3
- palenie tytoniu
- niemodyfikowalne3
- wiek
- płeć
- czynniki genetyczne i rodzinne
- modyfikowalne3
- Czynniki ryzyka zależne od płci3
- nadciśnienie/cukrzyca ciężarnych
- menopauza
- Inne czynniki ryzyka3
- socjalno-ekonomiczne
- środowiskowe (zanieczyszczenie powietrza)
- nadwaga/otyłość
- choroby autoimmunologiczne
- utrzymujący się przewlekly stan zapalny
- niewłaściwa dieta
- nadużywanie alkoholu
- stres
- zaburzenia snu
- brak aktywności fizycznej/siedzący tryb życia
ICD-10
- I70 Miażdżyca
- I70.2 Miażdżyca tętnic kończyn
- I70.9 Uogólniona i nieokreślona miażdżyca
- I73 Inne choroby naczyń obwodowych
- I73.9 Choroba naczyń obwodowych, nieokreślona
- Chromanie przestankowe
- Skurcz tętnicy
- I73.9 Choroba naczyń obwodowych, nieokreślona
- I74.3 Zatok i zakrzep tetnic kończyn dolnych
- I77 Inne zaburzenia czynności tętnic i tętniczek
- I77.1 Zwężenie tętnicy
- I77.3 Dysplazja włóknisto-mięśniowa tętnic
- I77.6 Zapalenie tętnicy, nieokreślone
Diagnostyka
Kryteria diagnostyczne
- Rozpoznanie wstępne na podstawie wywiadu i badania przedmiotowego.5
- kompleksowa ocena kliniczna układu naczyniowego z uwzględnieniem krążenia tętniczego3
- obecność czynników ryzyka sercowo-naczyniowego
- Potwierdzenie poprzez obliczenie wskaźnika kostka-ramię (ankle-brachial index — ABI).
- wartość ABI <0,9 potwierdza rozpoznanie PAD
- Przy podejrzeniu stwardnienia tętnic (ABI >1,4 – szczególnie u osób ≥65 r.ż., chorych z cukrzycą i/lub ciężką niewydolnością nerek) zaleca się dodatkowo pomiar ciśnienia w dużym palcu stopy z określeniem wskaźnika paluch-ramię (toe-brachial index – TBI) i/lub badanie USG Doppler Duplex3
- wartość TBI <0,7 potwierdza rozpoznanie PAD
- Przewlekłe niedokrwienie z zagrażającą martwicą3
- typowe objawy PAD oraz
- ciśnienie na wysokości kostki <50 mmHg, ciśnienie na dużym palcu stopy <30 mmHg lub TCPO2 <30 mmHg
Diagnostyka różnicowa
- Przyczyny pozanaczyniowe:
- chromanie przestankowe rdzeniowe (claudicatio spinalis) w zmianach zwyrodnieniowych, takich jak np. stenoza kanału kręgowego
- koksartroza albo gonartroza
- neuropatia cukrzycowa lub inna neuropatia obwodowa
- meralgia parestetyczna (neuropatia uciskowa nerwu skórnego bocznego uda)
- neuropatia uciskowa nerwu strzałkowego
- zapalenie ścięgna, zapalenie kaletki maziowej
- choroby hematologiczne (nadpłytkowość, krioglobulinemia, obecność zimnych aglutynin)
Wywiad
Objawy
- Ból związany z chromaniem przestankowym:
- typowa charakterystyka
- ból mięśni
- zależny od wysiłku
- w spoczynku poprawa po kilku minutach
- upośledzenie zdolności chodu z ograniczeniem bezbolesnego i maksymalnego dystansu
- lokalizacja (w zależności od zmiany naczyniowej)
- okolice pośladków
- udo
- łydka
- stopa
- typowa charakterystyka
- Ból w spoczynku:
- lokalizacja (często rozpoczyna się w przodostopiu)
- niekiedy poprawa po opuszczeniu kończyny w dół
- Zmiany skórne/owrzodzenia:
- gojące się źle albo wcale
- Obniżona jakość życia
- ocena aspektów fizycznych, psychicznych i społecznych za pomocą kwestionariuszy, np. HRQoL, PROMs i SF-36
Czynniki ryzyka
- Palenie papierosów
- Cukrzyca
- Hiperlipidemia
- Nadciśnienie tętnicze
- Otyłość/brak aktywności fizycznej
- Inne czynniki ryzyka - patrz wyżej
Choroby współistniejące
- Choroba niedokrwienna serca
- Niewydolność serca
- Przewlekła choroba nerek/niewydolność nerek
- Zaburzenia erekcji
Wywiad rodzinny
- W kierunku PAD i/lub innych chorób sercowo-naczyniowych
Badanie fizykalne
- Badanie przedmiotowe jest częścią podstawowej diagnostyki, ale bez obliczenia ABI często nie daje możliwości ustalenia ostatecznego rozpoznania
- Samo badanie palpacyjne tętna jest niewystarczające do rozpoznania PAD (czułość 20%)
Oglądanie (ocena obustronna)
- Skóra:
- kolor
- zmiany skórne
- owrzodzenia (często w okolicy kostki bocznej)
- owłosienie (wypadanie włosów)
- potliwość
- zaburzenia troficzne paznokci
- Mięśnie:
- zanik
Palpacja (ocena obustronna)
- Tętno:
- tętnica udowa, tętnica podkolanowa, tętnica piszczelowa tylna, tętnica grzbietowa stopy
- Temperatura skóry kończyny dolnej
Osłuchiwanie
- Aorta brzuszna
- Tętnica udowa
Test Ratschowa
- Wykonanie i interpretacja:
- pacjent leży na plecach z uniesionymi do góry pod kątem 90 stopni kończynami dolnymi, wykonuje ruchy zginania i prostowania stóp przez ok. 2 minuty, a następnie przyjmuje pozycję siedzącą z opuszczonymi kończynami dolnymi
- podejrzenie zaburzeń perfuzji w przypadku:
- opóźnionym > 20 sek. powrocie krwi na siedząco
- Mało dowodów, ale doświadczenie kliniczne wskazuje na przydatność badania
- Zobacz tabela: Różnicowanie PAD i neuropatii (badanie przedmiotowe)
Badania uzupełniające
Obliczenie wskaźnika kostka-ramię (ABI)
- W gabinecie lekarza rodzinnego można przeprowadzić podstawową diagnostykę z ukierunkowanym wywiadem lekarskim, badaniem przedmiotowym i obliczeniem ABI3
- jest niedrogim, łatwym i powszechnie stosowanym narzędziem do diagnostyki i monitorowania przebiegu PAD
- badanie zalecane szczególnie u osób bezobjawowych w wieku ≥45 lat, z czynnikami ryzyka (patrz wyżej), zwłaszcza u kobiet
- czułość 68-84%
- swoistość 84-99%
- Technika badania:
- pozostanie 5-10 min w pozycji spoczynkowej (bez większego wysiłku fizycznego wcześniej) i w temperaturze pokojowej przed badaniem
- pomiary wartości skurczowego ciśnienia tętniczego na obu ramionach
- wykorzystuje się średnią wartość z pomiarów na obu ramionach (jeśli różnica ≥10 mmHg, uwzględnia się wyższe ciśnienie)
- założenie i napompowanie mankietu do pomiaru ciśnienia tętniczego (o szerokości 10–12 cm) tuż nad kostką
- pomiar wartości skurczowego ciśnienia krwi na tętnicy piszczelowej tylnej i tętnicy piszczelowej przedniej za pomocą sondy dopplerowskiej (8–10 MHz)
- obliczenie ABI dla każdej kończyny dolnej: najniższe ciśnienie na wysokości kostki podzielone przez średnie ciśnienie w tętnicy ramieniowej
- jeśli ABI jest prawidłowy, ale występują kliniczne objawy PAD, czułość można zwiększyć poprzez pomiar 1 min. po kilkakrotnym stawaniu na palcach (spadek ciśnienia na wysokości kostki o >30 mmHg lub zmniejszenie ABI o 20% jest wtedy uznawane za dowód PAD)
- Zobacz tabela: Kategorie ABI do oceny ciężkości PAD
Test chodu/ergometria na bieżni
- Obiektywizacja chromania
- Ilościowa ocena dystansu chodu do momentu pojawienia się dolegliwości (dystansu chromainia)
Badania laboratoryjne
- Krew:
- glukoza/HbA1c
- lipidogram (cholesterol całkowity, LDL-C, HDL-C)
- eGFR/kreatynina
- Mocz:
- badanie ogólne moczu pod kątem obecności białkomoczu/albuminurii
Diagnostyka specjalistyczna
Przezskórny pomiar ciśnienia parcjalnego tlenu (transcutaneus oxygen pressure - TcPO2)
- Pozwala ocenić żywotność tkanek i ocenić ryzyko amputacji w przypadku krytycznego niedokrwienia3
- TcPO2 >30 mmHg: korzystny wskaźnik gojenia ran
- TcPO2 <10 mmHg: złe rokowanie w zakresie gojenia ran i ryzyko martwicy u pacjentów z krytycznym niedokrwieniem leczonych komórkami macierzystymi
- Dokonując pomiaru należy uwzględnić czynniki zakłócające, takie jak grubość skóry, temperaturę sondy, obecność stanu zapalnego i/lub obrzęku kończyny.3
USG – doppler kolorowy
- Metoda z wyboru w diagnostyce naczyniowej PAD3
- czułość 88%
- swoistość 95%
- przydatna również do monitorowania pacjentów z PAD po zabiegu rewaskularyzacji
- Ocena anatomii i hemodynamiki, ilościowe określenie stopnia zwężenia3
- w połączeniu z oceną ABI i TBI, pozwala na określenie istotnych hemodynamicznie zmian w tętnicach
- przydatne do odróżniania zmian miażdżycowych (również subklinicznych) od niemiażdżycowych
- pacjenci z PAD, zarówno objawowi, jak i bezobjawowi, powinni zostać jednocześnie poddani badaniom przesiewowym w kierunku tętniaka aorty brzusznej
- Jeśli wyniki badań są niejednoznaczne, można zastosować dodatkowe metody obrazowania (MRA, CTA, DSA).
Angiografia metodą tomografii komputerowej (computed tomography angiography – CTA)
- Czułość 95%, swoistość 96%.
- Zalety: wysoka rozdzielczość obrazu, krótki czas badania
- Wady: nefrotoksyczne środki kontrastowe, narażenie na promieniowanie
Angiografia rezonansu magnetycznego (magnetic resonance angiography – MRA)
- W diagnostyce klinicznie istotnych zwężeń czułość i swoistość 95%
- Zalety: brak narażenia na promieniowanie, brak nefrotoksycznych środków kontrastowych
- Wady: zawyżanie stopnia zwężenia w przypadku zwapnień, przeciwwskazania do RM (metalowe implanty, w niektórych przypadkach stymulatory serca)
Cyfrowa angiografia subtrakcyjna (digital subtraction angiography – DSA)
- Złoty standard w obrazowaniu naczyń krwionośnych
- Metoda wykorzystywana w diagnostyce przed leczeniem chirurgicznym lub gdy jednoczasowo jest przeprowadzany zabieg wewnątrznaczyniowy
Pletyzmografia segmentarna
- Zalety: niezależna od stwardnienia tętnic, przydatna do lokallizacji poziomu zwężenia
Badania przesiewowe
- Międzynarodowe zalecenia dotyczące badań przesiewowych w kierunku PAD różnią się między sobą, również z powodu niepewności danych
- Zaleca się, aby nieinwazyjnym badaniem przesiewowym i diagnostycznym pierwszego wyboru w była ocena ABI
- przesiewową ocenę lub w kierunku PAD należy rozważyć u osób w wieku ≥65 lat obciążonych czynnikami ryzyka, a można ją rozważyć w tej grupie wiekowej również u osób nieobciążonych czynnikami ryzyka sercowo-naczyniowego3
- w ramach badań przesiewowych w kierunku PAD u osób z cukrzycą lub przewlekłą chorobą nerek i prawidłowym ABI w spoczynku należy rozważyć pomiar TBI3
Wskazania do skierowania do specjalisty/szpitala
- Objawowa PAD w celu diagnostyki lokalizacji i ewentualnie – po rozważeniu indywidualnych czynników i odpowiedniej anatomii naczyń – zaplanowania leczenia chirurgicznego/interwencyjnego
- Krytyczne niedokrwienie kończyn do szybkiej oceny i leczenia za pomocą przezskórnej interwencji wewnątrznaczyniowej/operacji
Lista kontrolna dotycząca skierowania
PAD, chromanie przestankowe
- Cel skierowania
- Diagnostyka? Leczenie? Inne?
- Wywiad lekarski
- Objawy:
- chromanie przestankowe (dystans marszu?), ból w spoczynku
- Czynniki ryzyka:
- Choroby współistniejące:
- choroba wieńcowa, niewydolność serca, przewlekła choroba nerek/niewydolność nerek.
- Leki
- Objawy:
- Badanie fizykalne
- Stan skóry, rany/owrzodzenia
- Tętno: palpacja i osłuchiwanie
- Test Ratschowa, wyznaczenie wskaźnika kostka-ramię
- Badania uzupełniające
- Badania laboratoryjne: glukoza (w przypadku powtarzających się podwyższonych wartości), HbA1c, lipidogram (cholesterol całkowity, LDL-C, HDL-C), eGFR/kreatynina
- Badanie USG doppler duplex naczyń kończyn dolnych (w ramach Opieki Koordynowanej)
Leczenie
- Leczenie pacjenta z PAD powinno odbywać się w ramach interdyscyplinarnej współpracy wielospecjalistycznej (m.in. angiolog, chirurg naczyniowy, kardiolog, nefrolog, diabetolog, radiolog)3
Cele leczenia
- Zahamowanie progresji PAD
- Zmniejszenie ryzyka wystąpienia obwodowych zdarzeń naczyniowych
- Zmniejszenie liczby zdarzeń sercowo-naczyniowych i mózgowo-naczyniowych
- Poprawa jakości życia (zmniejszenie bólu, poprawa sprawności poruszania się/chodu)
- Zapobieganie konieczności leczenia inwazyjnego (rewaskularyzacja/zabieg chirurgiczny)
Ogólne informacje o leczeniu
- Główne punkty leczenia w zależności od stadium klinicznego:
- stadium I według Fontaine'a:
- zmniejszenie ryzyka zdarzeń sercowo-naczyniowych
- stadium II według Fontaine'a:
- poprawa w zakresie bezbolesnego i maksymalnego dystansu marszu
- zachowanie mobilności i tym samym poprawa jakości życia
- stadium III i IV według Fontaine'a: zapobieganie amputacjom kończyny
- stadium I według Fontaine'a:
- Elementami leczenia są:
- zmiana stylu życia i leczenie czynników ryzyka
- nadzorowana aktywność fizyczna (supervised exercise training - SET)3
- farmakoterapia
- rewaskularyzacja wewnątrznaczyniowa/chirurgiczna
- leczenie ran
- Podstawowe leczenie polega na kontroli czynników ryzyka, aktywności fizycznej i leczeniu przeciwzakrzepowym
- Rewaskularyzacja jest leczeniem objawowym, bez wpływu na postępującą miażdżycę; decyzja o leczeniu powinna być zatem dokonana po uwzględnieniu bilansu korzyści i ryzyka, nasilenia bólu i preferencji pacjenta dotyczących leczenia
Zmiana stylu życia i leczenie czynników ryzyka
- Dodatkowe informacje na temat działań profilaktycznych – zobacz także: Profilaktyka pierwotna chorób układu krążenia
- Wdrożenie programów edukacyjnych dla pacjentów
- Wsparcie psychologiczne
Dieta/aktywność fizyczna
- Dieta powinna być zróżnicowana i uwzględniająca zalecenia dotyczące diety śródziemnomorskiej3
- bogata w rośliny strączkowe, błonnik, orzechy, owoce i warzywa
- unikanie niedożywienia i zaburzeń metabolicznych
- W przypadku nadwagi lub otyłości podstawą leczenia jest redukcja masy ciała
- dążenie do wartości BMI 20-25 kg/m2
- obwód talii: <80 cm (kobiety), <94 cm (mężczyźni)
- W przypadku PAD zalecana jest nadzorowana aktywność fizyczna (supervised exercise training - SET) - patrz niżej.
- dostosowana indywidualnie do możliwości pacjenta
Palenie papierosów
- Palenie tytoniu jest najważniejszym czynnikiem ryzyka a abstynencja nikotynowa ma udokumentowany (korzystny) wpływ na progresję PAD
- Więcej informacji na temat leczenia uzależnienia od nikotyny w artykule: Zaprzestanie palenia
Cukrzyca
- Zaleca się indywidualizację docelowych wartości HbA1c, w zależności od obecności chorób współistniejących, czasu trwania cukrzycy oraz oczekiwanej długości życia zgodnie z obowiązującymi wytycznymi
- Szczegóły dotyczące aktualnych wytycznych na temat leczenia znajdują się w artykułach: Cukrzyca typu 2 oraz Cukrzyca typu 1
Hiperlipidemia
- Korzystny efekt przyjmowania statyn w odniesieniu do prewencji zdarzeń sercowo-naczyniowych i wydłużenie dystansu chodu u wszystkich pacjentów z PAD3,6
- Zaleca się zmniejszenie stężenia LDL u pacjentów z PAD3:
- >50% wartości wyjściowej i <1,4 mmol/l (<55 mg/dl)
- dawka powinna być ustalona indywidualnie w zależności od ryzyka sercowo-naczyniowego i osiągania celów terapeutycznych
- Jeśli docelowe wartości LDL nie zostały osiągnięte pomimo stosowania maksymalnych tolerowanych dawek statyn, należy dołączyć ezetynib3
- w razie dalszego braku skuteczności, należy zastosować inhibitor PCSK93
- u pacjentów z wysokim ryzykiem sercowo-naczyniowym, którzy nie tolerują leczenia statynami i nie uzyskali optymalnej wartości LDL podczas leczenia ezetynibem, należy zastosować kwas bempediowy w monoterapii lub w połączeniu z inhibitorem PCSK93
- Zobacz również artykuł: Hiperlipidemia
Nadciśnienie tętnicze
- Leczenie ciśnienia tętniczego zmniejsza ryzyko zdarzeń sercowo-naczyniowych i liczbę amputacji
- docelowa wartość ciśnienia tętniczego: ≤120-129/70-79 mmHg3
- w razie złej tolerancji i braku możliwości osiągnięcia ciśnienia skurczowego (SBP) ≤120-129 mmHg, należy dążyć do uzyskania wartości SBP tak niskiej, jak to rozsądnie możliwe3
- w przypadku utrzymujących się ciśnienia rozkurczowego (DBP) ≤80 mmHg pomimo stosowanego leczenia, można rozważyć intensyfikację terapii hipotensyjnej w celu osiągnięcia wartości DBP 70-79 mmHg.3
- docelowa wartość ciśnienia tętniczego: ≤120-129/70-79 mmHg3
- W leczeniu początkowym zaleca się stosowanie inhibitorów ACE/sartanów i antagonistów kanału wapniowego 7
- przy braku przeciwskazań, u pacjentów z PAD zaleca się rozważenie stosowania ACE inhibitorów/sartanów, niezależnie od wartości ciśnienia tętniczego3
- Beta-blokery nie pogarszają objawów chromania i ich prszyjmowanie może być kontynuowane, jeśli są wskazane (niewydolność serca, choroba wieńcowa, migotanie przedsionków)7
- Zobacz również artykuł: Nadciśnienie tętnicze.
Nadzorowana aktywność fizyczna (supervised exercise training - SET)
- Oprócz leczenia czynników ryzyka, istotnym elementem leczenia zachowawczego jest nadzorowany trening.3
- łagodzi objawy
- wydłuża dystans chodu
- poprawia jakość życia
- zmniejsza ryzyko sercowo-naczyniowe
- poprawia sprawność
- U pacjentów po zabiegu rewaskularyzacji wewnątrznaczyniowej, SET jest zalecany jako terapia uzupełniająca.3
- Ćwiczenia powinny być prowadzone w warunkach opieki stacjonarnej (szpital), a jeśli nie jest to możliwe - w domu (home-based exercise training - HBET).3
- optymalnie prowadzenie przez profesjonalistę specjalizującego się w rehabilitacji naczyniowej
- w przypadku treningu odbywającego się w domu, należy zapewnić możliwość jego monitorowania - rozmowy z pacjentem (np. telefoniczne), prowadzenie dziennika, aplikacje
- Głównym postępowaniem powinien być trening chodu3
- należy rozważyć trening chodu o wysokiej intensywności (77-95% maksymalnego tętna lub 14-17 pkt w skali Borga)
- pozwala na znaczne zwiększenie bezbolesnego i maksymalnego dystansu chodu.8
- gdy nie jest to możliwe, można rozważyć alternatywne ćwiczenia, np. trening siłowy, jazda na rowerze, krążenia ramion.
- należy rozważyć trening chodu o wysokiej intensywności (77-95% maksymalnego tętna lub 14-17 pkt w skali Borga)
- Częstotliwość i czas treningów3,8-9:
- co najmniej 3 razy w tygodniu
- czas trwania sesji treningowej: min. 30 minut
- całkowity czas trwania: min. 12 tygodni.
- w zależności od tolerancji pacjenta, można rozważyć stopniowe (co 1-2 tygodnie) zwiększanie intensywności treningów
Leczenie przeciwzakrzepowe
- U objawowych pacjentów należy prowadzić leczenie przeciwpłytkowe w celu zmniejszenia ryzyka zdarzeń sercowo-naczyniowych3,10:
- kwas acetylosalicylowy 75-160 mg 1x dobę lub klopidogrel 75 mg 1x na dobę
- pacjenci z wysokim ryzykiem zdarzeń niedokrwiennych i niskim ryzykiem krwawienia oraz pacjenci po zabiegu rewaskularyzacji naczynia:
- riwaroksaban 2,5 mg 2x na dobę + kwas acetylosalicylowy 100 mg 1x na dobę
- w przypadku pacjentów po rewaskularyzacji, podwójnej terapii przeciwpłytkowej nie należy prowadzić dłużej niż 1 miesiąc
- pacjenci bezobjawowi z cukrzycą
- kwas acetylosalicylowy 75-100 mg
- ASA posiada w Polsce wskazanie rejestracyjne w profilaktyce innych chorób przebiegających z zakrzepami w naczyniach i jest generalnie lekiem z wyboru, klopidogrel powinien być podawany w przypadku nietolerancji/przeciwwskazań do stosowania ASA lub u pacjentów wysokiego ryzyka
- Bezobjawowi pacjenci z PAD bez innych objawów miażdżycy tętnic nie powinni otrzymywać leku przeciwpłytkowego
- Pacjentom stosującym doustne leczenie przeciwkrzepliwe z innych wskazań, nie należy podawać dodatkowego leku przeciwpłytkowego ze względu na PAD
Substancje wazoaktywne
- Celem stosowania substancji wazoaktywnych jest zwiększenie dystansu chromania; dostępne są przede wszystkim dwie substancje11-12:
- cilostazol (inhibitor fosfodiesterazy typu 3)
- należy stosować wybiórczo w fazie chromania tylko wtedy, gdy jakość życia pacjenta jest znacznie obniżona, dystans chodu jest mniejszy niż 200 m, a trening marszowy nie może być prowadzony lub jest ograniczony
- pentoksyfilina była szeroko stosowana, ale dowody na jej skuteczność są mniej wiarygodne
- cilostazol (inhibitor fosfodiesterazy typu 3)
- Działania niepożądane i przeciwwskazania ograniczają możliwości zastosowania; substancje wazoaktywne nie są więc traktowane jako leczenie pierwszego wyboru
Leczenie inwazyjne - rewaskularyzacja
- Rewaskularyzację można przeprowadzić z wykorzystaniem przezskórnego zabiegu wewnątrznaczyniowego lub zabiegu chirurgicznego, w wybranych przypadkach również poprzez interwencje hybrydowe13
- Interwencje wewnątrznaczyniowe i zabiegi chirurgiczne są leczeniem objawowymi, bez wpływu na progresję choroby podstawowej
- profilaktyczne zabiegi nie powinny być wykonywane w bezobjawowej PAD.
- Pacjenci powinni być włączeni w proces podejmowania decyzji, który powinien brać pod uwagę ból, ryzyko i korzyści, koszty oraz osobiste preferencje
- Przy określaniu wskazań należy wziąć pod uwagę następujące kwestie:
- stadium PAD według Fontaine'a lub Rutherforda
- lokalizację, warunki anatomiczne i złożoność zmian naczyniowych
- choroby towarzyszące
- indywidualne życzenia terapeutyczne pacjenta dotyczące terapii
Przezskórne zabiegi wewnątrznaczyniowe
- W ostatnich latach nowe techniki i materiały poszerzyły spektrum zabiegów wewnątrznaczyniowych o możliwość stosowania ich w zmianach złożonych
- Zasadniczo w ramach przezskórnej angioplastyki wewnątrznaczyniowej (percutaneous transluminal angioplasty – PTA) dostępne są następujące techniki:
- poszerzenie zwężenia balonem
- umieszczenie niepowlekanych stentów metalowych
- poszerzenie za pomocą balonów pokrytych lekiem (paklitaksel)
- umieszczenie stentów uwalniających lek (paklitaksel, sirolimus)
- aterektomia.
Leczenie chirurgiczne
- Obecnie operacje wykonuje się głównie w przypadku zmian długoodcinkowych, złożonych
- Do pomostowania stosuje się głównie protezy z tworzyw sztucznych lub przeszczepy z żyły odpiszczelowej.
Krytyczne niedokrwienie kończyn3
- Przyczyny krytycznego niedokrwienia to najczęściej:
- postępująca PAD
- zator aorty
- zakrzepica w tętniaku
- zespół usidlenia tętnicy podkolanowej
- powikłania jatrogenne po zabiegach naczyniowych
- Stan nagły wymagający natychmiastowego postępowania - kluczowe znaczenie dla skuteczności leczenia
- pacjent powinien zostać poddany leczeniu w specjalistycznym ośrodku w ciągu 4-6 godzin.
- wydłużenie czasu oczekiwania istotnie zwiększa ryzyko martwicy.
- W przypadku rozpoznania krytycznego niedokrwienia w celu zapobiegania dalszej embolizacji, należy3:
- rozpocząć leczenie przeciwbólowe
- zastosować leczenie przeciwzakrzepowe:
- heparyna niefrakcjonowana: bolus 5000 UI dożylnie lub 70-100 UI/kg m.c., a następnie wlew ciągły z dostosowaniem dawki w zależności od parametrów krzepnięcia (czasu krzepnięcia i APTT) lub
- heparyna drobnocząsteczkowa (np. enoksaparynę) w dawce 1 mg/kg m.c. na dobę
- w przypadku całkowitego niedokrwienia należy niezwłocznie przeprowadzić leczenie wewnątrznaczyniowe lub chirurgiczne - patrz artykuł: Ostre niedokrwienie kończyn
Przebieg, powikłania i rokowanie
Powikłania
- Zaburzenia gojenia się ran
- Zakażenie, martwica
- Krytyczne niedokrwienie kończyn
- Amputacja
- Zawał mięśnia sercowego
- Udar
Przebieg i rokowanie
- Rozwój obrazu klinicznego w przypadku obecności chromania:
- poprawa u ok. 1/4 pacjentów
- niewielka zmiana u ok. 1/3 –1/2 pacjentów
- pogorszenie u ok. 1/4 pacjentów.
- Im bardziej nasilone jest chromanie, tym szybsza progresja
- Ryzyko krytycznego niedokrwienia kończyn przy chromaniu jest niewielkie, 10-letnie ryzyko amputacji wynosi 2%
- u pacjentów z towarzyszącą cukrzycą - 5-krotnie zwiększone ryzyko amputacji
- u pacjentów z krytycznym niedokrwieniem kończyn odsetek amputacji wynosi 25% w ciągu jednego roku
- Istnieje bezpośrednia korelacja pomiędzy zmniejszeniem ABI a wzrostem zachorowalności i śmiertelności z przyczyn sercowo-naczyniowych
- ABI <0,9 wiąże się z podwojeniem 10-letnich wskaźników zdarzeń wieńcowych, śmiertelności sercowo-naczyniowej i śmiertelności z wszystkich przyczyn.
- nawet bezobjawowa PAD niesie ze sobą znacznie zwiększone ryzyko zdarzeń sercowo-naczyniowych i zgonu
- 10-letnia śmiertelność:
- przy bezobjawowej PAD: 23%
- przy chromaniu: 30%
- przy krytycznym niedokrwieniu kończyn: 40%
Dalsze postępowanie
- Kontrole prowadzone są przez lekarza rodzinnego i angiologa lub chirurga naczyniowego
- Ustrukturyzowany program opieki pooperacyjnej obejmuje następujące elementy:
- doradztwo i zarządzanie czynnikami ryzyka
- kontrolne badania przedmiotowe
- informacje o dalszych możliwościach leczenia
- kontrola po inwazyjnych procedurach leczniczych (chirurgicznych i wewnątrznaczyniowych).
- Pacjentów należy kierować na regularne treningi marszowe
Informacje dla pacjentów
Materiały edukacyjne dla pacjentów
- Choroba tętnic obwodowych
- Zalecenia dietetyczne w przypadku podwyższonego poziomu lipidów we krwi
- Pełnowartościowa dieta
- Żywność niskotłuszczowa
- Błonnik w żywności
- Odżywianie i ruch — dla zdrowego serca
- Nadwaga i redukcja masy ciała
- Prawidłowa pielęgnacja stóp
- Dlaczego warto rzucić palenie i jak to zrobić?
- Alkohol a choroby układu krążenia
Ilustracje
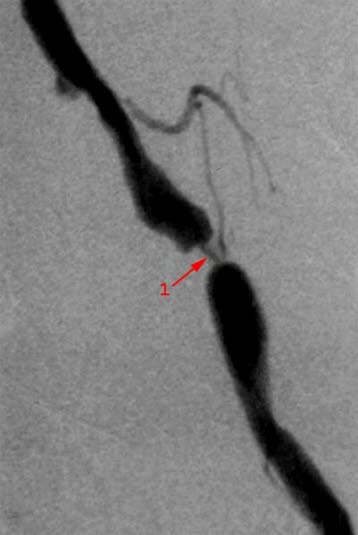
Zwężenie w tętnicy biodrowej, zdjęcie rentgenowskie w trakcie angiografii
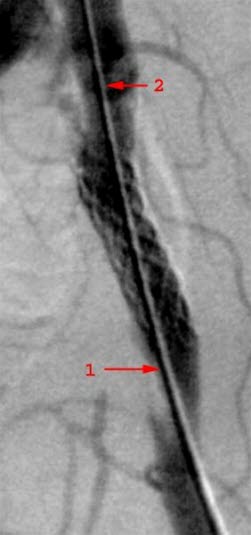
Zwężenie w tętnicy biodrowej leczone stentem, zdjęcie rentgenowskie w trakcie angiografii
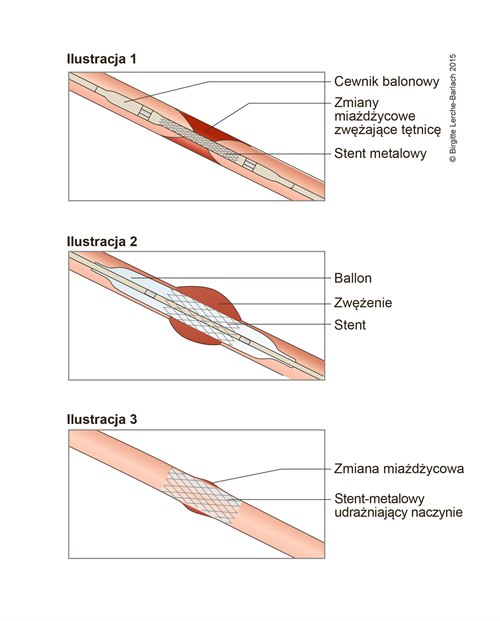
Stentowanie zwężonego naczynia krwionośnego
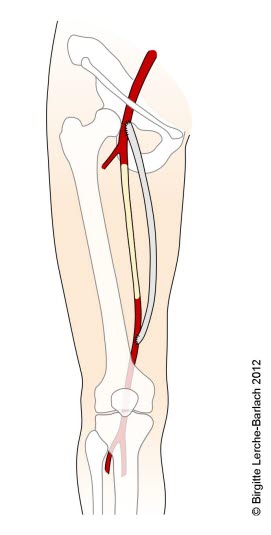
Pomostowanie okluzji obwodowej
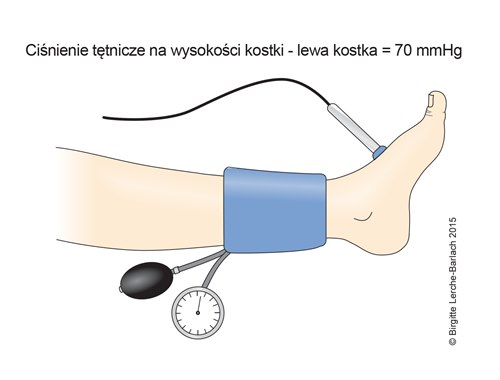
Pomiar ciśnienia tętniczego na kostce
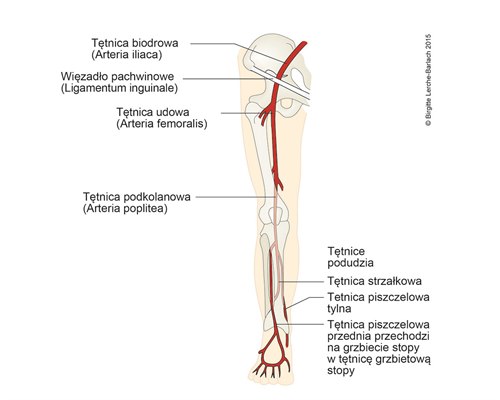
Tętnice kończyn dolnych
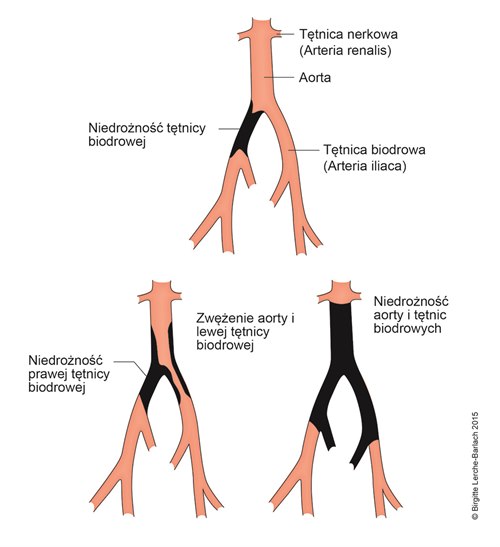
Zaburzenie przepływu w tętnicach biodrowych
Źródła
Wytyczne
- 2024 ESC Guidelines for the management of peripheral arterial and aortic diseases. Developed by the task force on the management of peripheral arterial and aortic diseases of the European Society of Cardiology (ESC) Endorsed by the European Association for Cardio-Thoracic Surgery (EACTS), the European Reference Network on Rare MultisystemicVascular Diseases (VASCERN), and the European Society of Vascular Medicine (ESVM). Eur Heart J 2024; 45: 3538–3700. escardio.org
Piśmiennictwo
- Hirsch AT, Criqui MH, Treat-Jacobsen D, et al. Peripheral arterial disease detection, awareness, and treatment in primary care. JAMA. 2001; 286: 1317-24. www.ncbi.nlm.nih.gov
- Belch JJ, Topol EJ, Agnelli G, et al, Prevention of Atherothrombotic Disease Network. Critical issues in peripheral arterial disease detection and management: a call to action. Arch Intern Med. 2003; 163: 884-92. PubMed
- Mazzolai L., Teixido-Tura G., Lanzi S. et al. 2024 ESC Guidelines for the management of peripheral arterial and aortic diseases. Developed by the task force on the management of peripheral arterial and aortic diseases of the European Society of Cardiology (ESC) Endorsed by the European Association for Cardio-Thoracic Surgery (EACTS), the European Reference Network on Rare MultisystemicVascular Diseases (VASCERN), and the European Society of Vascular Medicine (ESVM). Eur Heart J 2024;45:3538–3700. academic.oup.com
- Malyar N, Furstenberg T, Wellmann J, et al. Recent trends in morbidity and inhospital outcomes of in-patients with peripheral arterial disease: a nationwide population-based analysis. Eur Heart J. 2013; 34: 2706-14. eurheartj.oxfordjournals.org
- Firnhaber J, Powell C. Lower Extremity Peripheral Artery Disease: Diagnosis and Treatment. Am Fam Physician. 2019; 99: 362-9. www.aafp.org
- Paraskevas KI, Wierzbicki AS, Mikhailidis DP. Statins and noncardiac vascular disease. Curr Opin Cardiol. 2012; 27(4): 392–7. www.ncbi.nlm.nih.gov
- McEvoy JW., McCarthy CP., Bruno RM., et al. 2024 ESC Guidelines for the management of elevated blood pressure and hypertension Eur Heart J. 2024; 45(38): 3912-4018. www.escardio.org
- Lane R, Ellis B, Watson L, Leng GC. Exercise for intermittent claudication. Cochrane Database of Systematic Reviews 2014, Issue 7. Art. No.: CD000990. DOI: 10.1002/14651858.CD000990.pub3. DOI
- Fokkenrood HJP, Bendermacher BLW, Lauret GJ, et al. Supervised exercise therapy versus non-supervised exercise therapy for intermittent claudication. Cochrane Database of Systematic Reviews. 2013; Issue 8. Art. No.: CD005263. DOI: 10.1002/14651858.CD005263.pub3. DOI
- Frołow M. Leśniak W. Przewlekłe niedokrwienie kończyn dolnych w: Gajewski P, Jaeschke R (red.) Interna Szczeklika 2023. Medycyna Praktyczna, Kraków 2023; 531-7.
- Stevens JW, Simpson E, Harnan S, et al. Systematic review of the efficacy of cilostazol, naftidrofuryl oxalate and pentoxifylline for the treatment of intermittent claudication. Br J Surg. 2012; 99: 1630-8. pmid:23034699 PubMed
- Bedenis R, Stewart M, Cleanthis M, et al. Cilostazol for intermittent claudication. Cochrane Database Syst Rev 2014; 10: CD003748. DOI:10.1002/14651858.CD003748.pub4. DOI
- Malgor RD, Alalahdab F, Elraiyah TA, et al. A systematic review of treatment of intermittent claudication in the lower extremities. Vasc Surg. 2015; 61: 54S-73S. DOI: 10.1016/j.jvs.2014.12.007 DOI
- Sieradzki J. Cukrzyca typu 2. w: Gajewski P, Jaeschke R (red.) Interna Szczeklika 2023. Medycyna Praktyczna, Kraków 2023, s. 1561-76
Opracowanie
- Natalia Jagiełła, (redaktor)
- Marek Oleszczyk (recenzent)
- Adam Windak (redaktor)
- Michael Handke (recenzent/redaktor)
- Günther Egidi (recenzent/redaktor
- Joanna Dąbrowska-Juszczak (recenzent)
