informacje ogólne
Definicja
- niezstąpione jądra, wnętrostwo
- Nieprawidłowość rozwojowa: jądra nie zstąpiły do moszny; wymagane jest leczenie.
- Samoistne zstąpienie jąder występuje stosunkowo często przed ukończeniem 1. roku życia.
- ektopia
- Występuje, gdy jądro znajduje się poza fizjologiczną ścieżką zstępowania jąder.
- Wnętrostwo (prawdziwe zatrzymanie jąder)
- ukryte jądra
- Jądra wędrujące1
- Spowodowane przez nadaktywny mięsień dźwigacz jądra i powinny być odróżniane od prawdziwego zatrzymania jąder, ponieważ często nie wymagają leczenia.
częstość występowania
- Badania wskazują na rosnącą częstość występowania.
- Chorobowość przy urodzeniu
- U 2–4% osób dotkniętych tą chorobą jądro (lub jądra) w mosznie nie jest (nie są) wyczuwalne po urodzeniu.
- Chorobowość u jednolatków
- U 0,5–1,5% zatrzymanie jąder utrzymuje się po 1. urodzinach.
- Obustronne zatrzymanie jąder
- Występuje w około 15–25% przypadków.
- Dzieci urodzone przedwcześnie
- U 20–30% wcześniaków jądra nie są wyczuwalne po urodzeniu.
Fizjologiczny rozwój jąder
- Zstępowanie jąder odbywa się w dwóch fazach2.
- Pierwsza faza jest kontrolowana przez insulinopodobny peptyd 3 (INSL3) i testosteron, który jest produkowany przez komórki Leydiga.
- Druga faza jest kontrolowana przez androgeny i peptyd związany z genem kalcytoniny (CGRP).
- W 3.–5. tygodniu ciąży rozpoczyna się w rozwój gonad.
- Prawidłowy rozwój jąder (różnicowanie) rozpoczyna się po 7 tygodniach.
- Po około 9 tygodniach komórki Leydiga rozwijają się i zaczynają produkować testosteron.
- Pod koniec 28. tygodnia jądra przesuwają się w kierunku otworu kanału lędźwiowego.
- W okresie od 28. do 40. tygodnia jądra schodzą do moszny.
Etiologia i patogeneza
przyczyny
- Pusta połowa moszny jest wynikiem wewnątrzmacicznego skrętu jądra lub zatrzymania jądra3
.- Możliwymi czynnikami wyzwalającymi mogą być:
- zaburzenie wzrostu nasieniowodów podczas wzrostu chłopca
- zachowanie włóknistej pozostałości wyrostka pochwowego
- powstanie ektopowego wyrostka pochwowego
- Możliwymi czynnikami wyzwalającymi mogą być:
- Przyczyna zatrzymania jąder jest niejasna, ale jest wieloczynnikowa.
patofizjologii
- Niewyczuwalne palpacyjnie jądro może, ale nie musi, znajdować się w jamie brzusznej, w kanale pachwinowym lub w pozycji ektopowej.
- Nie ma miejsca fizjologiczna spermatogeneza.
- wnętrostwo
- Jądro może znajdować się od punktu początkowego w pobliżu dolnego bieguna nerki do miejsca bezpośrednio przed zewnętrznym otworem pachwinowym.
- Samoistne zstąpienie jąder po 1. roku życia nie jest powszechne. Zwykle zejście utrudniają naczynia krwionośne.
- U niektórych dzieci jądra wydostają się z moszny na późniejszym etapie („wnętrostwo wtórne“). Przyczyna takiego stanu nie jest znana.
- ektopia
- Jądra ektopowe schodzą fizjologicznie przez pierścień pachwinowy, ale następnie trafiają na niewłaściwy tor.
- Zwykle znajdują się w powierzchownej kieszeni pachwinowej (najczęstszy przypadek), w okolicy nadłonowej, w kanale udowym, kroczu lub w przeciwległej połowie moszny (najrzadszy przypadek).
- Odpowiada za mniej niż 1% przypadków zatrzymania jąder.
- Anorchia
- brak jąder
- Może być spowodowana agenezją lub brakiem dopływu krwi do macicy (np. z powodu skręcenia).
- Jądra wędrujące
- Jądra wędrujące to zatrzymanie rzekome spowodowane nadaktywnością mięśnia dźwigacza jądra
- Jądra zstąpiły, ale podciągane są z powrotem do pozycji nadmosznowej.
- Siła skurczu mięśnia dźwigacza jądra różni się znacznie u poszczególnych osób, w zależności od wieku i warunków badania przedmiotowego.
- Jądro można obniżyć z pozycji pachwinowej do moszny poprzez ruch przypominający „dojenie“.
- Po przesunięciu jądro pozostaje w mosznie przez krótki czas lub przemieszcza się z powrotem do pachwiny. Przy zmęczeniu mięśnia dźwigacza jądra, jądra przechodzą w stan spoczynku.
- Stan ten wymaga dalszej obserwacji, ale nie wymaga natychmiastowego leczenia.
czynniki predysponujące
- Wcześniactwo
- Niska waga urodzeniowa
- Bliźniak
- Stan przedrzucawkowy
- Poród z pozycji miednicowej
- Wnętrostwo w wywiadzie rodzinnym
ICD-10
- Q53 Niezstąpienie jąder
- Q53.0 Jądro przemieszczone
- Q53.1 Niezstąpienie jąder, jednostronne
- Q53.2 Niezstąpienie jąder, obustronne
- Q53.9 Niezstąpienie jąder, nieokreślone
diagnostyka
- Cały rozdział opiera się na tych źródłach literaturowych3.
Kryteria diagnostyczne
- Wnętrostwo można rozpoznać na podstawie badania przedmiotowego.
- Wyzwaniem diagnostycznym jest identyfikacja jąder wędrujących, które nie wymagają leczenia.
Wywiad lekarski
- Rodzice nie są w stenie mogą zobaczyć/wyczuć jąder.
- Należy ustalić, czy rodzice kiedykolwiek widzieli jądra w mosznie.
- Jądra są niewykrywalne w badaniu pediatrycznym.
Badanie fizykalne
- Cały rozdział opiera się na tych źródłach literaturowych.4-5
- Asymetria moszny może być oznaką wnętrostwa.
- Wyczuwalne palpacyjnie zatrzymane jądro jest zwykle mniejsze niż przeciwległe, zdrowe jądro.
- Wnętrostwo może być częścią wrodzonego zespołu i powinno skłonić do dalszej diagnostyki.
Badanie
- Pacjent powinien być spokojny i zrelaksowany, najlepiej w pozycji ze skrzyżowanymi nogami i rozebranym podbrzuszem. Niemowlęta mogą być badane w pozycji leżącej lub mogą siedzieć na kolanach rodzica.
- Ręka osoby wykonującej badanie powinna być ciepła; w przypadku małych dzieci zaleca się stosowanie lampy grzewczej, aby jądra nie podciągały się w kierunku doczaszkowym z zimna. Mydło może zmniejszyć tarcie dłoni i zwiększyć szansę na wykrycie jąder.
- W pierwszej kolejności podejmowana jest próba zidentyfikowania zewnętrznego otworu kanału pachwinowego i przeprowadzane jest ostrożne badanie palpacyjne wzdłuż przebiegu kanału pachwinowego.
- Jeśli nie udaje się znaleźć jądra, należy wykonać badanie palpacyjne w celu znalezienia jądra ektopowego przed kością łonową, w kroczu i w górnej części uda.
- Pomocna może być fluoroskopia moszny przy użyciu lampy w celu odgraniczenia wodniaka (= prześwitujący płyn).
- Dodatkowe możliwe wyniki obejmują spodziectwo, przepuklinę pachwinową i wodniaka.
Różne wyniki
- Jądra wędrujące (jo-jo)
- Jądra były wyczuwalne palpacyjnie w mosznie po urodzeniu.
- Jądro można umieścić w mosznie w sprzyjających warunkach (ciepłe ręce, dziecko siedzące ze skrzyżowanymi nogami, mydło lub olej na palcach).
- Nadaktywny mięsień dźwigacz jądra ponownie ciągnie jądro do góry.
- Stan ten jest wariantem prawidłowym i nie wymaga leczenia.
- Niewyczuwalne
- Występuje w 20–30% przypadków wnętrostwa (ukrytych jąder).
- Jądra albo znajdują się wewnątrz jamy brzusznej (w 5–10% wszystkich przypadków), albo są nieobecne (w 20–40% przypadków niewyczuwalnych jąder).
- Wyczuwalne
- pachwinowo (68%)
- przedmosznowo (22%)
- ektopowo (10%)
- Jądro można wyczuć palpacyjnie poza zwykłą ścieżką zejścia, w kroczu lub po wewnętrznej stronie uda.
Badania dodatkowe
- Cały rozdział opiera się na tych źródłach literaturowych3.
- Planowanie diagnostyki obrazowej we współpracy z pediatrą
- Badania ultrasonograficzne
- Po badaniu przedmiotowym zwykle wykonuje się badanie ultrasonograficzne kanału pachwinowego.
- RM6
- Jądra daje się wykryć za pomocą RM w kanale pachwinowym lub poniżej niego.
- Jednak do wykonania RM u małych dzieci wymagane jest znieczulenie ogólne.
- Jeśli jądra znajdują się wewnątrz jamy brzusznej, czułość USG wynosi 45%, a swoistość 78%.
- RM wykazuje nieco lepsze wartości.
- Diagnostyka obrazowa nie jest zatem wiarygodną metodą lokalizacji jąder niewyczuwalnych palpacyjnie.
- Laparoskopia
- Laparoskopia pozwala odróżnić wrodzony skręt jądra od jąder zlokalizowanych wewnątrz jamy brzusznej.
- Według norweskiego badania, laparoskopia jest podstawową metodą badania chłopców w wieku powyżej 1. roku życia
.- Celem jest ustalenie, czy jądra są obecne, czy należy przeprowadzić zabieg chirurgiczny, a jeśli tak, to jakiego rodzaju.
- Pacjenci z brakującymi jądrami powinni być chronieni przed dalszymi operacjami.
- Badanie hormonów i chromosomów
- w celu wykluczenia interseksualności
- W razie potrzeby progesteron, testosteron, LH, FSH
- W razie potrzeby stymulacja hCG produkcji testosteronu; może być przydatna w przypadku podejrzenia obustronnego zatrzymania jąder.
Wskazania dla skierowania do specjalisty
- W przypadku zatrzymania jąder
Leczenia
Cele terapii
- Przemieszczenie jądra w dół do moszny3
- Zapobieganie wtórnym uszkodzeniom poprzez przemieszczenie jądra do moszny przed ukończeniem 1. roku życia
- płodność w wieku dorosłym, zmniejszenie ryzyka nowotworu złośliwego, w razie potrzeby wsparcie psychologiczno-kosmetyczne
Ogólne informacje o leczeniu
- Zaleca się odczekanie w ciągu pierwszych 6 miesięcy życia, ponieważ nadal istnieje możliwość spontanicznego zejścia.
- Terapia chirurgiczna3,7
- Pierwotna operacja jest najczęściej stosowana w przypadku zatrzymania jąder, jądra ektopowego i wtórnej ektopii.
- Jeśli zatrzymanie jąder zostanie wykryte u chłopców w wieku powyżej 6 miesięcy, istnieje wskazanie do skierowania na operację.
- Terapia hormonalna8
- niski wskaźnik skuteczności
- Biopsja jądra
- niewskazana jako badanie rutynowe
- tylko u chłopców po okresie dojrzewania z nieleczonymi wrodzonymi niezstąpionymi jądrami w celu wykluczenia śródnabłonkowych nowotworów jąder (testicular intraepithelial neoplasia — TIN)
Mężczyźni po okresie dojrzewania z wnętrostwem
- Wiek poniżej 32 lat z jednostronnym zatrzymaniem jąder
- zalecana orchiektomia
- Wiek powyżej 32 lat z jednostronnym zatrzymaniem jąder
- zalecane dokładne monitorowanie i kontrole
- Każdy mężczyzna z obustronnym zatrzymaniem jąder
- wskazania do biopsji jąder i orchidopeksji
Leczenie farmakologiczne
Terapia hormonalna
- Terapia hormonalna mająca na celu osiągnięcie zejścia jąder może być prowadzona w postaci izolowanego podawania GnRH (3 x 400 mcg/dobę w formie aerozolu do nosa przez 4 tygodnie), hCG (1 x 500 j.m. tygodniowo w formie wstrzyknięcia przez 3 tygodnie) lub w formie terapii skojarzonej z GnRH z późniejszym podawaniem hCG.
- Jest przedmiotem dyskusji8.
- Terapia hormonalna nie jest zbyt skuteczna. Rodzice powinni zostać poinformowani o wskaźniku skuteczności.
- Współczynnik powodzenia zstąpienia wynosi ok. 20 %.
- Im bliżej moszny znajduje się jądro, tym wyższy wskaźnik powodzenia.
- W przypadku GnRH jest to 21% (jeśli wykluczyć jądra wędrujące, w przypadku których nie ma potrzeby leczenia — tylko 12%; jeśli wykluczyć jądra zlokalizowane wewnątrzbrzusznie — 45%), w przypadku hCG 19% (13–25%), a w przypadku placebo ok. 4 %.
- Ponowne wstąpienie jądra następuje w ok. 25%.
- Terapia hormonalna nie jest zbyt skuteczna. Rodzice powinni zostać poinformowani o wskaźniku skuteczności.
- Terapia hormonalna nie powinna być prowadzona po ukończeniu 1. roku życia.
- Ogólne zalecenia dotyczące pooperacyjnej terapii hormonalnej nie mogą być obecnie podane ze względu na dostępne dane lub powinny być przeprowadzane wyłącznie w kontekście badań.
Inne formy leczenia
Terapia chirurgiczna
- Jeśli zatrzymanie jąder zostanie wykryte w wieku >6 miesięcy, istnieje wskazanie do skierowania na operację.
- Odpowiedni czas na leczenie chirurgiczne jest przedmiotem dyskusji7,9-10, na arenie międzynarodowej operacja zatrzymania jąder jest zalecana w wieku 6–12 miesięcy.
- Interwencja chirurgiczna w wieku <6 miesięcy nie jest zalecana ze względu na częste spontaniczne zstępowanie jąder w ciągu pierwszych 6 miesięcy życia.>
- Operacja niewyczuwalnych palpacyjnie jąder może być przeprowadzona laparoskopowo lub jako zabieg otwarty w jednej lub dwóch sesjach.
- Laparoskopia jest zalecana u chłopców bez wyczuwalnych palpacyjnie jąder, którzy są starsi niż 1 rok przed ustaleniem ostatecznego leczenia.
- Adjuwantowa terapia hormonalna GnRH w celu zwiększenia płodności po orchideopeksji jest kontrowersyjna i nie jest rutynowo wykonywana11.
- To, czy operacja zakończyła się powodzeniem, można ocenić najwcześniej po upływie roku od operacji.
- Wskaźnik sukcesu anatomicznego (jądra bez atrofii w mosznie) wśród specjalistów wynosi >95% u pacjentów, których jądra znajdują się w kanale pachwinowym.
- U pacjentów z jądrami wewnątrz jamy brzusznej wskaźnik powodzenia anatomicznego waha się od 74 do 90% zarówno w przypadku technik otwartych, jak i laparoskopowych.
- Jednak anatomiczny sukces operacji nie osiąga takich samych wartości jak fizjologiczne zstąpienie (prawidłowa produkcja hormonów i spermiogeneza).
- Czynność komórek Sertoliego i Leydiga jest lepsza u mężczyzn, którzy zostali poddani orchidopeksji w ciągu pierwszych 2 lat życia, niż u mężczyzn operowanych później.
- Powikłania są rzadkie w przypadku takich zabiegów chirurgicznych (<1%), ale obejmują zanik jądra, uszkodzenie nasieniowodów i inne rzadkie urazy.>
- Wpływ wczesnej orchidopeksji na czynność hormonalną jąder w wieku dorosłym nie jest znany.
Przebieg, powikłania i rokowanie
przebieg
- Około 75% chłopców z zatrzymaniem jąder po urodzeniu doświadcza spontanicznego zstąpienia jąder w ciągu 1. roku życia.
- Po 1. urodzinach spontaniczne zstąpienie jąder jest rzadkie.
- W grupie pacjentów z obustronnym wnętrostwem, którzy przeszli operację w dzieciństwie, około 28% miało ponad 20 milionów plemników/ml ejakulatu.
- W grupie pacjentów z jednostronnym wnętrostwem, którzy przeszli operację w dzieciństwie, około 70% miało ponad 20 milionów plemników/ml ejakulatu.
powikłania
Niepłodność12
- U pacjentów z wcześniejszym zatrzymaniem jąder płodność wynosi ok. 60% w porównaniu do ok. 90% w populacji ogólnej.
- Nieleczone obustronne wnętrostwo prowadzi do azoospermii.
- Nie odnotowano obniżonej płodności w przypadku leczonego jednostronnego zatrzymania jąder.
Nowotwór jądra13-14
- Ryzyko zachorowania na raka jąder jest od 5 do 40 razy wyższe w przypadku wewnątrzbrzusznego zatrzymania jądra.
- Względne ryzyko wystąpienia nowotworu jądra przy wnętrostwie u wszystkich pacjentów wynosi ok. 3–8, przy czym u pacjentów leczonych drogą orchidopeksji przed okresem dojrzewania ryzyko jest niższe (ryzyko względne 2–3).
- Wyższe ryzyko występuje w przypadku obustronnego wnętrostwa, powiązanych anomalii układu moczowo-płciowego oraz u pacjentów z nieleczonym wnętrostwem.
- U pacjentów z jednostronnym wnętrostwem ryzyko wystąpienia nowotworu jądra fizjologicznie zlokalizowanego w mosznie jest minimalne.
- Orchidopeksja wydaje się zmniejszać ryzyko rozwoju nasieniaka.
- W przypadku nieleczonego wnętrostwa nasieniaki występują w 74% przypadków nowotworu jąder.
- Przypadki nowotworu jąder rozwijającego się po orchidopeksji to w 37% nasieniaki.
- U chłopców operowanych przed ukończeniem 12. roku życia ryzyko zachorowania na nowotwór jąder jest znacznie niższe w porównaniu z pacjentami operowanymi po ukończeniu 12. roku życia lub w ogóle nieleczonymi.
- Orchiektomię należy rozważyć u pacjentów z przetrwałym wnętrostwem w wieku około 30 lat.
- Biopsja jąder może być przydatna u chłopców z obustronnym wnętrostwem w wieku od 10 lat w celu oceny, czy istnieje wskazanie do orchidopeksji lub orchiektomii.
Rokowania
- Nieleczone zatrzymanie prowadzi do utraty produkcji plemników (azoospermia).
- Jądra ektopowe prowadzą do zwiększonego ryzyka nowotworu jąder.
Dalsze postępowanie
- Cały rozdział opiera się na tych źródłach literaturowych.5,15
- W przypadku rozpoznania zatrzymania jąder zaleca się skierowanie pacjenta na oddział chirurgii/urologii dziecięcej najpóźniej w wieku 6 miesięcy.
- Jeśli jądro (jądra) samoistnie zstąpiło (zstąpiły) do moszny przed 6. miesiącem życia lub jest (są) wędrujące, rodzicom należy zalecić coroczne kontrole przez całe dzieciństwo, ponieważ istnieje znaczne ryzyko ponownego wciągnięcia poza mosznę.
- Jeśli jądro (jądra) nie zstąpiło (nie zstąpiły) w wieku 6 miesięcy, orchidopeksja jest wskazana przed ukończeniem 1. roku życia3.
- Jeśli rozpoznanie zostanie ustalone po 6. miesiącu życia, zaleca się natychmiastowe skierowanie pacjenta w celu ustalenia wskazań do operacji7.
informacje dla pacjentów
O czym należy poinformować pacjentów?
- Regularna samodzielna kontrola jąder
Informacje dla pacjentów w Deximed
Ilustracje
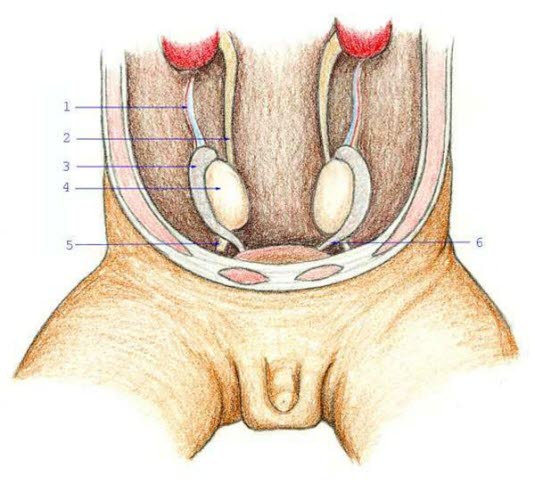
Rozwój męskich narządów płciowych: (1) naczynia krwionośne jąder, (2) moczowód, (3) najądrze, (4) jądro, (5) Gubernaculum testis (jądrowód), (6) Ductus deferens (nasieniowód)
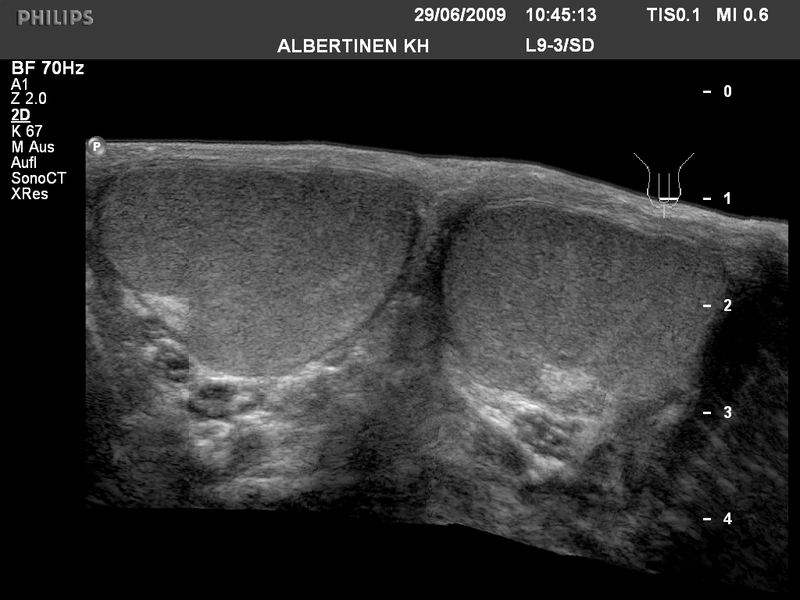
Sonografie Hoden-Normalbefund (Quelle: Albertinen KH)
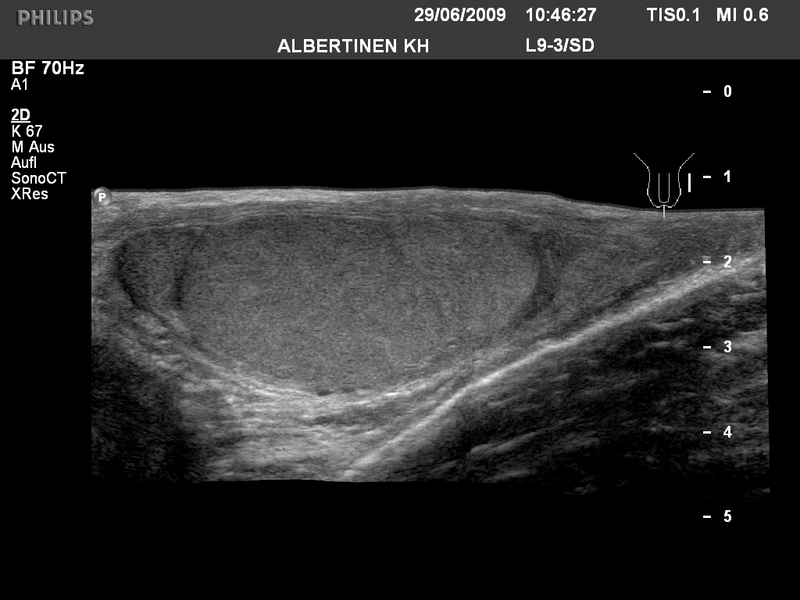
Sonografie Hoden-Normalbefund (Quelle: Albertinen KH)
Quellen
Literatur
- Keys C, Heloury Y. Retractile testes: a review of the current literature. J Pediatr Urol 2012; 8: 2-6. pubmed.ncbi.nlm.nih.gov
- Bay K, Main KM, Toppari J, et al. Testicular descent: INSL3, testosterone, genes and the intrauterine milieu. Nat Rev Urol 2011; 8: 187-96. pubmed.ncbi.nlm.nih.gov
- Boehme P, Degener S, Wirth S, Geis B, Aydin M, Lawrenz K, Troebs RB, Schmittenbecher P, Beume J, Pötzsch S, Schwarz B, Hensel KO. Multicenter Analysis of Acquired Undescended Testis and Its Impact on the Timing of Orchidopexy. J Pediatr 2020. doi:10.1016/j.jpeds.2020.04.037 DOI
- Cho A, Thomas J, Perera R, Cherian A. Undescended testis. BMJ 2019. doi:10.1136/bmj.l926 DOI
- Hutson JM, Vikraman J, Li R, Thorup J. Undescended testis: What paediatricians need to know . J Paediatr Child Health 2017. doi:10.1111/jpc.13744 DOI
- Tasian GE, Copp HL. Diagnostic performance of ultrasound in nonpalpable cryptorchidism: a systematic review and meta-analysis. Pediatrics 2011; 127: 119-28. pubmed.ncbi.nlm.nih.gov
- Stredele R, Apfelbeck M, Mainusch M, Lellig K, Karl A, Tritschler S, Stief C, Riccabona M. Undescended testis: current pathways of diagnostics and treatment. MMW Fortschr Med 2018. doi:10.1007/s15006-018-0709-4 DOI
- Ludwikowski B, González R. The controversy regarding the need for hormonal treatment in boys with unilateral cryptorchidism goes on: a review of the literature. Eur J Pediatr 2012. pmid:22395567 PubMed
- Hutson JM, Balic A, Nation T, Southwell B. Cryptorchidism. Semin Pediatr Surg 2010; 19: 215-24. PubMed
- Ritzén EM. Undescended testes: a consensus on management. Eur J Endocrinol 2008; 159 Suppl 1: S87-90. pubmed.ncbi.nlm.nih.gov
- Biers SM, Malone PS. A critical appraisal of the evidence for improved fertility indices in undescended testes after gonadotrophin-releasing hormone therapy and orchidopexy. J Pediatr Urol 2010; 6: 239-46. pubmed.ncbi.nlm.nih.gov
- Goel P, Rawat JD, Wakhlu A, Kureel SN. Undescended testicle: An update on fertility in cryptorchid men . Indian J Med Res 2015. doi:10.4103/0971-5916.155544 DOI
- Cook MB, Akre O, Forman D, et al. A systematic review and meta-analysis of perinatal variables in relation to the risk of testicular cancer--experiences of the son. Int J Epidemiol 2010; 39: 1605-18. www.ncbi.nlm.nih.gov
- Wood HM, Elder JS. Cryptorchidism and testicular cancer: separating fact from fiction. J Urol 2009; 181: 452-61. pubmed.ncbi.nlm.nih.gov
- Stein R, Loersch F, Younsi N. German guideline on undescended testis-what is relevant in daily routine?. Urologe A 2020. doi:10.1007/s00120-020-01183-z DOI
- Wampler SM, Llanes M. Common scrotal and testicular problems. Prim Care 2010; 37: 613-26. pubmed.ncbi.nlm.nih.gov
- Lao OB, Fitzgibbons RJ Jr, Cusick RA. Pediatric inguinal hernias, hydroceles, and undescended testicles. Surg Clin North Am 2012; 92: 487-504. pubmed.ncbi.nlm.nih.gov
- Virtanen HE, Adamsson A. Cryptorchidism and endocrine disrupting chemicals. Mol Cell Endocrinol 2012; 355: 208-20. pubmed.ncbi.nlm.nih.gov
- Genetic and environmental contributors to cryptorchidism. Pediatr Endocrinol Rev 2009; 6: 476-80. pubmed.ncbi.nlm.nih.gov
- Guo J, Liang Z, Zhang H, et al. Laparoscopic versus open orchiopexy for non-palpable undescended testes in children: a systemic review and meta-analysis. Pediatr Surg Int 2011; 27: 943-52. pubmed.ncbi.nlm.nih.gov
- Papparella A, Romano M, Noviello C, et al. The value of laparoscopy in the management of non-palpable testis. J Pediatr Urol 2010; 6: 550-4. pubmed.ncbi.nlm.nih.gov
Autor*innen
- Moritz Paar, Dr. med., Arzt in Weiterbildung Allgemeinmedizin, Münster