Informacje ogólne
Definicja
- Ankylostomatoza należy do grupy zakażeń pasożytami przenoszonymi przez glebę, wywoływanych przez tęgoryjce (Ancylostoma duodenale, Ancylostoma braziliense i Necator americanus).1
- Trzy najczęstsze choroby wywołane przez robaki pasożytnicze to glistnica, trichurioza oraz ankylostomatoza. Często występują one razem; w szczególności dzieci mogą być przewlekle zarażone wszystkimi trzema robakami jelitowymi.
- Dochodzi tu do typowego zakażenia skóry (zespół larwy wędrującej)2 lub choroby jelit w postaci eozynofilowego zapalenia jelit.3
Częstość występowania
- 576–740 mln ludzi na całym świecie jest zarażonych tęgoryjcem.4
- Ponad 1 miliard ludzi na całym świecie jest zarażonych co najmniej jednym gatunkiem pasożyta.5
- Osoby szczególnie narażone to:5
- małe dzieci i dzieci w wieku szkolnym
- kobiety w wieku rozrodczym
- niektóre grupy zawodowe, takie jak zbieracze herbaty lub górnicy
- osoby powracające z podróży, które na przykład chodziły boso po plaży w niektórych obszarach
Etiologia i patogeneza
- Przenoszone przez glebę robaki jelitowe (helminty) to grupa pasożytniczych robaków, które mogą powodować zakażenia u ludzi poprzez kontakt z jajami i larwami złożonymi w ciepłych, wilgotnych glebach tropikalnych i subtropikalnych.1
- Larwy tęgoryjca albo przebijają skórę, albo są połykane wraz ze skażoną żywnością lub wodą.
- Dorosłe robaki mogą przetrwać kilka lat w przewodzie pokarmowym człowieka.
Cykl życiowy tęgoryjca
- Po kopulacji samica tęgoryjca składa kilka tysięcy jaj dziennie.
- Jaja są wydalane z kałem i muszą spaść na wilgotną, ciepłą glebę, aby larwy mogły przetrwać i rozwinąć się.
- W zależności od warunków środowiskowych larwy są zakaźne od kilku godzin do tygodnia.
- Po przeniknięciu przez skórę larwy docierają do naczyń włosowatych płuc poprzez krwiobieg. Tam przenikają do pęcherzyków płucnych, skąd za pomocą rzęsek docierają do jamy ustnej przez oskrzela i tchawicę.3
- Po połknięciu docierają do błony śluzowej górnego odcinka przewodu pokarmowego, gdzie przyczepiają się do ściany jelita.
- Tutaj rozwijają się aż do osiągnięcia dojrzałości płciowej i składają jaja po 5-9 tygodniach.
- Dorosłe robaki mogą żyć od 1 roku do 5 lat.
Patofizjologia
- W przypadku larw patogennych dla zwierząt ludzie są raczej przypadkowymi żywicielami; migrujące larwy prowadzą do miejscowej reakcji skórnej (zespół larwy wędrującej) ze swędzącym zapaleniem skóry, obrzękiem i grudkami.
- W większości przypadków widoczne są typowe nitkowate, zaczerwienione struktury przewodów.
- Po pewnym czasie larwy ponownie odpadają.
- Jeśli żywicielem ostatecznym jest człowiek, larwy migrują przez ciało, a następnie czasami prowadzą do zespołu płucnego podobnego do zespołu Löfflera6 z kaszlem, eozynofilią i krwiopluciem przed osiedleniem się w jelicie.
- Występują objawy jelitowe (biegunka i ból), a także niedożywienie i uczucie osłabienia.5
- Bardzo często utrata krwi w jelitach powoduje niedokrwistość z niedoboru żelaza.
- Zakażone dzieci mogą cierpieć na niedożywienie, zaburzenia wzrostu i rozwoju, zaburzenia poznawcze i mieć problemy z nauką.
- Jakość życia zakażonych dzieci jest znacznie niższa.7
- Infekcje te mogą zwiększać podatność na inne zakażenia, w tym malarię, gruźlicę i HIV.8-9
Czynniki predysponujące
- Klimat
- Wilgotne obszary tropikalne i subtropikalne; w kontekście globalnego ocieplenia może to również dotyczyć plaż w południowej Europie. 10
- Chodzenie boso
- Złe warunki sanitarne11
ICD-10
- B76 Choroby wywołane przez tęgoryjca
- B76.0 Ankylostomoza, zakażenie wywołane przez gatunki Ancylostoma
- B76.1 Nekatorioza, zakażenie wywołane przez Necator americanus
- B76.8 Inne choroby tęgoryjcowe
- B76.9 Choroba tęgoryjcowa, nieokreślona
Diagnostyka
Kryteria diagnostyczne
- Badanie mikroskopowe stolca w celu wykrycia jaj
Diagnostyka różnicowa
- Inne choroby wywołane przez robaki pasożytnicze
- Bilharcjoza
- Miejsca wniknięcia cerkarii często wyglądają bardzo podobnie (cerkariowe zapalenie skóry).3
- po kontakcie ze skażoną wodą
Wywiad lekarski
- Pobyt na obszarach ryzyka
- Chodzenie boso
- Wysypka skórna
- W miejscu wniknięcia larw pojawia się swędząca, rumieniowa wysypka grudkowo-krostkowa.
- Widoczne są czerwone, swędzące pręgi, które rozprzestrzeniają się zgodnie z migrującą larwą (zespół larwy wędrującej).
- Epizody z kaszlem, gorączką, krwawą plwociną
- Objawy ze strony przewodu pokarmowego
- Objawy ogólne jak w przypadku niedokrwistości z niedoboru żelaza
- letarg, bladość, duszność wysiłkowa, obniżona wydolność organizmu, zaburzenia koncentracji, kołatanie serca
Badanie przedmiotowe
- Zespół larwy wędrującej: czerwone pręgi pod skórą, obrzęk, grudki, pęcherzyki
Badania uzupełniające
- Wykrywanie typowych jaj w stolcu
- Morfologia krwi
- obniżony poziom Hb, MCH oraz MCV
- obniżony poziom ferrytyny, żelaza, transferyny, nasycenia transferyny
- eozynofilia, najwyższa w 5-9 tygodniu po wystąpieniu zakażenia3
Leczenie
Cele terapii
- Eliminacja pasożyta (lub zmniejszenie obciążenia pasożytami w krajach rozwijających się)
Ogólne informacje o terapii
- Leki przeciwrobacze12
- Ewentualnie poprawa warunków sanitarnych
Zalecenia dla pacjentów
- Poprawa warunków sanitarnych i higieny osobistej (w krajach endemicznych)
Leczenie farmakologiczne
- Mebendazol 2 x 100 mg przez 3 dni
- Jeśli choroba wywołana przez robaki pasożytnicze wymaga leczenia, mebendazol może być stosowany przez cały okres ciąży.
- Pyrantel w dawce dla dorosłych 10 mg/kg masy ciała dziennie przez 3 dni
- Albendazol 800 mg/dobę doustnie przez 3 dni
- Na obszarach endemicznych zaleca się regularne odrobaczanie dzieci w wieku szkolnym.13-14
- Dzieci w wieku poniżej 6 lat: miejscowe leczenie albendazolem 10% 3 razy dziennie przez 7-10 dni
Zapobieganie
- Poprawa warunków sanitarnych w krajach, w których choroby wywołane przez robaki pasożytnicze są powszechne
- Unikanie chodzenia boso
- W najbliższej przyszłości nie będzie szczepionki przeciwko tej chorobie.1
Przebieg, powikłania i rokowanie
Przebieg
- Larwy przenikają przez skórę (tęgoryjec) lub są spożywane z zanieczyszczoną żywnością lub wodą (tęgoryjec i włosogłówka).
- Larwy docierają do płuc przez układ krwionośny, gdzie są odfiltrowywane z krwi (tęgoryjec).
- Z płuc larwy migrują do gardła, skąd przedostają się do układu pokarmowego i tam pozostają.
- Przewlekłe stadium jelitowe z wydzielaniem jaj
Zespół larwy wędrującej
- Larwy przebijają nieuszkodzoną skórę.
- Rozprzestrzeniają się pod skórą i są widoczne jako czerwone pręgi, które powoli się powiększają.
- Zakażenie ma charakter samoograniczający się; larwy zwykle giną po 2-8 tygodniach.
Powikłania
- Niedokrwistość z niedoboru żelaza spowodowana jelitową utratą krwi1
- Wysypka skórna
- Stan zapalny płuc
- Niedrożność jelit5
- Ponowne zakażenie
Rokowanie
- Jeśli diagnoza zostanie postawiona i leczenie rozpocznie się przed wystąpieniem poważnych powikłań wtórnych, pacjentów można zwykle wyleczyć.
- Na obszarach endemicznych istnieje wyraźny związek między przewlekłymi chorobami wywołanymi przez robaki pasożytnicze a zaburzeniami wzrostu i rozwoju u dzieci.
Informacje dla pacjentów
Informacje dla pacjentów w Deximed
Illustrationen
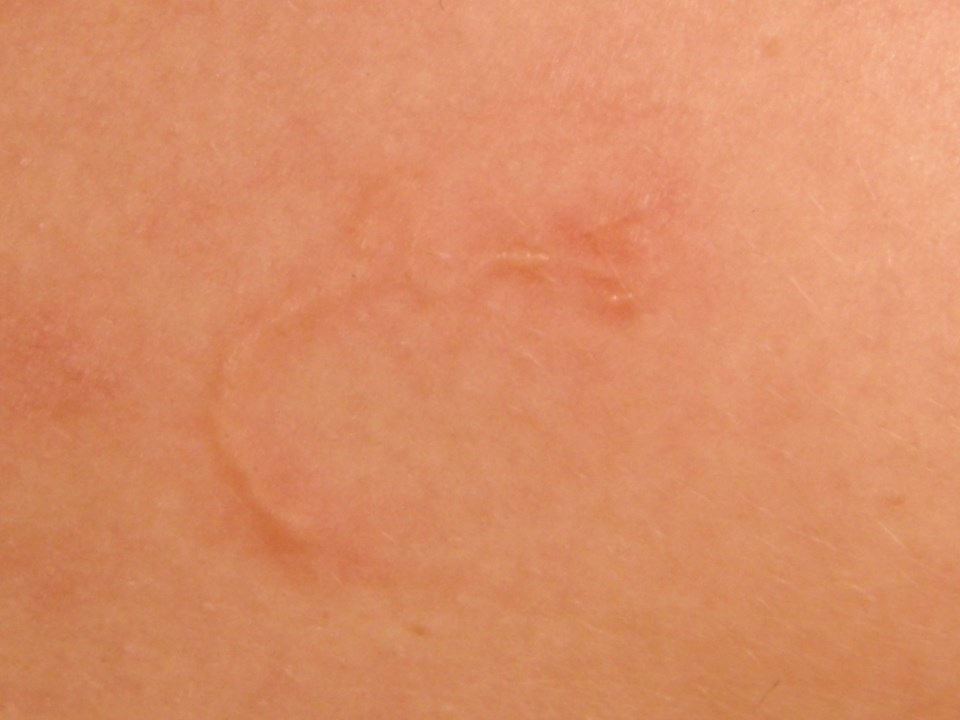
Larva migrans
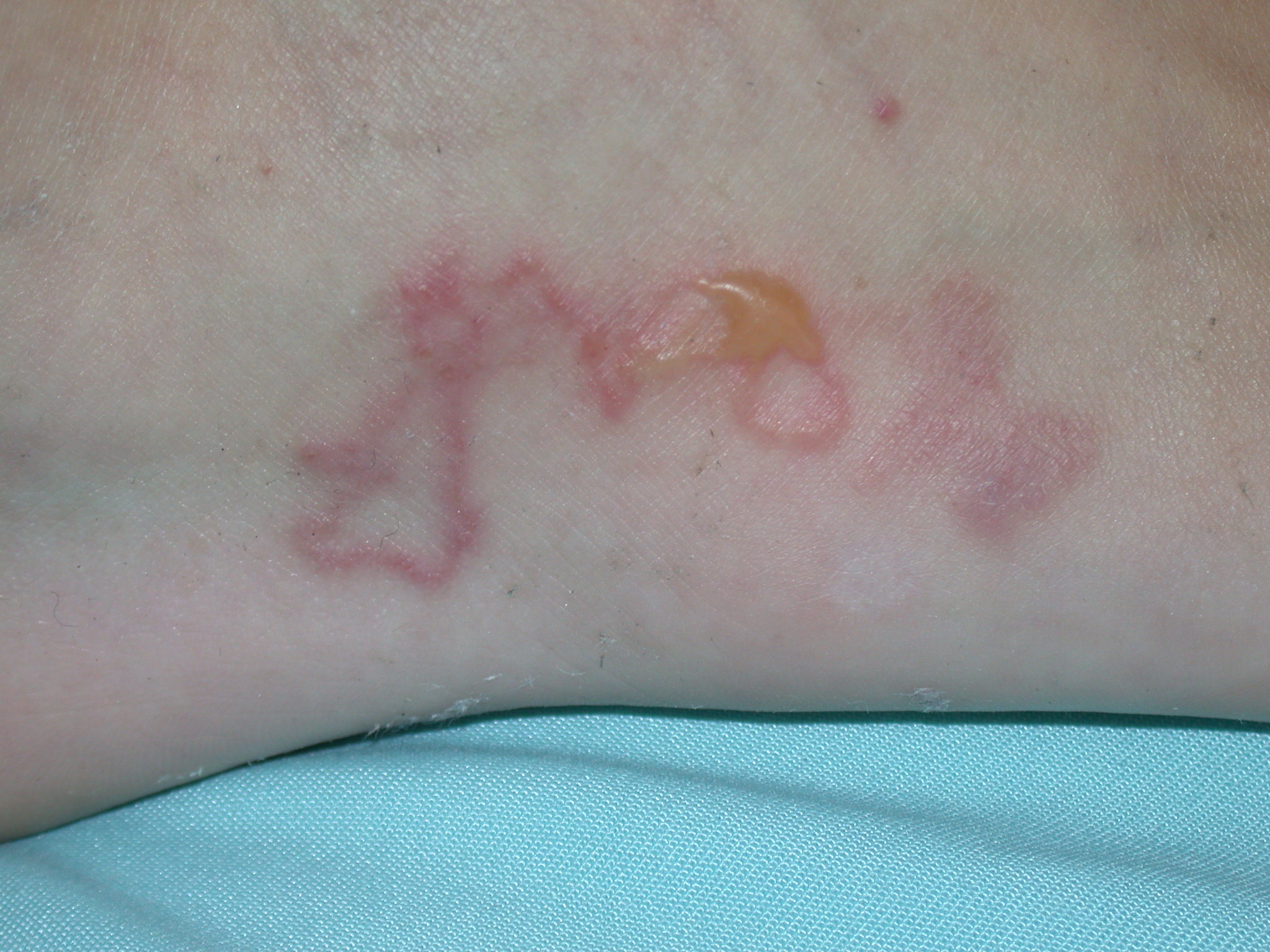
Larva migrans
Quellen
Literatur
- Bethony J, Brooker S, Albonico M, et al. Soil-transmitted helminth infections: ascariasis, trichuriasis, and hookworm. Lancet 2006; 367: 1521-32. PubMed
- Feldmeier H, Schuster A. Mini review: Hookworm-related cutaneous larva migrans. Eur J Clin Microbiol Infect Dis 2012; 31: 915-8. pmid:21922198 PubMed
- Hotez PJ, Brooker S, Bethony JM, Bottazzi ME, Loukas A and Xiao S. Hookworm infection. N Engl J Med 2004; 351: 799-807. New England Journal of Medicine
- CDC.Centers for Disease Control and Prevention. Parasites - Soil-transmitted helminths. 2013. Zugriff 17.05.2020 www.cdc.gov
- WHO. Soil-transmitted helminth infections. Fact sheet. Updated 2020 www.who.int
- Podder I, Chandra S, Gharami RC: Loeffler's syndrome following cutaneous larva migrans: An uncommon sequel. Indian J Dermatol 61(2); Mar-Apr 2016. www.ncbi.nlm.nih.gov
- Schuster A, Lesshafft H, Talhari S, et al. Life quality impairment caused by hookworm-related cutaneous larva migrans in resource-poor communities in Manaus, Brazil. PLoS Negl Trop Dis 2011; 5: e1355. pmid: 22087341 PubMed
- Le Hesran JY, Akiana J, Ndiaye HM, Dia M, Senghor P and Konate L. Severe malaria attack is associated with high prevalence of Ascaris lumbricoides infection among children in rural Senegal. Trans R Soc Trop Med Hyg 2004; 98: 397-99. PubMed
- Fincham JE, Markus MB and Adams VJ. Could control of soil-transmitted helminthic infection influence the HIV/AIDS pandemic? Acta Trop 2003; 86: 315-33. PubMed
- Gautret P, Cramer JP, Field V, et al. Infectious diseases among travellers and migrants in Europe, EuroTravNet 2010. Euro Surveill 2012; 17: 20205. pmid:22790534 PubMed
- de Silva NR, Brooker S, Hotez PJ, Montresor A, Engels D and Savioli L. Soil-transmitted helminth infections: updating the global picture. Trends Parasitol 2003; 19: 547-51. PubMed
- Keiser J, Utzinger J. Efficacy of current drugs against soil-transmitted helminth infections. Systematic review and meta-analysis. JAMA 2008; 299: 1937-48. pubmed.ncbi.nlm.nih.gov
- Savioli L, Stansfield S, Bundy DA et al. Schistosomiasis and soil-transmitted helminth infections: forging control efforts. Trans R Soc Trop Med Hyg 2002; 96: 577-9. PubMed
- Taylor-Robinson DC, Maayan N, Soares-Weiser K, Donegan S, Garner P. Deworming drugs for soil-transmitted intestinal worms in children: effects on nutritional indicators, haemoglobin, and school performance. Cochrane Database of Systematic Reviews 2015, Issue 7. Art. No.: CD000371. DOI: 10.1002/14651858.CD000371.pub6 DOI
Autoren
- Monika Lenz, Fachärztin für Allgemeinmedizin, Neustadt am Rübenberge