Informacje ogólne
Definicja
- Brak miesiączki przez okres co najmniej trzech cykli — mierzony wedle czasu trwania poprzedniej przerwy — lub przez co najmniej 6 miesięcy u kobiety niebędącej w ciąży i wcześniej spontanicznie miesiączkującej.1
- Brak menstruacji przez okres dziewięciu miesięcy lub dłużej u kobiet z wcześniej nieregularnym cyklem miesiączkowym2
Częstość występowania
- Zapadalność szacuje się na 8% kobiet w wieku od 16 do 24 lat w ciągu roku.
- Wtórny brak miesiączki występuje częściej niż pierwotny brak miesiączki.3
Diagnostyka
- Informacje ogólne
- Jeśli miesiączki brak krócej niż rok, rzadko wskazane jest przeprowadzenie badań wykraczających poza badanie ginekologiczne. W 75% przypadków miesiączka powraca w ciągu roku.
- Po zakończeniu karmienia piersią można odczekać sześć miesięcy z wyjaśnianiem.
- Najczęstsze przyczyny1,4
- brak miesiączki pochodzenia podwzgórzowego, często spowodowany:
- zaburzeniami odżywiania
- nadmiernym uprawianiem sportu wyczynowego
- przeciążeniem emocjonalnym lub fizycznym
- hiperprolaktynemią (prolaktynoma? Niedoczynność tarczycy? Leki?)
- antykoncepcją hormonalną
- szczególnie po zastosowaniu medroksyprogesteronu w postaci o przedłużonym uwalnianiu (depot) w dawce podawanej co trzy miesiące
- Preparat progestagenowy?
- Hormonalna wkładka domaciczna?
- niewydolność jajników
- przedwczesna menopauza
- ciężka niedoczynność tarczycy lub nadczynność tarczycy
- po radiochemioterapii
- w przypadku aberracji chromosomalnej (np. zespół łamliwego chromosomu X, zespół Turnera)
- wrodzona hiperplazja nadnerczy
- hiperandrogenemia, zwykle spowodowana zespołem policystycznych jajników
- brak miesiączki pochodzenia podwzgórzowego, często spowodowany:
- Rzadsze przyczyny1
- niedożywienie lub przewlekła choroba ogólnoustrojowa
- zespół pustego siodła
- Zespół Sheehana (poporodowa martwica przysadki)
- zespół po zapaleniu mózgu
- wytwarzający androgeny guz jajnika lub nadnercza
- autoimmunologiczna przedwczesna niewydolność jajników
- zespół Cushinga
- zespół Ashermana (synechie macicy, zwykle jatrogenne po łyżeczkowaniu)
- Po wykluczeniu ciąży, chorób tarczycy i hiperprolaktynemii jako możliwych przyczyn, pozostałe przyczyny klasyfikuje się jako normogonadotropowy brak miesiączki, hipogonadyzm hipogonadotropowy i hipogonadyzm hipergonadotropowy.5-6
- przyczyna leżąca w jajnikach: zawsze hipergonadotropowa niewydolność (wysoki poziom FSH)
- przyczyna podwzgórzowo-przysadkowa: dysfunkcja normo- lub hipogonadotropowa (prawidłowy lub niski poziom FSH)
Diagnostyka krok po kroku
- Brak miesiączki o podłożu fizjologicznym?
- Wykluczenie ciąży (najczęstsza przyczyna), brak miesiączki w okresie laktacji, stan poporodowy
- W przypadku pacjentki >40 lata: Menopauza, która wystąpiła w sposób fizjologiczny?
- W przypadku młodej pacjentki: Pierwsza miesiączka, która pojawiła się zaledwie kilka lat temu, z nawracającym brakiem miesiączki trwającym kilka miesięcy? (W przypadku pierwotnego braku miesiączki: wykluczyć ogólnoustrojowe opóźnienie rozwojowe)
- Przyczyny podwzgórzowe (ok. 60%): zaburzenia reaktywne i nieznane
- Obejmuje sportowców płci żeńskiej — w przypadku utraty masy ciała i ciężkiego treningu.
- Przyczyny przysadkowe: nowotwory, zwłaszcza prolaktynoma5
- Kora nadnerczy: guzy wytwarzające androgeny
- Jajniki: zespół policystycznych jajników, guzy wytwarzające androgeny
- Ciężkie zaburzenie czynności tarczycy: głównie nadczynność tarczycy, ale także niedoczynność tarczycy
Niebezpieczny odwracalny przebieg choroby
- Zaburzenia tarczycy
- Początek zaburzeń autoimmunologicznych
- Zaburzenia odżywiania
ICD-10
- N91.1 Wtórny brak miesiączki
- N91.2 Brak miesiączki, nieokreślony
Diagnostyka różnicowa
Ciąża
- Należy zawsze wykluczyć!
- Uwaga: Należy pamiętać o ciąży pozamacicznej!
Normo- lub hipogonadotropowa niewydolność jajników
- Zarówno psychologiczne, jak i somatyczne przeciążenie może prowadzić do zmniejszonego uwalniania GnRH przez podwzgórze. Prowadzi to do trzeciorzędowej niewydolności jajników wskutek zmniejszonego wydzielania gonadotropin.5-6
- Poziom gonadotropin we krwi jest często tylko nieznacznie obniżony lub mieści się w prawidłowym zakresie.
- Do możliwych przyczyn zalicza się np.:
- wyraźną utratę masy ciała
- anoreksja lub bulimia.
- choroby przewlekłe takie jak:
- przewlekła niewydolność nerek
- cukrzyca
- niewydolność układu immunologicznego
- nieswoiste zapalenie jelit
- zaburzenia tarczycy
- ciężką depresję
- stres psychospołeczny
- uszkodzenie przysadki lub podwzgórza, np. w wyniku:
- radioterapii mózgu
- guza przysadki (np. z akromegalią, patrz także sekcja Hiperprolaktynemia i artykuł Zaburzenia przysadki)
- zespołu Sheehana (poporodowa martwica przysadki)
- Nie wyjaśniono szczegółowo, w jaki sposób stres lub utrata masy ciała wpływają na uwalnianie GnRH.7-8
- Leczenie jest ukierunkowane na przyczynę.
Obciążenie psychiczne
- Przyczynami mogą być np. zmiana okoliczności życiowych (50%), podróże lub traumatyczne wydarzenia życiowe.
- Badanie somatyczne jest zwykle bez zastrzeżeń.
- Hormony we krwi są zwykle w normie (FSH i estradiol mogą być nieco poniżej normy).
- Badanie psychiatryczne w celu wykluczenia zaburzeń psychicznych, np. zespół stresu pourazowego, depresji, wypalenia, zaburzeń odżywiania.
- W większości przypadków dochodzi do samoistnej remisji; wystarcza obserwacja. Pacjentka powinna nadal stosować antykoncepcję.
Triada zawodniczek (female athlete triad)
- U młodych zawodniczek może pojawić się kombinacja kilku problemów zdrowotnych znanych jako „triada zawodniczek” (female athlete triad), która obejmuje zaburzenia odżywiania, brak miesiączki i osteoporozę.
- Hipogonadyzm hipogonadotropowy
- Miesiączka powraca po umiarkowanym zwiększeniu spożycia kalorii lub redukcji treningów.
- Utrata masy kostnej
- Podobnie jak w przypadku osób z zaburzeniami odżywiania zawodniczki z uporczywym brakiem miesiączki są również narażone na utratę masy kostnej.
- U nastoletnich zawodniczek ma to miejsce w okresie, w którym dochodzi do najbardziej intensywnego tworzenia masy kośćca; utrata minerału kostnego może być zatem nieodwracalna.9-10
- Trening siłowy z ciężarami może częściowo chronić przed osteoporozą.11
- Przeciwdziałanie utracie minerału kostnego
- Przyjmowanie doustnej antykoncepcji lub hormonalnej terapii zastępczej przy menopauzie może przyczynić się do mineralizacji i ochrony kości.11
- Podawany przezskórnie estradiol, ewentualnie w połączeniu z cyklicznie podawanym przezskórnie progestagenem, może pomóc zwiększyć gęstość kości u tych pacjentek.12
- Doustne podawanie estradiolu obniża poziom insulinopodobnego czynnika wzrostu-1 i testosteronu, a zatem nie ma takiego samego efektu troficznego jak podawanie przezskórne.
- Terapia przezskórna wiąże się również z niższym ryzykiem trombofilii niż terapia doustna.
- Bisfosfoniany są potencjalnie teratogenne i nie były jeszcze przedmiotem badań na kobietach w wieku rozrodczym w tym kontekście.
- ewentualnie zastępowanie wapnia i witaminy D
- Więcej informacji można znaleźć w artykule Jadłowstręt psychiczny.
Antykoncepcja hormonalna
- Normo- lub hipogonadotropowa niewydolność jajników
- Po odstawieniu doustnych środków antykoncepcyjnych miesiączka może nie wystąpić przez kilka miesięcy.
- Brak miesiączki występuje szczególnie często po zastosowaniu medroksyprogesteronu w postaci o przedłużonym uwalnianiu (depot) w dawce podawanej co trzy miesiące, hormonalnych wkładek wewnątrzmacicznych i preparatów zawierających wyłącznie progestagen.1
- Brak miesiączki może utrzymywać się przez od 1 do 2 lat po zastosowaniu preparatów w postaci depot.
Hiperprolaktynemia
- Jest to rzadkie.
- Przyczyną jest zwykle mikrogruczolak przysadki mózgowej wytwarzający prolaktynę (prolaktynoma)5, ale istnieje również wiele innych przyczyn.
- Może wystąpić brak miesiączki, mlekotok, niepłodność i hirsutyzm.
Wywołane przez leki
- Leki są drugim najczęstszym wyjaśnieniem prolaktynemii. Poziom prolaktyny zazwyczaj nie wzrasta powyżej 100 ng/ml.5 Możliwe przyczyny to np. :5
- neuroleptyki takie jak:
- haloperidol
- chlorpromazyna
- amisulpiryd
- rysperydon
- zotepina
- zyprazydon
- olanzapina
- leki przeciwdepresyjne (więcej informacji w artykule Depresja), takie jak:
- SSRI
- TCA
- inhibitory MAO
- metoklopramid
- estrogeny
- doustne środki antykoncepcyjne (20–30% kobiet poniżej 35 mcg etynyloestradiolu)
- leki hipotensyjne
- blokery receptora H2
- opiaty
- kokaina
- neuroleptyki takie jak:
prolaktynoma
- Podwyższony poziom prolaktyny (PRL) prowadzi do upośledzonego wydzielania GnRH, co z kolei prowadzi do niskiego poziomu FSH i LH. Niski poziom gonadotropin osłabia czynność jajników, a tym samym produkcję estradiolu.
- Poziom prolaktyny powyżej 100 ng/ml wskazuje na prolaktynomę i wymaga badania RM.
- U niektórych kobiet brak miesiączki jest jedynym objawem, ale występuje również mlekotok (30%), zmniejszone libido, suchość pochwy i osteoporoza (po długim czasie).
- Wraz ze wzrostem rozmiaru guza pojawiają się objawy związane z procesami rozrostowymi w okolicy siodła tureckiego, takie jak ograniczenie pola widzenia i bóle głowy.
- Test ciążowy
- U kobiet w ciąży przysadka mózgowa powiększa się o 100% i mogą wystąpić objawy wcześniej bezobjawowego guza.
- Analizy hormonalne wykazują wysoki poziom PRL i niskie poziomy FSH, LH i estradiolu.
- W przypadku małych guzów wewnątrz siodła tureckiego stosuje się agonistów dopaminy, głównie kabergolinę lub bromokryptynę.13
- Operacja jest wskazana w przypadku większych guzów lub jeśli leczenie farmakologiczne nie przynosi pożądanych rezultatów.
- Więcej informacji nt. chorób przysadki mózgowej
Hipogonadyzm hipogonadotropowy
Przedwczesna menopauza
- Kiedy kobiety poniżej 40. roku życia wchodzą w okres menopauzy14. Połowa z nich ma nieregularnie funkcjonujące jajniki15.
- Etiologia z reguły jest nieznana: Możliwymi przyczynami są zbyt mała liczba pęcherzyków, zakażenia wirusowe i procesy autoimmunologiczne15-16.
- Rozpoznanie wymaga obecności objawów menopauzy, w tym zaburzeń cyklu miesiączkowego.
- Testy hormonalne nie mogą ani wykryć ani wykluczyć przedwczesnej niewydolności jajników.
- Poziom estradiolu w surowicy jest często niski, FSH podwyższony, a PRL w normie.
- O menopauzie świadczy FSH >30 mIU/ml mierzony w dwóch punktach czasowych w odstępie 4–6 tygodni.
- Poziom glukozy na czczo, TSH i kortyzol poranny powinny być również mierzone w ramach ewentualnej diagnostyki różnicowej17.
- Nieleczona przedwczesna niewydolność jajników wiąże się ze zwiększonym prawdopodobieństwem wystąpienia osteoporozy, miażdżycy, suchości błon śluzowych i zmniejszenia piersi15,18-19.
- Leczenie polega na stosowaniu hormonalnej terapii zastępczej (więcej informacji w artykule Klimakterium) lub przyjmowaniu estrogenowo-progestagenowego preparatu złożonego do antykoncepcjidoustnej.
- Przebieg
- U ok. 20–40% kobiet z przedwczesną niewydolnością jajników pojawiają się zaburzenie autoimmunologiczne. Należą do nich cukrzyca, choroba Addisona lub zapalenie tarczycy autoimmunologiczne. Zaleca się regularne badania laboratoryjne.
- W przypadku odpowiednich wskazań ewentualnie analiza chromosomalna w celu wykrycia aberracji chromosomów płciowych (np. zespołu łamliwego chromosomu X, zespołu Turnera)1,15.
- Korzyści z biopsji jajników lub testów na obecność przeciwciał przeciwko antygenom jajnika nie zostały udowodnione15-16.
- Oznaczanie hormonu antymüllerowskiego również nie należy do rutynowej diagnostyki, ponieważ może on być zmieniony przez różne czynniki, w tym zespół policystycznych jajników lub stosowanie antykoncepcji hormonalnej i innych preparatów hormonalnych.
Inne przyczyny uszkodzenia gonad
- Zaburzenie autoimmunologiczne
- Chemioterapia
- Terapia radiacyjna, zwłaszcza w obrębie miednicy
- galaktozemia
- Genetyczny niedobór 17-hydroksylazy
- Zakażenia ogólnoustrojowe, np. świnka
Hiperandrogenemia
Zespół policystycznych jajników (PCOS)
- Liczne torbielowate pęcherzyki w jajnikach
- Najczęstsza przyczyna hiperandrogenemii, z zaburzeniami owulacji i cyklu oraz niepłodnością
- Występuje u około 5–10% wszystkich kobiet w wieku rozrodczym. Stopniowy początek między 15. a 25. rokiem życia.
- Zaburzenia miesiączkowania, niemożność zajścia w ciążę, trądzik, nadwaga i zespół metaboliczny, hirsutyzm
Inne przyczyny
- zespół Cushinga (typ endogenny)
- Guz (jajnika lub nadnercza) wydzielający androgeny
- Egzogenne androgeny (np. anaboliki)
- Nieklasyczny zespół nadnerczowo-płciowy
Przyczyny anatomiczne
- Najczęstszym jest zespół Ashermana z synechią wewnątrzmaciczną i bliznowaceniem, zwykle spowodowanym łyżeczkowaniem lub zakażeniem.
- Histerosalpingografia, histeroskopia lub sonohisterografia mogą być pomocne w postawieniu diagnozy.
- Zwężenie szyjki macicy
- mięśniaki macicy powodujące niedrożność
- Polipy
Wywiad lekarski
Na to należy zwrócić szczególną uwagę
Ciąża?
- U aktywnych seksualnie kobiet z wcześniejszą spontaniczną miesiączką: test ciążowy
Pierwsza miesiączka i wywiad dotyczący miesiączki
- Występowanie pierwotnego lub wtórnego braku miesiączki?
Wywiad dotyczący przyjmowanych leków
- Poszczególne leki mogą powodować hiperprolaktynemię, a tym samym brak miesiączki (patrz wyżej).
- Zażywanie narkotyków
- Antykoncepcja hormonalna
Utrata masy ciała?
Aktywność fizyczna
- Częste treningi
- Sport wyczynowy?
- Czy pacjentka uprawia więcej sportu niż wcześniej?
Stres psychiczny
- Podróżowanie, obciążenia psychiczne, zmiany w sytuacji życiowej (przeprowadzka, stres egzaminacyjny itp.)?
Inne choroby
- Choroby przewlekłe (patrz wyżej)
Wcześniejsze leczenie
- Zabiegi chirurgiczne?
- Chemioterapia?
- Terapia radiacyjna
- Mózgu?
- Narządów miednicy?
Obciążenia rodzinne?
- Szczegółowy wywiad rodzinny
Inne objawy?
- Nadmierne owłosienie/hirsutyzm?
- Trądzik?
- Wydzielina z piersi (mlekotok, występowanie przezroczystego i mlecznego płynu może mieć również charakter idiopatyczny)
- Ból głowy? Zaburzenia pola widzenia? Należy rozważyć guza przysadki.
- Objawy nadczynności lub niedoczynności tarczycy Należy rozważyć zaburzenia tarczycy.
- Objawy naczynioruchowe: Należy rozważyć przedwczesną niewydolność jajników.
Badanie przedmiotowe
W praktyce lekarza rodzinnego
- Stan odżywienia
- wzrost i masa ciała, BMI
- Kliniczne objawy nadczynności lub niedoczynności tarczycy
- Objawy wirylizacji
- hirsutyzm, trądzik, nadmierne owłosienie, przerost łechtaczki
- Zespół policystycznych jajników? Zespół Cushinga? Guzy wytwarzające androgeny?
U specjalisty
- Test ciążowy
- Badanie wzroku — pole widzenia
Badanie uzupełniające
Diagnostyka u specjalisty
- Badanie ginekologiczne i USG przezpochwowe
Analiza hormonów
- Estradiol, FSH, LH, PRL, TSH, FT4
- ewentualnie SHBG, testosteron, androstendion, DHEAS
- Jeśli pacjentka przyjmuje pigułki antykoncepcyjne lub otrzymuje hormonalną terapię zastępczą, oznaczanie estradiolu, FSH i LH jest bezcelowe.
- Hiperprolaktynemia
- Najczęstszą przyczyną jest prolaktynoma.
- Hamuje uwalnianie i działanie gonadotropin5.
- Wartości powyżej 100 ng/ml wskazują na prolaktynomę i są wskazaniem do badania RM5,20.
- Różne laboratoria stosują różne metody pomiaru prolaktyny. Jednostki ng/ml i mIU/l nie mogą być zatem porównywane ze sobą bezpośrednio. Podczas analizy wyników testów należy stosować wartości odniesienia dostosowane do danej metody analizy.
- Leki są drugą co do częstotliwości przyczyną i mogą powodować podwyższone wartości, ale zwykle poniżej 100 ng/ml.
- Innymi wyjaśnieniami mogą być:
- zmieniony metabolizm — niewydolność wątroby, niewydolność nerek
- Wytwarzanie ektopowe — rak płuca, rozrodczak zarodkowy, rak dolnego odcinka gardła, torbiel dermoidalna jajnika, rak nerkowokomórkowy, potworniak, karmienie piersią, stymulacja piersi, niedoczynność tarczycy5.
- Wysokie wartości FSH/LH
- Przemawiają za niewydolnością jajników, np. pierwotna niewydolność jajników 21 lub menopauza.
- Pierwotna niewydolność jajników występuje nawet u 1% wszystkich kobiet; pojawia się przed 40. rokiem życia z rzadkimi miesiączkami lub brakiem miesiączki.
- Wysoka wartość LH i niska wartość SHBG
- Może być objawem zespołu policystycznych jajników.
- Poziom androgenów w surowicy może być nieznacznie podwyższony.
- Niski poziom FSH, LH i estrogenów
- Objawy niewydolności przysadki/podwzgórza, np.: stres psychologiczny, utrata masy ciała, uprawianie sportu wyczynowego lub zaburzenia odżywiania3,22
- Wysoka wartość DHEAS
- Ponieważ DHEAS powstaje głównie w nadnerczach, może to wskazywać na guz nadnerczy wytwarzający androgeny.
- Niedoczynność tarczycy
- Ryzyko braku miesiączki jest niższe w przypadku subklinicznej niedoczynności tarczycy niż w przypadku jawnej niedoczynności tarczycy.
- Nie jest jasne, czy subkliniczna niedoczynność tarczycy ma znaczący wpływ na miesiączkowanie i płodność.
- Nieprawidłowy poziom hormonów tarczycy może wpływać na poziom prolaktyny23-24.
- Nadczynność tarczycy
- Ciężka nadczynność tarczycy prowadzi do braku miesiączki częściej niż łagodna nadczynność lub niedoczynność tarczycy25.
Badanie uzupełniające
- RM czaszki w przypadku podejrzenia choroby przysadki mózgowej
- Ewentualnie Densytometria do oceny gęstości kości w przypadku podejrzenia osteoporozy (więcej szczegółów tutaj).
Środki i zalecenia
Wskazania do skierowania do specjalisty
- W przypadku wszystkich pacjentek badania ginekologiczne i w razie potrzeby, równoległe leczenie
- Jeśli czynności diagnostyczne sugerują przyczyny somatyczne, np. w przypadku nieprawidłowych wartości prolaktyny w dwóch czasowych momentach pomiaru. W zależności od wyników: skierowanie do endokrynologa, neurologa lub okulisty.
- W przypadku zaburzeń odżywiania lub innych zaburzeń psychicznych: psychoterapia, psychosomatyka, psychiatria
Zalecenia
- W przypadku normo- lub hipogonadotropowej niewydolności jajników bez wskazań na choroby somatyczne lub podstawowe choroby psychiczne wymagające leczenia można w celu uspokojenia pacjentki wskazać na brak miesiączki przypuszczalnie związany ze stresem.
- Pacjentki z przedwczesną niewydolnością jajników należy poinformować o znaczeniu hormonalnej terapii zastępczej lub przyjmowania złożonego preparatu antykoncepcyjnego w zapobieganiu osteoporozy i miażdżycy, a także innym następstwom menopauzy. (IIb/B),
- Więcej szczegółów można znaleźć w artykule Klimakterium.
Czynnościowy brak miesiączki pochodzenia podwzgórzowego
- Leczenie: Przywrócenie odpowiedniej diety i unikanie stresu oraz nadmiernej aktywności fizycznej22.
- U niedożywionych pacjentek, takich jak te z anoreksją, miesiączka zwykle powraca przy odpowiednim odżywianiu26.
Zespół policystycznych jajników (PCOS)
- W przypadku pacjentek z nadwagą i z PCOS leczenie początkowo polega na zmniejszeniu masy ciała i zwiększeniu aktywności fizycznej27.
- Metformina może mieć pozytywny wpływ na metabolizm i owulację27-29. Jest wskazana przede wszystkim u kobiet bez otyłości z PCOS i insulinoopornością.
Gruczolak przysadki
- W przypadku wykrycia bezobjawowych mikrogruczolaków (mniejszych niż 10 mm) należy regularnie wykonywać pomiary prolaktyny i nowe zdjęcia RM w celu zauważenia ewentualnej progresji.
- Mikrogruczolaki rosną powoli i rzadko mają charakter złośliwy.
- Leczenie mikrogruczolaków można zasadniczo ograniczyć do objawów wywołanych przez hormony, takich jak niepłodność, mlekotok lub dyskomfort w piersi.
- Agoniści dopaminy mogą złagodzić objawy i przywrócić płodność. Bromokryptyna jest skuteczna, jednak kabergolina wydaje się być skuteczniejsza i lepiej tolerowana1,30.
- Makrogruczolaki mogą być leczone agonistami dopaminy lub, jeśli to konieczne, usuwane poprzez resekcję przezklinową lub kraniotomię.
Informacje dla pacjentów
Informacje dla pacjentów w Deximed
- Miesiączka, brak (wtórny brak miesiączki)
- Brak wystąpienia pierwszej miesiączki (pierwotny brak miesiączki)
Ilustracje
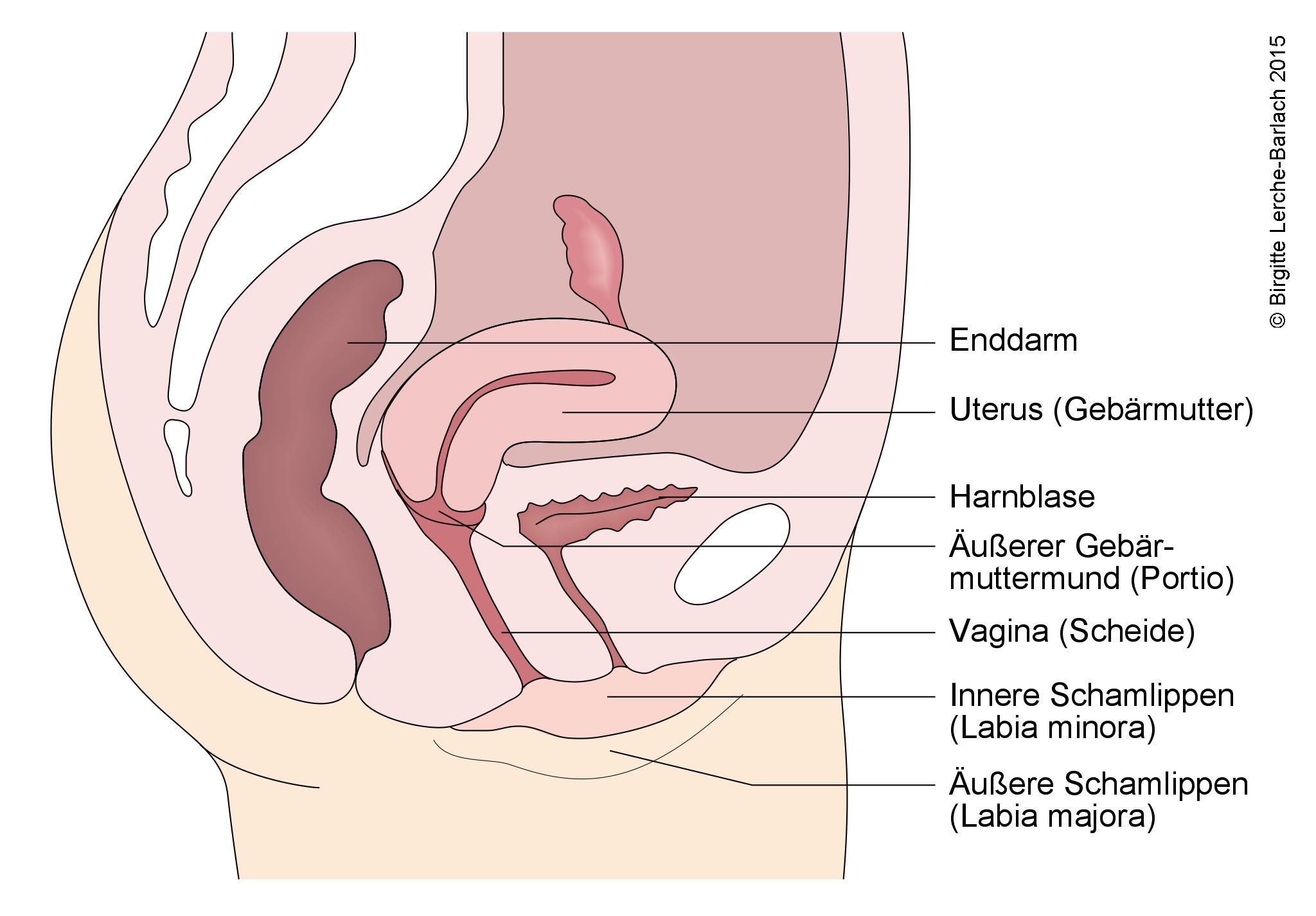
Widok boczny wewnętrznych narządów płciowych
Quellen
Literatur
- Solnik MJ. Assessment of secondary amenorrhoea. BMJ Best Practice. Last updated Dec 2018, last reviewed Feb 2020. bestpractice.bmj.com
- Master-Hunter T, Heiman DL. Amenorrhea: Evaluation and treatment. Am Fam Physician 2006; 73: 1374-82. PubMed
- Practice Committee of American Society for Reproductive Medicine. Current evaluation of amenorrhea. Fertil Steril. 2008;90(5 suppl):S219–S225. www.ncbi.nlm.nih.gov
- Klein DA, Poth MA. Amenorrhea: an approach to diagnosis and management. Am Fam Physician 2013; 87: 781-8. www.ncbi.nlm.nih.gov
- Pickett CA. Diagnosis and management of pituitary tumors: recent advances. Prim Care. 2003;30(4):765–789. www.ncbi.nlm.nih.gov
- Kiningham RB, Apgar BS, Schwenk TL. Evaluation of amenorrhea. Am Fam Physician 1996; 53: 1185-94. www.ncbi.nlm.nih.gov
- Miller KK, Parulekar MS, Schoenfeld E, Anderson E, Hubbard J, Klibanski A, et al. Decreased leptin levels in normal weight women with hypothalamic amenorrhea: the effects of body composition and nutritional intake. J Clin Endocrinol Metab 1998; 83: 2309-12. PubMed
- Welt CK, Chan JL, Bullen J, Murphy R, Smith P, DePaoli AM, et al. Recombinant human leptin in women with hypothalamic amenorrhea. N Engl J Med 2004; 351: 987-97. New England Journal of Medicine
- Drinkwater BL, Nilson K, Ott S, Chesnut CH III. Bone mineral density after resumption of menses in amenorrheic athletes. JAMA 1986; 256: 380-2. www.ncbi.nlm.nih.gov
- Robinson TL, Snow-Harter C, Taaffe DR, Gillis D, Shaw J, Marcus R. Gymnasts exhibit higher bone mass than runners despite similar prevalence of amenorrhea and oligomenorrhea. J Bone Miner Res 1995; 10: 26-35. PubMed
- Hergenroeder AC, Smith EO, Shypailo R, Jones LA, Klish WJ, Ellis K. Bone mineral changes in young women with hypothalamic amenorrhea treated with oral contraceptives, medroxyprogesterone, or placebo over 12 months. Am J Obstet Gynecol 1997; 176: 1017-25. PubMed
- Ackerman KE, Singhal V, Baskaran C, et al. Oestrogen replacement improves bone mineral density in oligo-amenorrhoeic athletes: A randomised clinical trial. Br J Sport Med 2018. PMID: 30301734 www.ncbi.nlm.nih.gov
- Martin N. Prolactinoma. BMJ Best Practise. Last udated Feb 2019. Last reviewed Feb 2020. bestpractice.bmj.com
- Kalantaridou S, Naka KK, Papanikolaou E, Kazakos N, Kravariti M, Calis KA, et al. Impaired endothelial function in young women with premature ovarian failure: normalization with hormone therapy. J Clin Endocrinol Metab 2004; 89: 3907-13. PubMed
- Kalantaridou S, Davis SR, Nelson LM. Premature ovarian failure. Endocrinol Metab Clin North Am 1998; 27: 989-1006. PubMed
- Anasti JN. Premature ovarian failure: an update. Fertil Steril 1998; 70: 1-15. PubMed
- Kim TJ, Anasti JN, Flack MR, Kimzey LM, Defensor RA, Nelson LM. Routine endocrine screening for patients with karyotypically normal spontaneous premature ovarian failure. Obstet Gynecol 1997; 89: 777-9. PubMed
- van der Schouw Y, van der Graaf Y, Steyerberg EW, Eijkemans JC, Banga JD. Age at menopause as a risk factor for cardiovascular mortality. Lancet 1996; 347: 714-8. PubMed
- Jacobsen BK, Nilssen S, Heuch I, Kvale G. Does age at natural menopause affect mortality from ischemic heart disease? J Clin Epidemiol 1997; 50: 475-9. PubMed
- Laufer MR, Floor AE, Parsons KE, Kuntz KM, Barbieri RL. Hormone testing in women with adult onset amenorrhea. Gynecol Obstet Invest 1995; 40: 200-3. PubMed
- Nelson LM. Clinical practice. Primary ovarian insufficiency. N Engl J Med. 2009;360(6):606–614. www.ncbi.nlm.nih.gov
- Gordon CM. Clinical practice. Functional hypothalamic amenorrhea. N Engl J Med. 2010;363(4):365–371. www.ncbi.nlm.nih.gov
- Kalro B. Impaired fertility caused by endocrine dysfunction in women. Endocrinol Metab Clin North Am 2003; 32: 573-92. PubMed
- Arojoki M, Jokimaa V, Juuti A, Koshinen P, Irajala K, Anttila L. Hypothyroidism among infertile women in Finland. Gynecol Endocrinol 2000; 14: 127-31. PubMed
- Kakuno Y, Amino N, Kanoh M, et al. Menstrual disturbances in various thyroid diseases. Endocr J. 2010;57(12):1017–1022. www.ncbi.nlm.nih.gov
- Falsetti L, Gambera A, Barbetti L, Specchia C. Long-term follow-up of functional hypothalamic amenorrhea and prognostic factors. J Clin Endocrinol Metab. 2002;87(2):500–505. www.ncbi.nlm.nih.gov
- American College of Obstetricians and Gynecologists. ACOG practice bulletin no. 108: polycystic ovary syndrome. Obstet Gynecol. 2009;114(4):936–949. www.ncbi.nlm.nih.gov
- Tang T, Lord JM, Norman RJ, Yasmin E, Balen AH. Insulin-sensitising drugs (metformin, rosiglitazone, pioglitazone, D-chiro-inositol) for women with polycystic ovary syndrome, oligo amenorrhoea and sub-fertility. Cochrane Database Syst Rev. 2010;(1):CD003053. Cochrane (DOI)
- Bridger T, MacDonald S, Baltzer F, Rodd C. Randomized placebo-controlled trial of metformin for adolescents with polycystic ovary syndrome. Arch Pediatr Adolesc Med. 2006;160(3):241–246. www.ncbi.nlm.nih.gov
- Webster J, Piscitelli G, Polli A, Ferrari CI, Ismail I, Scanlon MF, et al. A comparison of cabergoline and bromocriptine in the treatment of hyperprolactinemic amenorrhea. N Engl J Med 1994; 331: 904-9. New England Journal of Medicine
Autor*innen
- Thomas M. Heim, Dr. med., Wissenschaftsjournalist, Freiburg