Informacje ogólne
Definicja
- Szpiczak mnogi jest chorobą nowotworową charakteryzującą się niekontrolowaną proliferacją monoklonalnych komórek plazmatycznych.
- Komórki plazmatyczne to wyspecjalizowane limfocyty B, których każdy klon wytwarza konkretną immunoglobulinę.
- Przy niezakłóconym wzroście klony komórek plazmatycznych mogą wytwarzać duże ilości immunoglobulin., które można wykryć w proteinogramie z surowicy lub moczu. Prowadzą one do wysokiego stężenia białka M we frakcji gamma-globulin.
- Przewaga złośliwych komórek plazmatycznych w szpiku kostnym może prowadzić do wyparcia innych liniii komórkowych i powodować niedokrwistość, zwiększoną skłonność do infekcji (granulocytopenia) i zwiększoną skłonność do krwawień (małopłytkowość).
- Rozpoznanie opiera się na wynikach badania szpiku kostnego, ewentualnie wynikach biopsji guzów pozaszpikowych oraz badaniu stężenia globuliny M w surowicy i moczu. Ponadto należy ocenić, w jakim stopniu choroba powoduje objawy i czy występują objawy zaburzeń narządów.
- Patrz Kryteria diagnostyczne.
Warianty i choroby powiązane 1
- MGUS – gammapatia monoklonalna o nieokreślonym znaczeniu
- wykrywalna, ale łagodna gammapatia monoklonalna lub proliferacja monoklonalnych komórek plazmatycznych w szpiku kostnym
- brak potwierdzenia uszkodzenia narządów końcowych.
- Może rozwinąć się szpiczak mnogi, guz plazmocytowy odosobniony (patrz poniżej) lub amyloidoza.
- Szpiczak mnogi prawie zawsze poprzedza MGUS.2
- Wariant związany z IgM może rozwinąć się w makroglobulinemię Waldenströma, w amyloidozę i rzadziej w szpiczaka mnogiego.
- Wariant z wolnym łańcuchem lekkim może rozwinąć się w szpiczaka mnogiego lub amyloidozę.
- "Tlący się" szpiczak mnogi (Smouldering Myeloma)
- wariant bezobjawowy bez wykrywalnego uszkodzenia narządów końcowych, ale ze zwiększoną liczbą klonalnych komórek plazmatycznych w szpiku kostnym i białkiem monoklonalnym w surowicy
- stadium pośrednie między MGUS a szpiczakiem mnogim
- u około 10% osób dotkniętych chorobą każdego roku dochodzi do jej progresji do pełnoobjawowego szpiczaka mnogiego.
- Guz plazmocytowy odosobniony
- W przeszłości termin plazmocytoma był używany jako synonim szpiczaka mnogiego. Obecnie tylko pojedynczy złośliwy guz komórek plazmatycznych nazywa się plazmocytomą.
- Rozróżnia się pojedyncze guzy kości – ze zmianami osteolitycznymi i złamaniami kości – oraz guzy plazmocytowe pozaszpikowe.
- Rozwój w szpiczaka mnogiego w miarę postępu choroby.
- Białaczka plazmocytowa
- silny wzrost liczby komórek plazmatycznych we krwi obwodowej
- pozaszpikowy wariant szpiczaka mnogiego.
- Szpiczak niewydzielający
- Nie stwierdza się obecnosci białka monoklonalnego w immunofiksacji surowicy i moczu
- U większości występuje zwiększone stężenie monoklonalnych FLC i lub nieprawidłowy stosounek FLC κ/λ
- Zespół POEMS, który charakteryzuje się następująco:
- P = Polineuropatia
- O = Organomegalia
- E = Endokrynopatie
- M = gammapatia Monoklonalna
- S = zmiany Skórne
- Ogólnoustrojowa amyloidoza AL
- Czasami może przekształcić się w szpiczaka mnogiego.
Częstość występowania
- Trzeci najczęstszy nowotwór układu krwiotwórczego.
- Około 1% wszystkich nowotworów.
- Zapadalność
- mężczyźni: około 5/100 000
- kobiety: około 4/100 000.
- Wiek
- Średni wiek wystąpienia choroby wynosi około 70 lat.
- Częstość występowania choroby znacznie wzrasta od około 50. roku życia.
- Początek choroby przed 35. rokiem życia jest rzadkością.
Etiologia i patogeneza
- Przyczyny nie są znane.
- Jest prawdopodobne, że wady genetyczne powstające w dojrzałych komórkach plazmatycznych prowadzą do rozwoju komórek złośliwych.
- Wady genetyczne powstają w komórkach plazmatycznych i nie są dziedziczone.
- W miarę postępu choroby dochodzi do kaskady nieprawidłowości genetycznych.
- W około połowie przypadków występuje translokacja 14q lub hiperdiploidia.
- W przebiegu progresji szpiku kostnego od gammapatii monoklonalnej do szpiczaka mnogiego obserwuje się następujące mutacje: 3
- mutacje RAS
- nadekspresja Myc
- hipometylacja DNA
-
delecje chromosomu 13.
- W kontekście progresji pozaszpikowej można zaobserwować wzrost:
- mutacji NF-kB
- translokacji Myc
- utratę i insercję 1p.
- Szczególnie niekorzystne pod względem rokowania:
- utrata 17p
- translokacje (14;16), (14;20) i (4;14).
- Następujące czynniki mogą przyczyniać się do zwiększonego ryzyka szpiczaka:
- promieniowanie jonizujące
- pestycydy
- benzen
- otyłość
- przewlekłe infekcje.
Patologie
- Nadmierna proliferacja komórek plazmatycznych w szpiku kostnym.
- Prowadzi do niedokrwistości a później do ogólnej niewydolności szpiku kostnego.
- Zniszczenie kości, które wywołuje:
- ból kości
- osteoporozę
- osteolizę
- patologiczne złamania
- ewentualnie hiperkaliemię.
- Niewydolność nerek, która jest spowodowana:
- odkładaniem się wolnych łańcuchów lekkich immunoglobulin (białka Bence’a-Jonesa) w miąższu nerek
- złogami amyloidu
- hiperkalcemią.
ICD-10
- C90 Szpiczak mnogi i nowotwory złośliwe z komórek plazmatycznych
- C90.0 Szpiczak mnogi
- choroba Kahlera
- guz rdzenia
- szpiczakowatość
- szpiczak plazmocytowy
- C90.1 Białaczka plazmatycznokomórkowa
- C90.2 Pozaszpikowa postać szpiczaka
- C90.3 Guz plazmocytowy odosobniony
- miejscowy złośliwy nowotwór z komórek plazmatycznych nieokreślony
- szpiczak nieokreślony
- pojedynczy guz
- C90.0 Szpiczak mnogi
- M82.0 Osteoporoza w przebiegu szpiczaka mnogiego
Diagnostyka
Kryteria diagnostyczne
Szpiczak mnogi (kryteria SLiM-CRAB wg IMWG)
- Na podstawie nowych kryteriów diagnostycznych (kryteria SLiM) przedstawione przez International Myeloma Working Group (IMWG) w 2014 r. zakłada się rozpoznanie szpiczaka mnogiego, nawet jeśli nie doszło jeszcze do uszkodzenia narządów końcowych (kryteria CRAB), ale niektóre biomarkery wskazują na szpiczaka złośliwego3.
- Kryteria, rozpoznania szpiczaka mnogiego, są zatem następujące:
- ≥10% klonalnych komórek plazmatycznych w szpiku kostnym LUB potwierdzony biopsją guz plazmocytowy kostny lub pozaszpikowy ORAZ co najmniej jeden z poniższych objawów:
- jeden z biomarkerów choroby nowotworowej (kryteria SLiM):
- S = sixty percent (sześćdziesiąt procent): ≥60% klonalnych komórek plazmatycznych w szpiku kostnym
- Li = light chain ratio (współczynnik łańcucha lekkiego): stosunek stężenia klonalnych do nieklonalnych
wolnych łańcuchów lekkich w surowicy ≥100, przy czym stężenie łańcucha klonalnego w surowicy wynosi co najmniej 100 mg/l - M = MRT (rezonans magnetyczny): co najmniej jedna zmiana ogniskowa >5 mm w badaniu RM całego ciała
- LUB uszkodzenie narządów końcowych związane z proliferacyjną chorobą komórek plazmatycznych wykazane na podstawie jednego z kryteriów CRAB:
- C = calcium (wapń) (hiperkalcemia): stężenie wapnia w surowicy >11 mg/dl (>2,75 mmol) lub przekroczenie górnej granicy prawidłowego zakresu o więcej niż 1 mg/dl (0,25 mmol/l)
- R = renal insufficiency (niewydolność nerek): wskaźnik GFR (patrz klirens kreatyniny) <40 ml min lub stężenie w surowicy >2 mg/dl (>177 mcmol/l)
- A = anemia: Hb <10,0 g dl (<6,21 mmol/l) lub spadek poniżej dolnej granicy normy o więcej niż 2,0 g/dl (1,24 mmol/l)
- B = bones (kości) zmiany osteolityczne w badaniu rentgenowskim, TK lub PET-CT.
- jeden z biomarkerów choroby nowotworowej (kryteria SLiM):
Smouldering Myeloma („tlący się” szpiczak mnogi)
- Oba kryteria dotyczą:
- białka monoklonalnego (IgG lub IgA) w surowicy ≥30 g/l lub w moczu ≥500 mg/24 h lub klonalnych komórek plazmatycznych w szpiku kostnym 10–60%
- braku spełnienia kryteriów szpiczaka plazmocytowego lub amyloidozy łancuchów lekkich immunoglobulin
MGUS (gammapatia monoklonalna o nieokreślonym znaczeniu)
- MGUS nie-IgM
- wykrywalne białko monoklonalne inne niż IgM, stężenie poniżej 30 g/l
- wykrywalne klonalne plazmocyty w szpiku kostnym, odsetek poniżej 10%
- brak uszkodzeń narządów końcowych (CRAB, patrz wyżej) i brak amyloidozy, które można przypisać proliferacyjnej chorobie komórek plazmatycznych.
- MGUS IgM
- monoklonalne IgM wykrywalne w surowicy, stężenie poniżej 30 g/l
- naciek limfoplazmocytarny wykrywalny w szpiku kostnym, odsetek mniejszy niż 10%
- brak dowodów na:
- niedokrwistość
- objawy ogólnoustrojowe
- zespół nadmiernej lepkości krwi
- limfadenopatię
- hepatosplenomegalię
- inne uszkodzenia narządów końcowych, które można przypisać chorobie limfoproliferacyjnej.
- MGUS łańcuchów lekkich
- stosunek wolnych łańcuchów lekkich (FLC) kappa (κ) / lambda (λ) poza prawidłowym zakresem, tj. <0,26 lub>1,65
- zwiększone stężenie odpowiedniego FLC, tj. zwiększone stężenie κ-FLC u osób z FLC κ/λ >1,65 lub zwiększone stężenie λ-FLC u osób z FLC κ/λ <0,26
- brak ekspresji łańcuchów ciężkich immunoglobulin w immunofiksacji
- Brak uszkodzenia narządów końcowych (CRAB) i amyloidozy, które można przypisać proliferacyjnej chorobie komórek plazmatycznych.
- wykrywalne klonalne plazmocyty w szpiku kostnym, odsetek poniżej 10%
- białko monoklonalne w moczu <500 mg/24 h
Guz plazmocytowy odosobniony
- Pojedyncza zmiana w kości lub tkance miękkiej z biopsją wykazującą obecność klonalnych komórek plazmatycznych
- Prawidłowy szpik kostny bez klonalnych komórek plazmatycznych
- Warianty: guz plazmocytowy odosobniony z minimalnym zajęciem szpiku kostnego
- wykrywalne klonalne plazmocyty w szpiku kostnym, odsetek poniżej 10%
- Badanie rentgenowskie szkieletu, RM (lub TK) kręgosłupa i miednicy
- oprócz opisanej pojedynczej zmiany bez zmian
- brak uszkodzeń narządów końcowych zgodnie z kryteriami CRAB (patrz wyżej), które można przypisać chorobie profileracyjnej opartej na komórkach limfatyczno-plazmatycznych
Zespół POEMS
- Polineuropatia.
- Monoklonalna proliferacyjna choroba komórek plazmatycznych (prawie zawsze λ).
- Jedno z pozostałych trzech głównych kryteriów:
- sklerotyczne zmiany kostne
- choroba Castlemana (przerost węzłów chłonnych z rozrostem węzłów chłonnych)
- podwyższony VEGFA (czynnik wzrostu śródbłonka naczyniowego A).
- Jedno z sześciu kryteriów drugorzędnych:
- Organomegalia: splenomegalia lub hepatomegalia lub limfadenopatia.
- Wynaczynienie: obrzęk lub wysięk opłucnowy lub wodobrzusze.
- Endokrynopatia: nadnercza, tarczycy, przysadki mózgowej, gonad, przytarczyc lub trzustki (z uwagi na częste występowanie cukrzycy i chorób tarczycy - stwierdzenie chorób tylko tych narządów nie jest wystarczające do spełnienia kryterium).
- Zmiany skórne, takie jak przebarwienia, hipertrichoza, naczyniaki kłębuszkowe, akrocyjanoza, zaczerwienienie twarzy, białe paznokcie.
- Tarcza zastoinowa.
- Trombocytoza/czerwienica prawdziwa.
Ogólnoustrojowa amyloidoza AL
- Zespół ogólnoustrojowy spowodowany złogami amyloidu z zajęciem narzadów, np.:
- nerka
- wątroba
- serce
- przewód pokarmowy
- nerwy obwodowe
- Barwienie amyloidu czerwienią Kongo dodatnie w biopsji:
- tkanka tłuszczowa
- szpik kostny
- inne narządy
- Wykazanie, że amyloid jest związany z łańcuchem lekkim poprzez bezpośrednie badanie amyloidu:
- analiza proteomu oparta na spektrometrii mas lub
- mikroskopia immunoelektronowa
- Wykrywanie monoklonalnej proliferacyjnej choroby komórek plazmatycznych za pomocą:
- białka monoklonalnego w surowicy lub moczu
- stosunku FLC poza normalnym zakresem (patrz wyżej) lub
- klonalnych komórek plazmatycznych w szpiku kostnym.
Białaczka plazmocytowa1
- Komórki plazmatyczne ≥20% w morfologii WBC lub
- Klonalne komórki plazmatyczne ≥2 x 109/l we krwi.
Diagnostyka różnicowa
- Makroglobulinemia Waldenströma
- wykrycie chłoniaka limfoplazmocytowego w szpiku kostnym ze zwiększoną produkcją monoklonalnych IgM.
- Chłoniaki/białaczka.
- Choroba łańcuchów ciężkich
- rzadko, nadprodukcja immunoglobulin innych niż IgG/IgA/IgM.
- Infekcje.
- Choroby autoimmunologiczne.
- Choroby wątroby.
Plazmocytoza w szpiku kostnym
- Choroby wątroby.
- Przewlekłe infekcje.
- Przewlekłe stany zapalne.
Pojedyncze guzy kości
- Przerzuty do kości.
- Osteoporoza.
- Nadczynność przytarczyc.
- Amyloidoza.
- Fibrodysplazja kości.
Wywiad lekarski
- Osoby ze szpiczakiem mnogim mogą żyć bez objawów lub z niewielkimi objawami przez długi czas, zanim zostaną zdiagnozowane.
- Większość objawów jest spowodowana przez:
- niedokrwistość
- zmiany kostne
- infekcje
- hiperkaliemię
- niewydolność nerek
- zmniejszenie masy ciała
- neuropatię.
Kości
- Ból i złamania, często przy wyjątkowo małych urazach.
- Bardzo często ból w obszarze pleców i żeber, ale także kości długich i miednicy, ewentualnie czaszki.
- W wielu przypadkach objawem jest złamanie patologiczne.
- Ucisk na rdzeń przedłużony – powikłanie zagrażające życiu.
Niewydolność szpiku kostnego
- Niedokrwistość: zmęczenie (zmęczenie.), bladość, dusznica bolesna, duszność, zawroty głowy.
- Neutropenia lub niedobór przeciwciał: częste infekcje, często przedłużający się przebieg choroby i oporność na leczenie.
Niewydolność nerek
- Nudności, uczucie pragnienia, zmęczenie, świąd, obrzęk, spieniony mocz (białkomocz).
Gammapatia monoklonalna
- Zwykle bez objawów przy szpiczaku; jednak łańcuchy lekkie wydalane z moczem mogą prowadzić do niewydolności nerek.
- Przy makroglobulinemii Waldenströma (monoklonalne IgM) może rozwinąć się zespół nadmiernej lepkości krwi:
- skłonność do krwawień, np. krwawienie z błon śluzowych
- zawroty głowy
- nudności
- zaburzenia widzenia
- zaburzenia psychoorganiczne.
Amyloidoza
- W zależności od zajętego narządu możliwe są bardzo różne objawy.
Neuropatia
- Może wystąpić z powodu choroby lub sposobu leczenia (leki cytostatyczne).
- Neuropatia autonomiczna, np. z hipotonią ortostatyczną.
- Polineuropatia
- symetryczny, dystalnie zaakcentowany ból kończyn (głównie nóg), zaburzenia czucia
- w dalszym przebiegu ewentualnie niedowład, ataksja
- zapadalność przy szpiczaku mnogim 5–10%, przy MGUS 30–70%.
Badanie przedmiotowe
- Krwawienie i bladość skóry.
- Odwodnienie.
- Uszkodzenia nerwów obwodowych i korzeni nerwów rdzeniowych.
- Tkliwość kości.
- Ewentualnie obrzęki.
- Ewentualnie makroglosja w złogach amyloidu.
Badania uzupełniające w ramach podstawowej opieki zdrowotnej
Badania krwi
- Hb, hematokryt: niedokrwistość?
- OB>40 mm po 1 h (u 84%), często 3-cyfrowe
- CRP.
- Elektrolity
- Podwyższone: dehydrogenaza mleczanowa, ALT, ALP? (LDH-niedostępne w POZ)
- Wartości retencji nerkowej często podwyższone
- stężenie kreatyniny w tym obliczony eGFR (zgodnie ze wzorem CKD-EPI, patrz artykuł Niewydolność nerek)
- mocznik
- kwas moczowy.
- Białko całkowite i albumina w surowicy.
Diagnostyka specjalistyczna
- Proteinogram z określeniem białka M
- elektroforeza immunofiksacyjna w surowicy i moczu
- Pozwala wykryć 98% przypadków szpiczaka.
- Globulina M (składnik monoklonalny) może być widoczna jako wyraźne pasmo w zakresie gamma, ewentualnie w zakresie beta.
- immunoglobuliny (IgG, IgA, IgM) w surowicy, ilościowo
- wolne łańcuchy, typ kappa i wolne łańcuchy, typ lambda w surowicy, w tym obliczenie stosunku FLC κ/λ
- Osoby ze szpiczakiem niewydzielającym w 50% przypadków mają patologiczny test FLC.
- podwyższone stężenie łańcuchów lekkich typu kappa lub lambda.
- Znajdują się w surowicy 80% wszystkich pacjentów ze szpiczakiem i u 100%, jeśli występuje choroba łańcuchów lekkich.
- Dobowa zbiórka moczu w celu ilościowego oznaczenia wydalania białka i łańcuchów lekkich.
- Łańcuchy lekkie (białko Bence’a-Jonesa) można wykryć za pomocą elektroforezy moczu.
- Wymagane jest określenie ilościowe: większe immuoglobuliny M nie są wydalane wraz z moczem.
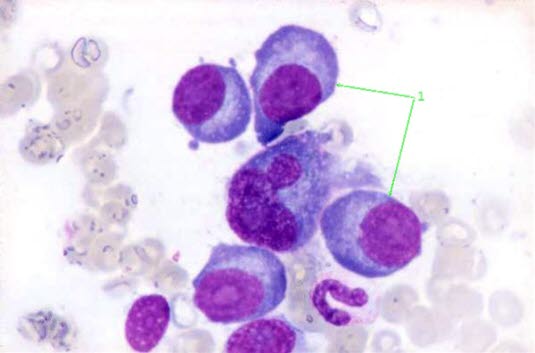 Rozmaz krwi przy szpiczaku mnogim
Rozmaz krwi przy szpiczaku mnogim
- Rozmaz krwi obwodowej
- może wykazać charakterystyczne tworzenie się czerwonych krwinek, które przypominają rulony monet.
- Komórki plazmatyczne są widoczne tylko w wyjątkowych przypadkach.
- Liczba neutrofilów i trombocytów jest początkowo w normie.
- Beta-2-mikroglobuliny we krwi: służy do określania stopnia zaawansowania i monitorowania aktywności choroby.
- Biopsja szpiku kostnego
- niezbędna do potwierdzenia diagnozy
- do badań cytologicznych
- w razie potrzeby pozyskiwanie materiału do analiz genetycznych, np.:
- cytogenetyka
- konwencjonalna analiza chromosomów
- fluorescencja hybrydyzacja in situ (FISH)
- biopsja guza w przypadku podejrzenia guza plazmocytowego odosobnionego.
- Podstawowa diagnostyka obrazowa
- niskodawkowa tomografia komputerowa całego ciała bez kontrastu
- do diagnozowania osteolizy, osteopenii i oceny stabilności
- wyższa czułość niż w przypadku popularnego wcześniej schematu paryskiego.
- Uzupełniające techniki obrazowania
- RM
- zwłaszcza jeśli podejrzewa się objawy pozaszpikowe
- obowiązkowe w przypadku objawów neurologicznych z podejrzeniem ucisku na rdzeń kręgowy.
- U osób z bezobjawowym szpiczakiem wykrycie zmian w szpiku kostnym w badaniu RM zwiększa prawdopodobieństwo przemiany w szpiczaka objawowego.
- FDG-PET
- czuła metoda wykrycia objawów pozaszpikowych.
- Dostarcza wczesnych informacji na temat odpowiedzi na leczenie.
- echokardiografia
- regularnie u pacjentów ze szpiczakiem z podejrzeniem amyloidozy serca
- przed chemioterapią zawierającą antracyklinę
- przed leczeniem wysokimi dawkami
- RTG klatki piersiowej i ewentualnie czynność płuc
- przed rozpoczęciem leczenia bortezomibem.
- RM
Markery cytogenetyczne1
Grupy ryzyka cytogenetycznego w szpiczaku plazmocytowym wg MayoClinic (mSMART 3.0)
- Duże ryzyko
• t(4;14)
• t(14;16)
• t(14;20)
• Del 17p
• Mutacje TP53
• Amp 1q
• RISS-3
• wysoki indeks proliferacyjny – komórki plazmatyczne w fazie S
• niekorzystna sygnatura w met. GEP (badanie profilu ekspresji genów.)
• „double hit”: dowolne 2 anomalie genetyczne wysokiego ryzyka
• „triple hit”: dowolne 3 lub więcej anomalie genetyczne wysokiego ryzyka
- Standardowe ryzyko
- Wszystkie inne, w tym:
• Trisomie
• t(11;14)
• t(6;14)
- Wszystkie inne, w tym:
Wskazania do skierowania do specjalisty
- W przypadku podejrzenia choroby: skierowanie do hematologa/onkologa.
Leczenie
Cele leczenia
- Całkowita remisja..
- Leczenie paliatywne i przedłużające życie
Ogólne informacje o leczeniu
Wskazanie zgodnie z kryteriami SLiM-CRAB wg IMWG2
- Uzasadnienie
- U 55–94% osób spełniających jedno z kryteriów SLiM w ciągu dwóch lat dochodzi do progresji choroby w szpiczaka mnogiego według kryteriów CRAB, a u 70% do uszkodzenia narządów końcowych.
- Zgodnie z konsensusem ekspertów leczenie jest wskazane w tej grupie pacjentów. Należy zaakceptować fakt, że u około 20% osób z pozytywnymi kryteriami SLiM doszłoby do nadmiernego leczenia, ponieważ nawet bez leczenia nie rozwinąłby się u nich szpiczak.
- Ograniczenie leczenia
- skutki uboczne leczenia wysokodawkowego i autologicznego przeszczepu komórek macierzystych.
- Trudno jest określić górną granicę wieku. Decydującymi czynnikami są wiek biologiczny z dobrym zachowaniem funkcji narządów i brak istotnych chorób współistniejących
- w przypadku starszych pacjentów, badanie geriatryczne, jeśli to konieczne.
- Wyjątek:
- Jeśli diagnoza „szpiczaka mnogiego” zostanie postawiona wyłącznie na podstawie stosunku łańcuchów lekkich >1 LUB wyłącznie na podstawie więcej niż jednej zmiany ogniskowej w badaniu RM, przed rozpoczęciem leczenia można poczekać na badanie kontrolne w celu oceny dynamiki choroby.
- w indywidualnych przypadkach objawy związane z nowotworem, które nie są uwzględnione w kryteriach SLiM-CRAB, również uzasadniają leczenie.
Leki stosowane przy ogólnoustrojowym leczeniu szpiczaka
- Cytostatyki
- Czynnik stymulujący tworzenie kolonii granulocytów (GCS-F)
- Glikokortykosteroidy
- Immunomodulatory / inhibitory angiogenezy
- talidomid
- lenalidomid
- pomalidomid
- Inhibitory proteaz
- Przeciwciała
- Inhibitor deacetylazy histonowej
Autologiczny przeszczep komórek macierzystych (HMAS)
- Zwiększa odsetek odpowiedzi i czas przeżycia w połączeniu z chemioterapią wysokodawkową.
Radioterapia
- Stosowana w przypadku guza plazmocytowego odosobnionego i jako część leczenia wspomagającego w przypadku miejscowych, bolesnych lub zagrażających złamaniom objawów, które postępują pod wpływem chemioterapii.
Zalecenia dla pacjentów
- Unikanie sytuacji stwarzających ryzyko infekcji.
Leczenie farmakologiczne
Leczenie pierwszej linii, jeśli można leczyć wysokimi dawkami
- Dla osób poniżej 65. roku życia i w zależności od sprawności poznawczej i fizycznej do ok. 75. roku życia można zaproponować chemioterapię wysokodawkową z autologicznym przeszczepem komórek macierzystych, jeśli nie ma przeciwwskazań.
- w przypadku osób w wieku powyżej 70 lat autologiczny przeszczep komórek macierzystych tylko w kontekście badań (w tym badań rejestrowych).
- Leczenie składa się z trzech etapów:
- Leczenie indukcyjne
- 3–6 cykli bortezomibu i deksametazonu, zwykle w skojarzeniu z lenalidomidem, cyklofosfamidem lub talidomidem
- Pobranie autologicznych komórek macierzystych
- 2–8 tygodni po leczeniu indukcyjnym
- następnie leczenie wysokimi dawkami melfalanu
- przeszczep autologicznych komórek macierzystych.
- Leczenie indukcyjne
- Leczenie wspomagające, np.:
- leczenie niedokrwistości
- odpowiednie leczenie bólu
- profilaktyka zakażeń oportunistycznych.
- Śmiertelność
- Śmiertelność związana z leczeniem wynosi mniej niż 3%.
- mediana przeżycia wynosi 6,9 roku dla pacjentów z beta-2-mikroglobuliną 2,3 mg/l lub niższą (43% wszystkich pacjentów ze szpiczakiem).
Leczenie pierwszej linii, jeśli nie można leczyć wysokimi dawkami
- Pacjenci, którzy nie kwalifikują się do leczenia wysokodawkowego z autologicznym przeszczepem komórek macierzystych, otrzymują leczenie skojarzone, np.:
Leczenie nawrotów
- Leczenie nawrotowego lub opornego na leczenie szpiczaka mnogiego zależy od następujących kwestii:
- wiek danej osoby
- choroby współistniejące
- wcześniejsze leczenie.
- Jeśli stężenie paraproteiny rośnie powoli, można poczekać.
- W przypadku nowych uszkodzeń narządów związanych ze szpiczakiem lub szybkiego wzrostu stężenia paraprotein wskazane jest leczenie nawrotów.
- U pacjentów z nawrotem choroby w dobrym stanie ogólnym bez istotnych chorób współistniejących można wprowadzić leczenie wysokimi dawkami melfalanu i zastosować autologiczny przeszczep komórek macierzystych.
- Inhibitory proteasomów, substancje immunomodulujące i klasyczne leki cytostatyczne odgrywają istotną rolę przy leczeniu nawrotów.
Inne opcje leczenia
Allogeniczny przeszczep komórek macierzystych
- Jest jedyną skuteczną metodą leczenia szpiczaka mnogiego.
- Udało się wykazać efekt przeszczep przeciwko szpiczakowi dzięki przeszczepionym komórkom immunokompetentnym.
- Efekt ten można dodatkowo wzmocnić poprzez późniejsze podanie limfocytów od dawcy.
- U pacjentów z bardzo wysokim ryzykiem (np. delecja 17p, choroba pozaszpikowa) korzystne jest łączone przeszczepienie autologicznych/allogenicznych komórek macierzystych..
Radioterapia
- Szpiczak mnogi jest wrażliwy na promieniowanie.
- Wskazanie do miejscowej radioterapii na dużym obszarze powinno odbywać się przed aferezą komórek macierzystych, ponieważ radioterapia może utrudniać pobieranie komórek macierzystych szczególnie w obszarze miednicy.
- Wskazaniami do radioterapii są:
- osteoliza z ryzykiem złamań
- leczone chirurgicznie złamania patologiczne
- pierwotny chirurgicznie leczony zespół paraplegii
- pozaszpikowe guzy plazmocytowe
- ból układu kostnego i niepowodzenie wszystkich innych możliwych metod leczenia bólu.
- W leczeniu bólu zwykle wystarcza dawka 10–20 Gy.
Bisfosfoniany4
- Regularne podawanie bisfosfonianów równolegle z leczeniem ogólnoustrojowym szpiczaka u wszystkich pacjentów z objawowym szpiczakiem
- opóźnia dalsze zdarzenia związane z układem kostnym
- łagodzi ból
- redukuje hiperkalcemię.
- Substancje czynne
- Zapobieganie martwicy kości żuchwy związanej z bisfosfonianami
- Przed rozpoczęciem leczenia należy dokładnie zbadać stan uzębienia.
- przekazać instrukcje dotyczące optymalnej higieny zębów i jamy ustnej
- Podczas leczenia bisfosfonianami należy w miarę możliwości unikać zabiegów inwazyjnych, takich jak ekstrakcje zębów.
- kontrola stomatologiczna przynajmniej raz w roku
- Jeśli interwencje stomatologiczne staną się konieczne, należy je przeprowadzić w taki sposób, aby w jak największym stopniu zachować zęby.
- Jeśli nie można uniknąć inwazyjnych zabiegów, takich jak ekstrakcja zęba, leczenie bisfosfonianami należy przerwać wcześniej i wznowić dopiero po zakończeniu gojenia się rany.
- Zalecany czas trwania leczenia: dwa lata
- W przypadku uzyskania bardzo dobrej częściowej remisji lub pełnej remisji leczenie można zakończyć już po roku.
- Jeśli odpowiedź jest słabsza, leczenie należy kontynuować.
- Obecnie nie można jednak ocenić, czy i – jeśli tak – w jakich okolicznościach leczenie trwające dłużej niż dwa lata jest przydatne.
- Nieograniczone podawanie nie powinno mieć miejsca.
Leczenie powikłań
- Sepsa lub zapalenie płuc
- antybiotykoterapia podawana pozajelitowo, o szerokim spektrum działania.
- Niewydolność nerek
- hemofiltracja lub dializa.
- Niewydolność szpiku kostnego
- Należy rozważyć zastosowanie erytropoetyny.
- Zespół nadmiernej lepkości krwi
- Plazmafereza?
- kontrowersyjna przy ostrej niewydolności nerek
- Osoby dializowane nie odnoszą korzyści.
- Więcej informacji patrz Makroglobulinemia Waldenströma.
- Plazmafereza?
- Hiperkaliemia
- nawodnienie
- bisfosfoniany
- przy ostrej niewydolności nerek początkowo tylko niskie dawki
- leki steroidowe.
- Ucisk na kręgosłup
- chirurgiczne odbarczenie i ewentualnie radioterapia.
- Patologiczne złamania
- leczenie bólu (nie podawać NLPZ ze względu na toksyczność dla nerek!)
- ewentualnie stabilizacja chirurgiczna
- bisfosfoniany.
- Złamanie lub niestabilność trzonu kręgu
- należy rozważyć wertebroplastykę lub kyfoplastykę.
- Infekcje
- Ryzyko ciężkich infekcji jest wysokie, a wczesne leczenie ma kluczowe znaczenie.
- W niektórych sytuacjach zaleca się profilaktyczne podawanie antybiotyków.
- Zapobieganie poprzez sczepienia przeciw grypie, pneumokokom, COVID-19, H. influenzae, półpaścowi1
- Zalecane są wyłącznie szczepionki inaktywowane.
- Zdarzenia zakrzepowo-zatorowe
- Pacjenci ze szpiczakiem mnogim otrzymujący immunomodulatory z chemioterapią lub deksametazonem powinni otrzymywać profilaktycznie heparynę drobnocząsteczkową lub aspirynę w małej dawce.5
Opieka paliatywna
- Ból.
- Nudności i wymioty.
- Zaparcia.
- Złośliwa niedrożność przewodu pokarmowego.
- Suchość błony śluzowej jamy ustnej.
- Kacheksja i odwodnienie.
- Duszność.
- Depresja.
- Lęk.
- Zaburzenia psychoorganiczne.
Obserwacja
- Ryzyko złamań patologicznych
- Ból układu kostnego jest sygnałem ostrzegawczym przed patologicznymi złamaniami.
- Ból pleców może wskazywać na złamania kręgów.
- Może prowadzić do ucisku na korzeń lub rdzeń kręgowy z deficytami neurologicznymi.
- Badania rentgenowskie układu kostnego
- wykrywanie osteolizy i złamań
- ocena stabilności kości
- należy zachować ostrożność podczas zmiany pozycji lub transportu pacjentów z bólem kości i wysokim ryzykiem złamań.
- Ryzyko infekcji
- Gorączka i dreszcze mogą być objawami rozpoczynającej się sepsy.
- ścisłe środki kontroli zakażeń w przypadku wysokiego ryzyka zakażenia
- Silne dreszcze mogą być oznaką bakteriemii: wykonać 2 x posiew krwi.
- Niedobór przeciwciał
- Pacjenci z wtórnym niedoborem odporności i klinicznie istotną podatnością na zakażenia powinni otrzymać dożylnie substytucję immunoglobulin .
- Ryzyko wystąpienia zespołu nadmiernej lepkości krwi
- Zespół nadmiernej lepkości krwi może powodować krwawienie z błon śluzowych, zawroty głowy, nudności, zaburzenia widzenia i zaburzenia psychoorganiczne.
- Niedokrwistość
- Hipoksemia?
- Tachykardia?
- Hipotonia ortostatyczna?
- Zmęczenie?
- Objawy niedokrwienia w EKG?
- Gazometria: Kwasica metaboliczna?
- transfuzja krwi w przypadku ciężkiej niedokrwistości
- Nie jest jasne, w jaki sposób transfuzje wpływają na i tak już znacznie obniżoną odporność pacjentów z hematologicznymi nowotworami złośliwymi lub poddawanych intensywnej chemioterapii. Należy zachować ostrożność również ze względu na ryzyko przeniesienia zakażenia, reakcji potransfuzyjnych i przeładowania żelazem.
- Konieczność transfuzji zależy nie tylko od stężenia hemoglobiny, ale także od czynników ryzyka i możliwych oznak zdekompensowanej hipoksji anemicznej (patrz wyżej).
- Wydaje się, że u pacjentów bez czynników ryzyka lub dekompensacji w wyniku niedotlenienia stężenie hemoglobiny <7 g/dL jest wystarczającym wskazaniem do transfuzji
- Hipoksemia?
- Ryzyko pogorszenia czynności nerek
- Regularna kontrola stężenia wapnia w surowicy, kreatyniny, kwasu moczowego, hemoglobiny, trombocytów, leukocytów.
- Odwodnienie?
- Powikłania i skutki uboczne leczenia.
Przebieg, powikłania i rokowanie
Przebieg
- Wraz z postępem choroby zwykle nasilają się
- bóle kostne
- nawracające infekcje.
- Pojedynczy guz rozwija się w szpiczaka mnogiego w ciągu 3–4 lat u około 50% wszystkich pacjentów.
Powikłania
- Przełom hiperkalcemiczny.
- Krwawienia.
- Żylna choroba zakrzepowo-zatorowa.
- Choroby zakaźne
- Populacyjne badanie kliniczno-kontrolne przeprowadzone w Szwecji wykazało 7-krotnie zwiększone ryzyko infekcji bakteryjnych i 10-krotnie zwiększone ryzyko infekcji wirusowych u pacjentów ze szpiczakiem w porównaniu do zdrowej populacji.6
- Ostra niewydolność nerek, często wywołana infekcjami dróg moczowych.
- Złamania.
- Ucisk na rdzeń kręgowy lub korzenie nerwowe spowodowany złamaniami kręgów lub wzrostem guza.
- Kacheksja.
- Neuropatia.
Rokowanie
- Międzynarodowy indeks prognostyczny (ISS)7 jest wykorzystywany do oceny zaawansowania w celach prognostycznych.
- Patrz tabela Zrewidowany międzynarodowy indeks prognostyczny dla szpiczaka mnogiego.
- Według badania przeprowadzonego na pacjentach z Niemiec i Stanów Zjednoczonych w latach 2002–2010 wskaźnik 5-letniej przeżywalności wynosi obecnie ponad 50%.8
- Zaawansowany wiek, upośledzona czynność nerek, hiperkalcemia, znaczna osteoliza i znacznie obniżone ogólne samopoczucie przyczyniają się do gorszego rokowania.
- Niektóre cechy cytogenetyczne (patrz rozdział Markery cytogenetyczne) mają znaczenie prognostyczne.
- Wiek <50 lat
- leczenie konwencjonalne, czas przeżycia około 4,5 roku
- leczenie wysokimi dawkami, czas przeżycia około 7,5 roku.
- Wiek >50 lat
- leczenie konwencjonalne, czas przeżycia >3 lat
- leczenie wysokimi dawkami >5,5 roku.
- Wskaźnik 10-letniego przeżycia dla osób poniżej 50. roku życia
- około 20% po leczeniu konwencjonalnym
- >40% po leczeniu wysokimi dawkami.
- Wskaźnik 10-letniego przeżycia dla osób powyżej 50. roku życia
- <10% po leczeniu konwencjonalnym
- <30% po leczeniu wysokimi dawkami
Dalsze leczenie w ramach podstawowej opieki zdrowotnej
Podczas leczenia ogólnoustrojowego
- W niektórych przypadkach lekarze podstawowej opieki zdrowotnej przejmują niektóre zadania między cyklami.
Monitorowanie infekcji
- Gorączka neutropeniczna
- Gorączka powyżej 38°C i liczba leukocytów <1,0 x 109/l we krwi obwodowej lub neutrofili <0,5 x 109/l.
- Kierowanie pacjentów do szpitala i leczenie tam sepsy!
- W fazie paliatywnej czasami właściwe może być leczenie takich infekcji antybiotykami podawanymi doustnie w domu.
- Często występuje neutropenia bez gorączki lub objawów infekcji.
- Możliwe dodatkowe działanie leków, np. cytostatyków lub immunomodulatorów.
- Temperaturę mierzyć w odbycie rano i wieczorem.
- Podwyższone stężenie CRP jest często spowodowane infekcją bakteryjną (a nie zwiększoną aktywnością komórek białaczkowych).
Cewnik do żył centralnych
- Często zakłada się pacjentom cewnik do żył centralnych (kaniula centralna, cewnik Hickmana) w celu pobrania próbek, transfuzji i leczenia farmakologicznego.
- Cewniki te powinien otwierać i zamykać wyłącznie przeszkolony personel pielęgniarski, który jest zaznajomiony z jego działaniem (ryzyko zatoru gazowego i infekcji).
- Ustanowienie dostępu obwodowego w celu pobrania próbek krwi i ewentualnego leczenia, gdy niemożliwe jest właściwe użycie kaniuli centralnej.
Inne kwestie
- Potrzeba transfuzji: ocena stopnia nasilenia objawów
- Jeśli stężenie hemoglobiny wynosi <8 g dl (<5 mmol l) lub stężenie trombocytów wynosi <10 000/mcl, należy rozwazyć potrzebę transfuzji
- Więcej informacji można znaleźć w rozdziale Transfuzja krwi w przypadku ciężkiej niedokrwistości oraz w artykule Małopłytkowość
- Leczenie przeciwkrzepliwe5
- Małopłytkowość w wyniku leczenia lub choroby prowadzi do zwiększonego ryzyka krwawienia.
- Jeśli stężenie trombocytów wynosi <50 000 /mcl, zespół hematoonkologiczny powinien rozważyć zmniejszenie dawki.
- Zmiana z doustnych leków przeciwkrzepliwych na heparynę drobnocząsteczkową (w zmniejszonej dawce) jest często wskazana, podobnie jak przerwanie leczenia w okresach znacznej małopłytkowości.
Po wypisaniu ze szpitala
- Szczepienia po indywidualnej konsultacji z kliniką, w której pacjent się leczy
- Po allogenicznym przeszczepie komórek macierzystych i wysokodawkowej chemioterapii z autologicznym przeszczepem komórek macierzystych może być wskazana ponowna podstawowa immunizacja.
- Zmęczenie, przewlekłe zmęczenie
- subiektywne uczucie zmęczenia i ograniczonej wydolności funkcjonalnej; brak poprawy nawet po odpoczynku i śnie
- szczególnie często występuje u pacjentów po radioterapii lub leczeniu lekami cytostatycznymi
- opisywane przez wiele pacjentów chorujących na raka jako najbardziej uciążliwy dyskomfort związany z leczeniem
- postępowanie
- dokładne, zrozumiałe wyjaśnienie stanu
- zalecany jest lekki i indywidualny program treningowy.
Dalsze postępowanie
- Biopsje szpiku kostnego są przydatne w diagnostyce nawrotów i kontroli remisji.
- MGUS (gammapatia monoklonalna o nieokreślonym znaczeniu)
- Każdego roku u około 1–2% rozwija się szpiczak mnogi lub inna gammapatia złośliwa (makroglobulinemia Waldenströma, chłoniak złośliwy).9
- Dlatego zaleca się regularne kontrole.
- Po allogenicznym przeszczepie komórek macierzystych
- wykrywanie nawrotów
- Przewlekła choroba przeszczep przeciw gospodarzowi?
- Późne następstwa?
- Badania kontrolne co 2–3 miesiące, w tym:
- Wywiad lekarski i badanie przedmiotowe
- morfologia krwi z WBC
- panel wątrobowy i nerkowy
- elektrolity
- parametry krzepnięcia
- proteinogram z surowicy
- wolne łańcuchy lekkie w surowicy i w dobowej zbiórce moczu.
- W przypadku podejrzenia nawrotu
- Należy powtórzyć te same badania, które wskazywały na rozpoznania wstępne.
Informacje dla pacjentów
O czym należy poinformować pacjentów?
- Działania związane z neutropenią, małopłytkowością i innymi zmianami w morfologii krwi po cyklach leczenia
Ilustracje

Rozmaz krwi przy szpiczaku mnogim z tworzeniem się czerwonych krwinek, które przypominają rulony monet. 1 = komórki plazmatyczne.
Źródła
- Rajkumar SV. Multiple myeloma: 2022 update on diagnosis, risk stratification, and management. Am J Hematol. 2022 97(8):1086-1107. doi: 10.1002/ajh.26590. PMID: 35560063; PMCID: PMC9387011 PubMed
- Polska grupa szpiczakowa. Zalecenia Polskiej Grupy Szpiczakowej dotyczące rozpoznawania i leczenia szpiczaka plazmocytowego oraz innych dyskrazji plazmocytowych na rok 2022/2023 szpiczak.org
Piśmiennictwo
- Polska grupa szpiczakowa. Zalecenia Polskiej Grupy Szpiczakowej dotyczące rozpoznawania i leczenia szpiczaka plazmocytowego oraz innych dyskrazji plazmocytowych na rok 2022/2023 szpiczak.org (dostęp 03.05.2025)
- Rajkumar SV, Dimopoulos MA, Palumbo A, et al. International Myeloma Working Group updated criteria for the diagnosis of multiple myeloma. Lancet Oncol 2014; 15: e538-48. PMID: 25439696 PubMed
- Rajkumar SV. Multiple myeloma: 2022 update on diagnosis, risk stratification, and management. Am J Hematol. 2022 97(8):1086-1107. doi: 10.1002/ajh.26590. PMID: 35560063; PMCID: PMC9387011
- Mhaskar R, Kumar A, Miladinovic B, et al. Bisphosphonates in multiple myeloma: an updated network meta-analysis. Cochrane Database of Systematic Reviews 2017, Issue 12. Art. No.: CD003188. pubmed.ncbi.nlm.nih.gov
- Lyman GH, Bohlke K, Khorana AA, Kuderer NM, et al. Venous thromboembolism prophylaxis and treatment in patients with cancer: American Society of Clinical Oncology clinical practice guideline update 2014. J Clin Oncol 2015;33(6). pubmed.ncbi.nlm.nih.gov
- Blimark C, Holmberg E, Mellqvist U-H. A population-based study on 9253 multiple myeloma patients. Haematologica 2014. doi:10.3324/haematol.2014.107714 DOI
- Palumbo A, Avet-Loiseau H, Oliva S, et al. Revised International Staging System for Multiple Myeloma: A Report From International Myeloma Working Group. J Clin Oncol 2015; 33: 2863-9. PMID: 26240224 PubMed
- Pulte D, Jansen L, Castro FA, et al. Trends in survival of multiple myeloma patients in Germany and the United States in the first decade of the 21st century. J Hematol Oncol. 2016; 22: 28. PMID: 26123295 PubMed
- Knop S, Liebisch P, Hebart H, et al. Autologous Followed By Allogeneic Versus Tandem-Autologous Stem Cell Transplant in Newly Diagnosed FISH-del13q Myeloma. Blood 2014 124:43 www.bloodjournal.org
Autorzy
- Sławomir Chlabicz (redaktor)
- Thomas M. Heim (redaktor/recenzent)