Informacje ogólne1
Definicja
- Definicja przewlekłej choroby nerek (chronic kidney disease – CKD)2
- patologiczne zmiany w strukturze lub funkcji nerek
- czas trwania ponad 3 miesiące (zmiany trwałe)
- wpływ na stan zdrowia.
- Kryteria przewlekłej choroby nerek (jedno z poniższych przez ponad 3 miesiące)
- oznaki uszkodzenia nerki (1 lub więcej)
- albuminuria: ≥30 mg/24h lub stosunek albuminy do kreatyniny (ACR) ≥30 mg/g (≥3 mg/mmol)
- patologiczny osad moczu (krwinkomocz, wałeczki)
- zaburzenia elektrolitowe i inne zmiany patologiczne wynikające z tubulopatii (kwasica cewkowa, moczówka prosta)
- histologiczne uszkodzenie nerek
- wykrycie patologicznych zmian w nerkach badaniami obrazowymi (wielotorbielowatość, dysplazja, wodonercze)
- stan po przeszczepie nerki.
- oznaki upośledzenia funcji nerek
- zmniejszenie GFR (<60 ml/min./1,73 m2).
- oznaki uszkodzenia nerki (1 lub więcej)
Klasyfikacja i podział na stadia2
- Klasyfikacja KDIGO (Kidney Disease Improving Global Outcomes) oparta jest na 3 kryteriach (klasyfikacja CGA – Cause, Glomerular filtration rate, Albuminuria [Przyczyna, wskaźnik filtracji kłębuszkowej, albuminuria]):
- C = choroba podstawowa
- Leżąca u podłoża choroba ogólnoustrojowa lub zmiany patologiczno–anatomiczne nerki.
- G = wskaźnik filtracji kłębuszkowej (ml/min./1,73 m2); pięć stopni zaawansowania
- G1: ≥90
- G2: 60–89
- G3a: 45–59
- G3b: 30–44
- G4: 15–29
- G5: <15 (przewlekła niewydolność nerek)
- A = albuminuria; trzy kategorie
- A1: <30 mg/24h (ACR <30 mg/g lub <3 mg/mol)
- A2: 30–300 mg/24h (ACR 30–300 mg/g lub 3–30 mg/mmol)
- A3: >300 mg/24h (ACR >300 mg/g lub >30 mg/mmol).
- C = choroba podstawowa
- Pogorszenie czynności filtracyjnej nerek i albuminuria są niezależnymi oznakami ryzyka progresji i zachorowalności/śmiertelności sercowo–naczyniowej.3
- Zobacz tabela przewlekła choroba nerek, ryzyko progresji, ocena ryzyka.
O terminologii
- Do tej pory bardzo powszechne było określenie „przewlekła niewydolność nerek”, jednak obecnie uważa się, że bardziej właściwym jest określenie „przewlekła choroba nerek (CKD)".2
- Uwzględnia to fakt, że „niewydolność nerek” odnosi się jedynie do upośledzonej funkcji filtracyjnej.
- „CKD” obejmuje natomiast również zmiany morfologiczne oraz równie istotny prognostycznie białkomocz.4
Epidemiologia
- W gabinetach lekarzy rodzinnych częstość występowania CKD szacuje się na minimum 10%, dominują pacjenci geriatryczni z zaburzeniem funkcji nerek związanym z wiekiem, we wczesnych stadiach CKD.5
- Z wiekiem następuje fizjologiczny spadek funkcji filtracyjnej nerek, choć klasyfikacja CKD nie pozwala jeszcze na dostosowanie do wieku (u osób powyżej 65. roku życia śmiertelność wzrasta dopiero od GFR<45 ml/min./1,73 m2).6
-
Według raportu Global Burden of Disease w 2017 r. na całym świecie: 1,2 miliona osób zmarło z powodu CKD; globalny wskaźnik umieralności we wszystkich grupach wiekowych wzrósł o 41,5% od 1990 r.; odnotowano 697,5 miliona przypadków PChN we wszystkich stadiach, co daje globalną częstość występowania 9,1%.7
-
W Polsce CKD może występowac nawet u 5 mln osób.8
- Około 2,3% osób w wieku 18–79 lat ma GFR<60 ml/min./1,73 m.3-6,9
- Częstość występowania wzrasta z wiekiem.10
- Rzadko pojawia się u osób poniżej 50. roku życia, za to w grupie wiekowej 70–79 lat dotyczy około 1 na 8 osób.9
- Tylko 28% osób dotkniętych CKD jest świadomych choroby, a jedynie 2/3 z osób, które o niej wiedzą, jest leczonych.
- Zwłaszcza osoby starsze nie są świadome istnienia tej choroby.11
Etiologia i patogeneza
- W gabinetach lekarzy rodzinnych, u pacjentów z upośledzoną funkcją nerek (III. stopień CKD, GFR średnio 52 ml/min.) występowały następujące choroby towarzyszące:12
- nadciśnienie tętnicze (88%)
- przewlekłe dolegliwości bólowe (30%)
- choroba wieńcowa (23%)
- cukrzyca (17%).
- Inne, rzadsze możliwe choroby podstawowe:
- przewlekłe kłębuszkowe zapalenie nerek
- nefropatia śródmiąższowa(w tym polekowe uszkodzenie nerek)
- torbielowatość nerek
- choroby ogólnoustrojowe: amyloidoza, nefropatia toczniowa, zespół Goodpasture'a, gammapatie monoklonalne, zapalenia naczyń, odmiedniczkowe zapalenie nerek lub polekowe uszkodzenie nerekzespół antyfosfolipidowy, zespół hemolityczno–mocznicowy, zakrzepowa plamica małopłytkowa
- choroby genetyczne.
Czynniki predysponujące
- Następujące czynniki zwiększają ryzyko rozwoju przewlekłej choroby nerek13-14:
- starszy wiek
- otyłość
- palenie papierosów
- nadwaga
- choroba serca
- choroby nerek w wywiadzie rodzinnym
- czynniki nefrotoksyczne
- pochodzenie azjatyckie lub afrykańskie.
ICD–10
- N18 Przewlekła niewydolność nerek.
- N18.0 Schyłkowa niewydolność nerek.
- N18.8 Inna przewlekła niewydolność nerek.
- N18.9 Przewlekła niewydolność nerek, nieokreślona.
- N28.9 Zaburzenia nerki i moczowodu, nieokreślone.
- N29* Inne zaburzenia nerki i moczowodu w przebiegu chorób sklasyfikowanych gdzie indziej.
Diagnostyka
Kryteria diagnostyczne
- Stwierdzenie cech uszkodzenia nerek (co najmniej 1):
- albuminuria: ≥30 mg/24h lub stosunek albuminy do kreatyniny (ACR) ≥30 mg/g (≥3 mg/mmol)
- patologiczny osad moczu (krwinkomocz, wałeczki)
- zaburzenia elektrolitowe i inne zmiany patologiczne wynikające z tubulopatii (kwasica cewkowa, moczówka prosta)
- histologiczne uszkodzenie nerek
- wykrycie patologicznych zmian w nerkach badaniami obrazowymi (wielotorbielowatość, dysplazja, wodonercze)
- stan po przeszczepie nerki.
- Stwierdzenie upośledzenia funkcji nerek
- zmniejszenie GFR (<60 ml/min./1,73 m2).
- Co najmniej jedno z tych kryteriów musi być spełnione przez okres powyżej 3 miesięcy.
Wywiad
- We wczesnych stadiach CKD często przebiega bezobjawowo.
- Objawy nieswoiste, niekiedy obecne dopiero przy zaawansowanej chorobie nerek:
- zmęczenie, osłabienie
- bóle i zawroty głowy
- nudności, pogorszenie apetytu
- obrzęki
- duszność
- kołatanie serca
- świąd
- zespół niespokojnych nóg
- skurcze mięśni
- bóle kostno–stawowe
- bezsenność.
- Wcześniej stwierdzone schorzenia (również w odniesieniu do czynników ryzyka chorób sercowo–naczyniowych):
- cukrzyca
- nadciśnienie tętnicze
- dyslipidemia
- palenie papierosów
- choroba sercowo–naczyniowa
- leki: substancje nefrotoksyczne
- choroby nerek w rodzinie.
Badanie fizykalne
- Pomiary antropometryczne: wzrost/waga (BMI).
- Ciśnienie tętnicze/tętno (nadciśnienie, zaburzenia rytmu serca).
- Skóra i tkanka podskórna
- Serce
- szmer tarcia osierdziowego (zapalenie osierdzia)
- tachykardia, niemiarowość.
- Płuca
- zastój w krążeniu płucnym (zatrzymanie wody, ewentualnie niewydolność serca)
- tarcie opłucnej (zapalenie opłucnej).
- Brzuch
- zapach mocznicowy (fetor ex ore)
- ból przy palpacji
- w zaawansowanej CKD niedrożność porażenna.
- Układ nerwowy
- zaburzenia czucia (polineuropatia).
Badania w praktyce lekarza rodzinnego
EKG
- Cechy przerostu lewej komory, tachykardia, zaburzenia rytmu (patrz również EKG, lista kontrolna).
RTG klatki piersiowej
- Przy klinicznym podejrzeniu zastoju w płucach, wysięku opłucnowego.
Badania laboratoryjne
- Diagnostyka laboratoryjna ma kluczowe znaczenie w wykrywaniu i stratyfikacji ryzyka chorób nerek.
- Ocena funkcji nerek poprzez oszacowanie wskaźnika filtracji kłębuszkowej (eGFR).
- Ocena uszkodzenia nerek poprzez określenie stężenia albuminy w moczu lub wskażnika UACR (albumina/kreatynina)
- Badanie moczu w kierunku oznak strukturalnego uszkodzenia nerek.
- Badania krwi
- Morfologia.
- eGFR (ml/min./1,73 m2), kreatynina.
- Wartość eGFR powinna być zawsze podana w raporcie laboratoryjnym.2
- Oznaczenie eGFR według wzoru MDRD (Modification of Diet in Renal Disease, modyfikacja diety w chorobach nerek) lub CKD–EPI (CKD Epidemiology Collaboration) – preferowany ten ostatni.
- W przypadku starszych pacjentów (>70 lat) wzory te są mniej wiarygodne. Możliwe, że zwalidowane wzory są lepsze, zwłaszcza w tej grupie wiekowej (BIS 1 – indeks bispektralny 1).
- Kreatynina nie jest przydatna jako marker wczesnej dysfunkcji nerek, jej stężenie wzrasta dopiero wtedy, gdy ponad połowa nefronów jest uszkodzona.
- Na, K.
- Glukoza.
- Lipidogram (cholesterol, HDL, LDL, trójglicerydy).
- Począwszy od IV. stadium CKD należy regularnie oznaczać poziom Ca, fosforanów, witaminy D, parathormonu.
- Podstawowa diagnostyka moczu:
- Test paskowy.
- W razie potrzeby badanie mikroskopowe osadu moczu (jeśli test paskowy wykaże nieprawidłowości).
- Diagnostyka białkomoczu poprzez określenie stosunku albuminy do kreatyniny (ACR) w moczu.
- Test paskowy do badania moczu może jako pierwszy sygnalizować rozpoczynające się strukturalne uszkodzenie nerek poprzez stwierdzenie:
- hematurii (krwinkomoczu/krwiomoczu)
- białkomoczu: niskie wydalanie albuminy <100 mg/l nie jest wykrywane przez standardowe testy paskowe
- zakażenia układu moczowego.
- Badanie mikroskopowe
- Może wskazywać np. na kłębuszkowe zapalenia nerek (obecność wałeczków, wyługowane erytrocyty), zaburzenia metaboliczne lub patogenezę kamicy nerkowej.
- Diagnostyka białkomoczu
- Badanie dowolnej próbki moczu, preferowany mocz z 2. porannej mikcji.
- Przy rozpoznaniu CKD (GFR<60 ml/min.) należy oznaczyć stosunek albuminy do kreatyniny w moczu.
- ACR >30 mg/g (lub >30 mg/24h) wskazuje na uszkodzenie nerek.
Stratyfikacja ryzyka/wskazania do konsultacji nefrologicznej
- W celu oceny ryzyka progresji CKD i sercowo–naczyniowego u pacjentów z CKD zaleca się:
- oznaczenie eGFR
- ilościowe oznaczenie albuminurii (np. ACR w dowolnej próbce moczu).
- Ryzyko niewydolności nerek można obliczyć za pomocą równania Kidney Failure Risk Equation.15
- Wymagane do tego stężenie wodorowęglanów można również oznaczyć w surowicy (badanie niedostępne w POZ).
- Pacjenci z łagodnymi zaburzeniami czynności nerek i (lub) łagodną lub umiarkowaną albuminurią mogą być monitorowani i leczeni przez lekarza rodzinnego.
- W przypadkach bardziej zaawansowanego upośledzenia czynności nerek i/lub umiarkowanej albuminurii należy skierować na konsultację nefrologiczną.2,16
- Zalecenia dotyczące skierowania – patrz wytyczne KDIGO 2023.1
- Pacjenci kierowani dopiero w późnym stadium choroby, cechują się gorszym rokowaniem.
Kierowanie pacjentów z CKD do specjalistów
- Wskazania do konsultacji nefrologicznej:
- Wszyscy pacjenci z eGFR <30 ml/min.
- W przypadku albuminurii w stadium A1 i CKD w stadium ≥G4 lub A2 i CKD w stadium ≥G3b lub ≥A3.
- AKI (ostre uszkodzenie nerek).
- Oporne na leczenie nadciśnienie tętnicze pomimo stosowania ≥4 leków hipotensyjnych.
- Utrzymujące się nieprawidłowe stężenie potasu.
- Obecność wałeczków erytrocytarnych w badaniu moczu lub erytrocyty >20 w polu widzenia, bez ewidentnej przyczyny.
- Inna wrodzona choroba nerek.
- Nawracająca lub objawowa kamica moczowa.
- Te kryteria skierowania nie stanowią jednak ogólnego zalecenia. Dla wielu pacjentów w praktyce lekarza rodzinnego upośledzona czynność nerek nie jest problemem priorytetowym ze względu na inne choroby współistniejące lub stan kliniczny (np. krótki oczekiwany czas przeżycia) i skierowanie nie jest w tych przypadkach bezwzględnie wskazane.
Leczenie
Cele leczenia
- Zwolnienie progresji choroby oraz powikłań, w tym hospitalizacji.8
- Uniknięcie rozwoju schyłkowej niewydolności nerek/dializ.
- Poprawa jakości życia.
- Leczenie powikłań związanych z CKD oraz chorób współistniejących, mogących przyspieszać progresję choroby.
- Profilaktyka choroby sercowo–naczyniowej.
- U dzieci zapewnienie odpowiedniego rozwoju fizycznego i psychicznego.
Ogólne informacje o leczeniu
- Spowolnienie postępu CKD.
- Leczenie CKD obejmuje zestaw ogólnych interwencji oraz leczenie farmakologiczne.
- Działania mające na celu leczenie choroby podstawowej, opóźnienie progresji i zapobieganie powikłaniom sercowo–naczyniowym zwykle są prowadzone równolegle.
- W przypadku np. nadciśnieniowej choroby nerek, należy leczyć również podłoże schorzenia – nadciśnienie tętnicze.
- Dobra kontrola ciśnienia tętniczego jest na ogół jedną z podstawowych interwencji hamujących progresję przewlekłej choroby nerek.
- Terapia hipotensyjna zmniejsza również ryzyko powikłań sercowo–naczyniowych.
- Blokada układu RAS (układu renina–angiotensyna) np. inhibitorami ACE, nie tylko obniża ciśnienie tętnicze, ale także zmniejsza albuminurię.
- Jeżeli nie można uniknąć progresji do schyłkowej niewydolności nerek, należy odpowiednio wcześnie omówić z pacjentem leczenie nerkozastępcze i go odpowiednio przygotować.
Spowolnienie postępu chorób sercowo–naczyniowych/zapobieganie
Ogólne zalecenia/styl życia
- Odżywianie
- Na postęp CKD, podobnie jak na ryzyko wystąpienia chorób sercowo-naczyniowych, ma wpływ rodzaj diety.
- Niekorzystna jest dieta z przewagą białka zwierzęcego i niską zawartością błonnika.
- Należy zalecić dietę bogatą w błonnik oraz różnorodne odżywianie, oparte o niskoprzetworzone produkty z dużą zawartością produktów roślinnych.8
- U pacjentów z eGFR wynoszącym <30 ml/min./1,73 m2 (kategoria G4–G5) spożycie białka należy ograniczyć.2
- W stadium G3–5 CKD, u pacjentów niedializowanych i bez cukrzycy – dieta ubogobiałkowa 0,55–0,6 g/kg m.c./dobę.
- W stadium G2–5 CKD, u pacjentów niedializowanych ze współistniejącą cukrzycą – spożycie białka na poziomie 0,6–0,8 g/kg m.c./dobę.
- Od 4. stadium CKD wszystkim pacjentom należy zaproponować poradnictwo dietetyczne (np. w ramach opieki koordynowanej).
- Spożycie soli
- Wysokie spożycie soli kuchennej jest istotnym czynnikiem ryzyka progresji CKD.
- W przypadku współistniejącego nadciśnienia tętniczego należy ograniczyć spożycie sodu do <2,3 g na dobę.2
- Nawodnienie
- Przyjmowanie płynów powinno być kontrolowane indywidualnie, z uwzględnieniem choroby podstawowej i chorób współistniejących.
- W większości przypadków zaleca się przyjmowanie 1,5–2 l płynów na dobę. Jeśli nie występuje niewydolność serca, restrykcja płynowa nie jest konieczna.
- Hiperurykemia
- Brak dowodów dotyczących wpływu terapii obniżającej poziom kwasu moczowego na progresję CKD (zarówno u objawowych, jak i bezobjawowych pacjentów z hiperurykemią).2
- Zaprzestanie palenia papierosów
- Zaleca się zaprzestanie używania nikotyny.2
- Palenie tytoniu jest istotnym czynnikiem ryzyka progresji CKD.17-18
- U palaczy z niewydolnością nerek istnieje zwiększone ryzyko poważnych zdarzeń sercowo–naczyniowych.19
- Masa ciała
- BMI powinno wynosić między 20 a 25 kg/m2.20
- Aktywność fizyczna
- Regularna aktywność fizyczna zgodna z wydolnością wysiłkową układu krążenia (docelowo co najmniej 5 razy w tygodniu po 30 min akywności fizycznej o umiarkowanym nasileniu).2
Spowolnienie progresji poprzez hamowanie SGLT–2
- Inhibitor SGLT–2 dapagliflozyna, empagliflozyna oprócz działania hipoglikemizującego, wykazują właściwości nefroprotekcyjne.21
- Dapagliflozyna 10 mg na dobę, została zatwierdzona w 2021 roku do leczenia przewlekłej choroby nerek, a empagliflozyna nieco później, u pacjentów z cukrzycą i bez cukrzycy, mogą być stosowana jako dodatek do inhibitora ACE/antagonisty AT1 (sartanu).
- Zaleca się stosowanie agonisty receptora glukagonopodobnego peptydu 1 (GLP–1) u pacjentów z cukrzycą typu 2 i przewlekłą chorobą nerek, nieosiągających indywidualnych celów terapeutycznych w trakcie stosowania SGLT2.
- Finerenon (ns–MRA) 20 mg na dobę, u pacjentów z cukrzycą typu 2, albuminurią i eGFR >25 ml/min./1,73 m2.
Ryzyko sercowo–naczyniowe w przewlekłej niewydolności nerek
- Spadek GFR wiąże się ze zwiększonym ryzykiem sercowo–naczyniowym niezależnie od innych czynników ryzyka.22
- Pacjenci z CKD ze znacznie obniżonym GFR (stadium G3–G5) mają z definicji wysokie lub bardzo wysokie ryzyko sercowo–naczyniowe.22
- Duże ryzyko sercowo–naczyniowe
- eGFR 30–44 i wskaźnik albumina/kreatynina <30 mg/g lub
- eGFR 45–59 i wskaźnik albumina/kreatynina 30–300 mg/g lub
- eGFR ≥60 i wskaźnik albumina/kreatynina >300 mg/g.
- Bardzo duże ryzyko sercowo–naczyniowe
- eGFR <30 lub eGFR 30–44 i wskaźnik albumina/kreatynina >30 mg/g.
- Duże ryzyko sercowo–naczyniowe
- Jednakże zwalidowane narzędzia do szacowania ryzyka sercowo–naczyniowego nie uwzględniają niewydolności nerek przy jego obliczaniu.
Nadciśnienie tętnicze/blokada układu renina–angiotensyna
- Leczenie hipotensyjne należy rozpocząć, jeśli BP >140/90 mmHg.23
- U pacjentów ze współistniejącą cukrzycą i/lub albuminurią wytyczne zalecają jako pierwszorzędowe docelowe wartości skurczowego ciśnienia tętniczego 130–139 mmHg oraz <70-79 mmHg rozkurczowego.
- Nowe polskie wytyczne rekomedują:8
- u osób dorosłych utrzymywanie wartości ciśnienia skurczowego <120mmHg, jeśli jest dobrze tolerowane
- u osób starszych (z zespołem kruchości, ryzykiem upadków, ograniczoną oczekiwaną długością życia, hipotonią ortostatyczną) mniej intensywne obniżenia ciśnień.
- Priorytetem w obniżaniu ciśnienia tętniczego jest blokowanie układu renina–angiotensyna (RAS) za pomocą inhibitorów ACE lub blokerów receptora AT1 (sartanów), ponieważ mają również korzystne działanie nefroprotekcyjne.23-24
- Jako terapię początkową należy zastosować połączenie blokera RAS/antagonisty wapnia lub blokera RAS/diuretyku (w przypadku eGFR <30 ml/min./1,73 m2 preferowany jest diuretyk pętlowy).23
- Przy występowaniu albuminurii pacjenci normotensyjni powinni również być leczeni blokerem RAS (pacjenci z cukrzycą przy ACR ≥30 mg/g, pacjenci bez cukrzycy przy ACR ≥300 mg/g).2
- Na początku leczenia spadek eGFR o 10–20% jest częsty i nie powinien budzić niepokoju.20,23
- Monitorowanie eGFR i elektrolitów, zwykle stabilizacja po kilku tygodniach.23
Cukrzyca
- Cele leczenia chorych na cukrzycę z CKD i bez CKD nie różnią się, należy ustalić cele indywidualne. Docelowa wartość HbA1c, aby zapobiec lub opóźnić rozwój powikłań mikronaczyniowych, w tym nefropatii cukrzycowej, wynosi 6,5–7%, a u osób starszych/osób o skróconej przewidywanej długości życia, dopuszczalne są również wartości do 8,0 - 8,5%.2
- W przypadku istnienia zwiększonego ryzyka hipoglikemii, można za docelowe przyjąć wyższe wartości HbA1c.2
- Niektóre doustne leki przeciwcukrzycowe wymagają dostosowania dawki w zależności od eGFR lub są przeciwwskazane w przypadku dysfunkcji nerek wyższego stopnia.
- W celu właściwego stosowania doustnych leków przeciwcukrzycowych konieczna jest więc ocena aktualnej funkcji nerek i monitorowanie jej postępu w odstępach od 3 do 6 miesięcy.
- Metmorminę należy stosować przy CKD i cukrzycy typu 2 do wartości eGFR wynoszącej ≥30 ml/min./1,73 m2, jeśli HbA1c nie mieści się w indywidualnym zakresie docelowym; zredukować dawkę metforminy do 1000 mg/dobę jeśli
eGFR wynosi 30–44 ml/min/1,73 m2 . - W wyższym stadium niewydolności nerek (eGFR<30 ml/min./1,73 m2) można stosować leki z następujących grup:
- glinidy
- inhibitory DPP–4
- GLP–1–RA
- insulina.
- W przypadku braku osiągnięcia docelowych efektów terapeutycznych, można połączyć insulinę bazową z jedną z wyżej wymienionych substancji czynnych.
- U pacjentów z cukrzycą i mikroalbuminurią należy rozpocząć leczenie blokerem RAS nawet jeśli eGFR nie jest jeszcze zmniejszona.
- Rekomendowane jest zastosowanie niesteroidowego MRA (finerenon) u pacjentów dorosłych z cukrzycą typu 2 i eGFR >25ml/min/1.73m2, prawidłowym poziomem K i albuminurią (>30mg/g) pomimo zastosowania maksymalnych tolerowanych dawek ACEi ARB.8
Dyslipidemia
- Ze względu na niespójne dane dotyczące tego, czy terapia obniżająca poziom cholesterolu ma korzystny wpływ na progresję CKD, jest to przedmiotem dyskusji.
- Pacjenci z niewydolnością nerek są niedostatecznie reprezentowani w badaniach nad statynami.
- Szczególną grupę stanowią pacjenci z zaawansowaną niewydolnością nerek, dializowani/po przeszczepie nerki, tu korzyść z leczenia obniżającego stężenie lipidów jest niepewna.25-26
- W przypadku pacjentów poddawanych dializie: nie należy rozpoczynać leczenia obniżającego stężenie lipidów, ale jeśli już zostało rozpoczęte – kontynuować.
- W przypadku pacjentów po przeszczepie nerki: wskazane podawanie statyn.
- Należy uwzględnić stopień wydolności nerek w przypadku stosowania statyn i odpowiednio dostosować ich dawkę.
Leczenie kwasicy
- Kwasica metaboliczna spowodowana jest zmniejszonym wytwarzaniem amoniaku, a tym samym – zmniejszoną zdolnością wydalania kwasów, jak również zmniejszoną reabsorpcją/syntezą wodorowęglanów.
- Zwiększająca się częstość występowania kwasicy metabolicznej wraz z obniżeniem GFR.
- Występuje u 3–5% pacjentów w III. stadium, 17–19% pacjentów w IV. stadium i 23% chorych w V. stadium.
- Kwasica sprzyja postępowi niewydolności nerek, ma ona również niekorzystny wpływ na gospodarkę wapniowo–fosforanową, a także na czynność serca i układ oddechowy.
- Z dietetycznego punktu widzenia korzystne działanie ma dieta alkalizująca z dużą ilością owoców i warzyw.
- Pacjentom, u których stężenie wodorowęglanów w surowicy wynosi <22 mmol/l, należy podawać wodorowęglany doustnie, aby utrzymać ich poziom w prawidłowym zakresie.2
Leczenie innych chorób wtórnych do CKD
Niedokrwistość
- Niedokrwistość w CKD rozwija się zwykle od poziomu GFR<60 ml/min./1,73 m2 (stadium G3).
- Niedokrwistość jest głównie spowodowana spadkiem produkcji erytropoetyny wraz z postępującą utratą funkcji nerek.
- Niedokrwistość normocytarna, normochromiczna, retikulocyty zwykle nieznacznie podwyższone.
- Ponadto występuje niedostateczna dostępność wolnego żelaza (czynnościowy niedobór żelaza) oraz zmniejszone wchłanianie z przewodu pokarmowego.
- Jednakże normalizacja poziomu hemoglobiny poprzez intensywne leczenie erytropoetyną (EPO) lub środkami stymulującymi erytropoezę (erythropoiesis–stimulating agents – ESA) nie wykazała żadnych korzyści prognostycznych.27-29
- Docelowa wartość Hb 12 g/dl nie wiąże się też z istotną poprawą jakości życia.30
- Wobec bardziej restrykcyjnych wskazań do stosowania EPO/ESA, w ostatnich latach coraz częściej stosuje się wysokodawkową dożylną terapię żelazem.
- Zarys wytycznych KDIGO (Kidney Disease: Improving Global Outcomes) dotyczących rozpoznawania i leczenia niedokrwistości nerkopochodnej.31
- diagnostyka
- Rozpoznanie niedokrwistości przy stężeniu Hb<12 g/dl (<7,5 mmol/l) (kobiety) lub 13 g/dl (8 mmol/l) (mężczyźni).
- U pacjentów z niedokrwistością (niezależnie od stopnia upośledzenia czynności nerek) należy oznaczyć: morfologię krwi, retikulocyty, ferrytynę, wysycenie transferyny żelazem (TSAT), witaminę B12, kwas foliowy.
- terapia żelazem
- Rozważenie korzyści i ryzyka (np. reakcja anafilaktoidalna przy podaniu dożylnym).
- Próba leczenia dożylnego (u pacjentów niedializowanych również rozważyć podawanie doustne przez 1–3 miesiące), jeśli:
- dąży się do zwiększenia stężenia Hb (np. w celu poprawy tolerancji objawów)
- wysycenie transferyny (TSAT) ≤30%,
- stężenie ferrytyny ≤500 ng/ml (lub ≤50 mcg/l lub 105 pmol/l).
- terapia ESA
- Jeśli stężenie Hb≥10 g/dl (≥6,2 mmol/l), nie zaleca się terapii ESA.
- Przed rozpoczęciem terapii ESA należy najpierw wykluczyć inne odwracalne przyczyny niedokrwistości (np. niedobór żelaza, stan zapalny).
- Jeśli stężenie Hb≤10 g/dl (≤6,2 mmol/l), indywidualna decyzja opiera się na obrazie klinicznym, dynamice spadku Hb, odpowiedzi na leczenie żelazem, ryzyku związanym z leczeniem ESA.
- przetoczenie koncentratu krwinek czerwonych (KKCz).
- Należy unikać, jeśli to możliwe.
- Gdy terapia ESA jest nieskuteczna lub zbyt ryzykowna.
- diagnostyka
Osteodystrofia nerkowa/metabolizm wapniowo–fosforanowy
- Zmiany w metabolizmie gospodarki wapniowo–fosforanowej u pacjentów z CKD zaczynają się na wczesnym etapie choroby.
- Do zmian spowodowanych przez ten proces należy osteodystrofia nerkowa, jak również wapnienie naczyń (sercowo–naczyniowe).
- Coraz częściej preferuje się termin „zespół CKD–MBD” (chronic kidney disease – mineral and bone disorder – zaburzenia mineralne i kostne w przewlekłej chorobie nerek), aby uniknąć skupienia się wyłącznie na kościach oraz ująć wzajemne oddziaływanie choroby nerek, metabolizmu kostnego i zwapnienia naczyń.
- W miarę postępu choroby nerek dochodzi do zmniejszenia przemian witaminy D do jej aktywnych metabolitów, zmniejszenia wchłaniania wapnia, a mniej więcej od stadium G4 (GFR<30 ml/min./1,73 m2) – do wtórnej nadczynności przytarczyc.
- Konsekwencją jest zmniejszona mineralizacja kości i osteomalacja, występują bóle kostne, a w stadium G5 – dwukrotnie zwiększone ryzyko złamań.
- Rozwijająca się ostatecznie hiperfosfatemia w znacznym stopniu przyczynia się do rozwoju zwapnień naczyniowych.
- Wczesne rozpoznanie nieprawidłowości w badaniach laboratoryjnych jest ważne dla rozpoczęcia działań terapeutycznych.
- U pacjentów z CKD w stadium 3b i wyższym (eGFR<45ml/min./1,73 m2) należy zlecić oznaczenie wapnia, fosforanów, stężenie PTH i 25(OH)witaminy D3.32
- Ograniczenie fosforanów w diecie w przypadku hiperfosfatemii (doustna terapia wiążąca fosforany zatwierdzona tylko u pacjentów dializowanych).
- Kalcytriol i analogi witaminy D nie powinny być stosowane rutynowo u pacjentów w stadium G3–5 (bez dializ), natomiast są stosowane w stadiach G4 i G5 przy ciężkiej nadczynności przytarczyc.32
Inne zalecenia terapeutyczne
Szczepienia
- Wraz z narastającym upośledzeniem czynności nerek zwiększa się ryzyko wystąpienia chorób zakaźnych oraz ciężkich przebiegów tych chorób.
- Dlatego wszyscy pacjenci z CKD powinni regularnie sprawdzać stan swoich szczepień i je aktualizować.
- Dzieci: szczepienie zgodnie z Programem Szczepień Ochronnych.
- Dorośli:
- szczepienie przeciwko grypie co roku
- szczepienie przeciwko pneumokokom; błonicy, tężcowi i krztuścowi dawką przypominającą; przeciwko COVID-19 i inne wg aktualnych zaleceń.8
Leczenie bólu
- Leki z grupy NLPZ nie powinny być przewlekle stosowane w CKD o dowolnej etiologii.
- NLPZ mogą wywoływać ostrą niewydolność nerek oraz pogorszyć przebieg CKD i kontrolę nadciśnienia tętniczego.
- Sporadyczne stosowanie (np. raz w tygodniu) może być akceptowane w wyjątkowych przypadkach, gdy inne leki przeciwbólowe nie są wystarczająco skuteczne.
- Leczenie przeciwbólowe powinno być prowadzone przede wszystkim z wykorzystaniem:
- W razie potrzeby można zastosować opioidy; jeśli GFR wynosi <60 ml/min./1,73 m2, należy dostosować ich dawkę.
Badania radiologiczne w CKD
- Stosowanie radiologicznych środków kontrastowych może pogorszyć czynność nerek.
- Z drugiej strony nie należy unikać diagnostyki z ich zastosowaniem, jeśli jest wskazana u pacjentów z CKD.
- Ryzyko wystąpienia wywołanej przez radiologiczny środek kontrastowy RTG ostrej niewydolności nerek jest prawdopodobnie zwykle znacznie zawyżane.
- Zgodnie z ostatnimi zaleceniami, w przypadku cięższego upośledzenia funkcji nerek (stadium 4–5, tj. GFR <30 ml/min./1,73 m2), należy bardziej starannie rozważyć korzyści diagnostyczne wynikające z podania kontrastu RTG/RM i ewentualnego zmniejszenia zachorowalności i śmiertelności w porównaniu z potencjalnym ryzykiem.
- Zalecane działania w zakresie nefroprotekcji:2
- odpowiednie nawodnienie przed badaniem, w trakcie i po nim
- wstrzymanie przyjmowania leków potencjalnie nefrotoksycznych przed badaniem i po nim
- oznaczenie kreatyniny i eGFR 48–96 godzin po badaniu.
Schyłkowa niewydolność nerek/procedury nerkozastępcze/transplantacja
- W końcowym stadium CKD występują objawy i oznaki mocznicy (m.in. apatia, wymioty, zaburzenia świadomości, zapalenie błon surowiczych, zespół niespokojnych nóg), zaburzenia równowagi elektrolitowej i zatrzymanie wody.33
- Tempo postępu schyłkowej niewydolności nerek i przebiegu powikłań jest bardzo indywidualne.
- Począwszy od stadium G4 (GFR<30 ml/min./1,73 m2), należy informować pacjentów o rodzajach i wskazaniach do leczenia nerkozastępczego.
- Tutaj również wartością referencyjną jest eGFR, a nie stężenie kreatyniny.
- Czynnikiem decydującym o wskazaniu do dializoterapii jest przebieg kliniczny i objawy potwierdzające początki mocznicy.
- Leczenie nerkozastępcze może być prowadzone za pomocą hemodializy w ośrodku specjalistycznym lub w warunkach domowych w przypadku dializy otrzewnowej.
- Nie stwierdzono różnic prognostycznych pomiędzy tymi procedurami, wspólna decyzja o sposobie leczenia nerkozastępczego powinna być podejmowana po uwzględnieniu preferencji pacjenta.
- U pacjentów wymagających leczenia nerkozastępczego należy w każdym przypadku rozważyć możliwość transplantacji (postępowanie najbardziej korzystne rokowniczo); w tym przypadku należy również brać pod uwagę choroby współistniejące, przewidywany czas przeżycia.
Świąd mocznicowy
- Pacjenci ze schyłkową niewydolnością nerek, a zwłaszcza pacjenci dializowani, często zgłaszają występowanie świądu.
- Opcje terapeutyczne to:
- leczenie miejscowe (np. kapsaicyna)
- leczenie farmakologiczne (np. gabapentyna)
- leczenie promieniowaniem ultrafioletowym (UVB).
- Całkowite ustąpienie dolegliwości tylko po przeszczepie nerki.
Zespół niespokojnych nóg
- Zespół niespokojnych nóg występuje u 20–40% pacjentów wymagających dializ.
- Leczeniem z wyboru jest w wyżej wymienionych przypadkach przeszczep nerki, gdyż udana transplantacja powoduje ustąpienie objawów.
- Inne możliwości terapeutyczne można znaleźć w artykule zespół niespokojnych nóg.
Wskazania do leczenia nerkozastępczego
- Występowanie jednego lub więcej z następujących kryteriów:2
- objawy niewydolności nerek (mocznica, zapalenie błony surowiczej, zaburzenia równowagi kwasowo–zasadowej lub elektrolitów, świąd)
- brak kontroli równowagi płynowej i ciśnienia tętniczego
- postępujące pogorszenie stanu odżywienia
- zaburzenia poznawcze.
Wskazania do przeszczepu nerki
- Wyprzedzające przeszczepienie (pre–emptive transplant) nerki od żywego dawcy należy rozważyć, jeśli:
- GFR<20 ml/min./1,73 m2 oraz
- spodziewana schyłkowa niewydolność nerek w ciągu najbliższych 6–12 miesięcy.2
- W każdym przypadku należy w pierwszej kolejności rozważyć przeszczep od żywego, spokrewnionego dawcy.
Dostosowanie farmakoterapii w przewlekłej chorobie nerek
- Dostosowanie dawkowania leków u pacjentów z CKD jest częstym problemem zarówno w warunkach ambulatoryjnych, jak i szpitalnych.2
- Niedostosowane lub niewłaściwe dawkowania leków u pacjentów z CKD może powodować wzrost ryzyka toksyczności lub nieskuteczność leczenia.34
- Już od poziomu wartości GFR <60 ml/min./1,73 m2 (stadium G3) niektóre leki wymagają dostosowania dawkowania lub są przeciwwskazane.35
- Podstawą dostosowania dawki jest oznaczenie eGFR (wzór MDRD lub CKD–EPI).
- Oznaczenie samej kreatyniny w surowicy potencjalnie naraża pacjentów na ryzyko.
- W przypadku większości leków wybiera się mniejszą dawkę, ale są wyjątki:
- W przypadku antybiotyków nie należy zmniejszać dawki początkowej, aby móc osiągnąć odpowiednio wysoki poziom substancji czynnej, następnie dostosowanie dawek dopiero w trakcie dalszego leczenia.
- W przypadku diuretyków pętlowych należy zwiększać dawkę wraz ze wzrostem zaawansowania niewydolności nerek.
Leki hipotensyjne/leki kardiologiczne
- Blokery układu RAS (inhibitory ACE, blokery receptora angiotensyny/sartany, antagoniści aldosteronu)
- Jeśli GFR<45 ml/min./1,73 m2, leczenie należy rozpoczynać od małych dawek i zwiększać je stopniowo.
- Należy skontrolować GFR i stężenie potasu po tygodniu od rozpoczęcia leczenia lub każdego zwiększenia dawki.
- Nie należy rutynowo odstawiać leku u pacjentów z GFR <30 ml/min./1,73 m2, gdyż nadal wykazuje działanie nefroprotekcyjnie.
- Beta–blokery
- Zmniejszyć dawkę o połowę, jeśli GFR <30 ml/min./1,73 m2.
- Digoksyna
- Dostosowanie dawek w zależności od poziomu stężenia w osoczu.
Leki przeciwbólowe
- NLPZ
- Należy unikać rutynowego podawania w przypadku GFR<30 ml/min./1,73 m2.
- Nie zaleca się przewlekłego stosowania przy GFR<60 ml/min./1,73 m2.
- Należy unikać jednoczesnego podawania z blokerami RAS i litem.
- Opioidy
- Zmniejszenie dawki przy GFR<60 ml/min./1,73 m2.
- Ostrożnie przy GFR<15 ml/min./1,73 m2.
- W przypadku niewydolności nerek lub u pacjentów dializowanych, najbezpieczniejszymi opioidami są buprenorfina (lek pierwszego wyboru w przypadku CKD), metadon, fentanyl.
Antybiotyki
- Penicylina
- przy GFR<15 ml/min./1,73 m2 jest neurotoksyczna w dużych dawkach (maksymalnie 6 g/dobę).
- Makrolidy
- zmniejszenie dawki o 50% przy GFR<30 ml/min./1,73 m2.
- Fluorochinolony
- zmniejszenie dawki o 50% przy GFR <15 ml/min./1,73 m2.
- Tetracykliny
- dostosowanie dawki przy GFR <45 ml/min./1,73 m2.
- Aminoglikozydy
- Zmniejszenie dawki lub wydłużenie odstępu pomiędzy dawkami w przypadku stosowania przy GFR <60 ml/min./1,73 m2.
- Oznaczanie stężenia leku w surowicy (leczenie szpitalne).
- Unikanie jednoczesnego podawania innych substancji ototoksycznych, takich jak furosemid.
Leki przeciwgrzybicze
- Amfoterycyna
- unikać stosowania przy GFR<60 ml/min./1,73 m2, jeśli dostępne są alternatywne terapie.
- Flukonazol
- zmniejszenie dawki o 50% przy GFR<45 ml/min./1,73 m2.
- Flucytozyna
- zmniejszenie dawki przy GFR<60 ml/min./1,73 m2.
Leki przeciwcukrzycowe
- Metformina
- Stosowanie bezpieczne przy GFR>45 ml/min./1,73 m2.
- Ponownie ocenić konieczność dalszego stosowania przy GFR<45 ml/min./1,73 m2 i następnie zmniejszyć dawkę o 50% (maksymalnie 2g na dobę), unikać stosowania przy GFR<30 ml/min./1,73 m2.
- Pochodne sulfonylomocznika
- Unikanie stosowania tych substancji, które są wydalane głównie przez nerki.
Leki immunosupresyjne
- Metotreksat
- Zmniejszenie dawki przy GFR<60 ml/min./1,73 m2.
- Unikać, jeśli to możliwe, przy GFR <15 ml/min./1,73 m2.
Antykoagulanty
- Heparyny drobnocząsteczkowe
- zmniejszyć dawkę o połowę, jeśli GFR<30 ml/min./1,73 m2.
- Warfaryna
- mniejsza dawka i ścisłe monitorowanie przy GFR <30 ml/min./1,73 m2.
Lit
- Substancja nefrotoksyczna, która może pogorszyć czynność nerek również w stężeniach terapeutycznych.
- Kontrola eGFR, elektrolitów i stężenia litu co 6 miesięcy.
- Unikać jednoczesnego podawania leków z grupy NLPZ.
Przebieg, powikłania i rokowanie
- CKD wiąże się ze zwiększonym ryzykiem powikłań, hospitalizacji i zgonu, jak również z wyższymi kosztami opieki zdrowotnej.36
- Wielu pacjentów przez lata pozostaje bezobjawowych.
- Nierzadko zdarza się, że choroba zostaje wykryta dopiero w momencie wystąpienia pierwszych powikłań.
- CKD wiąże się ze zwiększonym ryzykiem sercowo–naczyniowym.37-38
- U pacjentów w stadium G3, ryzyko przedwczesnego zgonu z powodu zdarzeń sercowo-naczyniowych jest większe niż ryzyko wystąpienia wskazań do dializ.
- W stadium G3b (eGFR 30–44 ml/min. na 1,73 m2) śmiertelność z powodu chorób sercowo–naczyniowych jest zwiększona 11–krotnie, w stadium 4 (<30 ml/min./1,73 m2) – 21–krotnie.
- Również albuminuria jest predyktorem śmiertelności z przyczyn ogólnoustrojowych i sercowo–naczyniowych.
- Ryzyko progresji CKD w kierunku schyłkowej niewydolności nerek jest również istotnie zależne od GFR i albuminurii.2
- Zobacz tabela przewlekła choroba nerek, ryzyko progresji, ocena ryzyka.2
- Rzadkim (50–60 przypadków/rok), ale zagrażającym życiu powikłaniem jest kalcyfilaksja.
- To odkładanie się związków wapnia w małych naczyniach skóry i tkanki podskórnej, powodujące martwicę niedokrwionych tkanek.
- Charakteryzuje się niebieskawo–sinym przebarwieniem skóry z bardzo bolesnym owrzodzeniem/martwicą (ryzyko nadkażenia/sepsy) i zwapnieniem tętnic.
Kontrola przebiegu
- U wszystkich pacjentów z CKD co najmniej raz w roku należy oznaczać GFR i albuminurię.2
- Częstotliwość badań i wizyt kontrolnych, zależy od obrazu klinicznego i ryzyka progresji.
- Jeśli ryzyko progresji wzrasta, KDIGO zaleca kontrolę przebiegu od 2 do 4 razy w roku:
- zobacz tabela przewlekła choroba nerek, ryzyko progresji, ocena ryzyka.2
Informacje dla pacjentów
Materiały edukacyjne pacjentów
Ilustracje
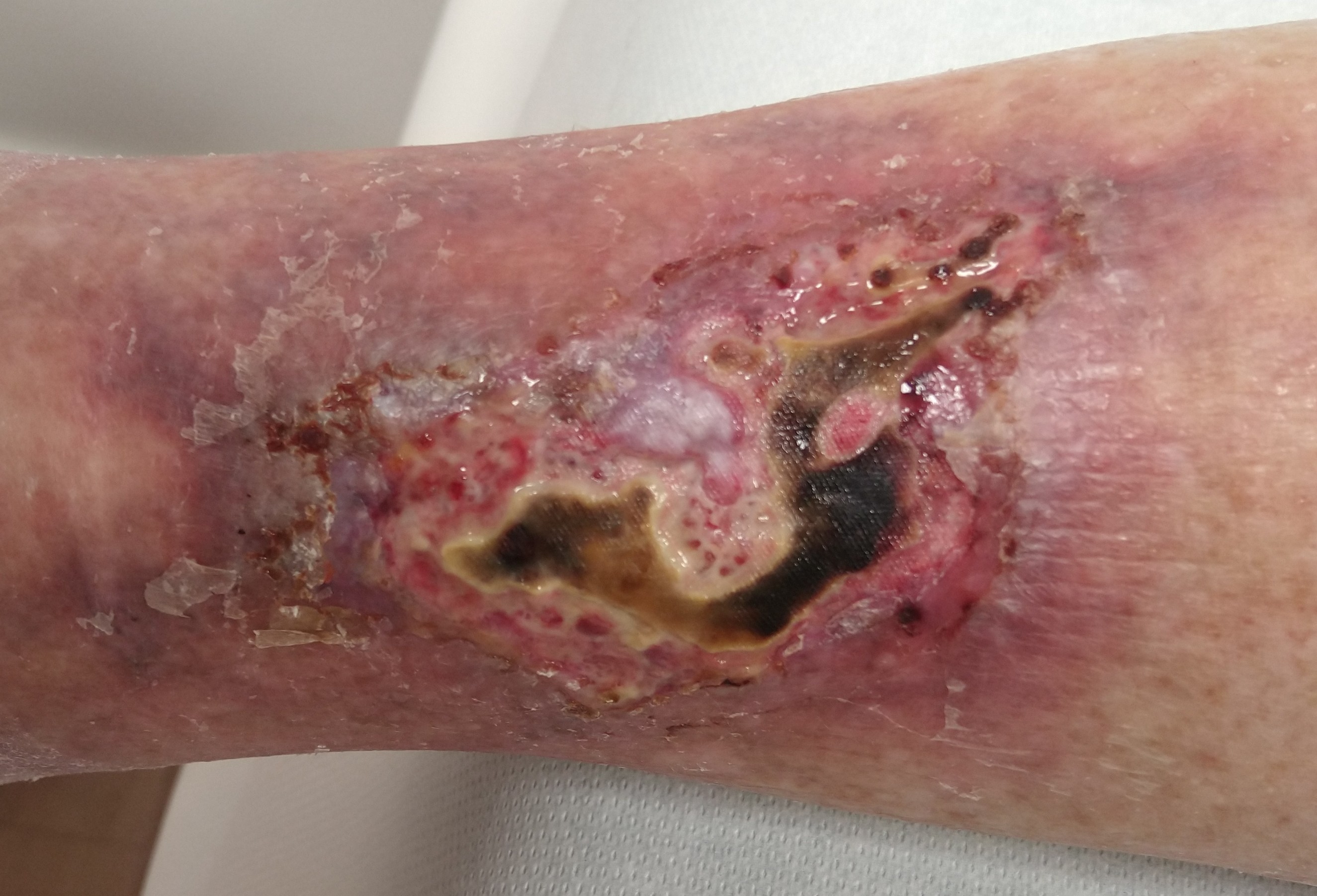
Kalcyfilaksja z widoczną miejscową martwicą tkanek (dzięki uprzejmości dr med. Christiny Linz)
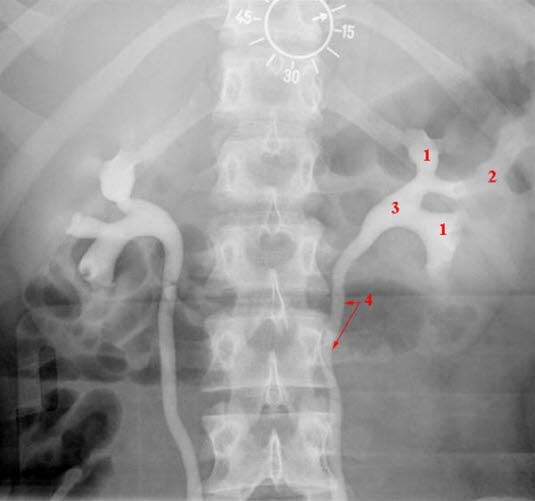
Urografia nerek, wyniki prawidłowe. Obustronne zakontrastowanie nerek i proksymalnych części moczowodów. 1+2 = kielichy nerkowe, 3 = miedniczka nerkowa, 4 = moczowód
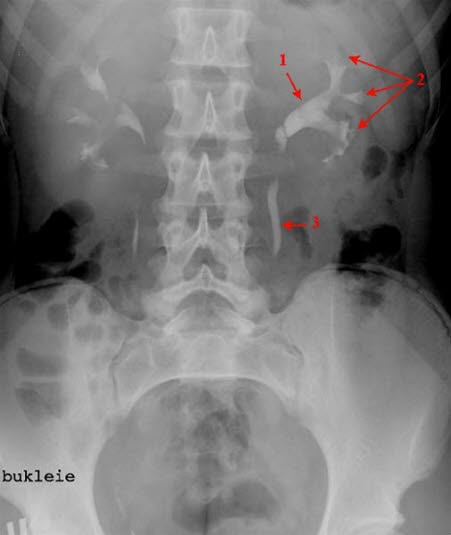
Urografia, zdjęcie przeglądowe jamy brzusznej. Objawy zastoju moczu po lewej stronie: opóźnione wydalanie kontrastu, poszerzona miedniczka nerkowa (1) i poszerzone, nieforemne kielichy nerkowe (2). Moczowód (3).
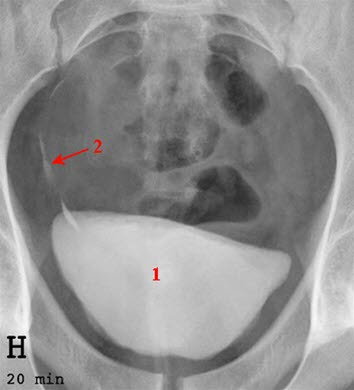
Urografia pęcherza moczowego (1). Opóźnione wydalanie kontrastu w prawym moczowodzie (2).
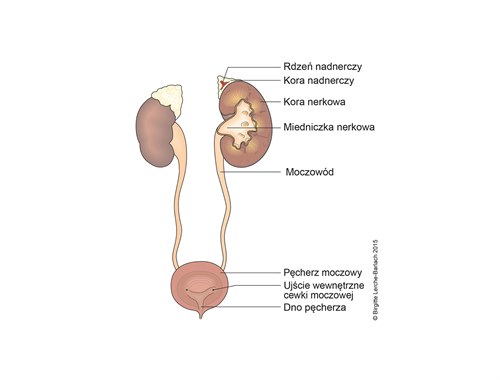
Rysunek poglądowy nerek, dróg moczowych, pęcherza moczowego
Źródła
Wytyczne
- Gellert R, Mastalerz-Migas A, Krajewska M, Ledwoch J. Wytyczne konsultanta krajowego w dziedzinie nefrologii, konsultanta krajowego w dziedzinie medycyny rodzinnej oraz prezesa Polskiego Towarzystwa Nefrologicznego, dotyczące diagnostyki i leczenia przewlekłej choroby nerek w POZ, z uwzględnieniem opieki koordynowanej, z dnia 19 lipca 2024. Ministerstwo Zdrowia. www.gov.pl
- Kidney Disease Improving Global Outcomes (KDIGO), Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease, 2024 www.kdigo.org
- Europejskie Towarzystwo Kardiologiczne (ESC). Wytyczne postępowania w nadciśnieniu tętniczym, stan na 2024 r., www.escardio.org
Piśmiennictwo
- Kidney Disease Improving Global Outcomes (KDIGO), Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease, dostęp: 18.11.2023, kdigo.org
- Kidney Disease Improving Global Outcomes (KDIGO). KDIGO 2012 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease, Kidney International supplements 2013, 3(1): 869-76, kdigo.org
- Hemmelgarn B.R., Manns B.J., Lloyd A., et al. Relation between kidney function, proteinuria, and adverse outcomes, JAMA 2010, 303: 423-9, PubMed
- Schultze G. „Chronic kidney disease“ ungleich chronische Niereninsuffizienz. Internist 2017, 58: 643, doi:10.1007/s00108-017-0233-0, DOI
- Gergei I., Klotsche J., Woitas R.P., Pieper L., Wittchen H-U., Krämer B.K., et al. Chronic kidney disease in primary care in Germany, J Public Health, 2017, 25: 223-30, link.springer.com
- Delanaye P., Jager K., Bökenkamp A., et al. CKD: A Call for an Age-Adapted Definition, JASN 2019, 30: 1785-805, doi:10.1681/ASN.2019030238, DOI
- GBD Chronic Kidney Disease Collaboration. Global, regional, and national burden of chronic kidney disease, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet. 2020 Feb 29;395(10225):709-733. pubmed.ncbi.nlm.nih.gov
- Gellert R, Mastalerz-Migas A, Krajewska M, Ledwoch J. Wytyczne konsultanta krajowego w dziedzinie nefrologii, konsultanta krajowego w dziedzinie medycyny rodzinnej oraz prezesa Polskiego Towarzystwa Nefrologicznego, dotyczące diagnostyki i leczenia przewlekłej choroby nerek w POZ, z uwzględnieniem opieki koordynowanej z dnia 19 lipca 2024. Ministerstwo Zdrowia. www.gov.pl
- Girndt M., Trocchi P., Scheidt-Nave C., et al. The prevalence of renal failure—results from the German Health Interview and Examination Survey for Adults, 2008–2011 (DEGS1), Dtsch Arztebl Int 2016, 113: 85-91, doi:10.3238/arztebl.2016.0085, DOI
- Zhang Q.L., Koenig W., Raum E., Stegmaier C., Brenner H., Rothenbacher D. Epidemiology of chronic kidney disease: results from a population of older adults in Germany, Prev Med 2009, 48(2): 122-7, pmid:19041887, PubMed
- König M., Gollasch, Demuth I., et al. Prevalence of Impaired Kidney Function in the German Elderly: Results from the Berlin Aging Study II (BASE-II). Gerontology 2017, 63: 201-9, doi:10.1159/000454831, DOI
- Fraser S., Roderick P., May C., et al. The burden of comorbidity in people with chronic kidney disease stage 3: a cohort study, BMC Nephrology 2015, 16: 193, doi:10.1186/s12882-015-0189-z, DOI
- Mayo Clinic Patient Care and Health Information. Chronic Kidney Disease - Risk Factors, dostęp: 24.05.2019, www.mayoclinic.org
- Haroun M., Jaar B., Hoffman S., et al. Risk Factors for Chronic Kidney Disease: A Prospective Study of 23,534 Men and Women in Washington County, Maryland, J Am Soc Nephrol 2003, 14: 2934-41, doi:10.1097/01.ASN.0000095249.99803.85, DOI
- Tangri N., Grams M.E., Levey A.S., et al.; CKD Prognosis Consortium. Multinational Assessment of Accuracy of Equations for Predicting Risk of Kidney Failure: A Meta-analysis, JAMA, 12.01.2016, 315(2): 164-74, doi: 10.1001/jama.2015.18202. Erratum in: JAMA, 23.02.2016, 315(8):822, PMID: 26757465, PMCID: PMC4752167, pubmed.ncbi.nlm.nih.gov
- Paige N.M., Nagami G.T. The top 10 things nephrologists wish every primary care physician knew, Mayo Clin Proc 2009, 84(2): 180-6, www.ncbi.nlm.nih.gov
- Orth S.R. Effects of smoking on systemic and intrarenal hemodynamics: influence on renal function, J Am Soc Nephrol 2004, 15 Suppl 1:S58, pubmed.ncbi.nlm.nih.gov
- Orth S.R., Hallan S.I. Smoking: a risk factor for progression of chronic kidney disease and for cardiovascular morbidity and mortality in renal patients absence of evidence or evidence of absence? Clin J Am Soc Nephrol 2008, 3:226, PubMed
- Staplin N., Hynes R., Herrington W., et al. Smoking and Adverse Outcomes in Patients With CKD: The Study of Heart and Renal Protection (SHARP), Am J Kidney Dis 2016, 68: 371-80, pubmed.ncbi.nlm.nih.gov
- Levey A.S. Clinical practice. Nondiabetic kidney disease, N Engl J Med 2002, 347: 1505-11, New England Journal of Medicine
- Heerspink H., Stefansson B., Correa-Rotter R., et al. Dapagliflozin in Patients with Chronic Kidney Disease, N Engl J Med 2020, 383: 1436-46, doi:10.1056/NEJMoa2024816, DOI
- Mach F., Baigent C., Catapano A., et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk, Eur Heart J 2020, 41: 111-88, doi:10.1093/eurheartj/ehz455, DOI
- Williams B., Mancia G., Spiering W., et al. 2018 ESC/ESH Guidelines for the management of arterial hypertension, Eur Heart J 2018, 39: 3021-104, doi:10.1093/eurheartj/ehy339, DOI
- Siebenhofer A., Plank J., Horvath K., Berghold A., Sutton A.J., Sommer R., et al. Angiotensin receptor blockers as anti-hypertensive treatment for patients with diabetes mellitus; meta-analysis of controlled double-blind randomized trials, Diabet Med 2004, 21: 18-25, PubMed
- Wong M., Perkovic V. Knowing what we do not know: statin therapy in advanced chronic kidney disease, Lancet Diabetes Endocrinol 2016, 4: 801-3, www.thelancet.com
- Palmer S.C., Craig J.C., Navaneethan S.D., et al. Benefits and harms of statin therapy for persons with chronic kidney disease: a systematic review and meta-analysis, Ann Intern Med 2012, 157: 263-75, pubmed.ncbi.nlm.nih.gov
- Pfeffer M., Burdmann E., Chen C., et al. A Trial of Darbepoetin Alfa in Type 2 Diabetes and Chronic Kidney Disease, N Engl J Med 2009, 361: 2019-32, doi:10.1056/NEJMoa0907845, DOI
- Drüeke T., Locatelli F., Clyne N., et al. Normalization of hemoglobin level in patients with chronic kidney disease and anemia, N Engl J Med 2006, 355: 2071-84, doi:10.1056/NEJMoa062276, DOI
- Singh A., Szczech L., Tang K., et al. Correction of Anemia with Epoetin Alfa in Chronic Kidney Disease, N Engl J Med 2006, 355: 2085-98, doi:10.1056/NEJMoa065485, DOI
- Clement F.M., Klarenbach S., Tonelli M., Johnson J.A., Manns B.J. The impact of selecting a high hemoglobin target level on health-related quality of life for patients with chronic kidney disease, Arch Intern Med 2009, 169: 1104-12, PubMed
- KDIGO 2012 Clinical Practice Guideline for Anemia in Chronic Kidney Disease, kdigo.org
- KDIGO 2017 Clinical Practice Guideline Update for the Diagnosis, Evaluation, Prevention, and Treatment of chronic kidney disease–mineral and bone disorder, kdigo.org
- Meyer T.W., Hostetter TH. Uremia, N Engl J Med 2007, 357: 1316-25, PubMed
- Munar M.Y. Drug dosing adjustments in patients with chronic kidney disease, Am Fam Physician 2007, 75: 1487-96, PubMed
- Hartmann B., Czock D., Keller F. Drug Therapy in Patients With Chronic Renal Failure, Dtsch Arztebl Int 2010, 107: 647-56, doi:10.3238/arztebl.2010.0647, DOI
- Baumgarten M., Gehr T. Chronic kidney disease: detection and evaluation, Am Fam Physician 2011, 84: 1138-48, PubMed
- Angelantonio E., Chowdhury R., Sarwar N., et al. Chronic kdney disease and risk of major cardiovascular disease and non-vascular mortality: prospective population based cohort study. BMJ 2010; 341: c4986. pubmed.ncbi.nlm.nih.gov
- Lee M, Saver JL, Chang K-H, et al. Low glomerular filtration and risk of stroke: meta-analysis. BMJ 2010; 341: c4249. BMJ (DOI)
Opracowanie
- Tomasz Tomasik (redaktor)
- Natalia Jagiełła (recenzent)
- Adam Windak (redaktor)
- Michael Handke (recenzent/redaktor)
- Guido Schmiemann (recenzent/redaktor)