Informacje ogólne
Definicja
- Choroba wieńcowa jest istotną klinicznie manifestacją miażdżycy w tętnicach wieńcowych.
- Jest to choroba przewlekła, zwykle postępująca, w której różnej długości fazy pozornej stabilności przeplatają się z fazami niestabilności (przewlekły zespół wieńcowy - PZW).
- Typowe objawy kliniczne to dławica piersiowa i duszność podczas wysiłku.
Terminologia
- Stosowany od dawna termin „stabilna choroba wieńcowa” jest mylący, ponieważ u pacjentów stale występuje zwiększone ryzyko zdarzeń sercowo–naczyniowych i zmienny przebieg kliniczny.1
- Nowo wprowadzony termin „przewlekły zespół wieńcowy” uwzględnia dynamikę przebiegu choroby, a także możliwość wpływania na jej przebieg poprzez zmianę stylu życia, farmakoterapię i rewaskularyzację.
- Termin „przewlekły zespół wieńcowy” (PZW) należy uznać za uzupełnienie znanego od dawna terminu „ostry zespół wieńcowy” (OZW).
Postaci przewlekłego zespołu wieńcowego (PZW) na podstawie wytycznych ESC 2024
- Podejrzenie lub rozpoznanie poniższych2:
- ból w klatce piersiowej lub jego ekwiwalent bez zmian miażdżycowych w naczyniach wieńcowych: ANOCA/INOCA -angina with non-obstructive coronary arteries/ischaemia with non-obstructive coronary arteries (dawna nazwa: zespół X lub choroba Prinzmetala)
- bezobjawowy PZW ze zmianami anatomicznymi w naczyniach wieńcowych lub testach czynnościowych
- ból wywołany wysiłkiem/stresem (lub jego ekwiwalent) ze zmianami miażdżycowymi w naczyniach wieńcowych
- pacjent po OZW, PCI, CABG
- ekwiwalent wieńcowy w postaci niedokrwiennej niewydolności serca
Epidemiologia
- Przyczyna zgonu:
- Przewlekła choroba niedokrwienna serca ze wskaźnikiem śmiertelności na poziomie około 8% według klasyfikacji ICD–10 jest najczęstszą przyczyną zgonów w krajach uprzemysłowionych.
- Jednak wskaźniki śmiertelności systematycznie maleją – od końca XX. wieku zmniejszyły się mniej więcej o połowę, przy czym mężczyźni umierają z powodu choroby wieńcowej dwa razy częściej niż kobiety.
- Chorobowość:
- Częstość występowania w ciągu całego życia wynosi około 8%.
- W Polsce na chorobę niedokrwienną serca choruje około 4,2% populacji.3
- Podział według płci:
- Stosunek liczby mężczyzn do kobiet – około 2:1.
- Status społeczny:
- Chorobowość wśród osób o niskim statusie społecznym jest blisko dwukrotnie wyższa niż u osób o wysokim statusie społecznym.
- Częstość występowania w praktyce lekarza rodzinnego:
- 7–11% dorosłych pacjentów w praktyce lekarza rodzinnego.
Etiologia i patogeneza
Patofizjologiczne przyczyny PZW2
- Nasierdziowe
- strukturalne
- miażdżyca
- krwiak wewnątrznaczyniowy
- mostek mięśniowy
- tętniak wieńcowy
- czynnościowe
- wazospazm (dawniej: choroba Prinzmetala)
- dysfunkcja śródbłonka/mięśniówki gładkiej/zaburzenia układu współczulnego
- wazospazm (dawniej: choroba Prinzmetala)
- strukturalne
- Mikrokrążeniowe (dawniej: zespół X)
- strukturalne
- remodeling naczynia
- rozrzedzenie mikrokrążenia
- nacieczenie komórkowe
- włóknienie okołonaczyniowe
- wzmożone ciśnienie śródścienne (przerost mięśnia sercowego, wzrost ciśnienia końcowo-rozkurczowego)
- czynnościowe
- upośledzenie dilatacji
- wzmożenie konstrykcji
- strukturalne
- Według wczesnych koncepcji patofizjologię miażdżycy postrzegano przede wszystkim jako nagromadzenie i magazynowanie lipidów i komórek mięśni gładkich w ścianie naczynia.4
- Obecnie przyjmuje się, że występuje złożona interakcja różnych czynników, przy czym decydującą rolę we wszystkich stadiach miażdżycy odgrywają procesy zapalne.5
- Powstawaniu blaszki miażdżycowej sprzyjają różne czynniki, z których część wzajemnie się potęguje, m.in. oksydacja LDL, aktywacja śródbłonka, rekrutacja komórek zapalnych, wytwarzanie cytokin.6
- W przebiegu procesu miażdżycowego mogą rozwijać się różne zmiany o odmiennych następstwach klinicznych:4
- Zmiany zwężające (mały rdzeń lipidowy, liczne zwłóknienia i zwapnienia, gruba otoczka włóknista blaszki miażdżycowej): prowadzą do zmniejszenia perfuzji i niedokrwienia wysiłkowego z kliniczną dławicą piersiową i/lub dusznością.
- Zmiany niezwężające (duży rdzeń lipidowy z cienką otoczką włóknistą): są podatne na pęknięcie blaszki/zakrzepicę, co może prowadzić do OZW.
- Większość zmian toczy się głównie poza światłem naczynia (na zewnątrz), tak więc nasilona choroba miażdżycowa może istnieć bez istotnych zwężeń bądź zwężenia powodujące niedokrwienie mogą być jednym z elementów całego zmienionego chorobowo układu naczyniowego.4,7
- Manifestacja kliniczna PZW (wysiłkowe niedokrwienie z dławicą piersiową i/lub dusznością) w przebiegu choroby zależy w przeważającej mierze od liczby, rozmieszczenia i nasilenia zwężeń.
- W dowolnym momencie może też wystąpić OZW, w zależności od stopnia i nasilenia miażdżycy oraz podatności blaszek miażdżycowych.1
- Zasadniczo nastąpiła zmiana paradygmatu w rozumieniu choroby wieńcowej, której towarzyszy zwężenie naczyń: podczas wysiłku fizycznego i obciążenia psychicznego zwężone naczynie wywołuje dolegliwości stenokardialne. Przy zwężeniach naczyń wieńcowych często dochodzi też do pęknięcia blaszki miażdżycowej. W większości przypadków jednak same zwężone naczynia nie ulegają uszkodzeniu – co tłumaczyłoby również, dlaczego poszerzenie zwężenia przy stabilnej chorobie wieńcowej za pomocą PCI nie przynosi korzyści pod względem rokowania.
- Oprócz makronaczyniowej miażdżycy ze zwężeniową chorobą wieńcową do przewlekłego niedokrwienia mięśnia sercowego mogą prowadzić także inne zmiany:
- Zmiany mikronaczyniowe, dysfunkcja śródbłonka8
- Dysfunkcja śródbłonka wiąże się również z klasycznymi czynnikami ryzyka (hiperlipidemia, palenie papierosów, nadciśnienie tętnicze, cukrzyca), przy czym częściej dotyczy kobiet.
- Dławica naczynioskurczowa (prinzmetala).
- Przerost mięśnia sercowego ze zwiększonym zapotrzebowaniem na tlen (nadciśnienie tętnicze, zwężenie zastawki aortalnej, kardiomiopatia przerostowa).
- Przyczyny niesercowe (niedokrwistość, hipoksemia płucna).
- Zmiany mikronaczyniowe, dysfunkcja śródbłonka8
Czynniki predysponujące
Modyfikowalne czynniki ryzyka
- Wzrost ryzyka powoduje:
- hiperlipidemia
- palenie papierosów
- cukrzyca
- nadciśnienie tętnicze
- otyłość brzuszna (stosunek obwodu talii do obwodu bioder)9-12
- stres psychospołeczny.13-14
- Obniżenie ryzyka powoduje:
Niemodyfikowalne czynniki ryzyka
- Wiek:
- Płeć:
- Do pewnego stopnia hormonalna ochrona kobiet przed menopauzą.
- Statystycznie kobiety doznają pierwszego zawału mięśnia sercowego 9 lat później niż mężczyźni.17
- Jednak 80% tej różnicy wynika z zależnego od wieku rozkładu czynników ryzyka u mężczyzn i kobiet.17
- Wywiad rodzinny:
- Predyspozycje genetyczne odgrywają pewną rolę, w niektórych rodzinach występuje zwiększona częstość występowania choroby wieńcowej.
- Wzrost ryzyka wynikający z dodatniego wywiadu rodzinnego jest związany z liczbą chorych krewnych i wiekiem, w którym choroba się ujawniła.18
Diagnostyka różnicowa
- Liczne rozpoznania różnicowe (zobacz również artykuły ból w klatce piersiowej oraz duszność u dorosłych), m.in.:
- zespół ściany klatki piersiowej
- choroba refluksowa
- zapalenie żołądka/choroba wrzodowa
- POChP/astma
- zakażenie dróg oddechowych z zapaleniem opłucnej
- zaburzenia psychogenne
- wywołane przez leki (np. tryptany).
ICD–10
- I20 Choroba niedokrwienna serca.
- I20.1 Choroba niedokrwienna serca z udokumentowanym skurczem naczyń wieńcowych.
- I20.8 Inne postaci choroby niedokrwiennej serca.
- I20.9 Choroba niedokrwienna serca, nieokreślona.
- I25 Przewlekła choroba niedokrwienna serca.
- I25.0 Choroba serca i naczyń krwionośnych w przebiegu miażdżycy.
- I25.1 Choroba serca w przebiegu miażdżycy.
- I25.9 Przewlekła choroba niedokrwienna serca, nieokreślona.
Diagnostyka
- U osób zgłaszających objawy podejrzewanego niedokrwienia mięśnia sercowego zaleca się szczegółową ocenę czynników ryzyka sercowo-naczyniowego, wywiadu medycznego i charakterystyki objawów (w tym czasu ich wystąpienia, czasu trwania, rodzaju, lokalizacji, czynników wyzwalających, czynników łagodzących, pory dnia).2
Kryteria diagnostyczne
- Rozpoznanie wstępne i ocena prawdopodobieństwa na podstawie:
- objawów klinicznych
- profilu ryzyka.
- Jeżeli prawdopodobieństwo oceniono wstępnie jako średnie, ewentualne potwierdzenie rozpoznania badaniami nieinwazyjnymi, a w indywidualnych przypadkach – badaniami inwazyjnymi.
Wywiad lekarski
- Przewlekła choroba wieńcowa jest powodem konsultacji z lekarzem rodzinnym u 8–11% pacjentów zgłaszających się z bólem w klatce piersiowej.
- Wysoce prawdopodobne podejrzenie rozpoznania można wysnuć już na podstawie dokładnego wywiadu lekarskiego, choć badania fizykalne i dodatkowe są pomocne w potwierdzeniu diagnozy, wykluczeniu rozpoznań różnicowych i ocenie nasilenia choroby.2
- Jeżeli z pierwszej oceny wyniknie podejrzenie choroby wieńcowej, kolejnymi celami wywiadu lekarskiego są:
- Ocena prawdopodobieństwa choroby wieńcowej po wstępnej ocenie, ukierunkowująca wybór dalszej diagnostyki.
- Określenie profilu ryzyka sercowo–naczyniowego.
- Wczesne ustalenie niekorzystnego przebiegu, któremu można zapobiec.
- Ocena gotowości pacjenta do zmiany stylu życia.
- Objawy:
- Dławica piersiowa (angina pectoris)
- Umiejscowienie, promieniowanie (zamostkowe, w klatce piersiowej, w nadbrzuszu, bark(–i), ramię(–ona), szczęka/żuchwa, plecy).
- Charakter (ucisk, ciężar, wrażenie ciasnoty, ból, pieczenie).
- Czas trwania (w większości przypadków ≤10 minut)
- Ból w klatce piersiowej trwający kilka sekund nie jest zwykle spowodowany przez chorobę wieńcową.
- Zależność od wysiłku (rodzaj i stopień obciążenia fizycznego).
- Występowanie w ciągu dnia (typowe np. również rano po przebudzeniu).
- Inne czynniki wyzwalające (zimno, obfity posiłek, niepokój emocjonalny).
- Czynniki łagodzące: odpoczynek fizyczny, podanie azotanów.
- Duszność wysiłkowa
- Może być jedynym objawem choroby wieńcowej.
- Może współwystępować z zawrotami głowy2
- Wcześniej niedoceniana jako objaw choroby wieńcowej; obecnie duszność uznaje się za samodzielny czynnik w ocenie pacjenta.
- Inne możliwe objawy:
- nudności
- osłabienie
- lęk
- kołatanie serca
- zawroty głowy.
- zmęczenie
- Dławica piersiowa (angina pectoris)
- Czynniki ryzyka:
- hiperlipidemia
- nadciśnienie tętnicze
- palenie papierosów
- cukrzyca
- predyspozycje rodzinne
- nadwaga i otyłość (zwłaszcza otyłość brzuszna)
- brak aktywności fizycznej
- stres psychospołeczny.
- Inne współistniejące i istniejące wcześniej schorzenia, które wiążą się ze zwiększonym ryzykiem choroby wieńcowej, takie jak:
- choroba tętnic obwodowych (peripheral artery disease – PAD)
- zewnątrzczaszkowe zwężenie tętnic szyjnych, choroba naczyń mózgowych
- przewlekła choroba nerek
- niektóre choroby reumatologiczne, np. reumatoidalne zapalenie stawów
- stan po radioterapii.
- Wynik oceny w skali Marburg Heart Score pozwala bardzo szybko i już po jednym badaniu fizykalnym skategoryzować ryzyko kardiologiczne i zdecydować, czy dalsza diagnostyka jest w ogóle wskazana.19
Klasyfikacja dławicy piersiowej na podstawie jej nasilenia według Canadian Cardiovascular Society (CCS)
- Stopień I: dławica piersiowa tylko przy dużym wysiłku fizycznym.
- Stopień II: dławica piersiowa przy umiarkowanym wysiłku fizycznym (np. chodzenie pod górę, wchodzenie wyżej niż na 1 piętro schodów).
- Stopień III: dławica piersiowa przy lekkim wysiłku fizycznym (przejście 100–200 m w normalnym tempie, wejście na 1. piętro).
- Stopień IV: dławica piersiowa w spoczynku (występuje nawet bez wysiłku fizycznego).
Badanie fizykalne
Parametry pomiarowe
- Wzrost, masa ciała:
- Odradza się rutynowe wyliczanie wskaźnika BMI, stosunku obwodu talii do obwodu bioder w ocenie ryzyka sercowo–naczyniowego.
- Ciśnienie tętnicze, tętno (częstość, rytm).
- Zalecana wartość u pacjentów z PZW: 120-129 mmHg, pod warunkiem dobrej tolerancji leczenia hipotensyjnego.2
Obserwacja
- Kępki żółte (powieki, zazwyczaj wewnętrzny kącik oka), rzadko żółtaki (pochewki ścięgien, łokcie, stawy kolanowe) jako możliwy objaw hipercholesterolemii.
- Poszerzenie żył szyjnych (w niewydolności serca spowodowanej chorobą wieńcową).
- Obrzęki kończyn dolnych (w niewydolności serca spowodowanej chorobą wieńcową).
Palpacja
- Słabiej wyczuwalne tętno w uogólnionej miażdżycy z chorobą tętnic obwodowych (PAD).
Osłuchiwanie
- Serce:
- Badanie osłuchowe często w normie
- możliwy trzeci ton serca (wczesnorozkurczowy) w niewydolności serca
- możliwy szmer skurczowy w niedomykalności zastawki mitralnej (zobacz także artykuł szmery nad sercem u dorosłych).
- Badanie osłuchowe często w normie
- Płuca:
- Trzeszczenia nad płucami w niewydolności serca z zastojem w krążeniu płucnym.
- Tętnice:
- Szmery przy zwężeniach (np. w uogólnionej miażdżycy ze zwężeniem tętnicy szyjnej).
Określenie prawdopodobieństwa choroby niedokrwiennej serca - ocena wstępna
Marburg Heart Score
- Na poziomie podstawowej opieki zdrowotnej można stosować kryteria Marburg Heart Score:
- ocena prawdopodobieństwa wystąpienia choroby wieńcowej na podstawie pięciu prostych kryteriów
- kalkulator dostępny na mdcalc.com.
Kryteria
- Płeć i wiek (mężczyźni ≥55 lat i kobiety ≥65 lat): 1 punkt.
- Znana choroba naczyniowa: 1 punkt.
- Dolegliwości są zależne od wysiłku: 1 punkt.
- Bólu nie można odtworzyć w badaniu palpacyjnym: 1 punkt.
- Pacjent podejrzewa, że ból jest związany z sercem: 1 punkt.
Interpretacja
- Wartość punktowa 0–1: bardzo niskie (<1%) prawdopodobieństwo choroby wieńcowej ze zwężeniem jako przyczyny bólu w klatce piersiowej
- Wartość punktowa 2: niskie (ok. 5%) prawdopodobieństwo występowania choroby wieńcowej ze zwężeniem.
- Wartość punktowa 3: średnie (ok. 25%) prawdopodobieństwo występowania choroby wieńcowej ze zwężeniem.
- Wartość punktowa 4–5: wysokie (ok. 65%) prawdopodobieństwo występowania choroby wieńcowej ze zwężeniem.
Klasyfikacja Diamonda i Forrestera
- W wielu wytycznych wykorzystuje się klasyfikację Diamonda i Forrestera do oceny prawdopodobieństwa przy wstępnej ocenie (kryteria: wiek, płeć, klasyfikacja dławicy piersiowej, ostatnio również duszności), ale uzyskana ocena prawdopodobieństwa jest bardziej odpowiednia do stosowania w kardiologii niż w praktyce lekarza rodzinnego.2
| Wiek (lata) | 30–39 | 40–49 | 50–59 | 60–69 | ≥70 | |||||
| Płeć | M | K | M | K | M | K | M | K | M | K |
| Typowa dławica piersiowa | m | m | d | u | d | u | d | d | d | d |
| Atypowa dławica piersiowa | m | m | u | u | d | u | d | u | d | d |
| Ból niedławicowy | m | m | m | m | u | m | d | u | d | u |
| K – kobiety; M – mężczyźni
Prawdopodobieństwo: m – małe <5% [badania dodatkowe tylko w szczególnych przypadkach]; u – umiarkowane 5–15% [badania dodatkowe można rozważyć]; d – duże >15% [preferowane wykonanie badań dodatkowych]. |
||||||||||
Badania uzupełniające w gabinecie lekarza rodzinnego
Planowanie dalszej diagnostyki i terapii w zależności od prawdopodobieństwa przy wstępnej ocenie2
- U pacjentów z prawdopodobieństwem ≤5% przy wstępnej ocenie, należy rozważyć odroczenie badań diagnostycznych i rozważyć inną przyczynę objawów.
- U pacjentów z prawdopodobieństwem >5-15% przy wstępnej ocenie, w dalszej diagnostyce należy zastosować metody nieinwazyjne, np. ocenę indeksu zwapnień w tętnicach wieńcowych (coronary artery calcium score- CACS), aby z maksymalną dokładnością doprecyzować podejrzenie choroby wieńcowej ze zwężeniem.
- U osób z początkowym prawdopodobieństwem >5-15%, można rozważyć wykonanie EKG wysiłkowego oraz badania diagnostyczne w kierunku zmian miażdżycowych w innych tętnicach niż wieńcowe, w celu skorygowania prawdopodobieństwa wstępnej oceny.
- U pacjentów z wysokim prawdopodobieństwem przy wstępnej ocenie, należy bez dalszej diagnostyki przyjąć, że przyczyną objawów jest choroba wieńcowa ze zwężeniem, i rozpocząć planowanie terapii.
EKG
- U pacjentów z podejrzeniem choroby wieńcowej na podstawie wywiadu lekarskiego i wyników badań należy wykonać spoczynkowe EKG z 12 odprowadzeniami.
- EKG należy wykonać tylko wtedy, gdy prawdopodobieństwo według Marburg Heart Score oceniono co najmniej jako średnie.
- Objawy wskazujące na przebyty zawał (patologiczne załamki Q), zaburzenia repolaryzacji związane z niedokrwieniem, arytmia, zobacz również artykuły:
- Prawidłowy zapis spoczynkowego EKG nie wyklucza choroby wieńcowej.
- U osób z podejrzeniem naczynioskurczowej dławicy piersiowej, należy rozważyć ambulatoryjne monitorowanie EKG (holter EKG).2
RTG klatki piersiowej
- W niewydolności serca możliwe oznaki zastoju, powiększony cień sylwetki serca.
- Wykluczenie/potwierdzenie płucnych rozpoznań różnicowych.
Badania laboratoryjne – krew
- U wszystkich osób, w celu stratyfikacji ryzyka, poszukiwania chorób współistniejących oraz prawidłowego leczenia, należy wykonać następujące badania:
- Morfologia krwi (niedokrwistość).
- Glikemia na czczo
- Lipogram: cholesterol całkowity, LDL, TG, HDL, nie–HDL.
- eGFR, kreatynina.
- przy podejrzeniu PZW, należy przynajmniej raz ocenić czynnośc tarczycy (TSH).
- hsCRP i/lub stężenie fibrynogenu2
- Ewentualnie:
- Troponina (poza kontraktem POZ) tylko w przypadku podejrzenia OZW, jeśli pracownia hemodynamiki znajduje się daleko od gabinetu lekarza rodzinnego.
- NT–proBNP (jeżeli dostępne) tylko przy podejrzeniu niewydolności serca.
Badania laboratoryjne – mocz
- Przy podejrzeniu przewlekłej choroby nerek: testy paskowe, jeżeli wynik testu paskowego jest nieprawidłowy – ewentualnie także badanie ogólne moczu i oznaczenie wartości wskaźnika albuminowo–kreatyninowego (albumin/creatinine ratio – ACR) w pojedynczej próbce moczu, jeżeli dostępne.
Próba wysiłkowa EKG
- Próba wysiłkowa EKG (tylko w ramach opieki koordynowanej) ma tylko ograniczone znaczenie diagnostyczne. Nawet jeżeli prawdopodobieństwo choroby wieńcowej ze zwężeniem w ocenie wstępnej wynosi 30%, a następnie spadnie o połowę z uwagi na wynik w normie, pozostałe ryzyko wynoszące 15% nadal jest znacząco zbyt wysokie. W związku z tym badanie ergometryczne jest obecnie zalecane tylko jako badanie o mniejszym znaczeniu przy prawdopodobieństwie oceny wstępnej wynoszącym 15–35%. W pierwszej kolejności należy rozważyć scyntygrafię mięśnia sercowego i ECHO wysiłkowe, to pierwsze zwłaszcza przy bloku lewej odnogi pęczka Hisa (LBBB), gdy nie ma możliwości oceny odcinków ST–T w badaniu EKG.
- Wady to między innymi niewystarczająca wartość informacyjna lub jej brak, m.in. w przypadku:
- niewystarczającego obciążenia fizycznego
- obniżenia odcinka ST >1 mm w spoczynkowym EKG
- przerostu lewej komory serca (LVH)
- bloku lewej odnogi pęczka Hisa (LBBB).
- Średnia czułość i swoistość wynosi odpowiednio 68% i 77%.
- Znaczenie jest niższe u kobiet niż u mężczyzn.
EKG metodą Holtera (Holter–EKG)
- Przy podejrzeniu istotnych klinicznie nadkomorowych lub komorowych arytmii.
- Badanie dostępne w POZ tylko w ramach opieki koordynowanej.
Ogólna ocena prawdopodobieństwa klinicznego
- Przybliżone prawdopodobieństwo w ocenie wstępnej uzupełnia się o indywidualną ocenę lekarza w celu uzyskania ogólnej oceny prawdopodobieństwa choroby wieńcowej.
- Jeśli prawdopodobieństwo PZW w ocenie wstępnej jest wysokie, można rozpoznać PZW, skierować pacjenta do kardiologa, włączyć ASA i statynę. PCI nie wpływa na poprawę rokowania. Diagnostyka inwazyjna może co najwyżej wykryć chorobę wielonaczyniową, w przypadku której operacja wszczepienia by–passów (CABG) może zmniejszyć śmiertelność o mniej więcej 3%.
Diagnostyka psychospołeczna
- Prawdopodobieństwo wystąpienia zaburzeń depresyjnych należy ocenić za pomocą pytań przesiewowych w wywiadzie lekarskim lub wystandaryzowanych kwestionariuszy.
- Prawdopodobieństwo innego istotnego rokowniczo zaburzenia psychicznego (zaburzenia lękowe, zespół stresu pourazowego, schizofrenia, zaburzenie dwubiegunowe) lub konstelacji ryzyka psychospołecznego (niski status socjoekonomiczny, izolacja społeczna, brak wsparcia społecznego, stres zawodowy lub rodzinny) należy oceniać przy użyciu odpowiednich pytań w wywiadzie lekarskim lub kwestionariuszy.
Diagnostyka specjalistyczna
- W zależności od oszacowanego ryzyka wystąpienia zmian miażdżycowych w naczyniach wieńcowych, zaleca się przeprowadzenie specjalistycznych badań diagnostycznych2:
- bardzo wysokie ryzyko (>85%):
- koronarografia
- wysokie ryzyko (>50-85%):
- RM
- SPECT/PET
- echokardiografia wysiłkowa
- umiarkowane ryzyko (>15-50%):
- tomografia komputerowa naczyń wieńcowych (angio-TK) lub
- SPECT/PET lub
- RM lub
- echokardiografia wysiłkowa
- niskie ryzyko (>5-15%):
- kliniczna ocena prawdopodobieństwa zwężenia naczyń wieńcowych (zmiany w spoczynkowym EKG, dysfunkcja lewej komory, nieprawidłowy wynik próby wysiłkowej, arytmie komorowe, PAD, obecność zwapnień naczyń wieńcowych we wcześniej wykonanym badaniu TK) lub
- angio-TK naczyń wieńcowych
- bardzo wysokie ryzyko (>85%):
Echokardiografia (ECHO)
- Przy podejrzeniu choroby wieńcowej należy wykonać przezklatkową echokardiografię w spoczynku:
- ocena globalnej kurczliwości lewej komory serca
- wykrywanie regionalnych zaburzeń kurczliwości jako objaw wskazujący na chorobę wieńcową
- wykluczenie/wykrycie w diagnostyce różnicowej
Obrazowanie czynnościowe (diagnostyka niedokrwienia)
- Wybór procedury nieinwazyjnej powinien być uzależniony od:
- prawdopodobieństwa choroby wieńcowej ze zwężeniem w ocenie wstępnej
- kwalifikacji pacjenta do odpowiedniego badania
- ryzyka związanego z badaniem
- wyposażenia dostępnego na miejscu i wiedzy specjalistycznej personelu lokalnej placówki.
- Diagnostykę niedokrwienia należy przeprowadzić za pomocą obrazowania czynnościowego szczególnie w przypadkach umiarkowanego prawdopodobieństwa przy wstępnej ocenie.2
- Nie można co prawda uwidocznić bezpośrednio zwężeń wieńcowych, ale można stwierdzić ich wpływ na perfuzję i/lub kurczliwość mięśnia sercowego w warunkach obciążenia fizycznego lub farmakologicznego.
- Dostępne są echokardiografia wysiłkowa (stress ECHO), scyntygrafia mięśnia sercowegom RM (rezonans magnetyczny) i tomografia komputerowa naczyń wieńcowych (angio-TK).2
- Procedury te są porównywalne pod względem wartości diagnostycznej niedokrwienia i dlatego powinny być wybierane przede wszystkim w zależności od dostępności, lokalnego doświadczenia i preferencji pacjenta:
- czułość i swoistość 80–90%.
Echokardiografia wysiłkowa (próba dobutaminowa, stress ECHO)
- Najczęściej stosowana procedura obrazowania czynnościowego; echokardiografia wysiłkowa może być wykonywana przez praktykujących w rejonie kardiologów.
- Obciążenie jest wytwarzane ergometrycznie lub z użyciem leków (dobutamina).
- Niedokrwienie jest dokumentowane poprzez rejestrację zaburzeń ruchomości ścian w warunkach obciążenia.
- Lokalizacja i zakres zaburzeń ruchomości ścian są rejestrowane w 16–segmentowym modelu lewej komory.
- W celu zwiększenia dokładności diagnostycznej zaleca się stosowanie dożylnych środków kontrastowych (słabo rozpuszczalnych w osoczu mikropęchrzyków gazu).2
Tomografia emisyjna pojedynczych fotonów (single photon emission computed tomography - SPECT)
- Uwidocznienie zmniejszenia perfuzji pod wpływem obciążenia (ergometrycznego lub farmakologicznego) po wstrzyknięciu substancji radioaktywnej.
- Do oceny stopnia zaburzeń perfuzji służy tzw. klasyfikacja SDS (summed difference score – różnica sumy punktów pomiędzy badaniem wysiłkowym i badaniem w spoczynku).
- Im wyższy SDS, tym bardziej nasilone zaburzenia perfuzji.
- Ponadto rejestruje się frakcję wyrzutową lewej komory w warunkach obciążenia i w spoczynku.
Pozytonowa tomografia emisyjna (positron emission tomography - PET)2
- Pozwala na dokładną nieinwazyjną ilościową ocenę ukrwienia (perfuzji) i procesów metabolicznych serca.
- W połączeniu z tomografią komputerową (PET-CT) dostarcza wiarygodnych danych bez konieczności wydłużania czasu napromieniania.
RM serca
- Wykrywanie zaburzeń perfuzji i kurczliwości w warunkach obciążenia lekowego (adenozyną lub dobutaminą).
- Ocena perfuzji po wstrzyknięciu środka kontrastowego zawierającego gadolin.
- Obrazowanie naczyń wieńcowych jest teoretycznie możliwe, ale na razie nie uzyskano jeszcze wystarczającej rozdzielczości obrazu, która umożliwiałaby jego klinicznie istotne zastosowanie.
TK naczyń wieńcowych (angio–TK naczyń wieńcowych i wskaźnik uwapnienia)
- Badanie TK (tomografia komputerowa) serca może być opcją pozwalającą wykluczyć chorobę wieńcową jako przyczyny objawów w sytuacji, gdy jej prawdopodobieństwo w ramach wstępnej oceny określono jako niskie (wysoka ujemna wartość predykcyjna). Ekspozycja na znaczne promieniowanie przemawia jednak przeciwko stosowaniu TK w obszarze o niskim prawdopodobieństwie chorobowości.
- W przyszłości chorobę wieńcową ze zwężeniem naczynia być może łatwiej będzie lokalizować w badaniu obrazowym naczyń wieńcowych metodą angiografii TK, co może też wpłynąć na zmniejszenie liczby zabiegów koronarografii.
- Często trudno jest dokładnie ocenić stopień zaawansowania wykrytych zwężeń.
- Ustalenie całkowitego zakresu zwapnień w naczyniach wieńcowych poprzez określenie wskaźnika uwapnienia (wskaźnik Agatstona, calcium score) o znaczeniu prognostycznym.
Koronarografia
- W przeciwieństwie do OZW inwazyjna koronarografia nie jest na ogół częścią podstawowej diagnostyki przy podejrzeniu PZW.
- Koronarografię należy proponować ze względów prognostycznych jako element planowania leczenia tylko wtedy, gdy pacjent wyraża chęć poddania się operacji wszczepienia by–passów (CABG).
- Natychmiastową strategię inwazyjną można rozważyć tylko w przypadkach wysokiego klinicznego prawdopodobieństwa choroby wieńcowej i opornych na leczenie, ciężkich objawów występujących nawet przy niewielkim wysiłku fizycznym.
- Nie należy wykonywać koronarografii:
- Przy niskim prawdopodobieństwie choroby wieńcowej ze zwężeniem.
- Przy umiarkowanym prawdopodobieństwie choroby wieńcowej ze zwężeniem, jeżeli nie potwierdzono niedokrwienia metodami diagnostyki nieinwazyjnej.
- Przy wysokim obciążeniu chorobami współwystępującymi, gdy ryzyko wykonania koronarografii jest większe niż korzyść z potwierdzenia rozpoznania i wynikających z niego działań terapeutycznych.
- U pacjentów bez wskazań objawowych, którzy po konsultacji nie chcą poddać się operacji wszczepienia by–passów z przyczyn rokowniczych.
- Należy zalecić wykonanie koronarografii:
- U pacjentów z wysoce prawdopodobnym podejrzeniem choroby wieńcowej ze zwężeniem po wykonaniu diagnostyki nieinwazyjnej, którzy po konsultacji są gotowi poddać się operacji wszczepienia by-passów ze wskazań rokowniczych.
- U pacjentów z wysoce prawdopodobnym podejrzeniem choroby wieńcowej ze zwężeniem po wykonaniu diagnostyki nieinwazyjnej, u których objawy utrzymują się mimo optymalnego leczenia zachowawczego (wskazanie objawowe).
- szczególnie w grupie chorych, u których objawy występują przy niskim poziomie wysiłku2
- W przypadku podjęcia decyzji o wykonaniu koronarografii, zaleca się dostęp przez tętnicę promieniową.2
- Przed wyborem metody rewaskularyzacji zaleca się pomiar cząstkowej rezerwy wieńcowej (fractional flow reserve - FFR) z rozkurczową oceną gradientu ciśnienia (instantaneous wave-free ratio - iFR).2
Wskazania do hospitalizacji
- Podejrzenie ostrego zespołu wieńcowego (OZW).
- Ból w klatce piersiowej z podejrzeniem innej ostrej choroby zagrażającej życiu.
Lista kontrolna dotycząca skierowania
Ból w klatce piersiowej
- Cel skierowania
- Diagnostyka potwierdzająca? Leczenie?
- Wywiad lekarski
- Ból w klatce piersiowej: początek, czas trwania? Postęp? Lokalizacja, promieniowanie? Czynniki ryzyka? Związany z wysiłkiem/obciążeniem?
- Objawy towarzyszące: duszność? Gorączka? Kaszel? Plwocina? Ból brzucha?
- Historia chorób i choroby współwystępujące? Wcześniej rozpoznana choroba naczyniowa? Czynniki ryzyka sercowo–naczyniowego? Depresja/zaburzenie somatyzacyjne?
- Leki?
- Badanie fizykalne
- Ogólny stan fizyczny? Zaburzenia świadomości? Zimne poty?
- Ciśnienie tętnicze, tętno, rytm serca?
- Poszerzenie żył szyjnych? Obrzęki?
- Szmery nad sercem? Zastój w krążeniu płucnym?
- Badania uzupełniające:
- EKG.
- Ewentualnie szybki test troponinowy.
Leczenie
Cele leczenia
- Główne cele leczenia PZW:
- obniżenie śmiertelności
- zmniejszenie zachorowalności na choroby układu krążenia (uniknięcie OZW, zawału mięśnia sercowego, przewlekłej niewydolności serca)
- utrzymanie wydolności fizycznej
- poprawa jakości życia związanej z chorobą, m.in. poprzez:
- zmniejszenie częstości występowania objawów
- zmniejszenie nasilenia innych dolegliwości somatycznych i psychicznych.
Ogólne informacje o leczeniu
- Zalecane jest multidyscyplinarne podejcie do podejście do procesu leczenia, włącznie z podjęciem działań zmierzających do zmiany stylu życia, niezależnie od prowadzonej farmakoterapii.2
- Opcje leczenia:
- Zmiana stylu życia
- aktywność fizyczna
- odżywianie i masa ciała
- zaprzestanie palenia papierosów i e-papierosów.2
- Farmakoterapia
- hamowanie agregacji płytek krwi
- terapia statynami
- leki przeciwdławicowe.
- Rewaskularyzacja
- Opcja jako terapia objawowa w opornej dławicy piersiowej przy optymalnej farmakoterapii.
- W chorobie wielonaczyniowej – operacja wszczepienia by–passów (CABG) w celu poprawy rokowania.
- Leczenie chorób współistniejących.
- Poprawa czynników psychospołecznych.
- Dalsze działania - patrz niżej.
- Zmiana stylu życia
- Zobacz także:
Konsultacje i wspólne podejmowanie decyzji
- Nawet jeśli wskazanie do leczenia jest ewidentne z punktu widzenia lekarza, należy przeprowadzić konsultacje z pacjente w celu wspólnego podejmowania decyzji, z zachowaniem następujących podstawowych zasad:
- Poinformować pacjenta o konieczności podjęcia decyzji o terapii i zaoferować mu możliwość włączenia się w proces decyzyjny.
- Przekazać zrozumiałe informacje o opcjach leczenia oraz korzyściach i zagrożeniach z nimi związanych.
- Aktywnie dopytywać, czy pacjent wszystko zrozumiał.
- Uwzględnić oczekiwania, cele i preferencje pacjentów.
- Osiągnąć porozumienie w sprawie konkretnego planu leczenia.
- Zaangażować członków rodziny w akceptację uzgodnionych terapii oraz przestrzeganie i stosowanie się do zaleceń lekarskich (adherence).2
Zmiana stylu życia
Doradztwo w zakresie stylu życia ukierunkowane na zachowanie pacjenta
- Poradnictwo powinno obejmować dążenie do samomotywacji pacjenta z ukierunkowaniem na zmianę wzorców zachowań.
- Obejmują one:
- wezwanie do podjęcia decyzji w sprawie zmiany zachowania
- ustalenie wspólnego celu szczegółowego
- sprawdzanie realizacji wcześniej wyznaczonych celów
- wezwania do samoobserwacji zachowania
- przekazywanie informacji zwrotnych dotyczących zachowania.
Aktywność fizyczna
- Regularna aktywność fizyczna ma korzystny wpływ na czynniki ryzyka sercowo–naczyniowego i pomaga chorym lepiej radzić sobie z niepewnością spowodowaną chorobą serca.2,20-22
- Elementy programu ćwiczeń fizycznych w ramach wtórnej profilaktyki choroby wieńcowej:
- Tlenowe ćwiczenia wytrzymałościowe (np. marsz, nordic walking, jazda na rowerze, pływanie) o niskiej lub umiarkowanej intensywności powinny być wykonywane >5 razy w tygodniu przez minimum 30-60 minut dziennie lub 75-150 minut tygodniowo w przypadku ćwiczeń o dużej intensywności.2
- Dodatkowo 2 do 3 razy w tygodniu należy wykonywać dynamiczny trening siłowy.
- Należy unikać obciążeń siłowych o znacznej komponencie izometrycznej.
- Samokontrola przez pacjenta stopnia zmęczenia podczas wysiłku fizycznego, np. przy użyciu skali Borga lub zmodyfikowanej skali Borga.
- Przykłady intensywności treningu:23
- wysiłek lekki: spacer, lekkie prace domowe (10–11 w skali Borga)
- wysiłek umiarkowany: szybki chód, wolna jazda na rowerze, aerobik wodny (12–13 w skali Borga)
- wysiłek ciężki: jogging, jazda na rowerze z prędkością >15 km/h, szybkie pływanie po torach (14–16 w skali Borga).
- Należy rozważyć rehabilitację kardiologiczną w warunkach domowych i wykorzystanie mobilnych aplikacji do ćwiczeń, w celu zwiększenia szansy na przestrzeganie zaleceń dotyczących aktywności fizycznej w długim okresie czasu.2
Odżywianie
- Pacjentom z chorobą wieńcową należy zalecać zdrową, zbilansowaną dietę (o dużej zawartości błonnika, bogatą w owoce i warzywa, o małej zawartości tłuszczów nasyconych).
- Należy zadbać o zróżnicowane odżywianie, wprowadzając elementy diety śródziemnomorskiej.
- Codziennie:
- Produkty zbożowe: 1–2 porcje na posiłek w postaci pieczywa, makaronu, ryżu, kuskusu itp. (najlepiej produkty pełnoziarniste).
- Warzywa: co najmniej 200 g24, 2 lub więcej porcji na posiłek, co najmniej jedna porcja dziennie w postaci surowej.
- Owoce: co najmniej 200 g24, 1–2 porcje na posiłek, np. jako deser, urozmaicone.
- Płyny: w miarę możliwości 1,5–2l wody i niesłodzonej herbaty dziennie.
- Nabiał: 2 porcje dziennie, najlepiej jako produkty niskotłuszczowe, np. jogurt lub ser.
- Oliwa z oliwek: składnik podstawowy, bogaty w jednonienasycone kwasy tłuszczowe jako źródło tłuszczów.
- Oliwki, orzechy, ziarna/nasiona: np. jako źródło tłuszczów, białka, witamin.
- Przyprawy, zioła, czosnek, cebula: jako przyprawy dla urozmaicenia smaku i zmniejszenia spożycia soli.
- Alkohol: umiarkowane spożycie do 1 kieliszka wina dziennie (kobiety) lub 2 kieliszków (mężczyźni) do posiłków.
- Co tydzień:
- Ryby/owoce morza: 2 lub więcej porcji.
- Białe mięso: 2 porcje.
- Jajka: 2–4 porcje (w tym gotowane i pieczone).
- Czerwone mięso: mniej niż 2 porcje, najlepiej cienko pokrojone; mięso przetworzone przemysłowo (np. kiełbasa, dania gotowe) – mniej niż 1 porcja.
- Ziemniaki: do 3 porcji, w miarę możliwości świeżo przyrządzone.
- Brak danych z kontrolowanych badań dotyczących diety wyłącznie wegetariańskiej, wegańskiej lub w inny sposób selektywnej u pacjentów z przewlekłą chorobą wieńcową.
Masa ciała
- Zaleca się redukcję nadwagi lub otyłość oraz utrzymywanie BMI na poziomie 18,5-25 kg/m2.2
Palenie papierosów i e-papierosów2
- Zaprzestanie palenia papierosów i e-papierosów jest co najmniej tak samo istotne z punktu widzenia rokowania jak farmakoterapia.25
- Wszystkich pacjentów należy pytać o używanie nikotyny i je dokumentować.
- U wszystkich pacjentów należy dążyć do całkowitej abstynencji od palenia zarówno czynnego, jak i biernego.
- Zaprzestanie palenia papierosów i e-papierosów jest najbardziej racjonalnym pod względem kosztów środkiem zapobiegawczym.26
- W zaprzestaniu palenia papierosów i e-papierosów pomagają różne formy terapii, w razie potrzeby także:
- procedury niskoprogowe (krótkie poradnictwo, poradnictwo telefoniczne, procedury z wykorzystaniem internetu lub smartfona)
- interwencje psychoterapeutyczne
- farmakoterapia.
- Nie należy zalecać e–papierosów jako środka wspomagającego rzucenie palenia papierosów lub ograniczającego szkody zdrowotne.
Alkohol
- Należy zalecić zaprzestanie spożywania alkoholu.2
- U pacjentów spożywających alkohol, należy ograniczyć go do <100 g na tydzień (15g/dzień).
- Uwaga: Przy braku wprowadzenia działań modyfikujących dotychczasowy styl życia, nawet umiarkowane spożycie alkoholu ma działanie niekorzystne dla układu sercowo-naczyniowego!
Farmakoterapia - informacje ogólne
- Zalecane jest stosowanie uproszczonych schematów lekowych (fixed-dose combination - FDC, polypill, preparaty złożone)2, np. statyna+ASA lub ACE-inhibitor+beta-bloker
- Ogólny schemat leczenia pacjenta z PZW2:
- ASA 75-100 mg lub klopidogrel lub połączenia tych leków z innymi lekami przeciwpłytkowymi (patrz niżej)
- Statyna (atorwastatyna/rosuwastatyna) w maksymalnej dawce lub statyna/ezetynib lub statyna/ezetynib/inhibitor PSK9 lub kombinacje z kwasem bempediowym (patrz niżej)
- U większości pacjentów z PZW, ze względu na współwystępowanie innych chorób, należy stosować ACE-inhibitor/sartan lub ARNI (walsartan/sakubitril) - patrz niżej
- Beta-bloker lub/i antagonista wapnia lub/i długodziałający azotan lub/i ranolazyna (patrz niżej)
- Beta-blokery są lekami obowiązkowymi u pacjentów z niewydolnością serca i podwyższoną częstością akcji serca (HR>70/min)
- U każego pacjenta z PZW i cukrzycą, niezależnie od zaleceń diabetologicznych i wyrównania cukrzycy, zaleca się stosowanie flozyny lub agonisty GLP-1.
- Agonistę GLP-1 (semaglutyd) należy rozważyć u pacjenta z PZW bez cukrzycy z nadwagą/otyłością w celu redukcji ryzyka zgonu, zawału i udaru.
- U pacjentów z PZW i miażdżycą należy rozważyć zastosowanie małej dawki kolchicyny (0,5 mg/dobę) w celu zmniejszenia ryzyka zawału, udaru lub potrzeby rewaskularyzacji.
Farmakoterapia, która korzystnie wpływa na rokowanie
Leki przeciwpłytkowe i doustne leki przeciwkrzepliwe
- Leczenie przeciwpłytkowe należy proponować wszystkim pacjentom z przewlekłym zespołem wieńcowym (PZW).2
- W długoterminowej profilaktyce najlepiej przebadanym lekiem jest ASA (kwas acetylosalicylowy).23
- klopidogrel stanowi skuteczną i bezpieczną alternatywę w przypadku nietolerancji lub działań niepożądanych ASA. 7
- Pacjenci z PZW i wskazaniem do doustnego leczenia przeciwkrzepliwego (np. migotanie przedsionków) nie powinni przyjmować dodatkowej terapii przeciwpłytkowej.
- U pacjentów po implantacji stentu i ze wskazaniem do leczenia przeciwkrzepliwego (np. migotanie przedsionków) stosuje się przez określony czas terapię potrójną (ASA + klopidogrel + doustny antykoagulant).2
- Po operacji wszczepienia by–passów (CABG), zalecana jest ciągła, trwająca do końca życia, monoterapia ASA w dawce 75-100 mg, o ile nie ma przeciwskazań.
- U pacjentów ze zwiększonym ryzykiem niedorożności pomostu naczyniowego, można rozważyć stosowanie podwójnej terapii przeciwpłytkowej (dual antiplatelet therapy - DAPT).2
- U pacjentów ze zwiększonym ryzykiem krwawienia podczas terapii skojarzonej (lek przeciwpłytkowy i/lub doustny antykoagulant), zaleca się stosowanie inhibitora pompy protonowej (IPP).2
- Stosowanie IPP należy rozważyć w przypadku stosowania takich leków również w monoterapii, biorąc pod uwagę potencjalne ryzyko wystąpienia u pacjenta krwawienia z przewodu pokarmowego.2
- Szczegółowe zalecenia przedstawiono w artykułach:
Postępowanie u pacjentów z przewlekłym zespołem wieńcowym po PCI i brakiem wskazań do leczenia przeciwkrzepliwego7
- Rekomendowanym standardowym postępowaniem u pajentów z PCI z założeniem stentu jest stosowanie:
- podwójnej terapii przeciwpłytkowej (dual antiplatelet therapy - DAPT) przez 6 miesięcy
- ASA 75-100 mg raz na dobę + klopidogrel 75 mg raz na dobę przez 6 miesięcy
- następnie:
- ASA 75-100 mg raz na dobę lub klopidogrel 75 mg raz na dobę długoterminowo
- podwójnej terapii przeciwpłytkowej (dual antiplatelet therapy - DAPT) przez 6 miesięcy
- Wskazana jest ocena ryzyka krwawienia z jednoczesną oceną zagrożenia niedokrwienia mięśnia sercowego
- Niskie ryzyko krwawienia + wysokie ryzyko niedokrwienia
- Należy stosować DAPT: ASA 75-100 mg raz na dobę + klopidogrel 75 mg raz na dobę przez 6 miesięcy lub u pacjentów z wysokiem ryzykiem zakrzepicy można rozważyć, zamiast klopidogrelu, tikagrelor 60 mg 2 razy na dobę (lub alternatywnie prasugrel 10 mg 1 x na dobę) przez 1-6 miesięcy
- Po 6. miesiącach, należy rozważyć stosowanie:
- DAPT: ASA 75-100 mg raz na dobę + klopidogrel 75 mg raz na dobę (lub alternatywnie tikagrelor 60 mg 2 x na dobę) lub
- ASA 75-100 mg raz na dobę + riwaroksaban 2,5 mg 2 razy na dobę (lub alternatywnie prasugrel 10 mg 1 x na dobę) lub
- można rozważyć tikagrelor 90 mg 2 razy na dobę w monoterapii
- Niskie ryzyko krwawienia + niskie ryzyko niedokrwienia
- Należy stosować ASA 75-100 mg raz na dobę lub klopidogrel 75 mg raz na dobę
- Można rozważyć DAPT: ASA 75-100 mg raz na dobę + klopidogrel 75 mg raz na dobę przez 1-3 miesięcy
- Wysokie ryzyko krwawienia + niskie ryzyko niedokrwienia:
- Należy stosować DAPT: ASA 75-100 mg raz na dobę + klopidogrel 75 mg raz na dobę przez 1-3 miesięcy
- po 3 miesiącach należy stosować: ASA 75-100 mg raz na dobę lub klopidogrel 75 mg raz na dobę
- Niskie ryzyko krwawienia + wysokie ryzyko niedokrwienia
Postępowanie u pacjentów z przewlekłym zespołem wieńcowym po PCI i wskazaniami do leczenia przeciwkrzepliwego2
- W leczeniu przeciwkrzepliwym dostępne są następujące leki doustne (oral anticoagulant - OAC):
- leki będące antagonistami wit. K (VKA), np. acenokumarol, warfaryna
- leki niebędące antagonistami wit. K (NOAC), np. riwaroksaban, dabigatran, apiksaban, endoksaban
- W przypadku konieczności długotrwałego stosowania leczenia przeciwkrzepliwego (np. migotanie przedsionków), zaleca się dożywotnie stosowanie OAC w monoterapii.
- najlepiej leków przeciwkrzepliwych niebędących antagonistami wit. K u pacjentów bez przeciwwskazań
- U pacjentów po PCI ze wskazaniami do OAC, należy na początku leczenia podać małą dawkę ASA w połączeniu z OAC i klopidogrelem (terapia potrójna).
- podczas stosowania potrójnej terapii z ASA, nie zaleca się stosowania prasugrelu i tikagreloru
- Po PCI przeprowadzonym bez powikłań, u pacjentów z PZW zaleca się:
- wczesne zaprzestanie podawania ASA (≤1 tydzień)
- Należy rozważyć kontynuację ASA >1 miesiąc w połączeniu z OAC i klopidogrelem u pacjentów z wysokim ryzykiem niedokrwienia i anatomicznymi/okołozabiegowymi czynnikami ryzyka (np. suboptymalne umieszczenie stentu, całkowita niedrożność naczynia, długość stentu >60 mm).
- kontynuację stosowania OAC + klopidogrel
- do 6 miesięcy u pacjentów z niskim ryzykiem niedokrwienia
- do 12 miesięcy u pacjentów z wysokim ryzykiem niedokrwienia
- w przypadku, gdy ryzyko krwawienia przeważa nad ryzykiem wystąpienia zakrzepicy w stencie, należy rozważć zmniejszenie dawki riwaroksabanu z 20 mg na 15 mg na dobę oraz dabigatranu ze 150 mg na 110 mg 2 razy na dobę.
- podczas takiej terapii należy utrzymywać wskaźnik INR na dolnym poziomie zalecanego zakresu terapeutycznego
- a następnie OAC w monoterapii, jeśli jest konieczne
- wczesne zaprzestanie podawania ASA (≤1 tydzień)
Terapia obniżająca poziom lipidów (hipolipemizująca)
- Wszystkim pacjentom z PZW należy zaoferować leczenie statyną, niezależnie od wyjściowego stężenia lipidów.2
- Obecnie wśród ekspertów nie ma pełnej zgody co do sposobu podawania statyn.
- Obowiązujący w Polsce konsensus sześciu towarzystw medycznych z 2021 roku24 zaleca stosowanie statyn o wysokiej intensywności w najwyższej tolerowanej przez pacjenta dawce, tak aby osiągnąć:
- Złożony poziom redukcji stężenia cholesterolu LDL, właściwy dla jego poziomu ryzyka sercowo–naczyniowego oraz
- ≥50% redukcję w stosunku do wartości wyjściowej.
- Stopień ryzyka sercowo–naczyniowego a wartość docelowa cholesterolu LDL:24
-
- ekstremalne: <40 mg/dl (1 mmol/l)
- bardzo duże: <55 mg/dl (1,4 mmol/l)
- duże: <70 mg/dl (1,8 mmol/l)
- umiarkowane: <100 mg/dl (2,6 mmol/l)
- małe: <115 mg/dl (3,0 mmol/l).
-
- Statyny w wysokiej dawce (np. atorwastatyna 80 mg) we wtórnej profilaktyce kardiologicznej obniżają wskaźniki ponownego zawału, a także śmiertelność ogólną i sercowo–naczyniową27. Uwaga: Statyny mogą wywoływać działania niepożądane, zwłaszcza u osób w podeszłym wieku. 28-31
- Z reguły podawanie statyny w wysokiej dawce jest zasadne.
- Nie są wymagane żadne dalsze oznaczenia lipidów ani korekty.
- Inne leki obniżające poziom lipidów należy rozważyć tylko w przypadku częściowej lub całkowitej nietolerancji statyn.
- W wytycznych ESC z 2024 roku2 zaleca się jeszcze bardziej radykalne obniżenie LDL niż dotychczas (wartość docelowa <55 mg/dl (1,4 mmol/l) i redukcja ≥50% w stosunku do wartości wyjściowej).
- Ponieważ tej wartości docelowej często nie udaje się osiągnąć w terapii wyłącznie statyną, ESC zaleca dodatkowo podawanie ezetymibu i/lub kwasu bempediowego lub dostępnych w Polsce w ramach programu lekowego – inhibitorów PCSK9 (ewolokumab i alirokumab).2,32
- U chorych nie tolerujących leczenia statynami, u których nie można osiągnąć docelowych wartości LDL podczas stosowania ezetynibu, należy rozważyć dołączenie kwasu bempediowego.2,33
- U pacjentów z nawracającymi zdarzeniami zakrzepowymi na tle miażdżycowym (również innego typu niż pierwsze zdarzenie) pomimo przyjmowania maksymalnie tolerowanej dawki statyny, można rozważyć ustalenie bardziej ambitnego celu wartości docelowej LDL<40 mg/dl (<1,0 mmol/l). 2
- Ponieważ tej wartości docelowej często nie udaje się osiągnąć w terapii wyłącznie statyną, ESC zaleca dodatkowo podawanie ezetymibu i/lub kwasu bempediowego lub dostępnych w Polsce w ramach programu lekowego – inhibitorów PCSK9 (ewolokumab i alirokumab).2,32
- Dawki statyn i ich wpływ na poziom LDL:
- Umiarkowana dawka (obniżenie poziomu LDL o 30–49%)
- atorwastatyna 10–20 mg24
- rosuwastatyna 5–10 mg
- simwastatyna 20–40 mg
- prawastatyna 40–80 mg
- lowastatyna 40 mg.
- Wysoka dawka (redukcja LDL ≥50%)
- atorwastatyna 40–80 mg
- rosuwastatyna 20–40 mg.
- Umiarkowana dawka (obniżenie poziomu LDL o 30–49%)
- Wytyczne ESC 2024 rekomendują stosowanie u pacjentów z PZW atorwastatyny i rosuwastatyny.2
- Trzecia najsilniejsza statyna to pitawastatyna, która pojawiła się na polskim rynku w 2021 roku.24
- Średnia redukcja cholesterolu LDL przez różne terapie/skojarzenia leków:
- umiarkowane dawki statyny: 30%
- statyna w wysokiej dawce: 50%
- statyna w wysokiej dawce + inhibitor wchłaniania cholesterolu (ezetymib): 65%
- inhibitor PCSK9: 60%
- statyna w wysokiej dawce + inhibitor PCSK9: 75%
- statyna w wysokiej dawce + inhibitor wchłaniania cholesterolu (ezetymib) + inhibitor PCSK9: 85%.
Farmakoterapia, która korzystnie wpływa na objawy
- Leczenie przeciwdławicowe obejmuje możliwość szybkiego, doraźnego leczenia napadu dławicy piersiowej przez pacjenta, jak również – w razie potrzeby – dłuższego leczenia chroniącego przed napadami dławicy piersiowej.
- Zaleca się indywidualne dostosowanie leczenia przeciwdławicowego do każdego pacjenta z uwzględnieniem ich tolerancji, chorób wspóistniejących i innych przyjmowanych leków.2
Szybko działające azotany (nitraty)
- Należy zapewnić dostęp do szybko działającego azotanu do stosowania doraźnego w ataku dławicy piersiowej.
- Lek w postaci aerozolu ma nieco szybszy początek działania niż lek do podawania podjęzykowego.2
- Dostępne są preparaty z nitrogliceryną oraz nitrogliceryną i tetraazotanem pentaerytrytylu.
- Lek najlepiej stosować w pozycji siedzącej lub leżącej, aby uniknąć omdlenia.2
- Zaletą doraźnego stosowania szybko działających azotanów jest również to, że nie obserwowano rozwoju tolerancji na te leki.
Długodziałające leki przeciwdławicowe
- Nie zdefiniowano optymalnej terapii zapobiegającej niedokrwieniu, dlatego należy ją dostosować indywidualnie, z uwzględnieniem chorób współistniejących.2
- Beta–blokery i antagoniści kanału wapniowego zostały najlepiej przebadane i są zalecane jako terapia pierwszego rzutu.2
- Zastosowanie innych substancji należy rozważyć w przypadku nietolerancji lub nieskuteczności beta–blokerów lub antagonistów kanału wapniowego.
- Iwabradyna zmniejsza częstotliwość rytmu zatokowego i jest opcją zalecaną szczególnie u pacjentów z przyspieszonym rytmem zatokowym i niewydolnością serca.34
- Tę substancję można stosować w przypadku nietolerancji beta–blokerów lub przeciwskazań do ich stosowania.
- Należy rozważyć jej stosowanie we wczesnej fazie leczenia, jako dodatkowego leku u pacjentów z niewydolnością serca i LVEF<40% oraz utrzymującymi się objawami dławicowymi.2
- Nie należy stosować iwabradyny u pacjentów z przewlekłym zespołem wieńcowym i LVEF>40% oraz bez objawów niewydolności serca.2
- Nie należy łączyć iwabradyny z niedihydropirydynowymi antagonistami wapnia (werapamil, diltiazem) oraz innymi silnymi inhibitorami CYP3A4.2
- Ranolazyna jest opcją leczenia w przypadku braku odpowiedzi na inne leki przeciwdławicowe.2
- Ranolazyna jest wskazana tylko u osób, u których objawy nie ustępują w wystarczającym stopniu podczas stosowania beta-blokerów lub występuje nietolerancja beta–blokerów lub antagonistów kanałów wapniowych.
- Może być dodawana do terapii pacjentów objawowych leczonych beta-blokerami lub antagonistami wapnia lub stosowana jako jako lek pierwszego rzutu u wyselekcjonowanych pacjentów.2
- Dostępne są doniesienia o wydłużeniu odcinka QT i interakcjach z cytochromem P450.
- Ranolazyna jest wskazana tylko u osób, u których objawy nie ustępują w wystarczającym stopniu podczas stosowania beta-blokerów lub występuje nietolerancja beta–blokerów lub antagonistów kanałów wapniowych.
- Długodziałające nitraty należy rozważyć jako leczenie uzupełniające u pacjentów z utrzymującymi się objawami pomimo leczenia beta-blokerami i/lub antagonistami wapnia lub jako element początkowego leczenia u wybranych pacjentów.7
- U takich pacjentów można też rozważyć stosowanie trimetazydyny lub nikorandil.
- W przypadku stosowania długodziałających nitratów, należy rozważyć przerwy w ich przyjmowaniu lub zmniejszenie dawki, w celu zmniejszenia ryzyka rozwoju tolerancji.
- W przypadku przyjmowania azotanów, należy zachować ostrożność u mężczyzn stosujących inhibitory PDE-5, ze względu na możliwość wystąpienia hipotonii.7
- Nitratów nie należy stosować u pacjentów z kardiomiopatią przerostową.
- Iwabradyna zmniejsza częstotliwość rytmu zatokowego i jest opcją zalecaną szczególnie u pacjentów z przyspieszonym rytmem zatokowym i niewydolnością serca.34
Farmakoterapia współwystępujących chorób sercowo–naczyniowych
- Choroby współwystępujące, takie jak nadciśnienie tętnicze, migotanie przedsionków oraz niewydolność serca, należy leczyć zgodnie z odnośnymi wytycznymi, przy czym szczególnie istotne są inhibitory ACE/receptora AT1 (sartany) oraz beta–blokery.
- Choroba wieńcowa sama w sobie nie jest jednak wskazaniem do stosowania inhibitorów ACE/receptora AT1 (sartanów).
- Leki blokujące układ RAA należy stosować u osób z PZW, jeśli współwystępuje2:
- niewydolność serca z obniżoną frakcją wyrzutową lewej komory (LVEF) oraz po zawale mięśnia sercowego z uszkodzeniem lewej komory
- nadciśnienie tętnicze
- cukrzyca i/lub uszkodzenie nerek
- wysokie ryzyko sercowo-naczyniowe
- po PCI z powodu STEMI/NSTEMI niezależnie od wartości LVEF
- W podgrupie pacjentów z niewydolnością serca i LVEF ≤35% należy rozważyć zmianę ACE-inhibitora na ARNI - połączenie inhibitora receptora angiotensyny II (walsartan) z inhibitorem neprylizyny (sakubitril).2
- Leki blokujące układ RAA należy stosować u osób z PZW, jeśli współwystępuje2:
Leki hipoglikemizujące
- Aby mniejszyć ryzyko wystąpienia poważnych zdarzeń sercowo-naczyniowych, u pacjentów z PZW i cukrzycą typu 2 należy stosować inhibitory SGLT2 i/lub agonistów receptora GLP-1, niezależnie od wyjściowego i docelowego poziomu HbA1C oraz niezależnie od innych stosowanych leków hipoglikemizujących.
- Należy rozważyć stosowanie agonisty receptora GLP-1 (semaglutyd) u pacjentów z PZW bez cukrzycy z nadwagą (BMI>27 kg/m2) lub otyłością, w celu zmniejszenia śmiertelności z przyczyn sercowo-naczyniowych, zawału oraz udaru.2
Intensyfikacja leczenia farmakologicznego
- W wybranych grupach pacjentów należy podjąć decyzję o bardziej intensywnym leczeniu, w zależności od występowania2:
- czynników silnie zwiększających ryzyko niedokrwienne, np. u pacjentów z:
- cukrzycą wymagającą leczenia
- wywiadem nawracających zawałów mięśnia sercowego
- miażdżycą wielołożyskową
- wielonaczyniową chorobą wieńcową
- przedwczesną miażdżycą (<45 r.ż.) lub miażdżycą przyspieszoną (nowe zmiany <2 lat) w naczyniach wieńcowych
- przewlekłym stanem zapalnym i/lub protrombotycznym (HIV, toczeń, reumatoidalne zapalenie stawów, zespół antyfosfolipidowy)
- czynników zabiegowych decydujących o przedłużeniu leczenia przeciwpłytkowego, np.:
- co najmniej 3 stenty zaimplantowane
- co najmniej 3 leczone zmiany wewnątrznaczyniowe
- długośc stentowanego odcinka >6 cm
- złożona rewaskularyzacja w wywiadzie (pień, bifurkacje naczyń leczone ≥2 stentami, przewlekłe zamknięcie naczynia, stentowanie jedynego drożnego naczynia)
- w wywiadzie zakrzepica w stencie dokonana na leczeniu przeciwpłytkowym.
- czynników silnie zwiększających ryzyko niedokrwienne, np. u pacjentów z:
Rewaskularyzacja
- O ile korzystny wpływ rewaskularyzacji na rokowanie w OZW jest dobrze udokumentowany, o tyle w PZW kwestia ta od dawna budzi kontrowersje.35
- W badaniach populacyjnych i metaanalizach z ostatnich lat wykazano, że rutynowa rewaskularyzacja nie przynosiła poprawy wskaźników przeżycia w porównaniu z samym leczeniem farmakologicznym.36-39
- Wniosek ten ponownie potwierdzono w badaniu ISCHEMIA w badanej populacji z umiarkowanym lub rozległym niedokrwieniem.40
- Z kolei w większości badań wykazano korzystny wpływ rewaskularyzacji na objawy, tj. złagodzenie dolegliwości związanych z dławicą piersiową.38,41-42
- Badanie ORBITA (randomizacja: PCI lub rzekoma PCI) wskazuje na możliwy komponent placebo w objawowej poprawie po PCI.43-44
- Rutynowa rewaskularyzacja nie jest obecnie wskazana u większości pacjentów z PZW, ale jest opcją w następujących przypadkach:45
- Wskazanie objawowe z opornymi na leczenie dolegliwościami przy optymalnej farmakoterapii.
- Wskazania rokownicze w grupach wysokiego ryzyka (które na dodatek są wykluczone z wielu badań):45
- zwężenie pnia głównego >50%
- choroba obejmująca 2 lub 3 naczynia z niską frakcją wyrzutową lewej komory <35%
- tylko jedno drożne naczynie wieńcowe ze zwężeniem >50%.
- Pacjentom należy wyjaśnić, czy interwencję rozważa się głównie ze względu na korzyści rokownicze, czy też głównie ze względu na przewidywany korzystny wpływ na objawy.46-48
- Decyzja o rodzaju interwencji (PCI lub wszczepienie by–passów) powinna być poprzedzona omówieniem indywidualnego profilu ryzyka i korzyści w zespole sercowym, złożonym z kardiologów i kardiochirurgów (Heart Team), przy czym ważnymi kryteriami są:45
- złożoność uwidocznionych zmian w naczyniach wieńcowych
- ryzyko związane z interwencją
- choroby współwystępujące o podłożu kardiologicznym i niekardiologicznym
- preferencje pacjentów.
- Choroba wielonaczyniowa, złożoność uwidocznionych zmian w naczyniach wieńcowych oraz cukrzyca to kryteria, które bardziej przemawiają za operacją wszczepienia by–passów (CABG) niż za PCI.45,49-51
Wskazania do rewaskularyzacji
- W przypadku objawów, których nie można odpowiednio leczyć zachowawczo (dławica piersiowa lub równoważne schorzenie), należy zaproponować rewaskularyzację, jeśli anatomia naczynia jest odpowiednia (po diagnostyce inwazyjnej).
- W przypadku choroby wielonaczyniowej lub zwężenia pnia głównego należy przeprowadzić konsultację z zespołem sercowym (Heart Team).
- W przypadku uwidocznienia złożonych zmian w naczyniach wieńcowych (wskaźnik SYNTAX) decyzję o proponowanej terapii należy podjąć w zespole sercowym.
- Pacjentom z cukrzycą i wielonaczyniową chorobą wieńcową należy zaproponować rewaskularyzację metodą pomostowania (CABG).
- Pacjentom z proksymalnym lub przyśrodkowym zwężeniem pnia głównego i wskaźnikiem SYNTAX ≤22 można proponować zarówno PCI, jak i operację pomostowania (CABG).
- Pacjentom ze zwężeniem pnia głównego w bifurkacji lub zwężeniem proksymalnego/środkowego pnia głównego i umiarkowaną wielonaczyniową chorobą wieńcową (wskaźnik SYNTAX od 23 do 32) należy proponować przede wszystkim operację pomostowania (CABG), a w drugiej kolejności PCI.
- Pacjentom ze zwężeniem pnia głównego i wielonaczyniową chorobą wieńcową (wskaźnik SYNTAX ≥33) należy zaproponować operację pomostowania (CABG).
Poprawa czynników psychospołecznych
- Stres psychospołeczny, depresja i lęk są związane z gorszym rokowaniem i utrudniają zmianę stylu życia oraz przestrzeganie zaleceń terapeutycznych.2,52
- W odpowiedzi na stres psychospołeczny, którego doświadcza pacjent, lekarze rodzinni mogą:
- Samodzielnie podjąć działania w ramach podstawowej opieki psychosomatycznej, takie jak:
- nauka radzenia sobie z chorobą
- terapia łagodnych i umiarkowanych objawów depresji i lęku.
- W razie dalszej potrzeby należy skierować pacjenta do specjalisty.
- Samodzielnie podjąć działania w ramach podstawowej opieki psychosomatycznej, takie jak:
- Pacjentom z przewlekłą chorobą wieńcową i obciążeniami psychospołecznymi należy w miarę możliwości proponować multimodalne interwencje behawioralne w celu poprawy dobrostanu psychospołecznego i wtórnej profilaktyki choroby wieńcowej:
- edukacja na temat zdrowego stylu życia
- ćwiczenia fizyczne
- interwencje psychologiczne ukierunkowane na ograniczenie psychospołecznych czynników ryzyka i pomoc w radzeniu sobie z chorobą.
Dalsze działania i dodatkowe rekomendacje
Szczepienia
- Pacjentom z PZW należy zalecić szczepienia2:
- corocznie przeciw grypie
- przeciw pneumokokom
- innym zakażeniom, np. COVID-19
Ocena jakości snu
- W przypadku występowania u pacjenta zespołu bezdechów obturacyjnych, należy rozpocząć odpowiednie leczenie.
Czynniki środowiskowe2
- Pacjentom z przewlekłym zespoem wieńcowym należy zalecić unikanie:
- biernego palenia
- hałasu
- zanieczyszczeń powietrza
Terapie komplementarne i alternatywne
- Nie należy stosować terapii komplementarnych/alternatywnych, takich jak fitoterapia, suplementy witaminowe czy preparaty z kwasami tłuszczowymi omega–3.
Przebieg, powikłania i rokowanie
Powikłania
- OZW/zawał mięśnia sercowego, wstrząs kardiogenny.
- Przewlekła niewydolność serca.
- Tachykardia komorowa, migotanie komór.
- Częstoskurcze nadkomorowe.
- Konieczność wszczepienia stymulatora serca (USS).
Przebieg i rokowanie
- Roczna śmiertelność: 1,2–2,4%.
- Mniej korzystny przebieg w przypadku:
- Upośledzenia czynności lewej komory i niewydolności serca.
- Choroby wielonaczyniowej.
- Proksymalnego zwężenia naczyń wieńcowych.
- Wyraźnego niedokrwienia
- Echokardiografia z obciążeniem dobutaminą: wysokie ryzyko przy zaburzeniach ruchomości ściany w ≥3 segmentach.
- RM z obciążeniem: wysokie ryzyko przy zaburzeniach ruchomości ściany w ≥3 segmentach lub zaburzeniach perfuzji w ≥2 segmentach.
- Scyntygrafia mięśnia sercowego: wysokie ryzyko, jeżeli obszar niedokrwienia zajmuje ≥10% mięśnia sercowego.
- Zmniejszona sprawność fizyczna.
- Depresja.
Długoterminowa opieka realizowana przez lekarza rodzinnego, rehabilitacja kardiologiczna
- Opieka długoterminowa jest świadczona przede wszystkim przez lekarzy rodzinnych we współpracy ze specjalistami, szpitalami i placówkami rehabilitacyjnymi.
- Opieka strukturalna:
- regularne, indywidualnie ustalane kontrole
- uzgodnienie celów terapii
- terapia oparta na dowodach naukowych (styl życia, leki)
- edukacja (np. w zakresie nadciśnienia, cukrzycy, stosowania leków przeciwkrzepliwych), ewentualnie rozpoczęcie psychoterapii
- dołączenie do grup wsparcia dla pacjentów kardiologicznych, w indywidualnych przypadkach rozpoczęcie ambulatoryjnych lub stacjonarnych procedur terapeutycznych w ramach rehabilitacji kardiologicznej.
- Pacjentów z chorobą wieńcową należy zapraszać/wzywać na regularne konsultacje u lekarza rodzinnego (raz na kwartał do pół roku), niezależnie od konsultacji z powodu np. ostrych dolegliwości lub chorób współwystępujących.
- Pacjentów z chorobą wieńcową należy skierować do kardiologa, jeśli w praktyce lekarza rodzinnego nie można uzyskać wystarczającej kontroli objawów lub odpowiednio realizować postępowania, które skutecznie wpływa na rokowanie (np. z powodu nietolerancji leków).
- Pacjentom z chorobą wieńcową należy zalecać wizyty u innych specjalistów, jeśli może to poprawić kontrolę objawów lub rokowanie.
- Pacjentom z chorobą wieńcową, zwłaszcza po OZW, interwencji wieńcowej lub operacji wszczepienia by–passów (CABG), należy zalecić udział w ambulatoryjnej grupie wsparcia dla pacjentów kardiologicznych lub innych programach promujących regularne ćwiczenia fizyczne i inne zmiany stylu życia obniżające ryzyko, jeśli są one dostępne.
- Turnusy rehabilitacyjne w specjalistycznych placówkach rehabilitacyjnych (w trybie ambulatoryjnym lub stacjonarnym) należy zalecać w następujących przypadkach, o ile pacjent nie wymaga interwencji w stanie ostrym:
- objawy obniżające jakość życia mimo standardowej terapii
- wyraźny i niewystarczająco ustabilizowany profil ryzyka
- nasilone problemy psychospołeczne
- ryzyko niezdolności do wykonywania zawodu/zarobkowania albo potrzeby opieki.
Informacje dla pacjentów
Akademia Pacjenta Kardiologicznego (serwis Polskiego Towarzystwa Kardiologicznego)
- Dieta dla zdrowia.
- Aktywność fizyczna dla pacjentów ze schorzeniami układu krążenia.
Materiały edukacyjne dla pacjentów
Ilustracje
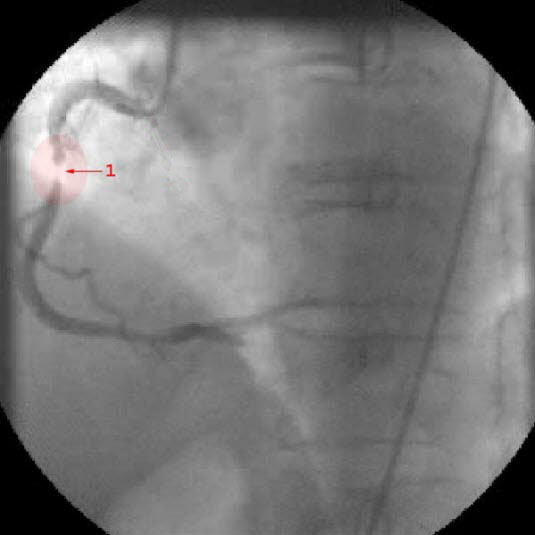
Koronarografia: uwidocznienie zwężenia w prawej tętnicy wieńcowej (1 – zwężenie dużego stopnia)
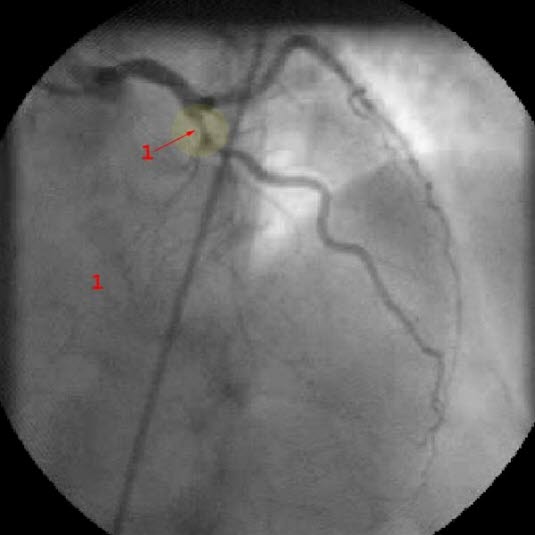
Koronarografia: wyraźne zwężenie gałęzi międzykomorowej przedniej (1) (ramus intraventricularis anterior – RIVA)
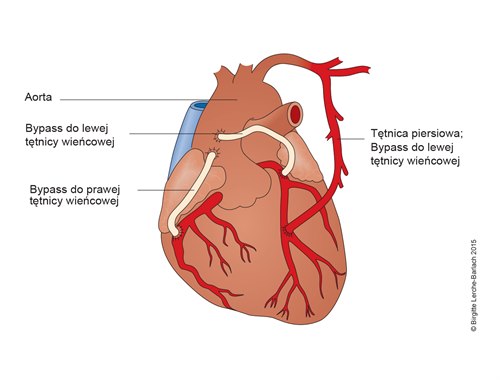
Potrójny pomost wieńcowy
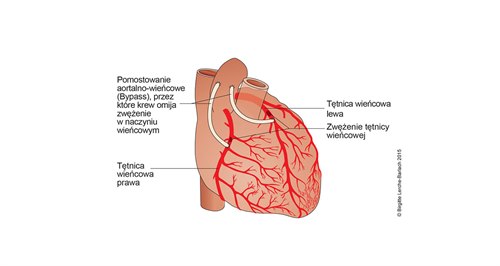
Pomostowanie aortalno–wieńcowe
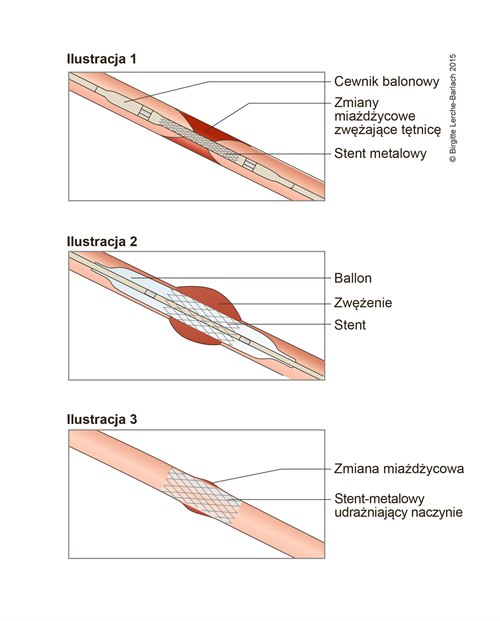
Stentowanie zwężonego naczynia krwionośnego
Źródła
Wytyczne
- 2024 ESC Guidelines for the management of chronic coronary syndromes. Developed by the task force for the management of chronic coronary syndromes of the European Society of Cardiology (ESC). Endorsed by the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2024; 45: 3415-3537. escardio.org
- 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice: Developed by the Task Force for cardiovascular disease prevention in clinical practice with representatives of the European Society of Cardiology and 12 medical societies With the special contribution of the European Association of Preventive Cardiology (EAPC). Eur Heart J, 2021; 42(34): 3227-337. www.escardio.org, (po polsku na ptkardio.pl)
- 2018 ESC/EACTS Guidelines on myocardial revascularization. Eur Heart J 2018; 40(2): 87-165. www.escardio.org, (po polsku na ptkardio.pl)
- 2021 PoLA/CFPiP/PCS/PSLD/PSD/PSH guidelines on diagnosis and therapy of lipid disorders in Poland 2021,. Arch Med Sci. 2021, 17(6): 1447-54, 08.10.2021, doi:10.5114/aoms/141941 24 termedia.pl, po polsku termedia.pl
Piśmiennictwo
- Fox K., Metra M., Morais J., et al. The myth of ‘stable’ coronary artery disease, Nat Rev Cardiol 2020, 17: 9-21, doi:10.1038/s41569-019-0233-y, DOI
- Vrints C., Andreotti F., Koskinas KC., et al. 2024 ESC Guidelines for the management of chronic coronary syndromes: Developed by the task force for the management of chronic coronary syndromes of the European Society of Cardiology (ESC) Endorsed by the European Association for Cardio-Thoracic Surgery (EACTS) Eur Heart J 2024, 45: 3415-3537. www.escardio.org
- NFZ o zdrowiu. Choroba niedokrwienna serca (24.04.2020). https://ezdrowie.gov.pl/portal/home/badania-i-dane/zdrowe-dane/raporty/nfz-o-zdrowiu-choroba-niedokrwienna-serca, dostęp: 30.09.2023, ezdrowie.gov.pl
- Libby P, Theroux P. Pathophysiology of Coronary Artery Disease, Circulation 2005, 111: 3481-8, doi:10.1161/CIRCULATIONAHA.105.537878, DOI
- Libby P., Hansson G. From Focal Lipid Storage to Systemic Inflammation. J Am Coll Cardiol 2019, 74: 1594-607, doi:10.1016/j.jacc.2019.07.061, DOI
- Poston R. Atherosclerosis: integration of its pathogenesis as a self-perpetuating propagating inflammation: a review, Cardiovasc Endocrinol Metab 2019, 8: 51-61, doi:10.1097/XCE.0000000000000172, DOI
- Schoenhagen P., Ziada R.M., Kapadia S.P., Crowe T.D., Nissen S.E., Tuzcu E.M. Extent and direction of arterial remodeling in stable versus unstable coronary syndromes: an intravascular ultrasound study, Circulation 2000, 101: 598-603, pubmed.ncbi.nlm.nih.gov
- Halcox J.P., Schenke W.H., Zalos G., et al. Prognostic value of coronary vascular endothelial dysfunction, Circulation 2002, 106: 653-8, pubmed.ncbi.nlm.nih.gov
- Lakka H-M., Lakka T.A., Tuomilehto J., Salonen J.T. Abdominal obesity is associated with increased risk of acute coronar events in men, Eur Heart J 2002, 23: 706-13, PubMed
- Bogers R.P., Bemelmans W.J., Hoogenveen R.T., et al. Association of overweight with increased risk of coronary heart disease partly independent of blood pressure and cholesterol levels: A meta-analysis of 21 cohort studies including more than 300 000 persons, Arch Intern Med 2007, 167: 1720-8, PubMed
- Yusuf S., Hawken S., Ôunpuu S. et al. Obesity and the risk of myocardial infarction in 27 000 participants from 52 countries: a case-control study, Lancet 2005, 366: 1640-9, PubMed
- McGill H.C., McMahan A., Herderick E.E., Zieske A.W., Malcom G.T., Tracy R.E., Strong J.P., for the pathobiological determinants of atherosclerosis in youth (PDAY) research group, Obesity accelerates the progression of coronary atherosclerosis in young men. Circulation 2002, 105: 2712-8, PubMed
- Rosengren A., Hawken S., Ôunpuu S., et al. Association of psychosocial risk factors with risk of acute myocardial infarction in 11 119 cases and 13 648 controls from 52 countries (the INTERHEART study): case-control study, Lancet 2004, 364: 953-62, PubMed
- Hemingway H., Marmot M. Psychosocial factors in the primary and secondary prevention of coronary heart disease: a systematic review. I: Yusuf S., Cairns J.A., Camm A.J., Fallen E.L., Gersh B.J., red. Evidence based cardiology, London: BMJ Books, 1998: 269-85.
- Yusuf S., Hawken S., Ounpuu S., et al. Effect of potentially modifiable risk factors associated with myocardial infarction in 52 countries (the INTERHEART study): case-control study. Lancet 2004, 364: 937-52, doi:10.1016/S0140-6736(04)17018-9, DOI
- Dhingra R., Vasan R. Age as a Cardiovascular Risk Factor, Med Clin North Am 2012, 96: 87-91, www.ncbi.nlm.nih.gov
- Anand S., Islam S., Rosengren A., et al. Risk factors for myocardial infarction in women and men: insights from the INTERHEART study, Eur Heart J 2008, 29: 932-40, doi:10.1093/eurheartj/ehn018, DOI
- Roncaglioni M., Santoro L., D'Avanzo B., et al . Role of Family History in Patients With Myocardial Infarction. Circulation 1992, 85: 2065-72, pubmed.ncbi.nlm.nih.gov
- Harskamp R.E., Laeven S.C., Himmelreich JCI, et al. Chest pain in general practice: a systematic review of prediction rules, BMJ Open. 2019, 9(2): e027081, pubmed.ncbi.nlm.nih.gov
- Larcombe J.H. Review: exercise based cardiac rehabilitation reduces all cause and cardiac mortality in coronary heart disease, Evid Based Med 2004, 9: 175, www.ncbi.nlm.nih.gov
- Hambrecht R., Walther C., Mobius-Winkler S., et al. Percutaneous coronary angioplasty compared with exercise training in patients with stable coronary artery disease: a randomized trial, Circulation 2004, 109: 1371-8, PubMed
- Iestra J.A., Kromhout D., van der Schouw Y.T., Grobbee D.E., Boshuizen H.C. and van Staveren W.A. Effect size estimates of lifestyle and dietary changes on all-cause mortality in coronary artery disease patients: a systematic review. Circulation 2005, 112: 924-34, pubmed.ncbi.nlm.nih.gov
- Smolis-Bąk E. Zalecenie dotyczące aktywności fizycznej dla pacjentów ze schorzeniami układu krążenia, https://dlapacjenta.ptk.waw.pl/dzialanie/aktywnosc-fizyczna, dostęp: 1.10.2023, dlapacjenta.ptk.waw.pl
- Banach M., Burchardt P., Chlebus K., et al. Wytyczne PTL/KLRwP/PTK/PTDL/PTD/PTNT diagnostyki i leczenia zaburzeń lipidowych w Polsce. Lekarz POZ Suplement, 2021. www.termedia.pl
- Stead L.F., Buitrago D., Preciado N., Sanchez G., Hartmann-Boyce J., Lancaster T. Physician advice for smoking cessation. Cochrane Database of Systematic Reviews 2013, Issue 5. Art. No.: CD000165, pubmed.ncbi.nlm.nih.gov
- Piepoli M., Hoes A., Agewall S., et al. 2016 European Guidelines on cardiovascular disease prevention in clinical practice, Eur Heart J 2016, 37: 2315-81, academic.oup.com
- Koskinas et al. Effect of statins and non-statin LDL-lowering medications on cardiovascular outcomes in secondary prevention: a meta-analysis of randomized trials, European Heart Journal (2017) 0, 1-9, boris.unibe.ch
- Leutner M. et al. Diagnosis of osteoporosis in statin-treated patients is dose-dependent, Ann Rheum Dis 2019, 78: 1706-11, ard.bmj.com
- Jende et al. Association of Serum Cholesterol Levels With Peripheral Nerve Damage in Patients With Type 2 Diabetes, JAMA Network Open 2019, 2(5): e194798, pubmed.ncbi.nlm.nih.gov
- Caughey et al. Association of Statin Exposure With Histologically Confirmed Idiopathic Inflammatory Myositis in an Australian Population, JAMA Intern Med., jamanetwork.com
- Naci H. et al. Comparative Tolerability and Harms of Individual Statins. Circulation 2013, www.ahajournals.org
- Schmidt A., Pearce L., Wilkins J., et al. PCSK9 monoclonal antibodies for the primary and secondary prevention of cardiovascular disease, Cochrane Database Sys Rev 2017, 4: CD011748. doi:10.1002/14651858.cd011748.pub2, DOI
- Nissen S., Lincoff A., Brennan D., et al. Bempedoic Acid and Cardiovascular Outcomes in Statin-Intolerant Patients, N Engl J Med 2023, 388: 1353-64, doi:10.1056/NEJMoa2215024, pubmed.ncbi.nlm.nih.gov
- Fox K. et al. Ivabradine for patients with stable coronary artery disease and left-ventricular systolic dysfunction (BEAUTIFUL): a randomised, double-blind, placebo-controlled trial, Lancet 06.09.2008, 372(9641): 807-16, pubmed.ncbi.nlm.nih.gov
- Holmes D., Taggart D. Revascularization in stable coronary artery disease: a combined perspective from an interventional cardiologist and a cardiac surgeon, Eur Heart J 2016; 37: 1873-82, doi:10.1093/eurheartj/ehw044, DOI
- Stergiopoulos K., Boden W., Hartigan P. et al. Percutaneous Coronary Intervention Outcomes in Patients With Stable Obstructive Coronary Artery Disease and Myocardial Ischemia A Collaborative Meta-analysis of Contemporary Randomized Clinical Trials, JAMA Intern Med. 2014, 174(2): 232-40, www.ncbi.nlm.nih.gov
- Sedlis S.P. Hartligan P.M., Teo K.K. et al.: Effect of PCI on long-term survival of patients with stable ischemic heart disease, N Engl J Med, październik 2015, 372: 20. 1937-46, www.ncbi.nlm.nih.gov
- Bangalore S., Maron D., Stone G., et al. Routine Revascularization Versus Initial Medical Therapy for Stable Ischemic Heart Disease - A Systematic Review and Meta-Analysis of Randomized Trials, Circulation 2020, 142: 841-57, doi:10.1161/CIRCULATIONAHA.120.048194, DOI
- Boden W., O'Rourke R., Teo K., et al, for the COURAGE Trial Research Group, Optimal medical therapy with or without PCI for stable coronary disease, N Engl J Med 2007, 356: 1503-16, PubMed
- Maron D., Hochman J., Reynolds H., et al. Initial Invasive or Conservative Strategy for Stable Coronary Disease, N Engl J Med 2020, 382: 1395-407, doi:10.1056/NEJMoa1915922, DOI
- Weintraub W., Spertus J., Kolm P., for the COURAGE Trial Research Group. Effect of PCI on quality of life in patients with stable coronary disease, N Engl J Med 2008, 359: 677-87, doi:10.1056/NEJMoa072771, DOI
- Wijeysundera H.C., Nallamothu B.K., Krumholz H.M., et al. Meta-analysis: Effects of percutaneous coronary intervention versus medical therapy on angina relief, Ann Intern Med 2010, 152: 370-9, pubmed.ncbi.nlm.nih.gov
- Al-Lamee R., Thompson D., Dehbi H., et al. Percutaneous coronary intervention in stable angina (ORBITA): a double-blind, randomised controlled trial, Lancet 2018, 391: 31-40, pubmed.ncbi.nlm.nih.gov
- Albuquerque L., Gomes W. ORBITA Trial: Redefining the Role of Intervention in the Treatment of Stable Coronary Disease? Braz J Cardiovasc Surg 2018, 3: 3-5,. doi:10.21470/1678-9741-2017-0243, DOI
- Neumann F., Sousa-Uva M., Ahlsson A., et al. 2018 ESC/EACTS Guidelines on myocardial revascularization, Eur Heart J; 40: 87-165. doi:10.1093/eurheartj/ehy394, DOI
- Kureshi F., Jones P., Buchanan D., Abdallah M., Spertus S. Variation in patients’ perceptions of elective percutaneous coronary intervention in stable coronary artery disease: cross sectional studyBMJ 2014, 349: g5309, www.bmj.com
- Goff S., Mazor K., Ting H., Kleppel R., Rothberg M. How Cardiologists Present the Benefits of Percutaneous Coronary Interventions to Patients With Stable Angina A Qualitative Analysis, JAMA Intern Med., istopad 2014, 174(10): 1614-21, www.ncbi.nlm.nih.gov
- Rothberg M., Scherer L., Kashef M. et al. The Effect of Information Presentation on Beliefs About the Benefits of Elective Percutaneous Coronary Intervention, JAMA Intern Med listopad 2014, 174(10): 1623-9, www.ncbi.nlm.nih.gov
- Weintraub W.S., Grau-Sepulveda M.V., Weiss J.M., et al. Comparative effectiveness of revascularization strategies, N Engl J Med 2012. doi:10.1056/NEJMoa1110717.
- Hlatky MA, Boothroyd DB, Bravata DM, et al. Coronary artery bypass surgery compared with percutaneous coronary interventions for multivessel disease: a collaborative analysis of individual patient data from ten randomised trials. Lancet 2009; 373: 1190-7. PubMed
- Sipahi I, Akay MH, Dagdelen S, et al. Coronary artery bypass grafting vs percutaneous coronary intervention and long-term mortality and morbidity in multivessel disease. Metaanalysis of randomized clinical trials of the arterial grafting and stenting era. JAMA 2013. doi:10.1001/jamainternmed.2013.12844 DOI
- Whooley MA, de Jonge P, Vittinghoff E et al. Depressive symptoms, health behaviors, and risk of cardiovascular events in patients with coronary heart disease. JAMA 2008; 300: 2379-88. PubMed
Opracowanie
- Joanna Dąbrowska-Juszczak (recenzent)
- Tomasz Tomasik (recenzent)
- Adam Windak (redaktor)
- Małgorzata Marczewska (recenzent/redaktor)
- Michael Handke (recenzent/redaktor)