Informacje ogólne1-2
Definicja
- Zakażenie HIV
- Przewlekłe zakażenie wywołane ludzkim wirusem niedoboru odporności (Human Immunodeficiency Virus – HIV).
- AIDS
- Aquired Immunodeficiency Syndrome (zespół nabytego niedoboru odporności).
- Objawy kliniczne ciężkiego upośledzenia odporności komórkowej spowodowane zakażeniem HIV.
- W USA i niektórych innych krajach definicja AIDS obejmuje również osoby zakażone HIV z liczbą komórek CD4 (limfocyty T CD4) <200/mcl bez klinicznych objawów upośledzenia odporności komórkowej.
- Choroby definiujące AIDS
- Zakażenia oportunistyczne.
- Niektóre choroby nowotworowe.
- Inne ciężkie objawy kliniczne, które prawdopodobnie wynikają z zaawansowanego zakażenia HIV, a których patogeneza jest jednak niepewna.
- Zmiana paradygmatu
- W krajach o wysokich średnich dochodach nastąpiło znaczne zmniejszenie zachorowań i zgonów spowodowanych zakażeniem HIV po wprowadzeniu w 1996 r. wysoce aktywnej terapii przeciwretrowirusowej (HAART, w skrócie ART).
- Chorobę obecnie uważa się za zakażenie przewlekłe.
- Długość życia pacjentów otrzymujących odpowiednie leczenie nie różni się od populacji niezakażonej.
- Zwiększyła się częstość występowania chorób płuc, serca, przewodu pokarmowego i nerek niezwiązanych bezpośrednio z podstawowym zakażeniem HIV.
Epidemiologia
- Zakażenie HIV/AIDS odkryto w 1981 r.
- Na całym świecie HIV/AIDS jest najczęstszą przyczyną śmierci młodych dorosłych.
- Epidemia uległa stagnacji w krajach o wysokich średnich dochodach, ale nadal rośnie w większości krajów rozwijających się.
- Częstość występowania1
- Według danych UNAIDS (Wspólny Program Narodów Zjednoczonych ds. HIV/AIDS) w 2022 roku około 39 milionów osób było zakażonych wirusem HIV.
- Wśród nich było około 1,5 miliona dzieci poniżej 15. roku życia.
- Około 70% osób zakażonych HIV mieszka w krajach Afryki Subsaharyjskiej
- prawie 60% wszystkich chorych w tym regionie to kobiety.
- W Polsce od wdrożenia badań w 1981 roku do końca 2022 roku zakażenie stwierdzono u 29 676 osób.
- Według danych UNAIDS (Wspólny Program Narodów Zjednoczonych ds. HIV/AIDS) w 2022 roku około 39 milionów osób było zakażonych wirusem HIV.
- Zapadalność
- Każdego roku HIV zakaża się ponad 2 miliony osób.
- Przeniesienie HIV z matki na dziecko
- Ryzyko waha się między 15% a 35%, jeśli nie zostanie zastosowane leczenie przeciwwirusowe.
- Stosowanie ARV (terapia antyretrowirusowa) podczas ciąży zmniejsza ryzyko przeniesienia choroby na dziecko do około <1%.
- Jeśli w czasie ciąży nie zastosowano leczenia, wdrożenie ARV u matki (po porodzie) i/lub leczenie profilaktyczne noworodka znacznie zmniejszają u niego ryzyko zachorowania.
- Śmiertelność
- Szacowana liczba zgonów z powodu AIDS w 2022 roku w skali globalnej wyniosła około 630 000.
Przyczyna i rozwój choroby2
- Zakażenie HIV, ludzkim wirusem niedoboru odporności
- HIV jest retrowirusem.
- Istnieją dwa główne typy: HIV–1 i HIV–2.
- Niemal wszystkie zakażenia HIV w Europie są spowodowane przez HIV–1.
- HIV–2 występuje głównie w Afryce Zachodniej i jest endemiczny dla tego regionu.
- Większość dostępnych wytycznych i badań dotyczy zakażeń HIV–1.
- Dane te nie w pełni pokrywają się z przebiegiem i postępowaniem w przypadku zakażeń HIV–2.
- Podtypy
- U ludzi wyróżnia się obecnie 9 podtypów HIV–1 grupy M oraz co najmniej 15 szeroko rozpowszechnionych form rekombinowanych (circulating recombinant form — CRF).
- Ponadto istnieje grupa O (Outlier) HIV–1, w dużej mierze ograniczona do Afryki Zachodniej (Kamerun).
- Ostatnio opisano bardzo rzadko występujące grupy wirusów N i P.
- CD4
- Antygeny CD4 na powierzchni limfocytów T (antygen ten występuje również na innych komórkach) pełnią rolę receptorów, do których wirus HIV ma powinowactwo.
- Transkrypcja wirusa
- Odbywa się w limfocytach T.
- Materiał genetyczny wirusa zostaje wbudowany do materiału genetycznego komórek, gdzie może przez długi czas pozostać nieaktywny.
- W nieaktywnych immunologicznie komórkach może odbywać się ciągła replikacja wirusa.
- Wirus jest z nich uwalniany i dochodzi do zakażania innych komórek.
- Ostre zakażenie HIV
- Najczęściej od 2 do 6 tygodni.
- Dochodzi do masowej replikacji i uwalniania kopii wirusów.
- Krótkotrwałe, przejściowe zmniejszenie liczby komórek CD4.
- Swoista, mierzalna po raz pierwszy odpowiedź immunologiczna przeciwko HIV (serokonwersja).
- Okres utajenia od zakażenia do rozwoju objawów z powodu obniżenia odpowiedzi immunologicznej może być krótszy niż 1–2 lata, średnio wynosi 7–12 lat.
- Zakażenia HIV rzadko przebiegają trwale bezobjawowo.
- Po serokonwersji przeciwciała HIV są wykrywalne do końca życia.
- Progresja: spadek odporności spowodowany stałą redukcją limfocytów T pomocniczych
- Limfocyty T pomocnicze odgrywają kluczową rolę w aktywacji innych komórek odpornościowych, dochodzi więc do zaburzenia działania całego układu immunologicznego.
- Klinicznie prowadzi to do zwiększonej skłonności do zakażeń.
- Przy zaawansowanym niedoborze odporności (AIDS) rozwijają się zagrażające życiu zakażenia oportunistyczne i wzrasta ryzyko rozwoju nowotworów.
Przenoszenie wirusa HIV
Drogi przenoszenia
- Kontakt seksualny.
- Zakażona krew lub produkty krwiopochodne dostające się do krwiobiegu.
- Przeszczepy tkanek i narządów
- przeniesienie okołoporodowe z matki na dziecko.
Płyny ustrojowe
- Z reguły największe stężenie wirusa u osób zakażonych HIV występuje we krwi, płynie nasiennym, wydzielinie z pochwy i na powierzchni błony śluzowej jelit.
- W innych płynach ustrojowych HIV jest obecny w znacznie niższym stężeniu, więc przeniesienie jest teoretycznie możliwe, ale nie zostało jeszcze opisane.
- Przypadkowe przeniesienie HIV podczas wykonywania zawodu zostało dotychczas udokumentowane jedynie w związku z kontaktem z krwią lub płynem z hodowli wirusów.
- HIV nie jest przenoszony drogą kropelkową.
Ryzyko zakażenia
- Jest największe w ciągu pierwszych 3 miesięcy po zakażeniu i w fazie AIDS.
- Koreluje z wiremią i czasem trwania ekspozycji.
- Nie ma jednoznacznej możliwości oceny ryzyka zakażenia podczas niezabezpieczonych stosunków seksualnych z partnerami zakażonymi HIV.
- Ryzyko jest większe, gdy osoby zakażone HIV mają wysoką wiremię, gdy partnerzy mają choroby weneryczne oraz gdy stroną bierną jest osoba niezakażona.
- Jeśli zakażeni partnerzy nie są leczeni farmakologicznie, ryzyko zakażenia w przypadku każdego niezabezpieczonego stosunku seksualnego jest nie większe niż 0,1%.
- Jeśli osoba zakażona jest leczona, ryzyko jest jeszcze mniejsze.
- Jeśli wiremia utrzymuje się na stałym poziomie poniżej 50 kopii/ml, przeniesienie wirusa HIV jest mało prawdopodobne.
- Ryzyko zakażenia jest znacznie większe w przypadku zmian śluzówkowych i towarzyszącej im choroby przenoszonej drogą płciową.
- W przypadku stosunku analnego na zakażenie bardziej narażona jest strona receptywna niż insertywna.
- Patrz tabela ryzyko zakażenia przez nieleczone osoby zakażone HIV.
- Przyjmuje się, że podczas waginalnego stosunku seksualnego ryzyko zakażenia kobiety przez mężczyznę jest większe niż mężczyzny przez kobietę.
- Używanie tej samej igły do dożylnych iniekcji substancji odurzających wiąże się z bardzo wysokim ryzykiem transmisji HIV.
- Rany kłute osób postronnych przez rozrzucony zużyty sprzęt do zastrzyków.
- Ryzyko przeniesienia wirusa HIV jest przypuszczalnie niskie, ponieważ do igieł po ich użyciu przylegają tylko niewielkie ilości krwi i są one zazwyczaj wysuszone.
Przeniesienie z matki na dziecko
- Ryzyko przeniesienia wirusa koreluje z wiremią we krwi matki, stadium choroby i formą porodu.
- W większości przypadków przeniesienie z zakażonej matki na dziecko następuje na krótko przed lub w trakcie porodu lub poprzez mleko matki.
- Terapia przeciwretrowirusowa zmniejsza ryzyko zakażenia
- jeśli wiremia matki została zredukowana do <50 kopii wirusowych na ml osocza, ryzyko w przypadku porodu pochwowego jest mniejsze niż 1%
- przy wyższej wiremii cięcie cesarskie w trybie planowym prowadzi do mniejszej liczby przeniesień wertykalnych niż poród pochwowy.
- Wykazano, że karmienie piersią jest czynnikiem ryzyka przeniesienia HIV, ale ryzyko można zmniejszyć poprzez leczenie antyretrowirusowe.3
Transfuzja krwi
- Ryzyko zakażenia HIV podczas transfuzji w przypadku zakażonej krwi: 90 do 100%.
- Od wprowadzenia bezpośrednich badań sprawdzających obecność genomu wirusa HIV, ryzyko zakażenia w następstwie transfuzji praktycznie wyeliminowano.
Personel medyczny i HIV
- Ukłucie zanieczyszczoną igłą wiąże się z ryzykiem transmisji na poziomie 0,3%.
- W większości przypadków ryzyko jest jeszcze mniejsze.
- Opisywano serokonwersje po kontakcie śluzówki lub skóry z krwią osoby HIV–pozytywnej, ale w przypadku nieuszkodzonej skóry zakażenia są bardzo mało prawdopodobne.
- Decydujące znaczenie dla przeniesienia zakażenia miała ilość krwi, okres kontaktu z krwią oraz naruszona bariera skórna.
- Leczenie lekami antyretrowirusowymi bezpośrednio po ekspozycji może zmniejszyć ryzyko zakażenia o ponad 80%.
ICD–10
- B20 Choroba wywołana przez ludzki wirus upośledzenia odporności [HIV], której skutkiem są choroby zakaźne i pasożytnicze.
- B21 Choroba wywołana przez ludzki wirus upośledzenia odporności [HIV], której skutkiem są nowotwory złośliwe.
- B22 Choroba wywołana przez ludzki wirus upośledzenia odporności [HIV], której skutkiem są inne określone choroby.
- B22 .0 Choroba wywołana przez HIV, której skutkiem jest encefalopatia.
- B22.1 Choroba wywołana przez HIV, której skutkiem jest limfoidalne śródmiąższowe zapalenie płuc.
- B22.2 Choroba wywołana przez HIV, której skutkiem jest zespół wyczerpania.
- Choroba wywołana przez HIV, której skutkiem jest brak prawidłowego rozwoju i wzrostu.
- Zespół wyniszczenia.
- B22.7 Choroba wywołana przez HIV, której skutkiem są mnogie choroby sklasyfikowane gdzie indziej.
- B23 Choroba wywołana przez ludzki wirus upośledzenia odporności [HIV], której skutkiem są inne stany chorobowe.
- B23.0 Ostry zespół zakażenia HIV.
- B23.1 Choroba wywołana przez HIV, której skutkiem jest (przewlekła) uogólniona limfadenopatia.
- B23.2 Choroba wywołana przez HIV, której skutkiem są zaburzenia układu krwiotwórczego i odpornościowego niesklasyfikowane gdzie indziej.
- B23.8 Choroba wywołana przez HIV, której skutkiem są inne określone stany chorobowe.
- B24 Choroba wywołana przez ludzki wirus upośledzenia odporności [HIV], nieokreślona; w tym:
- zespół związany z AIDS [ARC], BNO.
- nabyty zespół upośledzenia odporności [AIDS] BNO.
- Z21 Bezobjawowy stan zakażenia ludzkim wirusem upośledzenia odporności [HIV]; w tym osoby HIV–dodatnie BNO.
- O98.7 Choroba wywołana przez ludzki wirus upośledzenia odporności [HIV] wikłająca ciążę, poród i połóg.
- Z20.6 Styczność i narażenie na zakażenie ludzkim wirusem upośledzenia odporności [HIV].
- R75 Wyniki badań laboratoryjnych wskazujące na zakażenie ludzkim wirusem upośledzenia odporności [HIV]; w tym: nierozstrzygające wyniki testu w kierunku zakażenia HIV u dzieci.
Diagnostyka
Diagnostyka zakażenia HIV2,4
- Rozpoznanie zakażenia HIV opiera się na wykryciu specyficznych przeciwciał w połączeniu z wykryciem antygenu wirusowego lub wirusowych kwasów nukleinowych (diagnostyka dwuetapowa z testem przesiewowym i potwierdzającym).
- Lekarze podstawowej opieki zdrowotnej
niemają możliwościćskierowaniakierowania na diagnostykę pod kątem zakażenia HIV,(testy przesiewowe IV generacji). Pacjenci mogąnatomiast skierowaudaćpacjentasię doPoradni Chorób Zakaźnych lubPunktu Diagnostyczno–Konsultacyjnego (możliwość wykonania testu bez skierowania). - Swoiste przeciwciała są wykrywalne średnio po 22 dniach u osoby zakażonej, a antygen wirusa już po 16–18 dniach.
- Szybkie testy są mniej czułe niż nowoczesne testy laboratoryjne, które wykrywają zakażenie już po 1–2 tygodniach.
- Wirusowe kwasy nukleinowe można wykryć średnio już po 11 dniach.
- Pewne wykluczenie zakażenia wymaga jednak znacznie dłuższego okresu niż podane wartości średnie:
- Przy zastosowaniu diagnostyki dwuetapowej opierającej się jedynie na wykazaniu przeciwciał HIV w teście przesiewowym (ELISA III. generacji) ustalony jest jeszcze zawsze 12–tygodniowy okres okna serologicznego, pozwalający na pewne zdiagnozowanie lub wykluczenie zakażenia HIV.
- W przypadku gdy stosuje się nowoczesne testy przesiewowe HIV Ag/Ab, wcześniej znane jako testy IV generacji, które poza przeciwciałami wykazują obecność antygenu p24 HIV, czas trwania okna serologicznego skracany jest do 6 tygodni.
- Oznacza to również, że po 6 tygodniach od ewentualnej ekspozycji negatywny wynik testu przesiewowego na obecność przeciwciał/antygenów HIV może z dużą dozą pewności wykluczyć zakażenie (brak wykrywalnych specyficznych przeciwciał oraz antygenu p24).
- Lekarze podstawowej opieki zdrowotnej
Diagnostyka dwuetapowa
- Krok 1: wysoce czuły test przesiewowy na obecność przeciwciał i/lub antygenów
- Na przykład ELISA, wykrywający przeciwciała przeciwko antygenom wirusowym (HIV–1 i HIV–2) i/lub wirusowy antygen p24.
- Krok 2: wysoce specyficzny test potwierdzający
- Obecnie odchodzi się od testów wykorzystujących techniki immuno/elektroblottingu (np. Western–Blot) na rzecz testów molekularnych (tzw. testy NAT/NAAT).
- Przyczynami są: brak możliwości wykrycia w fazie ostrego zakażenia i stosunkowo częstej, błędnej klasyfikacji zakażenia HIV–2 jako zakażenia HIV–1.
- Testy te wykrywają obecność (jakościowe) lub ilość (ilościowe) wirusowego RNA.
- Jedną ze stosowanych technik amplifikacji kwasów nukleinowych (Nucleic Acid Amplification Test – NAAT) jest łańcuchowa reakcja polimerazy (Polymerase Chain Reaction – PCR).
- Do wykonania oznaczeń jakościowych i ilościowych zaleca się używanie testów opartych na technologii PCR czasu rzeczywistego poprzedzonego etapem odwrotnej transkrypcji (Real–Time–PCR).
- Cechują się bardzo wysoką swoistością i czułością diagnostyczną: są w stanie wykryć od 15–20 kopii/ml do kilkunastu milionów kopii/ml.
- Ponadto umożliwiają wiarygodną ocenę wiremii różnych subtypów HIV–1.
- Testy PCR jakościowe i ilościowe swoiste dla każdego typu wirusa.
- Testy wykrywające RNA HIV–1 są ogólnodostępne.
- W przypadku testów dla HIV–2 istnieją ilościowe testy wykrywające wiremię, jednak dostępność ich jest znikoma.
- Wykorzystywane są głównie w celach naukowych, a diagnostyka i postępowanie w HIV–2 nie jest objęte przez wytyczne.
- Obecnie odchodzi się od testów wykorzystujących techniki immuno/elektroblottingu (np. Western–Blot) na rzecz testów molekularnych (tzw. testy NAT/NAAT).
Ujemny wynik testu lub niski sygnał
- Dostępne komercyjnie testy NAT nie mają takiej samej czułości w odniesieniu do wszystkich znanych grup i podtypów HIV–1.
- Może to prowadzić do obniżonych lub fałszywie ujemnych wyników badań.
- W przypadku niskiej lub niewykrywalnej wiremii:
- HIV-2
- inne, jeszcze rzadsze warianty wirusa.
- Jak dotąd nie jest dostępny żaden komercyjny test NAT do wykrywania HIV–2.
- Ujemny wynik NAT: potwierdzenie za pomocą testów serologicznych.
Diagnostyka AIDS
- Rozpoznanie AIDS w większości krajów poza Ameryką Północną stawiane jest klinicznie na podstawie obecności zakażeń oportunistycznych, niektórych rodzajów nowotworów złośliwych lub innych objawów klinicznych w zaawansowanym zakażeniu HIV.
- w Polsce oznaczanie liczby limfocytów T pomocniczych może służyć jako marker pomocniczy.
Diagnostyka zakażeń oportunistycznych
- Niekiedy rzadkie gatunki patogenów.
- Często reaktywacja zakażeń utajonych.
- Badania przeciwciał nie są zbyt miarodajne, ponieważ pacjenci mogą posiadać przeciwciała z wcześniejszych zakażeń, a zdolność do wytwarzania nowych przeciwciał jest zmniejszona.
- Aby postawić rozpoznanie, patogen musi zostać wykryty bezpośrednio w biopsji lub innym materiale, ewentualnie za pomocą specjalnego barwienia lub techniki PCR.
Etapy kliniczne zakażenia HIV
- Zastosowano stopniowanie stadiów przedstawione w 1993 r. przez amerykański urząd ds. kontroli chorób i zapobiegania im (Centers for Disease Control and Prevention – CDC).
Stadium kliniczne CDC–A
- Zakażenie bezobjawowe
- Obejmuje zarówno pacjentów, u których doszło do objawowego zakażenia pierwotnego, jak i tych, u których na początku zakażenie ma charakter subkliniczny.
- Może trwać od 1,5 roku do 20 lat, sporadycznie nawet dłużej.
- Trwała, uogólniona limfadenopatia
- Występuje w węzłach chłonnych o średnicy powyżej 1 cm w dwóch lub więcej miejscach pozawęzłowych, przez okres co najmniej 3 miesięcy.
- Można stwierdzić w przypadku około 30% chorych.
- Nie ma znaczenia dla rokowania.
- Ostre zakażenie HIV
- Objawy pojawiają się od 2 do 6 tygodni po zakażeniu i trwają zwykle od 1 do 2 tygodni.
- Objawy dotyczą 50–70% zakażonych.
- U 80–90% tych pacjentów występuje gorączka, pojawiająca się zwykle od 2 do 4 tygodni po zakażeniu.
- U około 40% występuje niespecyficzna grudkowo–plamista wysypka.
- Częsty ból gardła z limfadenopatią szyjną.
- Niekiedy afty jamy ustnej.
- Poczucie choroby i zmęczenie.
- Bóle stawów i mięśni.
- Utrata apetytu i spadek masy ciała.
- Obraz kliniczny przypomina łagodną mononukleozę.
Stadium kliniczne CDC–B
- Naczyniakowatość wywołana przez laseczki
- Objawy choroby lub chorób, które nie należą do kategorii C definiującej AIDS, ale które jednak można przypisać przyczynowo zakażeniu HIV lub które wskazują na zaburzenia komórkowej obrony immunologicznej:
- naczyniakowatość wywołana przez laseczki (bakterie Bartonella)
- zakażenie Candida jamy ustnej
- zakażenia Candida sromu i pochwy, które mają charakter przewlekły (dłuższy niż 1 miesiąc) lub słabo poddają się leczeniu
- dysplazja szyjki macicy lub rak in situ
- objawy konstytucjonalne, np.:
- gorączka powyżej 38,5°C
- biegunka trwająca dłużej niż 4 tygodnie
- leukoplakia włochata jamy ustnej (białe, pasmowate zmiany, zwłaszcza na brzegu języka).
- Objawy choroby lub chorób, które nie należą do kategorii C definiującej AIDS, ale które jednak można przypisać przyczynowo zakażeniu HIV lub które wskazują na zaburzenia komórkowej obrony immunologicznej:
- Leukoplakia włochata jamy ustnej
- półpasiec (≥2 epizody lub ≥2 dermatomy)
- pierwotna małopłytkowość immunologiczna (wcześniej: idiopatyczna plamica małopłytkowa)
- listerioza
- zapalenie narządów miednicy mniejszej (np. zapalenie przydatków), zwłaszcza w przypadku powikłań w postaci ropnia jajowodu lub jajnika
- neuropatia obwodowa.
Kliniczne stadium C na podstawie klasyfikacji CDC (choroby wskaźnikowe AIDS)
- Zapalenie płuc wywołane przez Pneumocystis jirovecii.
- Toksoplazmozowe zapalenie mózgu.
- Kandydoza przełyku lub zakażenie oskrzeli, tchawicy lub płuc.
- Przewlekłe zakażenie Herpes simplex, które może powodować owrzodzenie, zapalenie oskrzeli, zapalenie płuc lub zapalenie przełyku.
- CMV zapalenie siatkówki.
- Uogólnione zakażenie CMV (poza wątrobą lub śledzioną).
- Nawracająca posocznica wywołana przez Salmonella.
- Nawracające zapalenia płuc w ciągu jednego roku.
- Kryptokokoza pozapłucna.
- Przewlekłe zakażenie jelitowe Cryptosporidia.
- Przewlekłe jelitowe zakażenie pasożytem Isospora belli (izosporoza).
- Rozsiana lub pozapłucna histoplazmoza.
- Gruźlica.
- Zakażenia Mycobacterium avium complex lub M. kansasii, rozsiane lub pozapłucne.
- Mięsak Kaposiego
- zmiana nowotworowa skóry
- z komórek wrzecionowatych, sieci naczyń i komórek plazmatycznych
- przypisywany jest zakażeniu ludzkim herpeswirusem typu 8 (HHV8).
- Chłoniaki złośliwe (Burkitta, immunoblastyczny lub pierwotny chłoniak mózgu).
- Inwazyjny rak szyjki macicy.
- Encefalopatia HIV.
- Postępująca wieloogniskowa leukoencefalopatia.
- Zespół wyniszczenia
- niezamierzona utrata masy ciała o co najmniej 10%
- przewlekła biegunka lub gorączka.
Stadia laboratoryjne zakażenia HIV
- Według klasyfikacji CDC z 1993 r.
- CDC–1: liczba limfocytów CD4 ≥500/mcl
- CDC–2: liczba limfocytów CD4 200–499/mcl
- CDC–3: liczba limfocytów CD4 <200/mcl.
Diagnostyka różnicowa
- Zapalenie migdałków, zapalenie gardła i mononukleoza w fazie ostrego zakażenia.
- Inne przyczyny upośledzonej odporności.
- Gruźlica.
Wywiad lekarski
- Gorączka?
- Ból gardła?
- Afty błony śluzowej jamy ustnej?
- Zapalenie szyjnych węzłów chłonnych?
- Ewentualnie osutka plamisto–grudkowa?
- Przetrwałe powiększenie węzłów chłonnych?
- Poczucie choroby i zmęczenia?
- Bóle głowy?
- Bóle stawów i mięśni?
- Utrata apetytu i masy ciała?
- W dalszym przebiegu: objawy ogólne i objawy z różnych układów narządów z powodu niedoboru odporności.
- Stosunki płciowe bez zabezpieczenia?
- Partnerzy/partnerki o nieznanym statusie HIV?
- Częste zmiany partnerek/partnerów?
- Dalekie podróże?
- Zachowania ryzykowne pod wpływem środków odurzających?
- Partner/partnerka HIV–pozytywny: ARV? Poziom wiremii? Liczba komórek CD4?
- Zawód medyczny: potencjalna ekspozycja w przeszłości?
- Zakłucie igłą?
- Kontakt błony śluzowej lub uszkodzonej skóry z potencjalnie zakaźnym materiałem?
- Przetoczenie krwi lub produktów krwiopochodnych?
- Przed rokiem 2005?
- Zabiegi chirurgiczne w nieodpowiednich warunkach higienicznych?
- Odstęp czasu od możliwej ekspozycji?
- Ostatni test na HIV: u pacjenta/pacjentki i u partnerki/partnera?
Badanie fizykalne
Ostre zakażenie HIV
- Objawy ostrej choroby retrowirusowej pojawiają się zwykle po 2–4 tygodniach od transmisji wirusa.
- Gorączka.
- Zapalenie gardła i limfadenopatia szyjna.
- Zmiany chorobowe błony śluzowej jamy ustnej.
- Zmiany skórne.
- Wskazówki sugerujące zażywanie narkotyków.
Faza utajenia
- Może obejmować 10–30 lat lub dłużej
- Przez cały czas trwa aktywna replikacja wirusa ze stopniową redukcją komórek CD4 (limfocytów T pomocniczych).
- Przetrwałe powiększenie węzłów chłonnych.
- Częste przypadkowe odchylenia w wynikach badań: neutropenia, trombocytopenia, hipergammaglobulinemia (zwłaszcza IgG i IgA) i podwyższone OB lub CRP.
- Zmiany skórne takie jak w łojotokowym zapaleniu skóry, łuszczycy, i zapaleniu mieszków włosowych.
- Faza utajenia może również przebiegać całkowicie bez objawów klinicznych i bez odchyleń w wynikach badań laboratoryjnych.
Rozwój niedoboru odporności
- Kandydoza jamy ustnej.
- Nawracająca kandydoza pochwy, oznaki dysplazji szyjki macicy lub raka szyjki macicy.
- Gorączka, utrata masy ciała, biegunka, nowe zaburzenia wchłaniania.
- Uporczywy kaszel, zapalenie oskrzeli, duszność, zapalenia płuc.
- Zapalenie mózgu/encefalopatia
- napady drgawkowe
- deficyty poznawcze.
- Neuropatia
- bóle
- zaburzenia czucia.
- Trudności z przełykaniem.
- Nawracające, utrzymujące się epizody objawowe zakażenia wirusem opryszczki zwykłej (opryszczka wargowa lub opryszczka genitalna).
- Nawracający półpasiec.
- Mięsak Kaposiego.
- Powiększenie węzłów chłonnych.
- Chłoniak, gruźlica lub mykobakterie atypowe.
- Zapalenie siatkówki: zaburzenia widzenia.
Objawy w jamie ustnej
- Objawy zakażenia HIV często występują w jamie ustnej
- afty
- zapalenie dziąseł
- zapalenie jamy ustnej
- martwicze zapalenie przyzębia
- leukoplakia włochata (związana z zakażeniem wirusem EBV)
- kandydoza jamy ustnej.
- Objawy w obrębie jamy ustnej mogą być wczesnymi cechami zakażenia HIV, ale także pogorszenia w przebiegu zakażenia.
Choroby, które nie definiują AIDS
- U osób zakażonych wirusem HIV z liczbą CD4 powyżej 350/mcl istnieje zwiększona podatność na choroby niedefiniujące AIDS.
- Zakłada się, że wysoka częstotliwość replikacji wirusa osłabia lokalną odporność i zwiększa prawdopodobieństwo wystąpienia choroby.
- różne rodzaje nowotworów złośliwych
- rak oskrzela
- rak odbytu
- chłoniak Hodgkina
- nowotwory złośliwe w zakresie laryngologicznym
- nefropatia
- choroby sercowo–naczyniowe.
- różne rodzaje nowotworów złośliwych
- Do chorób tych należą:
- Przy ustalaniu wskazań do leczenia przeciwwirusowego zaleca się ocenę ryzyka wystąpienia tych chorób.5
Badania uzupełniające
- Badania na obecność zakażenia HIV możliwe do wykonania
m.in.w poradniach podstawowej opieki zdrowotnej oraz punktach diagnostyczno-konsultacyjnych, w poradniach dla osób żyjących z HIV- Skierowanie od lekarza POZ nie jest wymagane.
- Test na obecność HIV należy zaproponować w poniższych przypadkach:
- ryzykowne zachowania seksualne
- dożylne przyjmowanie narkotyków
- inne choroby przenoszone drogą płciową
- partnerzy/partnerki zakażeni/zakażone wirusem HIV
- pochodzenie z państw o wysokiej częstości występowania HIV
- proponowanie testów na HIV również partnerom/partnerkom
- zwłaszcza po zabiegach chirurgicznych w warunkach niedostatecznego przestrzegania zasad aseptyki
- ciąża
- matka, która przy porodzie dziecka jest zakażona wirusem HIV.
- Wykonanie testu na obecność HIV zawsze wymaga wcześniejszego poinformowania oraz zgody pacjenta/pacjentki.
- Przebieg procedury testowania HIV – patrz punkt pobieranie próbek krwi po narażeniu na HIV.
Diagnostyka specjalistyczna
- Potwierdzenie występowania drobnoustrojów oportunistycznych często można uzyskać bezpośrednio z biopsji lub z innego materiału.
- Często potrzebne są specjalistyczne badania, które wykonywane są jedynie przez nieliczne laboratoria.
Badania laboratoryjne
- Badanie potwierdzające i badanie oporności.
- Komórki CD4 i RNA HIV.
- Hb.
- Morfologia krwi z rozmazem.
- Bilirubina, GPT (ALT), ALP, CK.
- Ca.
- Kreatynina, GFR.
- Glukoza i HbA1C.
- Cholesterol całkowity, LDL, HDL i trójglicerydy.
- Test serologiczny (zakażenie HIV ogranicza czułość testów)
- Gruźlica
- próba tuberkulinowa lub testy wydzielania interferonu gamma (Interferon–gamma Release Assay – IGRA).
- Badanie moczu.
- Ewentualnie test przesiewowy na obecność narkotyków lub leków.
Dalsze badania
- Wymazy z narządów płciowych i odbytu
- chlamydie (u kobiet/mężczyzn) i gonokoki
- ewentualnie HPV
- cytologia szyjki macicy
- wysokie ryzyko zakażenia HPV i tym samym zwiększona częstość występowania zmian przednowotworowych szyjki macicy
- u kobiet i mężczyzn uprawiających seks z mężczyznami: badania profilaktyczne w kierunku dysplazji odbytnicy (patrz artykuł rak odbytu).
- Gruźlica – dalsze badania.
- Testy IGRA są bardziej swoiste niż próba tuberkulinowa
- Zakażenie HIV utrudnia wykrycie gruźlicy
- Zakażenie HIV może ograniczać czułość i swoistość obu testów, zwłaszcza przy niższej liczbie komórek CD4 (anergia).
- Dlatego ujemny wynik testu nie wyklucza jednoznacznie zachorowania na gruźlicę.
- Często pozapłucne formy gruźlicy, zwłaszcza przy niskiej liczbie komórek CD4.
- W przypadku gruźlicy płucnej objawy chorobowe i wyniki badań radiologicznych mogą być nietypowe, a nawet mogą pozostawać w normie.
- Zakażenie HIV może ograniczać czułość i swoistość obu testów, zwłaszcza przy niższej liczbie komórek CD4 (anergia).
- Dodatni wynik testu
- Po wykluczeniu aktywnej gruźlicy narządowej należy zaproponować profilaktyczne leczenie farmakologiczne.
- Z reguły w takich przypadkach polecany jest izoniazyd (INH).
- Po wykluczeniu aktywnej gruźlicy narządowej należy zaproponować profilaktyczne leczenie farmakologiczne.
- Aktywna gruźlica
- Łączona terapia przeciwgruźlicza w zależności od lekowrażliwości patogenów.
- Po włączeniu ARV współistniejąca gruźlica może spowodować wystąpienie zespołu rekonstrukcji immunologicznej (immune restoration inflammatory syndrome – IRIS), przez co może dojść do klinicznego pogorszenia gruźlicy.
- EKG
- Wskazane jest badanie podstawowe, ponieważ z leczeniem przeciwretrowirusowym wiąże się zwiększone ryzyko sercowo–naczyniowe.
- Atazanawir może wydłużać odstęp PR.
- RTG klatki piersiowej
- Jest wskazane ze względu na ryzyko wystąpienia licznych powikłań związanych z HIV, które mogą się objawiać chorobami płuc.
Wskazania do skierowania do specjalisty/szpitala
- Osoby z dodatnim wynikiem testu na obecność HIV powinny być jak najszybciej skierowane do poradni dla osób żyjących z HIV lub oddziału chorób zakaźnych, który ma doświadczenie w diagnozowaniu i leczeniu pacjentów z zakażeniem HIV.
Obowiązek zgłaszania
- Zgłoszenie podejrzenia lub rozpoznania zakażenia HIV/zachorowania na AIDS/zgonu osoby zakażonej HIV/chorej na AIDS, podlega zgłoszeniu na druku ZLK-4 (w formie elektronicznej lub papierowej)
Leczenie
- Poniższe zalecenia odnoszą się wyłącznie do leczenia zakażeń wirusem HIV–1.
- Niektóre leki są mniej skuteczne w zakażeniach HIV–2.
- Zakażenie HIV–2 powinno być zawsze leczone w specjalistycznym ośrodku.
Cele leczenia
- Podstawowym celem jest zwiększenie czasu przeżycia wolnego od choroby przy maksymalnym zahamowaniu replikacji wirusowej i zachowaniu funkcji układu immunologicznego.
- Biochemicznym celem leczenia jest obniżenie poziomu wirusowego RNA poniżej dolnej granicy wykrywalności (około 20 kopii wirusa/ml).
- Zapobieganie rozwojowi powikłanych zakażeń oportunistycznych.
- Leczenie powikłań.
- Unikanie przeniesienia zakażenia na inne osoby.
Ogólne informacje o leczeniu
- Leczenie powinno być prowadzone przez odpowiednio wyspecjalizowanych lekarzy.
- Oprócz terapii przeciwwirusowej leczenie obejmuje również opiekę psychiatryczną/psychologiczną i wsparcie społeczne, a także leczenie chorób współistniejących.
- Niezbędne jest ciągłe leczenie skojarzone za pomocą co najmniej 3 skutecznych leków:
- Terapia antyretrowirusowa, wcześniej nazywana wysoce aktywną terapią antyretrowirusową (highly active antiretroviral treatment – HAART).
- Dobry wynik leczenia wymaga motywacji i wysokiego poziomu przestrzegania zaleceń lekarskich.
- Wbudowany w DNA zakażonych limfocytów T wirus pozostaje w stanie latencji.
- Do ponownej replikacji dochodzi w wyniku przerwania dotychczasowego leczenia.
Wskazanie do terapii antyretrowirusowej (ARV/ART)
- Wskazanie
- Zakażenie HIV powinno być stale leczone terapią antyretrowirusową, niezależnie od stanu immunologicznego i poziomu wiremii w osoczu.
- Przy braku przeciwwskazań leczenie powinno być wdrożone w ciągu 7 dni, a jeżeli istnieje możliwość – w dniu rozpoznania, u wszystkich osób zakażonych HIV niezależnie od liczby limfocytów T CD4+.
Farmakoterapia
- Leczenie składa się z połączenia zazwyczaj trzech leków, których dawkowanie oparte jest na wynikach oznaczenia oporności, a także na ocenie działań niepożądanych, chorób towarzyszących i interakcji lekowych.
- Zgodnie z aktualną wiedzą leczenie trwa całe życie bez wprowadzania przerw.
- Zalety wczesnego rozpoczęcia terapii:
- mniejsza liczba powikłań klinicznych (np. chłoniak w przebiegu HIV)
- mniej działań niepożądanych
- poprawia się kontrola immunologiczna dodatkowo nabytych i powszechnych zakażeń o wysokim ryzyku reaktywacji (np. gruźlica)
- niskie ryzyko rozwoju zapalnego zespołu rekonstrukcji immunologicznej (IRIS).
Zarejestrowane i najczęściej stosowane w Polsce leki antyretrowirusowe i ich symbole
- Inhibitory integrazy (INI), takie jak:
- BIC – biktegrawir
- DTG – dolutegrawir
- EVG – elwitegrawir
- RAL – raltegrawir.
- Nukleozydowe inhibitory odwrotnej transkryptazy (nucleoside reverse transcriptase inhibitor – NRTI), takie jak:
- ABC – abakawir
- FTC– emtrycytabina
- 3TC – lamiwudyna
- TAF – alafenamid tenofowiru
- TDF – dizoproksyl tenofowiru.
- Nienukleozydowe inhibitory odwrotnej transkryptazy (non-nucleoside reverse transcriptase inhibitor – NNRTI), takie jak:
- DOR – dorawiryna.
- Inhibitory proteazy (protease inhibitor – PI), takie jak:
- DRV – darunawir.
- Substancje wzmacniające, takie jak:
- C – kobicystat
- r – ritonawir.
Schematy leczenia pierwszego rzutu
- Zalecane schematy sa dostępne w aktualnych wytycznych postępowania4
Działania niepożądane
- Leczenie początkowo może wiązać się z działaniami niepożądanymi, nawet jeśli stosowane leki są nowej generacji.
- Działania niepożądane często są przemijające lub ich nasilenie zmniejsza się stopniowo w czasie od 1 do 12 tygodni.
- Możliwa jest zmiana kombinacji leków tak, aby pacjenci lepiej tolerowali leczenie.
- Lipodystrofia, choroby sercowo–naczyniowe wtórne do zmian stężenia lipidów we krwi oraz inne działania niepożądane mogą skłaniać do przerwania leczenia.
- Zarówno wymienione powikłania oraz zaprzestanie terapii mogą mieć znaczenie dla długoterminowego rokowania.
Interakcje leków
- Występuje wiele możliwości interakcji pomiędzy lekami antyretrowirusowymi i lekami towarzyszącymi, suplementami diety, medycyną komplementarną i alternatywną, miękkimi i twardymi narkotykami.
- Duża zmienność osobnicza, np. z powodu polimorfizmu genowego.
- Szczególne znaczenie mają między innymi poniższe grupy substancji czynnych:
- leki przeciwpadaczkowe
- leki przeciwdepresyjne
- substancje wazoaktywne
- leki przeciwhistaminowe
- leki przeciwarytmiczne
- leki przeciwinfekcyjne
- leki antykoncepcyjne
- statyny (podwyższone ryzyko rabdomiolizy przy łączeniu z inhibitorami proteazy)
- steroidy, miejscowe lub ogólnoustrojowe.
- Ze względu na możliwe nowe odkrycia zdecydowanie zaleca się sprawdzanie konkretnych potencjałów interakcji przepisywanych leków (np. w bazach danych dotyczących interakcji, takich jak HIV Drug Interaction Checker).
Niewystarczający efekt terapeutyczny
- Może przyczynić się do rozwoju oporności.
- Niedostateczne przestrzeganie zaleceń lekarskich sprzyja rozwojowi oporności.
- W przypadku niepowodzenia leczenia może być wskazane połączenie więcej niż 3 leków.
- Podstawę przy wyborze leczenia stanowią testy oporności genotypowej wirusa na lek.
Ciąża i karmienie piersią
Test na obecność HIV
- W Polsce, zalecane jest dwukrotne wykonanie testu w kierunku HIV u ciężarnej: do 10. tygodnia ciąży lub w chwili pierwszego zgłoszenia się oraz między 33. a 37. tygodniem ciąży. Lekarz ma obowiązek zaproponować pacjentce badanie w kierunku zakażenia HIV, a odmowę odnotować w dokumentacji medycznej.
- Przeprowadzeniu testu na HIV powinna towarzyszyć oferta poradnictwa i informacja o możliwościach leczenia.
- Podczas poradnictwa powinno się podkreślić m.in. pozytywny wpływ terapii anty–HIV na zdrowie i długość życia osób zakażonych wirusem oraz na ryzyko przeniesienia zakażenia z matki na dziecko i na partnerów seksualnych.
- W razie potrzeby należy udostępnić kobiecie ciężarnej adresy i numery telefonu innych placówek z ofertą doradczą.
- Jeśli przyszła matka nie sprzeciwia się testowi, w ramach opieki prenatalnej rutynowo wykonuje się test przesiewowy i w razie potrzeby dodatkowy test na potrzeby potwierdzenia lub wykluczenia zakażenia HIV.
- Kobieta w ciąży powinna zostać poinformowana o wyniku testu w zrozumiały sposób – nawet jeśli zakażenie nie zostanie stwierdzone – tak, aby była w stanie zadawać pytania.
- Przeprowadzeniu testu na HIV powinna towarzyszyć oferta poradnictwa i informacja o możliwościach leczenia.
Wskazania terapeutyczne3-4
- U kobiet w ciąży zakażonych wirusem HIV obowiązują te same wskazania do stosowania skojarzonej terapii przeciwretrowirusowej (combined antiretroviral therapy – cART) co u kobiet, które nie są w ciąży.
- Każde zakażenie HIV w czasie ciąży jest wskazaniem do wprowadzenia leczenia.
- Terapia skojarzona lub profilaktyka z użyciem substancji przeciwretrowirusowych zmniejsza ryzyko przeniesienia choroby z matki na dziecko.
- W przypadku zakażenia HIV, które zostało nowo zdiagnozowane w czasie ciąży, należy rozpocząć leczenie najszybciej jak to możliwe. Leczenie powinno zostać wdrożone najpóźniej na początku II. trymestru.
- Skuteczna ART powinna być nadal kontynuowana. Dotychczas stosowana ART powinna zostać zmieniona, jeśli nie ma wystarczających dowodów na jej bezpieczeństwo.
- Celem cART w czasie ciąży jest skuteczna profilaktyka przeniesienia wirusa HIV na dziecko poprzez maksymalne zahamowanie replikacji wirusa u matki przy możliwie najlepszej tolerancji dla ciężarnej i płodu.
- Jeśli to możliwe, kobiety w wieku rozrodczym powinny być leczone cART, którą można stosować bez zmian w przypadku ciąży.
- Dolutegrawir może prowadzić do wad cewy nerwowej u nienarodzonego dziecka. Dlatego nie powinien on być stosowany u kobiet w ciąży, a u kobiet w wieku rozrodczym wyłącznie wtedy, gdy stosują skuteczne metody antykoncepcyjne. W przypadku zajścia chorej w ciążę należy zmienić dotychczasowe leczenie i zastosować alternatywne.
- Decyzję o przerwaniu terapii po porodzie powinni podejmować jedynie lekarze, którzy posiadają doświadczenie w leczeniu pacjentek zakażonych wirusem HIV. Taka decyzja powinna być podejmowana razem z pacjentką.
Zalecane kombinacje leków
-
-
- Schematy leczenia dostępne w aktualnych wytycznych4
-
Monitorowanie parametrów laboratoryjnych – pod kontrolą Poradni Chorób Zakaźnych/Poradni Leczenia HIV/AIDS
- Comiesięczne kontrole morfologii krwi (możliwość wystąpienia związanej z lekami niedokrwistości lub małopłytkowości).
- Badanie oporności
- przed rozpoczęciem cART w ciąży należy wykonać badanie oporności.
- Badanie stężenia leków
- Farmakokinetyka substancji antyretrowirusowych może zostać zmieniona przez ciążę.
- Z tego powodu badania poziomu leków we krwi w czasie ciąży mogą być przydatne, szczególnie w przypadku wystąpienia działań niepożądanych lub niewystarczającej redukcji wiremii.
- Nie należy podawać kombinacji elwitegrawiru/kobicystatu ani darunawiru/kobicystatu ze względu na małe stężenie w osoczu i związane z tym zwiększone ryzyko niepowodzenia leczenia oraz przeniesienia choroby z matki na dziecko w czasie ciąży.
Rodzaj porodu i profilaktyka ekspozycji
- Poród pochwowy jest zalecaną opcją w następujących warunkach:
- Ciężarna przyjmuje skojarzoną terapię antyretrowirusową.
- Wiremia HIV wynosi <50 kopii/ml pod koniec ciąży (co najmniej 4 tygodnie do terminu porodu).
- W takim przypadku profilaktyka śródporodowa nie jest konieczna, ale po porodzie może być konieczna profilaktyka poekspozycyjna (patrz poniżej).
- Ocena ryzyka związanego z porodem przez doświadczony personel położniczy.
- Uwzględnienie problemów logistycznych (np. odległość do odpowiedniej kliniki położniczej).
- Zakażone HIV ciężarne z wiremią HIV >50 kopii/ml w 36. tygodniu ciąży powinny rodzić przez planowe cięcie cesarskie wykonywane przez doświadczony zespół medyczny najwcześniej od 37. tygodnia ciąży.
- W tym przypadku powinna zostać zastosowana profilaktyka ekspozycji śródporodowej i poporodowej z użyciem zydowudyny.
- Natomiast w przypadku wiremii HIV >1000 kopii/ml w 36. tygodniu ciąży należy zastosować profilaktykę ekspozycji śródporodowej i przedłużoną profilaktykę ekspozycji poporodowej (patrz poniżej).
- W tym przypadku powinna zostać zastosowana profilaktyka ekspozycji śródporodowej i poporodowej z użyciem zydowudyny.
Sytuacje ryzyka
- Podwyższona wiremia na krótko przed porodem
- Jeśli wiremia do czasu porodu nie spadła poniżej 50 kopii/ml lub kiedy na krótko przed porodem dochodzi do wzrostu wiremii.
- Zmiana lub intensyfikacja przyjmowania leków przez matkę z pomocą doświadczonych specjalistów leczących HIV.
- Jeśli w niedługim czasie konieczny jest poród lub jeśli poród już trwa, a wiremia wynosi >50 kopii/ml, to matka powinna otrzymać dożylnie zydowudynę okołoporodowo, jeśli pozwala na to czas. Jednak terminowy poród ma najwyższy priorytet.
- W konkretnych przypadkach można rozważyć dalszą eskalację leków podawanych matce przed porodem
- Jeśli wiremia do czasu porodu nie spadła poniżej 50 kopii/ml lub kiedy na krótko przed porodem dochodzi do wzrostu wiremii.
- Brak terapii antyretrowirusowej u matki przed porodem
- Jeśli mimo znanego zakażenia HIV nie stosowano profilaktyki zakażenia do czasu porodu, to należy ją podać najpóźniej śródporodowo i poporodowo jako profilaktykę eskalowaną.
- Nawet w przypadku niepełnej profilaktyki zakażenia wewnątrzmacicznego można spodziewać się korzyści, jeśli profilaktyka ekspozycji poporodowej zostanie rozpoczęta najpóźniej do 72 godzin po porodzie.
- Jeśli – w zależności od zaawansowania fazy porodu – przy pierwszej prezentacji klinicznej nadal istnieje możliwość wykonania cięcia cesarskiego, należy podjąć taką próbę.
- Jeśli poród jest wymagany w niedługim czasie lub już trwa, to okołoporodowo powinna być podana dożylnie zydowudyna, jeśli czas na to pozwala.
- Jednak terminowy poród ma najwyższy priorytet.
- Terapia przeciwwirusowa matki nie powinna być z reguły intensyfikowana przed porodem, jednak w indywidualnych przypadkach można to rozważyć.
- Jeśli mimo znanego zakażenia HIV nie stosowano profilaktyki zakażenia do czasu porodu, to należy ją podać najpóźniej śródporodowo i poporodowo jako profilaktykę eskalowaną.
Po porodzie
- Przy niskim ryzyku przeniesienia zakażenia
- Skuteczna ART została rozpoczęta już przed ciążą, a RNA HIV wynosiło poniżej 50 kopii/ml przez całą ciążę: można zrezygnować z poporodowej profilaktyki transmisji.
- Jeśli miano wirusowe HIV u matki wynosi <1000 kopii/ml w momencie porodu, to poporodowe doustne podanie zydowudyny noworodkowi odbywa się w ciągu 6 godzin od porodu i trwa przez 4 tygodnie.
- Rozszerzanie (eskalowanie) profilaktyki transmisji postnatalnej
- Przy wysokim ryzyku przeniesienia zakażenia na dziecko, np. w przypadku braku terapii matki przed porodem lub zwiększonego miana wirusowego u matki na krótko przed porodem, można ewentualnie rozszerzyć profilaktykę poprzez podanie noworodkowi 2–3 substancji przeciwwirusowych zamiast samej zydowudyny.
- W przypadku braku terapii matki przed porodem zaleca się eskalację profilaktyki poporodowej noworodka za pomocą kombinacji z zastosowaniem newirapiny (pierwsza dawka jak najwcześniej po porodzie, co najmniej w ciągu 48 godzin, druga dawka 48 godzin po pierwszym podaniu i trzecia dawka 96 godzin po drugim podaniu) oraz zydowudyny przez 4 do 6 tygodni.
- Aby uniknąć oporności na newirapinę, można rozważyć połączenie tego schematu (3 dawki newirapiny + 6 tygodni zydowudyny) z 14–dniowym podawaniem noworodkowi lamiwudyny.
- W przypadku istniejącej lub prawdopodobnej oporności na NNRTI można zastosować raltegrawir.
- W każdym przypadku powinno nastąpić szczegółowe poradnictwo antykoncepcyjne w ramach rutynowego badania ginekologicznego 6–8 tygodni po porodzie.
- Karmienie piersią
- Zależy od miana RNA HIV.
- >50 kopii/ml: zaleca się rezygnację z karmienia piersią.
- <50 kopii/ml: wspólne podejmowanie decyzji po uzyskaniu informacji o ryzyku i korzyściach związanych z karmieniem piersią.
- Leczenie przeciwretrowirusowe matki i dziecka istotnie zmniejsza ryzyko przeniesienia zakażenia.3
- Karmienie piersią wiąże się jednak wówczas, oprócz minimalnego ryzyka transmisji wirusa, także ze znaczną ekspozycją niemowlęcia na leki.
- Warunki bezpiecznego karmienia piersią.
- Skuteczna ART potwierdzona przez utrzymywanie się miana RNA HIV na poziomie <50 kopii/ml przez wiele miesięcy.
- Wiarygodne zażywanie ART, potwierdzone m.in. przez dotychczasowe zaangażowanie i ciągłe przestrzeganie zaleceń lekarskich.
- Gotowość pacjentki na dodatkowe monitorowanie RNA HIV podczas karmienia piersią.
- Zależy od miana RNA HIV.
HIV u dzieci i młodzieży
- Niemowlęta powinny niezwłocznie otrzymać ART.
- Dzieci w wieku powyżej 12–36 miesiąca powinny otrzymać ART.
- Dzieci w wieku od 37 miesięcy do 12 lat
- bezobjawowe bez niedoboru odporności: powinny otrzymać ART
- objawowe i/lub z niedoborem odporności: powinny otrzymać ART.
- Młodzież w wieku powyżej 12 lat powinna być leczona jak dorośli.
- Liczba nowych zakażeń HIV u dzieci znacznie się zmniejszyła dzięki profilaktyce przeniesienia zakażeń okołoporodowych.
- Opieka medyczna nad dziećmi i młodzieżą z HIV powinna być odbywać się w ścisłej współpracy z pediatrycznym ośrodkiem specjalizującym się w leczeniu HIV.
- Zalecane kombinacje leków w terapii początkowej dostepne w aktualnych wytycznych
- Więcej informacji na temat dzieci zakażonych HIV w przedszkolu i innych placówkach publicznych znajduje się w rozdziale zapobieganie.
Choroby przenoszone drogą płciową u pacjentów/pacjentek zakażonych HIV
- Wszystkie osoby zakażone HIV, które są aktywne seksualnie, powinny być badane co roku pod kątem kiły, chlamydii (kobiety, mężczyźni) i gonokoków, a także przy zmianie partnera, przy zajściu w ciążę lub w przypadku wystąpienia objawów.
- W zależności od liczby partnerów mogą być uzasadnione krótsze odstępy między kontrolami.
- Powyżej 5 partnerów/partnerek: kontrole półroczne w kierunku HCV, kiły, zakażeń odbytnicy chlamydiami i gonokokami
- Powyżej 10 partnerów/partnerek: kwartalne badania w kierunku kiły, gonokoków i chlamydii
- W zależności od liczby partnerów mogą być uzasadnione krótsze odstępy między kontrolami.
- Badania u mężczyzn
- Badanie moczu (pierwszy strumień) w kierunku chlamydii i rzeżączki (NAAT).
- Wymaz z odbytu na obecność chlamydii i rzeżączki (NAAT).
- Wymaz z gardła na obecność rzeżączki (NAAT).
- Krew: serologia kiły (ewentualnie badania w kierunku wirusowego zapalenia wątroby typu B/C).
- Wykrywanie zakażenia chlamydiami u mężczyzn, którzy uprawiają seks z mężczyznami.
- Dalsze subtypowanie, w celu odpowiedniego leczenia oraz w celu wykrycia wariantów drobnoustroju, które mogą powodować ziarnicę weneryczną
- Badania u kobiet:
- Wymaz z pochwy na obecność chlamydii i rzeżączki (NAAT).
- Ewentualnie wymaz z odbytu na obecność chlamydii i rzeżączki (NAAT).
- Ewentualnie wymaz z gardła na obecność rzeżączki (NAAT).
- Krew: serologia kiły (ewentualnie wirusowe zapalenie wątroby typu B/C).
Leczenie
- Ustalenie źródła zakażenia, informacja.
- Brak współżycia płciowego podczas leczenia chorób przenoszonych drogą płciową towarzyszących zakażeniu HIV.
- Zalecenie stosowania prezerwatyw, co najmniej do czasu uzyskania wyniku badania próbki kontrolnej.
- Leczenie zakażenia chlamydiami
- Niepowikłane zakażenie chlamydiami układu moczowo–płciowego lub odbytnicy: doksycyklina 200 mg dziennie przez 7 dni.
- Kontrola 5 tygodni po leczeniu.
- Ewentualnie także kontrola w przypadku podejrzenia niepowodzenia terapii lub wznowienia infekcji.
- W ciąży: azytromycyna 1 g jako dawka pojedyncza.
- Kontrola 5 tygodni po leczeniu.
- Więcej informacji w artykułach zakażenie chlamydiami narządów płciowych u kobiet oraz zakażenie chlamydiami narządów płciowych u mężczyzn.
- Niepowikłane zakażenie chlamydiami układu moczowo–płciowego lub odbytnicy: doksycyklina 200 mg dziennie przez 7 dni.
- Leczenie rzeżączki
- Przy dodatnim wyniku NAAT: wykonać hodowlę bakterii i rozpocząć leczenie.
- Niepowikłana rzeżączka układu moczowo-płciowego/odbytu/gardła: dawka pojedyncza 1 g ceftriaksonu (domięśniowo lub dożylnie) i 1,5 g azytromycyny doustnie.
- Kontrola NAAT 2 tygodnie po leczeniu.
- Szczegóły w artykule rzeżączka.
- Leczenie epizodu opryszczki narządów płciowych (HSV) (więcej informacji w artykułach opryszczka genitalna u mężczyzn oraz opryszczka genitalna u kobiet) u pacjentów/pacjentek zakażonych HIV:6
- Pierwsze zakażenie.
- Acyklowir 5 x dziennie 400 mg przez 7–10 dni.
- Walacyklowir 2 x dziennie 500–1000 mg przez 10 dni.
- Famcyklowir 3 x dziennie 250–500 mg przez 10 dni.
- Opryszczka genitalna o piorunującym przebiegu.
- Acyklowir 5–10 mg/kg m.c. dożylnie co 8 godzin przez 2–7 dni.
- Przejście na leki doustne w przypadku poprawy klinicznej.
- Leczyć łącznie przez co najmniej 10 dni.
- Nawrót.
- U większości pacjentów wystarczy 5–dniowa kuracja.
- U pacjentów/pacjentek z wystarczającą liczbą komórek CD4 (> 500 komórek/mikrolitr) mogą być wystarczające krótsze schematy.
- W przypadku osób zakażonych wirusem HIV bez przesłanek niedoboru odporności, standardowe dawki wydają się być wystarczające (patrz artykuł opryszczka genitalna u mężczyzn oraz opryszczka genitalna u kobiet) (Ib/A).
- U pacjentów/pacjentek z zaawansowanym AIDS może być konieczne podwojenie standardowej dawki i leczenie przez dłużej niż 5 dni.
- Należy zachować ostrożność przy stosowaniu krótkich terapii, ponieważ nie zostały one wystarczająco dobrze przebadane w leczeniu pacjentów z obniżoną odpornością.
- Kobiety w ciąży.
- Leczenie supresyjne od 32. tygodnia ciąży u pacjentek z wcześniejszą opryszczką genitalną (i HIV): acyklowir 3 x dziennie 400 mg.
- Więcej informacji na temat leczenia opryszczki genitalnej w ciąży można znaleźć w artykule opryszczka genitalna u kobiet.
- Pierwsze zakażenie.
- Leczenie kiły
- Kiła wczesna, czas trwania poniżej 1 roku i bez powikłań:
- benzylopenicylina benzatynowa 2,4 miliona j.m. jako dawka pojedyncza.
- Zakażenie latentne lub późne, zakażenie powyżej 1 roku i bez powikłań:
- benzylopenicylina benzatynowa 2,4 miliona j.m. domięśniowo 1 x na tydzień przez 3 tygodnie.
- Kontrola serologii po 3, 6 i 12 miesiącach, a następnie co roku.
- Więcej szczegółów można znaleźć w artykule kiła.
- Kiła wczesna, czas trwania poniżej 1 roku i bez powikłań:
Zapalny zespół rekonstrukcji immunologicznej
- Zapalny zespół rekonstrukcji immunologicznej (immune reconstitution inflammatory syndrome – IRIS lub immune restoration disease – IRD):2
- Paradoksalna reakcja na utajone (ewentualnie jawne) zakażenie oportunistyczne, która może wystąpić kilka tygodni po rozpoczęciu ART.
- Zapadalność: 5–10% wszystkich osób leczonych ART.
- ART prowadzi do nadmiernej odpowiedzi immunologicznej i tym samym do klinicznego pogorszenia chorób oportunistycznych:
- wzrost liczby komórek CD4 i spadek miana wirusowego
- objawy aktywnych zakażeń oportunistycznych przypominają np.:
- gruźlicę
- zapalenie płuc wywołane przez Pneumocystis jirovecii
- kryptokokowe zapalenie opon mózgowo–rdzeniowych
- cytomegalię (CMV, więcej szczegółów w artykule choroby przenoszone drogą płciową u mężczyzn, którzy uprawiają seks z mężczyznami)
- Diagnostyka różnicowa
- skutki uboczne leków
- problemy z przestrzeganiem zaleceń lekarskich
- nowe zakażenie.
- Leczenie
- Leczenie zakażenia oportunistycznego zgodnie z obowiązującymi wytycznymi.
- W przypadku łagodnych objawów ewentualnie leki z grupy NLPZ.
- Glikokortykosteroidy.
- Mogą być skuteczne w przypadku zmian patologicznych w centralnym układzie nerwowym, zajętych węzłów chłonnych lub nasilających się problemów z oddychaniem.
- Wykazano ich korzyści, zwłaszcza w zespole IRIS związanym z zakażeniem prątkami gruźlicy.
- W zespole IRIS związanym z zakażeniem kryptokokami (ze wzrostem ciśnienia śródmózgowego): glikokortykosteroidy stosować przez co najmniej 2–6 tygodni.
- Wstrzymanie ART tylko w najcięższych przypadkach.
- Rokowanie jest dobre przy aktywnej diagnostyce i wczesnym leczeniu.
Leczenie po ekspozycji na HIV
Działania natychmiastowe po ekspozycji zawodowej na HIV
- Urazy spowodowane zakłuciem lub skaleczeniem
- Nie należy natychmiast zatrzymywać spontanicznego wypływu krwi, ponieważ umożliwia to wypłukanie potencjalnie zakaźnego materiału.
- Pozostawić do krwawienia przez co najmniej 1 minutę.
- Jeśli to możliwe, należy unikać innych manipulacji przy ranie, zwłaszcza ściskania i uciskania bezpośrednio w miejscu wkłucia, aby uniknąć rozprzestrzeniania się patogenu do głębszych warstw tkanek.
- Po spontanicznym krwotoku: ewentualnie rozszerzyć kanał zakłucia i dokładnie spłukać wodą/mydłem lub użyć środka antyseptycznego (środek do dezynfekcji rąk na bazie etanolu lub środek antyseptyczny do skóry).
- Nie należy natychmiast zatrzymywać spontanicznego wypływu krwi, ponieważ umożliwia to wypłukanie potencjalnie zakaźnego materiału.
- Zanieczyszczenie oka
- Natychmiastowe przepłukanie 0,9% NaCl lub wodą.
- Kontaminacja jamy ustnej
- Zakażony materiał natychmiast wypluć, w miarę możliwości całkowicie.
- Następnie kilkakrotnie przepłukać jamę ustną 0,9% NaCl lub wodą (4–5 razy).
- Wyplucie każdej porcji po około 15 sekundach energicznego płukania – ruchu tam i z powrotem w jamie ustnej
- Zanieczyszczenie uszkodzonej lub zmienionej zapalnie skóry
- Dokładne mycie wodą z mydłem.
- Następnie, jeśli to możliwe, obfite przetarcie powierzchni skóry wacikiem nasączonym antyseptykiem skórnym, objęcie nim okolicy skontaminowego obszaru.
- Bezpośrednio po podjęciu działań natychmiastowych
- Decyzja w sprawie ogólnoustrojowej farmakologicznej profilaktyki poekspozycyjnej.
- Dokumentacja powypadkowa (lekarz medycyny pracy).
- Pierwszy test na obecność przeciwciał HIV.
- Serologia wirusowego zapalenia wątroby.
Działania natychmiastowe po ekspozycji na HIV przez kontakt seksualny
- Po ekspozycji podczas stosunku płciowego z penetracją
- Umycie prącia pod bieżącą wodą z mydłem.
- W tym celu należy odciągnąć napletek i dokładnie oczyścić żołądź, a także wewnętrzną stronę napletka (bez wywierania nacisku na błonę śluzową).
- Umycie prącia pod bieżącą wodą z mydłem.
- Po przyjęciu spermy do jamy ustnej
- Całkowite wyplucie jej jak najszybciej.
- Następnie należy 4–5 razy przepłukać krótko (około 15 sekund) jamę ustną wodą.
- Nie jest jasne, czy połknięcie przyjętej spermy jest bardziej niekorzystne niż jej wyplucie; w przypadku wytrysku w tylnej części gardła połknięcie może być bardziej skuteczne w usuwaniu ejakulatu z jamy ustnej niż wyplucie.
- Jeśli ejakulat dostanie się do oka, należy natychmiast przepłukać je wodą.
Pobieranie próbek krwi po ekspozycji na HIV
- Próbki krwi od osoby narażonej – komplet badań zlecany przez specjalistę chorób zakaźnych:
- badanie HIV Ag/HIV Ab (ewentualnie szybki test)
- anty–HCV
- HBsAg i anty–HBs
- serologia kiły
- morfologia krwi z rozmazem
- kreatynina
- bilirubina, GPT (ALT), ALP
- glikemia, lipidogram
- ewentualnie test ciążowy
- ewentualnie test przesiewowy na obecność narkotyków lub leków
- test na inne choroby przenoszone drogą płciową do decyzji, ewentualne badania kontrolne po 2 i 6 tygodniach w razie potrzeby
- powtórzenie testu na obecność przeciwciał HIV i serologii wirusowego zapalenia wątroby po 6 tygodniach, a także po 3 i 6 miesiącach
- dodatkowo przy rozpoczynaniu PEP HIV, jak również po 2 tygodniach:
- glikemia
- morfologia krwi
- transaminazy
- bilirubina
- GGTP
- kreatynina
- badanie ogólne moczu oraz osad moczu
- Jeśli w ciągu 3 miesięcy po ekspozycji lub po zakończeniu profilaktyki farmakologicznej wystąpi ostry, gorączkowy obraz kliniczny, konieczne jest wyjaśnienie diagnostyczne pierwotnego zakażenia HIV. Jeśli badania przeciwciał są ujemne, to ewentualnie również należy wykonać wykrywanie kwasów nukleinowych wirusa (NAT, PCR HIV)
- szczególnie podejrzany jest ostry obraz kliniczny w ciągu pierwszych 4 tygodni po ekspozycji lub po zakończeniu PEP
- dodatni wynik PCR wymaga potwierdzenia za pomocą drugiego oznaczenia
- Rutynowe stosowanie procedury amplifikacji kwasów nukleinowych u bezobjawowych osób narażonych na HIV nie jest wskazane ze względu na niską pozytywną wartość predykcyjną.
- Próbka krwi od pacjenta źródłowego
- Oznaczenie przeciwciał HIV (HIV Ab) i antygenu HIV (HIV Ag)
- RNA HIV
- Anty–HCV i HCV RNA
- HBsAg i anty–HBs
- Ewentualnie test przesiewowy na obecność narkotyków lub leków
- Jeśli zakażenie HIV u pacjenta źródłowego zostanie potwierdzone i nie są dostępne aktualne wartości kontrolne, należy dążyć do ponownego oznaczenia liczby komórek CD4/mcl i aktualnego miana wirusowego.
- Jeśli są dostępne analizy oporności wirusa HIV pacjenta źródłowego, należy je uwzględnić w procesie podejmowania decyzji o zalecaniu PEP.
- Przed wykonaniem testu na obecność HIV i testu serologicznego pod kątem wirusowego zapalenia wątroby należy uzyskać zgodę osoby badanej.
- Należy respektować odmowę wykonania testu na obecność HIV pacjenta źródłowego.
- W niektórych krajach istnieją regulacje, które pozwalają na badanie pacjenta źródłowego w określonych warunkach (np. po gwałcie lub po napadzie z użyciem zużytej strzykawki) nawet bez jego zgody.
- Z reguły wymagany jest do tego nakaz sądow.
PEP
W przypadku narażenia zawodowego na HIV (pacjent źródłowy zakażony HIV)
- Należy przeprowadzić PEP HIV, gdy istnieje zwiększone ryzyko zakażenia:
- Przezskórna (krwawiąca) rana kłuta igłą do iniekcji lub inną wydrążoną igłą i miano wirusowe pacjenta źródłowego >50 kopii/ml lub nieznane.
- Rana cięta zadana skontaminowanym skalpelem, nożem lub podobnym narzędziem i miano wirusowe pacjenta źródłowego >50 kopii/ml lub nieznane.
- PEP HIV można przeprowadzić w następujących przypadkach:
- Przezskórna (krwawiąca) rana kłuta, zadana igłą do iniekcji lub inną wydrążoną igłą i miano wirusowe u pacjenta źródłowego <50 kopii/ml.
- Rana cięta zadana skontaminowanym skalpelem, nożem lub podobnym narzędziem i miano wirusowe pacjenta źródłowego <50 kopii/ml.
- Kontakt błony śluzowej lub kontakt uszkodzonej skóry (egzema skórna, świeża rana itp.) z płynami ustrojowymi pacjenta źródłowego o potencjalnie wysokim mianie wirusowym (>50 kopii/ml lub miano wirusowe nieznane).
- Widoczne, powierzchowne zranienia bez wypływu krwi, np. za pomocą zabrudzonej krwią igły chirurgicznej, przy potencjalnie wysokim mianie wirusowym pacjenta źródłowego (>50 kopii/ml lub miano wirusowe nieznane).
- Kontakt spojówki oka z materiałem potencjalnie zakaźnym, takim jak krew lub inny płyn ustrojowy pacjenta źródłowego, i potencjalnie wysokie miano wirusowe u pacjenta źródłowego (>50 kopii/ml lub miano wirusowe nieznane).
- Masywna inokulacja (>1 ml) krwi lub innego płynu ustrojowego, np. w otwarte pole operacyjne oraz potencjalnie wysokie miano wirusowe pacjenta źródłowego (>50 kopii/ml lub nieznane).
- PEP HIV nie jest wskazana w przypadku wszystkich wątpliwych ekspozycji na HIV bez ryzyka lub z niskim ryzykiem, np.:
- Kontakt ze skórą lub błoną śluzową, kontakt z płynami ustrojowymi niskiego ryzyka, takimi jak mocz lub ślina.
- Kontakt z materiałem zakaźnym, o jakimkolwiek ryzyku, z nieuszkodzoną skórą.
- Kontakt z błoną śluzową lub kontakt uszkodzonej skóry (egzema skórna, świeża rana itp.) z płynami ustrojowymi pacjenta źródłowego z mianem wirusowym <50 kopii/ml.
- W przypadku widocznych, powierzchownych zranień bez wypływu krwi, np. zranienie zabrudzoną krwią igłą chirurgiczną od pacjenta źródłowego z miano wirusowym < 50 kopii/ml.
W przypadku ran kąsanych lub ran ciętych
- Powinno się przeprowadzać PEP HIV w następujących przypadkach:
- Głębokie krwawiące ukąszenie przez osobę zakażoną wirusem HIV, która nie jest leczona lub nie jest wystarczająco dobrze leczona terapią przeciwretrowirusową, a także sama ma krwawiące uszkodzenia w jamie ustnej w momencie ugryzienia (np. ugryzienie w język podczas napadu padaczkowego).
- Zalecać PEP w następujących przypadkach:
- Seryjne, krwawiące obrażenia spowodowane tym samym narzędziem (np. w przypadku seryjnych zranień nożem) i nieznanego lub możliwego do ustalenia jedynie z opóźnieniem statusu HIV rannego.
W przypadku dożylnego stosowania narkotyków i urazów od igieł
- PEP powinna następować w następujących przypadkach:
- wspólne używanie sprzętu do iniekcji skontaminowanego wirusem HIV.
- PEP może być stosowana w następujących przypadkach:
- wspólne użytkowanie sprzętu do iniekcji bez wiedzy o statusie HIV innych osób zażywających wspólnie narkotyki.
- PEP nie powinno odbywać się w następujących przypadkach:
- rany kłute osób postronnych spowodowane przez leżący w pobliżu sprzęt do wstrzykiwania narkotyków (igły).
W razie stosunku płciowego z osobą zakażoną wirusem HIV
- Stosunek płciowy niezabezpieczony (np. w wyniku pęknięcia prezerwatywy) aktywny lub pasywny, pochwowy lub analny z osobą, o której wiadomo, że jest zakażona HIV.
- Zalecać PEP, jeśli osoba źródłowa jest nieleczona lub jeśli miano wirusowe >1000 kopii/ml, a także jeśli nie można określić statusu leczenia.
- Proponować PEP, jeśli miano wirusowe osoby źródłowej wynosi 50–1000 kopii/ml.
- Nie ma wskazań do PEP, jeśli osoba źródłowa jest skutecznie leczona (miano wirusowe <50 kopii/ml).
Jeśli status HIV partnerów/partnerek seksualnych jest nieznany
- Zaproponować PEP:
- Po stosunku analnym lub pochwowym bez zabezpieczenia (łącznie z gwałtem i innymi formami przemocy seksualnej), jeśli istnieje zwiększone prawdopodobieństwo, że u partnerki seksualnej/partnera seksualnego może występować nieznane lub nieleczone zakażenie HIV, np.:
- Przy stosunkach płciowych między mężczyznami lub
- Osobom heteroseksualnym, gdy ich partnerki lub partnerzy aktywnie zażywają narkotyki dożylnie, pochodzą z regionu o wysokiej częstości występowania HIV (np. z Afryki Subsaharyjskiej) lub są osobami biseksualnymi.
- Po stosunku analnym lub pochwowym bez zabezpieczenia (łącznie z gwałtem i innymi formami przemocy seksualnej), jeśli istnieje zwiększone prawdopodobieństwo, że u partnerki seksualnej/partnera seksualnego może występować nieznane lub nieleczone zakażenie HIV, np.:
- Brak wskazań do PEP w następujących przypadkach:
- stosunek oralny
- niezależnie od prawdopodobieństwa obecności nieleczonego zakażenia HIV
u partnerów/partnerek seksualnych i niezależnie od rodzaju seksu oralnego (aktywny, pasywny, połykanie nasienia)
- niezależnie od prawdopodobieństwa obecności nieleczonego zakażenia HIV
- pocałunki
- kontakt wirusa HIV ze skórą.
- stosunek oralny
Czas rozpoczęcia leczenia
- PEP należy rozpocząć natychmiast po stwierdzeniu wskazania
- Najlepszych efektów można się spodziewać, rozpoczynając profilaktykę w ciągu 24 godzin, a jeszcze lepiej – w ciągu 2 godzin.
- Jeśli między ekspozycją a potencjalnym rozpoczęciem profilaktyki upłynęło więcej niż 72 godziny, profilaktyka zwykle nie jest stosowana.
Schemat terapii PEP
- Standardowa kombinacja 2 NRTI + PI.
- Zalecane schematy leczenia
- TDF/FTC (dizoproksyl tenofowiru/emtricytabina) 245/200 mg 1 x 1 + RAL (raltegrawir) 400 mg 2 x 1
- RAL 600 mg 1 x 2
- TDF/FTC (jak wyżej) + DTG (dolutegrawir) 50 mg 1 x 1 (w razie potrzeby test ciążowy przed rozpoczęciem leczenia: szczegóły patrz punkt ciąża i karmienie piersią)
- TAF (alfenamid tenofowiru) + FTC + BIC (biktegrawir).
- TDF/FTC (dizoproksyl tenofowiru/emtricytabina) 245/200 mg 1 x 1 + RAL (raltegrawir) 400 mg 2 x 1
- Czas leczenia wynosi zazwyczaj 28–30 dni.
Dalsze leczenie
- Należy zwrócić uwagę na potrzebę wsparcia psychospołecznego zarówno przy podejrzeniu zakażenia HIV, jak i w razie pewnego dodatniego wyniku testu.
- Z rozpoznania zakażenia HIV mogą wyniknąć poważne problemy psychospołeczne.
- W rozwiązaniu tych często bardzo trudnych problemów pomagają specjalne instytucje działające w wielu miejscach, np. grupy samopomocowe czy poradnie psychologiczne.
- Należy dążyć do ścisłej współpracy z takimi instytucjami.
- Jeśli pozwala na to lokalna infrastruktura, należy rozważyć również zalecenie działań uświadamiających i edukacyjnych.
- Objawy psychiczne, takie jak lęk i depresja mogą wystąpić zarówno jako reakcja na zagrażające lub faktyczne zachorowanie, jak i jako skutek uboczny leczenia przeciwretrowirusowego.
- W przypadku stosowania efawirenzu obserwowano zwiększoną częstość występowania depresji i tendencji samobójczych.
- W trakcie leczenia farmakologicznego współistniejących chorób psychicznych należy wziąć pod uwagę potencjalne interakcje leków psychotropowych z leczeniem przeciwretrowirusowym.
- Na temat opieki paliatywnej w AIDS patrz również następujące artykuły:
Zapobieganie
Zalecenia
- Poinformowanie o sposobie transmisji.
- Zabezpieczenie prezerwatywą podczas stosunku płciowego.
- Skutkuje to co najmniej 80% zmniejszeniem zachorowalności na HIV przy konsekwentnym stosowaniu przez osoby heteroseksualne.
- Unikanie wspólnego korzystania ze strzykawek.
- Ograniczenie liczbę partnerów/partnerek seksualnych.
- Ustalenie źródła infekcji.
- Matki zakażone HIV nie powinny karmić piersią.
Leczenie zapobiegawcze – leki/szczepionki
- Kobiety w ciąży poddaje się leczeniu przeciwretrowirusowemu, aby zapobiec przeniesieniu choroby na dziecko.
- Profilaktyka pierwotna zakażeń oportunistycznych z zastosowaniem trimetoprimu/sulfametoksazolu, jeśli liczba komórek CD4 jest mniejsza niż 200/mcl.
- Przy braku przeciwciał HAV i/lub HBV wskazane jest odpowiednie szczepienie – należy sprawdzić wskazanie do szczepienia przeciwko HPV.
- Stosowanie szczepionek żywych, w tym BCG, jest przeciwwskazane.
- Profilaktyczne leczenie gruźlicy zaleca się u osób zakażonych HIV w przypadku:
- Dodatniej próby tuberkulinowej (Mantoux >5 mm) i dłuższego pobytu w kraju o wysokiej częstości występowania gruźlicy.
- Osób, u których wystąpiła zmiana wyniku próby tuberkulinowej, niezależnie od wieku i wcześniejszych szczepień BCG.
- Wyjątkiem są osoby zaszczepione wcześniej przeciw gruźlicy, u których zmiana wyniku próby jest związana z poprawą odporności komórkowej w wyniku leczenia przeciwwirusowego.
- Bliskiego kontaktu (przy liczbie komórek CD4 <2000/mcl) z osobami chorymi na gruźlicę zakaźną.
Profilaktyka przedekspozycyjna (PrEP)
Wskazania do doustnej profilaktyki przedekspozycyjnej
- Należy profilaktycznie zalecać osobom o znacznym ryzyku zakażenia HIV.
- Znaczne ryzyko zakażenia HIV w szczególności dotyczy następujących osób seronegatywnych:
- Mężczyzn, którzy uprawiają seks z mężczyznami (MSM) lub osób transpłciowych, które uprawiały seks analny bez prezerwatywy w ciągu ostatnich 3–6 miesięcy i/lub będą go przypuszczalnie uprawiały w ciągu najbliższych miesięcy, lub w przypadku zakażenia przenoszonego drogą płciową (sexually transmitted infection – STI) w ciągu ostatnich 12 miesięcy.
- Niezgodnych serologicznie układów z partnerami wiremicznymi seropozytywnymi nieleczonymi antyretrowirusowo, leczonymi antyretrowirusowo bez supresji lub w początkowej fazie leczenia przeciwretrowirusowego (tj. z HIV RNA, które nie jest od 6 miesięcy niższe niż 200 kopii RNA/ml).
- Jeśli partnerzy seropozytywni są poddawani leczeniu antyretrowirusowemu bez supresji, przed zleceniem profilaktyki przedekspozycyjnej należy w miarę możliwości przeprowadzić badania oporności, aby wykluczyć nieskuteczność TDF i/lub FTC.
- Ponadto może wystąpić znaczne ryzyko indywidualne, szczególnie w przypadku:
- Osób uprawiających seks bez prezerwatywy lub osób, u których niezdiagnozowane zakażenie HIV jest prawdopodobne.
- Osób przyjmujących iniekcyjnie narkotyki, które nie używają sterylnych materiałów do iniekcji.
Zalecane leki
- Profilaktyka przedekspozycyjna powinna obejmować doustne przyjmowanie preparatu złożonego emtricytabina/dizoproksyl tenofowiru (TDF/FTC).
- Profilaktyka przedekspozycyjna powinna polegać na stałym przyjmowaniu TDF/FTC raz dziennie.
- W indywidualnych przypadkach można rozważyć przerywane, okazjonalne stosowanie profilaktyki przedekspozycyjnej jako pozarejestracyjnego użycia leku (off–label).
Tylko w połączeniu z innymi środkami zapobiegawczymi
- Zalecenie profilaktyki przedekspozycyjnej HIV zawsze powinno być połączone z udzieleniem informacji o innych środkach ochrony przed zakażeniem HIV oraz STI, w tym wirusowym zapaleniem wątroby.
- Należy przy tym podkreślić, że profilaktyka przedekspozycyjna HIV zmniejsza ryzyko transmisji HIV, ale nie ryzyko innych zakażeń przenoszonych drogą płciową.
Wykluczenie przeciwwskazań
- Oprócz stopnia ryzyka zakażenia HIV należy sprawdzić możliwe przeciwwskazania, a także następujące kwestie:
- Aktualny, ujemny wynik badania serologicznego w kierunku HIV (ELISA IV generacji z p24–Ag), nie starszy niż 14 dni; powtórzyć 4 tygodnie po rozpoczęciu PrEP.
- Wykluczenie ostrego zakażenia WZW B przez wykonanie badań serologicznych (antygen HBs, przeciwciała anty–HBc) lub badań odporności na zakażenie HBV (przeciwciała HBs, w razie potrzeby szczepienie przeciwko HBV).
- Wykluczenie zaburzeń czynności nerek przez oznaczenie poziomu kreatyniny w surowicy (eGFR co najmniej 60, wskazane powyżej 80 ml/min).
- Wymóg systematycznego przyjmowania leków.
- Działanie ochronne następuje z opóźnieniem względem rozpoczęcia PrEP
- Dostateczne stężenie leku występuje w błonie śluzowej jelita grubego od 2. dnia przyjmowania, w żeńskich narządach płciowych – od 7. dnia przyjmowania.
- Zmniejszenie ryzyka o 75% w warunkach stosowania emtricytabiny/tenofowiru
- W 2016 r. dopuszczono emtricytabinę/tenofowir do stosowania w profilaktyce przedekspozycyjnej.
- Profilaktyka przedekspozycyjna nie jest w Polsce refundowana.
- Miesięczny koszt leczenia emtricytabiną/tenofowirem (lek generyczny) wynosi 160–240 zł (stan na październik 2023 r.).
Profilaktyka ekspozycji na HIV w parach z niezgodnym statusem serologicznym
- Oprócz konsekwentnego stosowania prezerwatyw istnieją dwie możliwości działania farmakologicznego:
- terapia przeciwretrowirusowa (ARV) partnerów(-ek) zakażonych HIV
- Zmniejszenie ryzyka transmisji choroby na niezakażonych partnerów/niezakażone partnerki o ponad 95%.
- chemoprofilaktyka dla niezakażonych partnerów(-ek).
- Nierutynowa profilaktyka ekspozycji (np. po pęknięciu prezerwatywy).
- Rutynowa stała profilaktyka (profilaktyka przedekspozycyjna)
- terapia przeciwretrowirusowa (ARV) partnerów(-ek) zakażonych HIV
- Profilaktyka przedekspozycyjna (PrEP) (patrz wyżej).
- Pary z niezgodnym statusem serologicznym należy poinformować o istniejących możliwościach działań farmakologicznych, aby umożliwić im podjęcie świadomej decyzji o tym, czy chcą wybrać jedną z tych opcji i aby mogły się do niej odpowiednio przygotować.
- Po podjęciu decyzji o PrEP: należy ustalić odstępy między badaniami.
- Jeśli przewidywana jest PEP w razie ewentualnych przyszłych przypadków ekspozycji: ustalenie trybu wizyt i porad, np. numer telefonu w razie pytań.
Dzieci w placówkach publicznych
- Według aktualnej wiedzy nie ma dowodów na to, że dzieci zakażone HIV niosą praktyczne ryzyko zakażenia wobec innych dzieci lub dorosłych w bliższym otoczeniu. Dzieci zakażone wirusem HIV mogą więc bez ograniczeń uczęszczać do placówek opiekuńczo–wychowawczych i innych placówek publicznych.
- Nie ma obowiązku informowania zainteresowanych instytucji, takich jak szkoła, świetlica czy przedszkole. Ponieważ HIV nie jest zaraźliwy w codziennych kontaktach, ryzyko stygmatyzacji osób zakażonych jest większe niż narażenie na niebezpieczeństwo osób trzecich.
- Jeżeli dziecko zakażone HIV wykazuje szczególne problemy z zachowaniem, które dla innych dzieci skutkują zwiększonym ryzykiem kontaktu z zakażoną krwią (gryzienie/drapanie), lub ma szczególne problemy skórne, które mogą zwiększyć zagrożenie dla personelu, przed przyjęciem do przedszkola i szkoły wskazana jest ocena sytuacji według standardów medycznych i edukacyjnych. Dotyczy to również dzieci, które zachorowały na AIDS.
HIV i praca
- Transmisja HIV w życiu zawodowym zachodziła do tej pory tylko przez kontakt z krwią lub preparatami skażonymi wirusem (kultury wirusa), tj. w przypadku:
- ran kłutych i ciętych
- kontaktu zakażonych płynów ustrojowych z otwartą raną lub skórą o przerwanej ciągłości (uszkodzoną) u osoby narażonej
- ekspozycji błon śluzowych (w tym tryśnięcia krwi do oka).
- W związku z tym nie istnieją zasadnicze ograniczenia w wykonywaniu pracy zawodowej.
- Pracownicy nie są zobowiązani do ujawniania pracodawcy swojego statusu serologicznego.
- Wyjątek stanowi personel medyczny wykonujący czynności o zwiększonym ryzyku transmisji HIV.
- Również zawody, w których osoba zakażona ma kontakt z żywnością, takie jak ubój, przetwórstwo ryb, gastronomia, mogą być wykonywane bez ograniczeń przez osobę zakażoną HIV.
- Nie ma dowodów na to, że wirus jest przenoszony przez żywność.
- W zawodach związanych z kontaktem z żywnością obowiązują zasady ogólne – niezależnie od HIV – zgodnie z którymi osoba z otwartymi lub zakażonymi ranami, zakażeniami skóry, uszkodzeniami skóry lub biegunką nie może mieć kontaktu z żywnością.
Uznanie za chorobę zawodową
- Jeżeli do zakażenia wirusem HIV doszło w związku z wykonywaną pracą, można to uznać za chorobę zawodową.
- Przeprowadza się szczegółowy wywiad zawodowy i wywiad dotyczący ryzyka, a o uznaniu za chorobę zawodową decyduje właściwy państwowy inspektor sanitarny.
Przebieg, powikłania i rokowanie
Przebieg
- Zakażenie HIV przebiega zwykle powoli, ze stopniową progresją na przestrzeni lat.
- W warunkach stosowania nowoczesnego leczenia przeciwretrowirusowego, dobrej kontroli i przestrzegania zaleceń lekarskich większość pacjentów może prowadzić normalne życie bez istotnego skrócenia jego przewidywanej długości.
Powikłania
- Zaburzenia psychiczne i samobójstwo.
- Zakażenia oportunistyczne.
- W układzie nerwowym
- zakażenia
- zaburzenia neuropoznawcze
- neuropatie, np. radikulopatie.
- W układzie sercowo–naczyniowym
- zwiększone ryzyko sercowo–naczyniowe
- uwaga: zwiększone ryzyko rabdomiolizy przy połączeniu inhibitorów proteazy i statyn.
- W układzie oddechowym
- zapalenie płuc wywołane przez Pneumocystis
- inne zakażenia płuc.
- W układzie pokarmowym
- kandydozy
- afty
- zapalenie przełyku
- przewlekłe zapalenie wątroby
- niealkoholowe stłuszczenie wątroby.
- W układzie moczowo–płciowym
- zakażenia
- choroby nerek.
- W układzie mięśniowo–szkieletowym
- Powikłania metaboliczne i endokrynologiczne
- zwiększone ryzyko insulinooporności, cukrzycy, dyslipidemii i lipodystrofii.
- Rozwój nowotworu złośliwego
- od czasu wprowadzenia skutecznego leczenia przeciwretrowirusowwgo nowotwory uwarunkowane HIV występują znacznie rzadziej.
Monitorowanie liczby komórek CD4
- Objawy zakażeń oportunistycznych związanych z HIV mogą wystąpić przy każdym poziomie CD4, ale częstość występowania zakażeń ciężkich i potencjalnie zagrażających życiu rośnie gwałtownie, gdy liczba komórek CD4 spada poniżej 200/mcl.
- CD4 na poziomie 200, 100 i 50 na mcl oznacza ryzyko zakażenia Pneumocystis jiroveci, Toxoplasma gondii oraz Mycobacterium avium i jest wskazaniem do profilaktyki antybiotykowej.
Rokowanie
- Zakażenie HIV z choroby o niemal stuprocentowej śmiertelności przekształciło się w chorobę przewlekłą, wymagającą leczenia przez całe życie.
- Bez leczenia
- Średni czas od zakażenia do rozwoju AIDS u chorych nieleczonych przeciwwirusowo wynosi 8–10 lat.
- Śmiertelność w przypadku w pełni rozwiniętego AIDS bez leczenia przeciwretrowirusowego wynosi 80% po 2 latach i 100% po 5 latach.
- Optymalne leczenie
- Nowoczesne leczenie skojarzone pozwala wydłużyć bezobjawowy okres zakażenia HIV.
- U pacjentów, u których rozwinęło się już AIDS, osłabiona odporność poprawia się w trakcie leczenia.
- U pacjentów, którzy systematycznie stosują i dobrze tolerują leczenie, występuje umiarkowane skrócenie oczekiwanej długości życia podobnie jak w innych chorobach przewlekłych, np. cukrzycy.
Dzieci zakażone wirusem HIV
- Zakażenie HIV u dzieci ma znacznie bardziej agresywny przebieg niż u dorosłych
- U niemowląt i małych dzieci dominują zaburzenia rozwoju i ciężkie zakażenia bakteryjne.
- 1/5 wszystkich nieleczonych niemowląt umiera w pierwszym roku życia lub doznaje uszkodzeń neurologicznych w przebiegu encefalopatii HIV.
- Dlatego leczenie przeciwretrowirusowe należy rozpocząć już w pierwszych miesiącach życia.
Dalsze postępowanie
- Koordynacją dalszego postępowania powinna się zająć placówka wyspecjalizowana w opiece nad pacjentami z HIV (poradnia specjalistyczna lub oddział).
- Ważna jest współpraca i zaangażowanie lekarzy rodzinnych.
- Należy utrzymywać kontakt z pacjentem i rozmawiać na takie tematy jak kontakty seksualne, partnerzy, profilaktyka, chęć posiadania dzieci.
- Systematyczne:
- monitorowanie sytuacji psychospołecznej
- coroczne szczepienie przeciwko grypie
- ogólne badania profilaktyczne
- coroczne badania profilaktyczne w kierunku dysplazji
- u kobiet: badanie szyjki macicy i odbytnicy (poradnia ginekologiczna)
- u mężczyzn, którzy uprawiają seks z mężczyznami: badanie odbytnicy
- ewentualne badanie w kierunku chorób przenoszonych drogą płciową (poradnia dermatologiczna/chorób zakaźnych).
Badania laboratoryjne (zlecone przez lekarza nadzorującego leczenie HIV)
- Komórki CD4 i RNA HIV.
- Hb, leukocyty z rozmazem, płytki krwi, bilirubina, GPT, AP, Ca, kreatynina, GFR.
- Glukoza, cholesterol całkowity, LDL, HDL i trójglicerydy.
- CK, amylaza, mleczan.
- Kontrola serologiczna w przypadku braku w wywiadzie wcześniejszego zapalenia wątroby typu A/B/C.
- Ewentualnie coroczne badanie w kierunku kiły.
- Badanie moczu.
- Ewentualnie monitorowanie stężenia leku we krwi.
- Ewentualnie test przesiewowy na obecność narkotyków lub leków.
Monitorowanie stężenia leku we krwi (Therapeutic Drug Monitoring – TDM)
- Związek między stężeniem w osoczu a skutecznością przeciwwirusową.
- Możliwe wskazania do oznaczenia poziomu leku w osoczu:
- stosowanie wielu leków/podejrzenie interakcji farmakokinetycznych
- znaczna niedowaga lub nadwaga u osoby leczonej
- wielooporność
- leczenie kobiet w ciąży
- leczenie dzieci
- zaburzenia wchłaniania jelitowego
- nasilone zaburzenia czynności wątroby
- utrata skuteczności leczenia przeciwretrowirusowego (diagnoza różnicująca: problemy z przestrzeganiem zaleceń lekarskich/oporność)
- podejrzenie toksyczności leku.
Oznaki progresji
- Wzrost HIV–RNA.
- Spadek liczby limfocytów T CD4
- zwykle dopiero po niepowodzeniu wirusologicznym
- nie zawsze oznacza niepowodzenie leczenia i progresję.
- znaczny spadek liczby limfocytów T CD4 bez niepowodzenia wirusologicznego może również wskazywać na powikłania (np. marskość wątroby, gruźlicę, chłoniaki złośliwe)
- Nowe lub nasilone objawy:
- utrzymująca się gorączka
- nocne poty
- uporczywa biegunka
- kaszel
- duszność
- utrata masy ciała
- problemy z gojeniem się ran
- obłożone gardło
- wykwity/nowotwory skóry
- zaburzenia widzenia.
- Choroby oportunistyczne mogą również występować w postaci zaostrzenia zakażeń subklinicznych w warunkach leczenia przeciwretrowirusowego (zespół rekonstytucji immunologicznej) i nie należy ich wówczas interpretować jako niepowodzenia leczenia.
Wzrost poziomu wiremii – możliwe przyczyny
- Najczęstszą przyczyną wzrostu poziomu wiremii w osoczu jest nieprzestrzeganie zaleceń lekarskich.
- Inne możliwe przyczyny:
- ograniczone wchłanianie lub przyspieszony metabolizm leków antyretrowirusowych
- interakcje lekowe
- oporność wirusów lub jej nabycie
- niewystarczające dawkowanie.
Odstępy między badaniami
- Liczbę komórek CD4 i RNA HIV należy oznaczyć w momencie rozpoznania, a następnie w odstępach od 3 do 6 miesięcy
- Wdrożenie i modyfikacja terapii mogą wymagać krótszych odstępów między badaniami.
- Pacjenci, którzy rozpoczynają leczenie przeciwretrowirusowe przy liczbie komórek CD4 mniejszej niż 200/mcl, a zwłaszcza z równoczesnym wysokim poziomem wiremii HIV, w pierwszych tygodniach powinni być poddawani ścisłej obserwacji klinicznej.
- Po zmniejszeniu poziomu RNA HIV pod wpływem leczenia do wartości poniżej 50 kopii/ml zaleca się kontrole co 2–4 miesiące.
Powodzenie i niepowodzenie leczenia
- Powodzenie leczenia objawia się poprawą stanu klinicznego i wzrostem liczby komórek CD4, zależy także od innych czynników, takich jak wiek pacjenta i ewentualne choroby towarzyszące.
- Za powodzenie leczenia uważa się trwały spadek poziomu wiremii w osoczu poniżej 50 kopii RNA HIV na 1 ml.
- W przypadku wyniku powtórnego badania poziomu RNA HIV powyżej 50 kopii/ml należy wykluczyć niepowodzenie wirusologiczne.
- Niepowodzenie wirusologiczne jest prawdopodobne przy stężeniu RNA HIV powyżej 200 kopii/ml.
Badanie oporności w przypadku niepowodzenia leczenia
- Jeśli poziom wiremii wynosi >200 kopii/ml, należy przeprowadzić badanie oporności.
- Potwierdzony poziom wiremii 50–200 kopii/ml jest wskazaniem do przeprowadzenia badania oporności.
Informacje dla pacjentów
O czym należy informowac pacjentów?
- O ryzyku zakażenia i środkach zapobiegawczych
- O dobrym rokowaniu w warunkach prawidłowego leczenia przeciwretrowirusowego
- przerywanie leczenia zwiększa ryzyko rozwoju oporności
- o ryzyku związanym z leczeniem farmakologicznym, w tym interakcjach potencjalnie zagrażających życiu.
- W przypadku objawów i dolegliwości, które są nowe lub trwają wyjątkowo długo: należy zasięgnąć porady lekarza
- Systematyczne monitorowanie obrony immunologicznej i pomiar poziomu wiremii we krwi są ważne, aby móc w porę rozpocząć leczenie lub w razie potrzeby je zmodyfikować.
- O prawach pacjentów i pracowników.
- O środkach profilaktycznych, np. szczepieniach.
Materiały edukacyjne dla pacjentów
Ilustracje
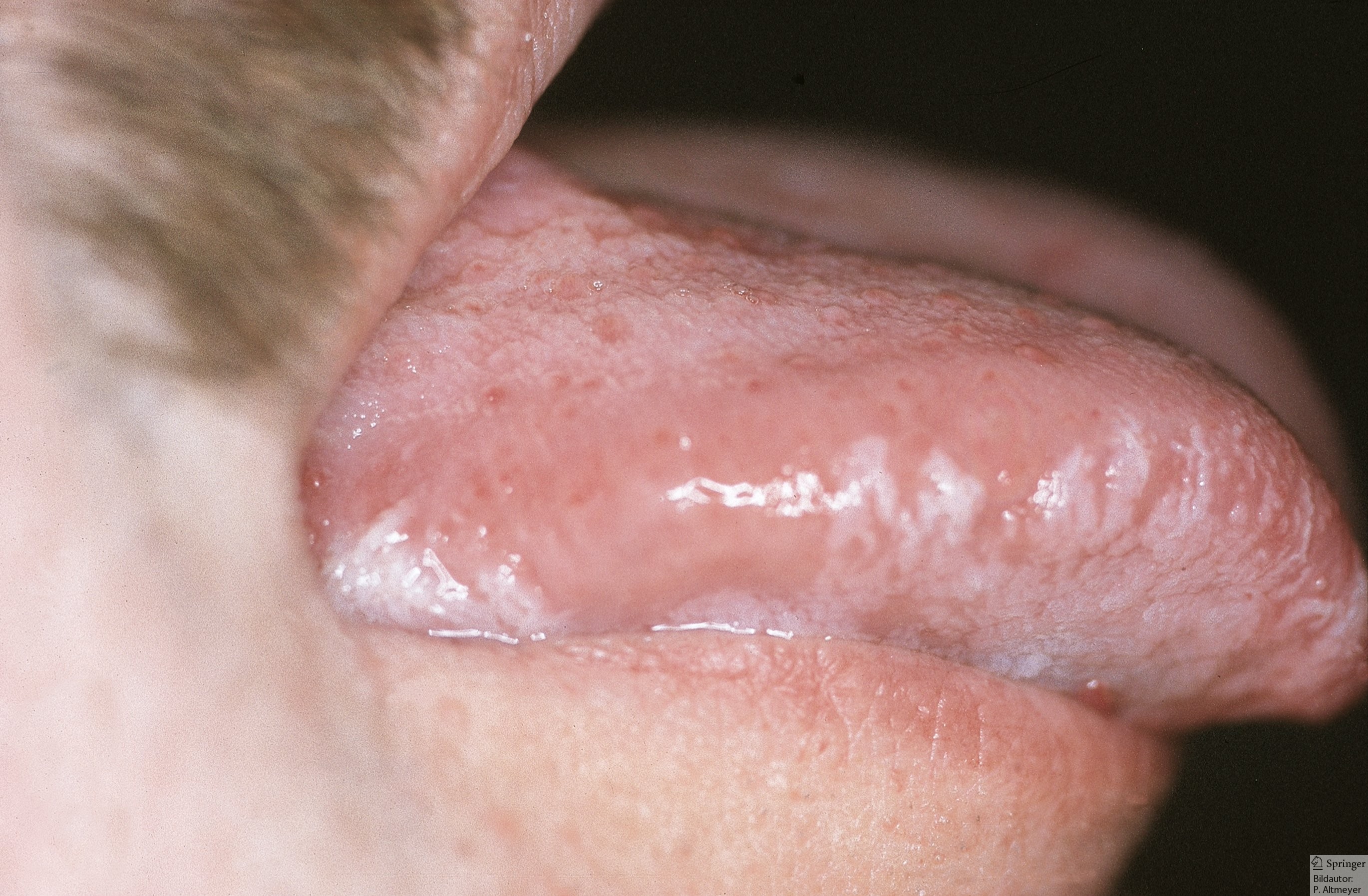
Leukoplakia włochata jamy ustnej (źródło: P. Altmeyer, Online Encyclopaedia Dermatology, Venereology and Environmental Medicine)
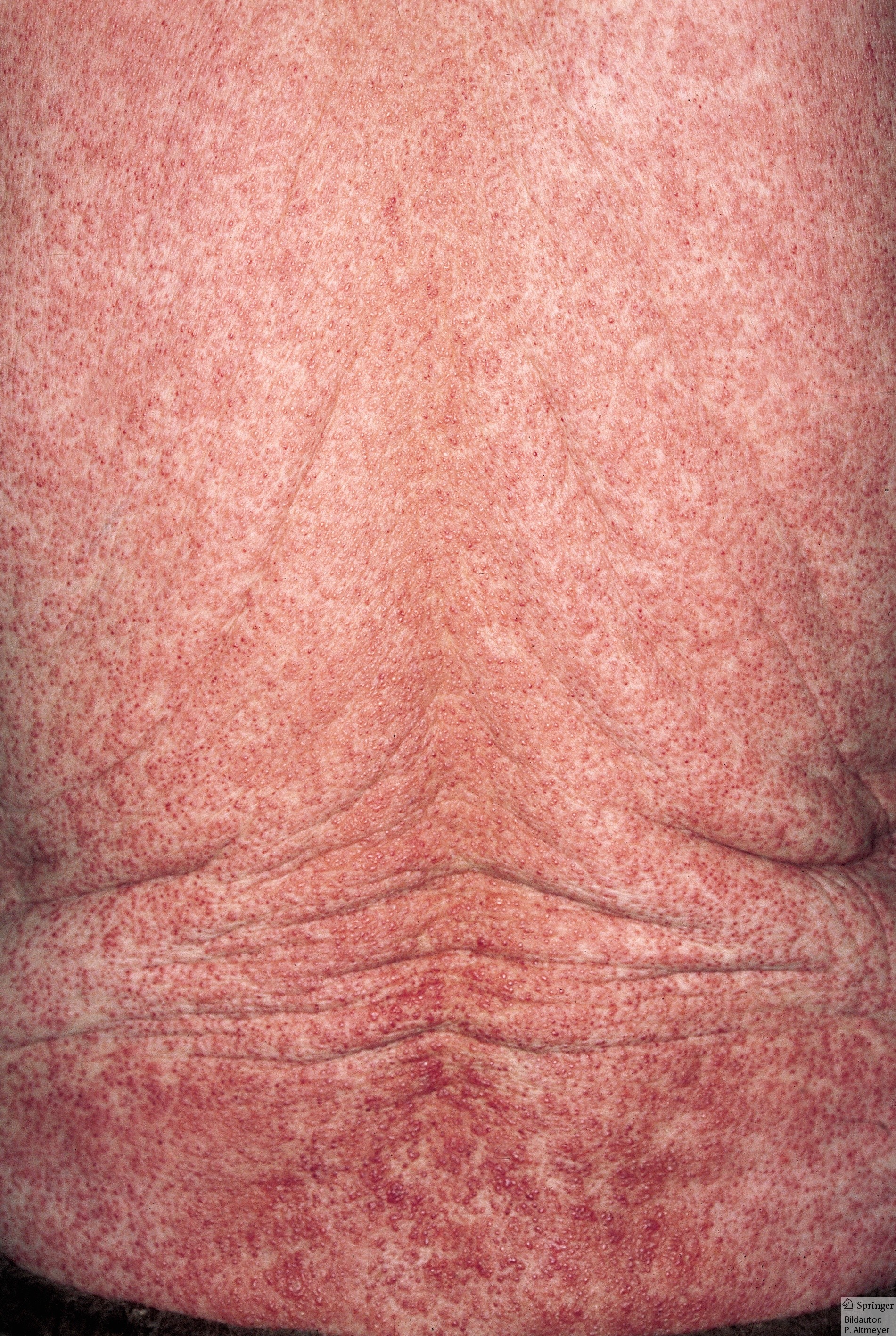
Naczyniakowatość bakteryjna
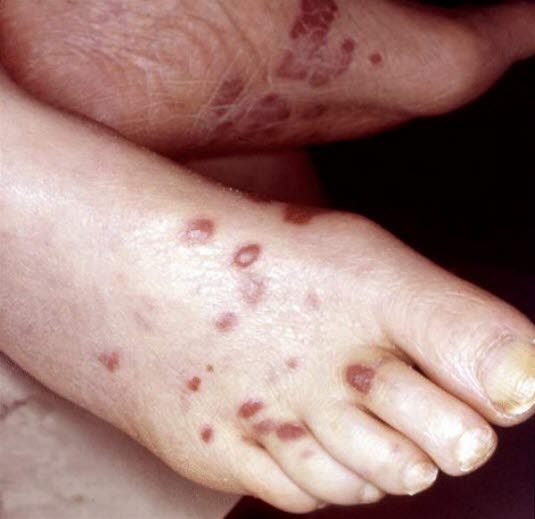
Mięsak Kaposiego
Źródła
- Centers for Disease Control and Prevention. Technical Update for HIV Nucleic Acid Tests Approved for Diagnostic Purposes. Division of HIV Prevention, National Center for HIV, Viral Hepatitis, STD, and TB Prevention, Centers for Disease Control and Prevention, maj 2023, cdc.gov, dostęp: 30.10.2023.
- Zakład Epidemiologii Chorób Zakaźnych i Nadzoru NIZP PZH – PIB: Choroby zakaźne i zatrucia w Polsce w 2022 roku, wwold.pzh.gov.pl, dostęp: 30.10.2023.
Piśmiennictwo
- UNAIDS. Global HIV & AIDS statistics – 2020 fact sheet, czerwiec 2020, www.unaids.org.
- European AIDS Clinical Society (EACS), Guidelines Version 12.0, October 2023, www.eacsociety.org.
- White A.B., Mirjahangir J.F., Horvath H., Anglemyer A., Read J.S. Antiretroviral interventions for preventing breast milk transmission of HIV. Cochrane Database of Systematic Reviews 2014, Issue 10. Art. No.: CD011323. DOI: 10.1002/14651858.CD011323, DOI.
- Zasady Opieki nad Osobami Zakażonymi HIV. Zalecenia PTN AIDS 2024, ptnaids.pl, dostęp: 15.01.2025
- Hammer S.M., Eron J.J., Reiss P., Schooley RT et al. Antiretroviral Treatment of Adult HIV Infection, 2008, Recommendations of the International AIDS Society–USA Panel. JAMA 2008, 300: 555-70, PubMed.
- European guideline for the management of genital herpes. IUSTI/WHO European STD guidelines Editorial Board, 2017, iusti.org.
Opracowanie
- Sławomir Chlabicz (redaktor)
- Marta Niwińska (recenzent)
- Thomas M. Heim (recenzent/redaktor)